2022 年 62 巻 1 号 p. 22-26
2022 年 62 巻 1 号 p. 22-26
73歳女性.夜間睡眠中の大声の寝言や日中覚醒時の異常言動,会話中に急に反応が乏しくなるエピソードが月単位で相次いで出現.他院にてレビー小体型認知症(dementia with Lewy bodies,以下DLBと略記)と診断されるも,これらの頻度が徐々に増加したため,当院にて精査入院.終夜睡眠ポリグラフィの“筋活動の低下を伴わないレム睡眠”および18F-FDG PETの辺縁系糖代謝亢進より,レム睡眠行動異常症を合併した辺縁系脳炎と診断.ステロイドパルス療法2コース実施後,症状は徐々に軽減した.本例は後に血清抗voltage-gated potassium channel(VGKC)複合体/leucine-rich glioma-inactivated protein 1(LGI1)抗体陽性が判明した.本抗体関連辺縁系脳炎は臨床像がDLBに重なることがあり,診断に際し注意が必要である.
A 73-year-old woman was admitted to our hospital owing to abnormal diurnal behavior, sudden brief episodes of impaired awareness, and loud nocturnal sleep talking. Her symptoms had developed gradually over several months and had been treated as dementia with Lewy bodies (DLB) at another clinic. Video-polysomnography revealed brief sleep talking and gross movements associated with REM sleep without atonia. 18F-FDG PET revealed increased glucose metabolism in both medial temporal lobes. These findings led to a diagnosis of limbic encephalitis (LE) comorbid with REM sleep behavior disorder (RBD). After two courses of intravenous methylprednisolone pulse therapy, her symptoms gradually improved. Her illness was later confirmed as anti-voltage-gated potassium channel (VGKC) complex/leucine-rich glioma-inactivated protein 1 (LGI1) antibody-associated LE using serum analyses. Clinical features of anti-VGKC complex/LGI1 antibody-associated LE can mimic those of DLB, particularly when comorbid with RBD.
中枢神経系の抗voltage-gated potassium channel(VGKC)複合体抗体関連疾患にはMorvan症候群や辺縁系脳炎がある1).抗VGKC複合体抗体関連辺縁系脳炎は,亜急性で進行する近時記憶障害や見当識障害,てんかん発作を特徴とし,しばしば不眠や過眠,レム睡眠行動異常症(REM sleep behavior disorder,以下RBDと略記)を合併する2).我々は,夜間の大声の寝言や精神症状,認知症状が相次いで出現し,抗VGKC複合体/leucine-rich glioma-inactivated protein 1(LGI1)抗体関連辺縁系脳炎と診断した高齢女性例を経験した.RBDを合併しうる点で臨床像がレビー小体型認知症(dementia with Lewy bodies,以下DLBと略記)に重なることがあり,互いに重要な鑑別疾患となりうるため報告する.
症例:73歳女性
主訴:夜間の大声の寝言,日中の独語,会話時の急な反応停止
既往歴:X-21年に卵巣癌にて子宮+両側付属器摘出術と化学療法を受け根治.高血圧症と骨粗鬆症に対し近医にて治療中.
生活歴:飲酒・喫煙歴はなく,生来右利き.
家族歴:特記事項なし.
現病歴:X年1月上旬より夜間睡眠中に頻繁に中途覚醒するようになり,大声で叫ぶような寝言を発するようになった.4月より家族と外出中に「亡くなった親戚が後ろから付いてくる」など奇異な言動や,小声で呟くような意味不明の独語もみられるようになった.また急に表情が固まり数秒間無反応となる状態が繰り返し見られるようになった.4月下旬に当院受診し,外来にて精査予定としたが,同時に他の認知症専門クリニックも受診し,先方でDLBの診断のもと投薬治療が開始された.その後,異常言動や独語,急な反応停止の頻度が増加したほか,7月には家族の顔が判別できなくなることがたびたび生じたため,当院にて精査入院となった.
入院時所見:身長143.7 cm,体重52.3 kg,体温36.1°C,血圧122/78 mmHg,脈拍94回/分・整,SpO2 99%.項部硬直ほか一般身体所見に異常は認めなかった.意識清明で礼節の保たれた会話が可能だが,急に表情が虚ろになり小声で意味不明な独語を発することがあった.疎通可能なときには失語や失行はなく,寡動や筋固縮などのパーキンソニズムは認めなかった.脳神経,運動・感覚系,深部腱反射,協調運動,自律神経系に異常はなかった.またfaciobrachial dystonic seizureらしい顔面・四肢の短時間の不随意運動・けいれんは認めなかった.
入院時検査所見:神経心理検査では,Mini-Mental State Examination(MMSE)がX年5月には29点であったが,7月入院時点では23点であった.リバーミード行動記憶検査(Rivermead Behavioral Memory Test,以下RBMTと略記)はスクリーニング4点/標準プロフィール16点,ベントン視覚記銘検査は正確数4/誤謬数14,コース立方体組み合わせテストは18点(IQ = 56),Frontal Assessment Batteryは12点と低下していた.一般血液検査は,随時血糖224 mg/dl,HbA1c 7.5%であった以外は血算,肝・腎機能,電解質に異常はなく,CRPは0.03 mg/dlと上昇はなかった.自己抗体は抗甲状腺ペルオキシダーゼ抗体11.2 IU/ml,抗サイログロブリン抗体20.4 IU/ml以外,検索しえた限り全て陰性であった.TSH・FT-3・FT-4およびビタミンB1,B12,葉酸は基準域内であった.感染症検査では血清梅毒反応は陰性で,血清HSV・VZV抗体はともにIgM陰性・IgG陽性であった.髄液検査は初圧70 mmH2O,細胞数2/mm3(単核球100%),蛋白42 mg/dl,糖78 mg/dl(同時血糖136 mg/dl)で,培養や細胞診は陰性であった.頭部MRIでは明らかな腫脹や信号変化,ガドリニウム造影効果は認めなかった(Fig. 1A~C).18F-FDG PETでは後頭葉の糖代謝低下やcingulate island sign(CIS)は認めなかった一方,両側内側側頭葉に糖代謝亢進を認めた(Fig. 1D~F).ルーチンの脳波検査では,繰り返し行うもてんかん性活動は認めなかった.両側浅指屈筋への表面筋電図増設によるビデオ同時記録終夜睡眠ポリグラフィ(video-polysomnography,以下vPSGと略記)では,レム睡眠中の寝言や四肢の活発な運動とともに筋活動の低下を伴わないレム睡眠(REM sleep without atonia,以下RWAと略記)を認め(Fig. 2),SINBAR groupの判定法3)で%RWA = 66.1%であった.傍腫瘍性自己免疫性脳炎の鑑別目的で実施した体幹部CT/18F-FDG PET,上部・下部消化管内視鏡検査では,明らかな異常を認めなかった.

Axial fluid-attenuated inversion recovery images (FLAIR; A, B) and gadolinium-enhanced T1-weighted images (Gd-T1WI; C) revealed no significant findings in the brainstem and medial temporal lobes (FLAIR: TR/TE/TI = 6,000/85/2,030 msec, thickness = 5 mm, three-dimensional Gd-T1WI: TR/TE = 600/7.8 msec, thickness = 2 mm). Mild high-signal intensities of the bilateral amygdala were regarded as a normal variation of the FLAIR signal intensity in the limbic lobe. 18F-FDG PET; D–F showed increased glucose metabolism in both medial temporal lobes (arrows). Neither decreased glucose metabolism in the occipital lobes nor obvious cingulate island sign was observed.
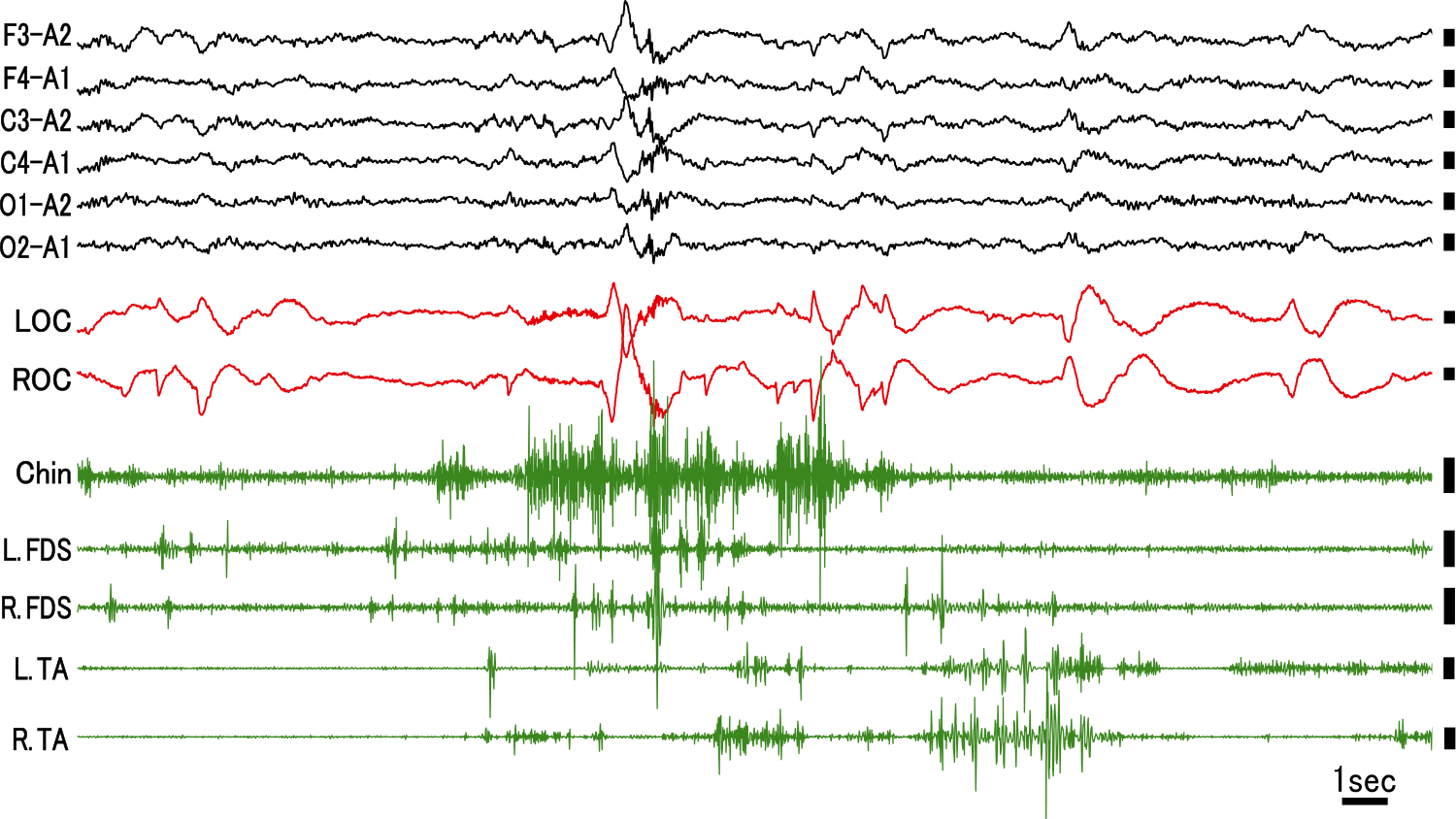
Electroencephalogram (black) shows low-amplitude mixed-frequency activity with the intrusion of eye movement artifacts, and electrooculogram (red) shows rapid eye movements. Electromyogram (green) of the chin, flexor digitorum superficialis (FDS), and tibialis anterior (TA) were activated tonically and/or phasically, which is indicative of RWA. LOC = left outer canthus; ROC = right outer canthus; L = left; R = right. Scale bar = 50 μV.
入院後経過(Fig. 3):他院でDLBと診断されたこともあり,入院当初は認知症の行動・心理症状への対応としてバルプロ酸Na投与を開始したが,その後も急な反応停止が繰り返し出現していた.入院中の症状や検査結果より,DLBよりも意識減損発作(focal impaired awareness seizure,以下FIASと略記)やRBDを合併した辺縁系脳炎が強く疑われるようになり,感染性脳炎が否定された時点でステロイドパルス療法(methylprednisolone 1,000 mg/day × 3日間)を2コース行い,さらにバルプロ酸Naをレベチラセタムに変更した.その直後よりFIASらしき急な反応停止は消失した一方,精神症状は一時的に悪化し,家族や友人に頻繁に電話をかけるなど多弁で落ち着かない状態が続いたが,抗てんかん薬をバルプロ酸Naに戻したところ改善した.その後は日中の異常言動や夜間の寝言も徐々に改善したため,9月に自宅退院とした.退院後に治療前血清および髄液で抗VGKC複合体抗体陽性が判明したが(抗体価:血清1,042.7 pM,髄液986.1 pM),臨床的には急な反応停止エピソードや精神症状は引き続き落ちついていたため,年齢や耐糖能異常を考慮し経口ステロイドによる維持治療は行わなかった.X + 1年3月時点では,神経心理検査でMMSEは22点,RBMTはスクリーニング7点/標準プロフィール19点,ベントン視覚記銘検査は正確数7/誤謬数6,コース立方体組み合わせテストは32点(IQ = 67)と改善はわずかであった.また血清抗VGKC複合体抗体価は806.4 pM,vPSGでの%RWAは57.3%で,ステロイドパルス療法前と比較してわずかな低下にとどまっていた.以降は血中アンモニア値上昇のためバルプロ酸Naをラコサミドに変更した以外に治療変更なく,年単位で外来経過観察を継続した.X + 4年時点では,MMSEは30点まで改善し,DLBらしい認知症状や精神症状,錐体外路症状のない状態を維持していたが,一方でRBDによる夜間の寝言は残存していた.なお本例は後日,診断時の血清で抗LGI1抗体陽性(間接蛍光抗体法)が確認された.また抗NMDA受容体抗体や傍腫瘍性神経症候群に関連する各種抗神経抗体は陰性であった.診断時の髄液オレキシン濃度も332 pg/mlと正常であった.血清抗contactin associated protein 2(Caspr 2)抗体測定およびDATスキャン,MIBG心筋シンチは診療上の必要性の理由で行っていない.

The patient developed abnormal diurnal behavior, sudden brief episodes of impaired awareness, and loud nocturnal sleep talking over several months. These symptoms gradually improved after two courses of intravenous methylprednisolone (IVMP) pulse therapy. VGKC = voltage-gated potassium channel; CSF = cerebrospinal fluid; RWA = REM sleep without atonia; MMSE = Mini-Mental State Examination; RBD = REM sleep behavior disorder.
本例は,高齢女性で変動をともなう亜急性の認知・精神症状,夜間異常言動を主徴とし,当初DLBと判断された.実際に夜間異常言動はvPSGでRBDと診断されたが,急な反応停止エピソードは認知症状の変動ではなく臨床的にFIASが疑われ,原因疾患はDLBではなく抗VGKC複合体/LGI1抗体関連辺縁系脳炎であった.ステロイドパルス療法と抗てんかん薬投与で認知・精神症状は改善し,急な反応停止エピソードも消失した一方,夜間の寝言が長期残存した.
抗VGKC複合体抗体はIsaacs症候群の疾患マーカーとして見出された自己抗体で,のちに多彩な睡眠関連症状や精神症状,自律神経障害,多臓器不全を呈するMorvan症候群や,一部の辺縁系脳炎でも陽性になることが報告された1).さらに疾患の標的抗原はMorvan症候群では抗Caspr2抗体,辺縁系脳炎では抗LGI1抗体であることが判明し,これらは一連の疾患スペクトラムであると考えられている.
抗VGKC複合体抗体関連疾患では,睡眠関連症状がたびたび報告されている2).Corneliusらの報告では,抗VGKC複合体抗体陽性のMorvan症候群や辺縁系脳炎15例中14例で,不眠や夢幻様行動,睡眠中のてんかん発作,日中過眠を認めたとされている4).またIranzoらの報告では,同複合体抗体関連辺縁系脳炎の6例中5例で病初期にRBDを合併したとされている5).なぜ本抗体関連辺縁系脳炎でRBD/RWAが生じるか未解明であるが,動物実験より扁桃体とsublaterodorsal tegmentum nucleus(ヒトの青斑下核に相当)を含む神経回路の障害でこれらが惹起されうると想定されており6)7),本例も間接的にこの部位の機能異常により夜間の大声の寝言が生じた可能性がある.なお本例の急な反応停止エピソードについて,当初は脳炎の視床下部への波及による症候性ナルコレプシーとしての睡眠発作も疑ったが,髄液オレキシン値に低下はなく否定的であった.
一方DLB診断の観点では,RBDの併存は有力な手がかりとされている.最終的に剖検で確定診断したDLB 234例の追跡研究では,診断基準にRBDを加えることで診断の正確性が大幅に向上することが報告され8),2017年に発表されたDLB診断基準第4版では,RBDが中核的特徴として新たに加えられている9).この診断基準を参照すると,本例は認知機能低下や注意・集中の変動,幻視とも受け取れる異常言動がみられたことから,解釈によってはRBDと合わせ中核的特徴2項目以上を満たし,probable DLBと判断することもできる.他方RBDの背景の観点では,抗VGKC複合体関連疾患のほか,脳血管障害や脳腫瘍,ナルコレプシーなどさまざまな神経疾患に併存することが知られており,必ずしもαシヌクレイノパチーの関連病態とは限らない10).本例の場合,MIBG心筋シンチ未施行であったものの,18F-FDG PETでDLBの特徴とされる後頭葉糖代謝低下やCISを認めなかったことや,発症後少なくとも4年の時点で認知・精神症状や錐体外路症状のない状態を維持していることから,DLBが背景にある可能性は低いと考えられた.
本例の認知・精神症状はステロイドに良好に反応した一方,夜間の寝言は長期残存していた.また治療後半年の再検査では,vPSGでの%RWA,血清抗VGKC抗体価の低下は軽度にとどまっていた.この点に関し,本抗体関連辺縁系脳炎はくすぶり型脳炎の経過を呈しうることが知られている11).本例も脳炎の活動性そのものは完全に沈静化していない可能性があり,慎重に経過観察を続けている.
RBDと変動する認知・精神症状からDLBが疑われるが,症状や経過が典型的でない症例では,抗VGKC複合体/LGI1抗体関連辺縁系脳炎の可能性も念頭におく必要がある.
謝辞:本症例の報告にあたり,血清抗NMDA受容体抗体を測定いただいた新潟大学脳研究所の田中惠子先生,髄液オレキシン濃度を測定いただいた秋田大学精神科学教室(現 筑波大学国際統合睡眠医科学研究機構)の神林崇先生に深謝いたします.
※著者全員に本論文に関連し,開示すべきCOI状態にある企業,組織,団体はいずれも有りません.