2017 Volume 34 Issue 2 Pages 118-122
2017 Volume 34 Issue 2 Pages 118-122
気管や輪状軟骨に悪性腫瘍や狭窄性疾患を生じると,病変の切除後に気道を再建する必要がある。既存の気道再建外科として,気管端々吻合,自己組織の移植などがあるが,術後管理や合併症,複数部位や複数回の手術侵襲,移植片の移動や吸収などの課題がある。
1990年代になって組織工学が登場し,臓器再生の三要素は足場,細胞,調節因子とされる。著者らはコラーゲンを足場としポリプロピレンで補強した生体内組織再生誘導型の人工気管の有効性,安全性を検証した上で,輪状軟骨と頸部気管の部分欠損の再建に臨床応用し,現在は実用化のための医師主導治験を実施している。選択基準は既存治療で気管孔を閉鎖できない患者と,悪性腫瘍などで気管切除(気管軟骨の1/2以上かつ3輪以上)が予想される患者である。
人工気管は非吸収性材料を使用しているため小児に適応がない。将来的には吸収性材料からなる新規人工気管や軟骨の再生医療技術の開発が望まれる。
気管や輪状軟骨に悪性腫瘍や狭窄性疾患を生じると気管や輪状軟骨の欠損や変形や狭窄を来し,病変の切除後に気道を再建する必要がある[1]。気道の再建には,管腔を保持する硬度を持つ枠組みと内腔面に線毛を持つ粘膜を同時に再建することが理想的である。とくに,進行甲状腺癌の気管浸潤例では十分な安全域をとった治癒切除が望まれるが,大きく切除すれば再建は難しくなる。この課題を解決するため,著者らは生体内組織再生誘導型人工気管の有効性,安全性を検証した上で,現在は実用化のための医師主導治験を実施している。
本稿では,気道再建外科の現状と再生医学研究の進歩について述べ,生体内組織再生誘導型の人工気管について解説する。
従来から行われている気道再建外科を表1にまとめる。1970年代からGrilloのグループが気管端々吻合術を報告してきたが[2],広範囲切除の限界,縫合不全や縦隔炎などの重篤な合併症,患者に苦しい頸部前屈姿勢など,容易な手術ではない。1980年代からCottonらにより移植を伴う再建術が報告されており[3],硬性再建には骨,軟骨が用いられ,内腔面には皮膚や粘膜が用いられるが,自家遊離移植では耳介軟骨,肋軟骨などの採取や頸部に留まらず胸部の有茎皮弁や遊離前腕皮弁を使って被覆するなど,複数部位や複数回にわたる手術侵襲が必要である。さらに,移植片の移動や吸収の問題があり気道の枠組みとしての長期的安定性を保持するのが難しい。人工材料にはシリコン,チタンなどの材料が用いられてきたが安定した成績をあげていない[4]。

既存の気道再建外科治療と問題点
1993年,LangerとVacantiは体外で細胞を培養して工学的手法により臓器や組織に近いものを再生させるtissue engineeringという概念を提唱したが[5],体外で作られた組織が体内への移植後に吸収されるなどの問題があり,臨床応用へのハードルは高い。一方,生体内で組織の再生を誘導する手法はin situ tissue engineeringと言われる。1995年以降,中村らは場の理論に基づいたコンセプトで,コラーゲンスポンジを主体とした足場を移植し,気管[6],食道,胃,小腸,末梢神経などの組織再生を報告した。
臓器が再生するには,①足場(scaffold),②細胞(cell),③調節因子(regulatory factor)の三要素が必要で,そこに血流が入って臓器が再生する。
足場としては,無機材料にハイドロキシアパタイト,リン酸三カルシウムなどがあり,骨,歯,軟骨の再生に用いられ,高分子材料のうち天然高分子としてコラーゲン,ゼラチン,ヒアルロン酸があり,合成高分子としてポリ乳酸(PLA),ポリL乳酸(PLLA),ポリグリコール酸(PGA)があり,骨,歯,軟骨,皮膚,血管,神経,筋,頸部気管・輪状軟骨の再生に用いられている。
細胞としては,多分化能と自己複製能を有しているものを幹細胞といい胚性幹細胞(ES細胞)と体性幹細胞がある。ES細胞は,受精卵が分裂して形成された胚盤胞のなかに存在する内部細胞塊から得られる細胞で,全ての組織に分化することができる。人工多能性幹細胞(iPS細胞)は,マウス線維芽細胞にレトロウイルスベクターとしてOct 3/4,Sox2,Klf4,cMycを導入して作製された[7]。iPS細胞から気管軟骨などへの分化が実験レベルで報告され,ヒトでは網膜色素上皮細胞へ分化させて移植した症例が報告されている。
体性幹細胞には,骨随由来間葉系幹細胞,造血幹細胞,血管内皮前駆細胞,角膜上皮幹細胞,神経幹細胞,脂肪組織由来幹細胞,精子幹細胞,色素幹細胞,心臓組織幹細胞などがある。
調節因子としては,成長因子やサイトカインがあり細胞の増殖や分化を促進あるいは抑制している。線維芽細胞増殖因子(bFGF),肝細胞増殖因子(HGF),骨形成因子(BMP),インスリン様増殖因子(IGF1)などがある。これらの調節因子を徐々に放出させて効果を持続する方法にDrug Delivery System(DDS)があり,生体吸収性ハイドロゲルなどが用いられている。
再生医療における臨床到達分野はまだ少ない(表2)。頭頸部領域では,上顎骨,下顎骨,鼻中隔軟骨,輪状軟骨・頸部気管,顔面神経,中耳粘膜,鼓膜などがあげられる。わが国で薬事承認された再生医療など製品には,ヒト軟骨由来組織による関節軟骨治療,ヒト表皮由来細胞シートによる皮膚欠損治療,ヒト骨格筋由来細胞シートによる重症心不全の治療,ヒト間葉系幹細胞による造血幹細胞移植後の急性移植片対宿主病治療がある。

再生医療における主な臨床到達分野
生体内組織再生誘導型の人工気管(図1)[6]は,気道としての管状の枠組みを保持するため,ポリプロピレン製メッシュを管状にし,同素材のリングで補強した。ポリプロピレン製メッシュは特定保険材料として従来から胸壁や腹壁の補強に臨床に使われている非吸収性材料である。ポリプロピレン管の表面に,組織再生の足場としてコラーゲンスポンジをグラフト化,重層コーティングして厚く付着させた。コラーゲンスポンジは医療用のブタ皮膚由来のⅠ型,Ⅲ型コラーゲンを用いた。コラーゲンスポンジは2~3カ月で吸収される。

人工気管
a:骨格,b:骨格のシェーマ,c:外観,d:外観のシェーマ。
頸部気管については,イヌの頸部気管を切除した後に人工気管を移植し,最長5年の観察で,気管の上皮再生は良好であった。組織学的評価では,炎症所見を認めず,内腔面は再生線毛上皮で覆われていた。再生気管の強度は機械的圧縮試験で正常気管と同程度であった。正常気管との接合部も安定した組織移行がみられ,長期に安全に使用できることがわかった[6,8]。輪状軟骨については,輪状軟骨の前半分を切除した後に人工気管をトリミングして移植し,最長1年の観察で,一部メッシュが露出したが上皮再生は良好で問題なく経過した[9]。
大型動物への移植実験で最長5年の経過観察で良好な内腔上皮再生が得られ安全性が確認されたことから,京都大学および福島県立医科大学の設内倫理委員会の承認の上,2002年より,生体内組織再生誘導型の人工気管を用いた気道再建手術を実施してきた。現在まで経験した成人12例において最長12年の経過観察で気道としての役割を果たし患者のQOL向上に寄与している[10~12]。人工気管はトリミングが容易で,欠損部に適した気道再建手術を安定して実施できるとともに,他の部位からの組織採取が不要で手術侵襲を軽減させる。
これまでの臨床使用を経験した12例のうち,甲状腺悪性腫瘍に対する症例としては,甲状腺癌の気管浸潤例に対する気管病変切除後の即時再建3例,甲状腺悪性腫瘍による気管切除後の気管欠損1例を合わせて4例で,人工気管による再建手術後の観察期間は3年5カ月~12年であった。人工気管は気管壁として機能し枠組みは保たれていた。内腔面の上皮化については,術後2カ月でおおむね上皮化し,3カ月するとほぼ全域で上皮化していた。First in humanの例について図2,図3に示す。
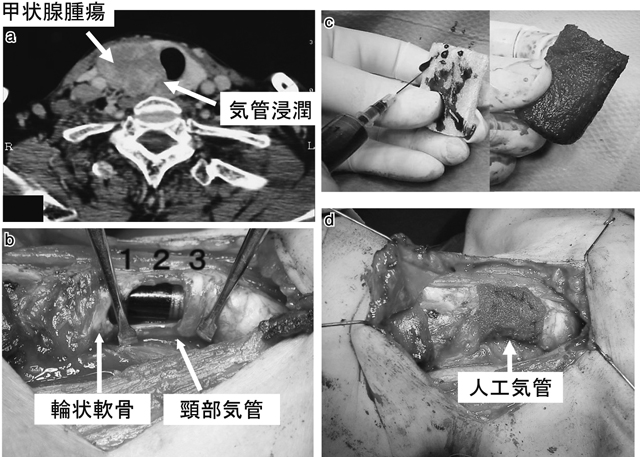
人工気管を用いた再建手術(甲状腺癌例)
a:CT所見
甲状腺右葉の腫瘍が頸部気管に浸潤している。
b:術中所見
輪状軟骨の一部,頸部第1,2,3気管の半周分を切除した。
c:移植サイズにトリミングした人工気管
人工気管の半周分をトリミングし血液を浸潤させる。
d:術中所見
人工気管で欠損部を再建した。
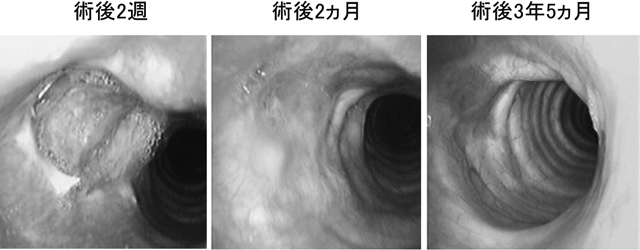
気管内視鏡所見
生体内組織再生誘導型の人工気管は,動物実験で最長5年の観察,その後の少数の臨床例における最長12年の観察で,頸部気管と輪状軟骨の部分欠損の再建については安全性,有効性は確認されている。製造方法は完成しており,足場のみを用いるため細胞移植に比べると製造管理や品質管理などのハードルは低い。人工気管が一般医療として広く用いられることが期待されており,医療機器としての実用化に向けて,QMS準拠の生産ライン構築,GLP準拠での生物学的安全性試験を実施し,PMDAで対面助言を受けた上で,GCP準拠で医師主導治験を開始した。選択基準は既存治療で気管孔を閉鎖できない患者と,悪性腫瘍などで気管切除(気管軟骨の1/2以上かつ3輪以上)が予想される患者である。
生体内組織再生誘導型の人工気管を輪状軟骨と頸部気管の部分欠損の再建に臨床応用し有用性を示してきた。現在は一般臨床での実用化を目指した医師主導治験を実施している。次の課題として,イヌを用いた実験では全周性の気管欠損にも使用が可能であり,また胸部気管でも再建が可能であることから,今後はこの領域への臨床使用も視野に入れて前臨床試験が行われるものと思われる。また,ポリプロピレンは非吸収性のため小児には適応がないのが現状であり,将来的には小児例へ適用可能な吸収性材料からなる新規人工気管や軟骨の再生医療技術の開発が望まれる。