2019 年 18 巻 1 号 p. 1-8
2019 年 18 巻 1 号 p. 1-8
金属表面に担持した酸化物超薄膜は特異的な触媒活性を示すことがある.我々はこのような酸化物/金属接合系の自動車排ガス浄化触媒としての可能性に着目し,NO-CO反応素過程を平面波基底密度汎関数計算により検討してきた.ここではTiO2/AgとZrO2/Cuの二つの格子整合系に関する計算結果を紹介する.いずれの系でも,金属からNOへの電子供与により,NOがカチオンサイト上で吸着活性化され,二量化してONNOとなる.ONNOはN2OとOに分解し,さらにN2OがN2とOに分解する.表面に残ったOはCOと反応してCO2を生成し,触媒サイクルが完結する.活性化障壁や吸着エネルギーの計算値から,TiO2/AgよりもZrO2/Cuが触媒として優れていると予想される.物質間の差を生じる要因として,カチオン正電荷やカチオン間距離の差が挙げられる.
今日の自動車社会において,自動車排ガス浄化触媒は大気汚染防止のため非常に大きな役割を果たしている [1].ガソリンエンジンの場合,排気ガスにはNO,CO,未燃焼炭化水素などの汚染物質が含まれており,これらを反応させてN2,CO2,H2Oに転化無害化するために,いわゆる三元触媒が用いられている.一般に三元触媒は,アルミナなどの金属酸化物粒子にプラチナ,パラジウム,ロジウムなどを分散担持したものであるが,これら白金族元素は高価で希少であり,また産出地が限られるので,供給リスクにさらされる.元素戦略的見地からは,これら希少金属を安価で豊富な金属により置き換えることが望ましい.文部科学省触媒・電池元素戦略プロジェクトにおいても,自動車触媒の汎用金属による代替が重要な研究目標となっている.
しかし銅やニッケルなどの汎用金属は,白金族元素と比べると反応性が高いので,腐食や被毒による劣化が懸念される.対策として,あらかじめ表面を薄い金属酸化物層で覆ってコアシェル化し,反応性を制御する方法が考えられる.このような触媒の候補となる物質の組み合わせを決めるためには,まず金属酸化物/金属接合モデル(Figure 1)に対する表面科学的実験や密度汎関数(DFT)計算により,活性を評価するのが効率的である.本稿では,酸化物/金属接合のCO酸化触媒活性を示した先行研究について触れた後,NO-CO反応に関する我々の理論研究を紹介し,浄化触媒としての可能性を議論する.

Schematic representation of a core-shell catalyst and an oxide/metal model system.
表面科学分野では,金属基板表面に酸化物層を堆積したものが酸化物表面のモデル系として以前から用いられてきた [2].興味深いことに,酸化物層が数原子層程度になると,基板金属から表面吸着種へ酸化物層を通した電子供与が可能になり,特異的な活性が発現することがある [3].例えば,Pt(111)基板表面をFeO単原子層で覆ったFeO/Pt接合系では,PtがCOで被毒するような低温においても, CO酸化反応が進行する [4].この触媒活性は,実験とDFT計算に基づいて次のように説明されている [5].まず,FeOに吸着したO2分子が,Pt基板からの電子供与により活性化し,FeO層を酸化してFeO2にする.FeO2のOは弱く結合しているので,COと反応してCO2を生じる(易還元性).最後に,ここで生じた酸素欠陥がガス中の酸素により修復されて,Mars-van Krevelen (MvK)型の触媒サイクルが完結する.しかし実験によると,この系のNO-CO反応活性は高くない [6].NOが酸素欠陥をブロックし,しかもこの状態のNOがCOにより還元されにくいことが原因とされている.易還元性は酸化物超薄膜の活性発現の一因であるが,NO-CO反応においては必ずしも有利に働かないようである.
一方,DFT計算によると, MgOのような還元不可能な酸化物でも金属との接合によりCO酸化触媒活性を示す可能性がある [7].MgO/Agの場合,銀基板からの電子供与によりO2がカチオンサイト上で吸着活性化し,そのままCOと反応すると予想されている.このようなO2活性化については,MgO/Moにおけるスーパーオキシド生成がEPR測定により確認されている [8].また我々のDFT計算も,TiO2/AuやTiO2/Agで同様のCO酸化活性が発現することを示唆している [9].
これら先行研究を踏まえて,我々はTiO2/AgとZrO2/Cu接合系に注目し,NO-CO反応をDFT計算により検討してきた [10,11].ZrO2は還元性がなく,TiO2は易還元性であるがFeO2に比べると安定である.また,TiO2のTiやZrO2のZrはMgOのMgと異なり,NOのπ*軌道と相互作用するd軌道を持っているので,NO活性化が期待できる.銀と銅を選んだのは,これらが白金族に比べると安価であり,それぞれTiO2,ZrO2との間に格子整合の良い方位関係が存在するからである.以下,これら二つの系の計算結果を紹介し,反応経路や活性の相違について議論する.
3.1 計算方法ここで紹介する計算には,平面波基底DFT計算プログラムVASPを用いた(入手法についてはhttps://www.vasp.at参照) [12,13,14,15].平面波展開のカットオフエネルギー400 eV,GGA-PBE型交換相関汎関数 [16]を用い,スピン偏極を考慮した計算を行った.価電子とイオンコア(C4+, N5+, O6+, Ti10+, Cu11+, Zr12+, Ag11+)の相互作用はprojector-augmented wave (PAW)法 [17,18]により取り扱った.オンサイトクーロン相互作用補正(DFT+U)にはDudarevの方法 [19]を用いた.DFT計算後のBader電荷解析には,Henkelmannグループのbaderを用いた [20].これはhttp://theory.cm.utexas.edu/henkelmanよりダウンロードできる.
安定構造は主にconjugate gradient (CG)法により最適化し,遷移状態はdirect inversion in the iterative subspace (DIIS)法により最適化した.DIIS法により収束しない場合は,ダイマー法 [21,22]を用いた.求めた遷移状態が一階の按点であることは振動解析により確認した.また,遷移状態から微小変位させた位置から構造緩和し,始状態と終状態にたどり着くことを確認した.
計算に用いた周期スラブ模型をFigure 2に示す.TiO2/Agとして,ルチル構造TiO2(110)二層をAg(112)二層にTiO2[001] // Ag[110]の方位で担持したモデルを用いた.金属の格子間隔dmetal,酸化物の格子間隔doxideのとき,格子不整合を
| (1) |

Oxide/metal slab models.
表面Sへの分子Xの吸着エネルギーEadは,吸着状態X/SのエネルギーをEX/S,表面SのエネルギーをES,孤立分子XのエネルギーをEXとして,
| (2) |
今回考慮した系では金属酸化物のd軌道がNO吸着に関与するので,結果のU依存性を検討する必要がある.TiO2/AgでのNO吸着エネルギーは,補正なしで−0.82 eV,U = 2 eVで−0.87 eVとなった.ZrO2/Cuでは,補正なしで−1.41 eV,U = 2 eVで−1.46 eVとなった.いずれも大きな差ではないが,TiO2/AgについてはTiサイトに余剰電子が局在するように,U = 2 eVの補正を適用した.ZrO2/Cuについては補正なしの結果を示す.
3.4節でNO二量化反応の計算結果を示すが,その始状態として,二つの吸着NO分子のスピンが反平行になる開殻一重項状態を用いた.高スピン状態からのスピン混入が懸念されるが,表面系における混入誤差はこれまでほとんど議論されることがなかった.我々はスピン近似射影法に基づく平面波DFT計算用混入誤差評価スキームを提案している [23].これによりNO二量化反応障壁を補正したところ,TiO2/Agでは0.03 eVの増加,ZrO2/Cuでは0.04 eVの低下となり [24],本稿の結論に影響するほどの差ではないことが確かめられた.
3.2 酸化物/金属接合の電子状態Figure 3にTiO2/AgとZrO2/Cuの部分状態密度(PDOS)を示す(1×1セルで計算).いずれも価電子帯はO2pバンド,伝導帯はカチオンdバンド(Ti3dとZr4d)となっている.銀のdバンドは価電子帯と重なり,銅のdバンドは価電子帯上部からエネルギーギャップ中に位置するが,フェルミレベル付近ではどちらもsバンドになっている.フェルミレベルは伝導帯の下端にかかっており,金属から酸化物への電子供与を示唆している.Bader解析によっても,AgからTiO2へ0.15電子,CuからZrO2へ0.12電子の供与が認められた(酸化物表面の単位胞あたり).界面の酸化物側の酸素アニオンにより,金属層に残った正電荷が安定化されることが,電子供与促進の要因として挙げられる.

Projected density of states (PDOS) for TiO2/Ag (top) and ZrO2/Cu (bottom) [10,11]. Reproduced with permission from the Chemical Society of Japan and Springer.
NO分子の吸着構造として,N端吸着(NO),O端吸着(NO),サイドオン吸着(NO)など検討したところ,TiO2/AgとZrO2/Cuのいずれにおいても,カチオンサイトにN端から吸着した構造(Figure 4)が最安定となった(以下,分子側の吸着位置を下線で示す).図中に示すように,NO分子の負電荷と吸着サイトの正電荷は,TiO2/AgよりZrO2/Cuで大きく,これに対応してNO吸着も強くなっている.このように,金属から酸化物層経由で電子を受容してアニオン化したNOが,カチオンサイト上で安定化される.これに対して酸化物層単独の場合,NOの吸着エネルギーはTiO2上で-0.22 eV,ZrO2上で-0.26 eVでしかない.金属酸化物の価電子帯から電子を取り出すのはエネルギー的に不利だからである.

NO adsorption on (a) TiO2/Ag and (b) ZrO2/Cu. Energies are referenced to gaseous NO (N–O: 117 pm and 1923 cm–1).
Figure 4に示すように,電子受容に伴いNO結合が伸長し,N-O伸縮の振動数が低下する.PDOS解析 [10,11]はカチオンd軌道とNO π*軌道の相互作用を示している.相互作用により安定化したπ*軌道に電子が流れ込み,N-O結合が軟化したと考えられる.
TiO2/Agにおいてルチル(110)層を二層から四層に増加すると,NOの吸着が若干弱くなり,吸着エネルギーは-0.78 eVとなる.よって,酸化物層の層厚制御が活性発現の鍵になると考えられる.一方,酸化物層が厚い場合でも,プラズモン共鳴吸収により金属から酸化物伝導帯への電子移動が引き起こされる可能性がある.Ag@TiO2コアシェル粒子の光触媒活性 [25]との関連で興味深い.
3.4 NO-NO二分子反応COによるNO還元反応の初めの素過程として,NO一分子解離,NO-CO二分子反応,NO-NO二分子反応などが考えられる.しかしTiO2/AgやZrO2/Cuの場合,NOの解離吸着状態は脱離状態に比べてそれぞれ1.81 eV, 0.74 eV不安定となった.NO-CO二分子反応によるNOCO中間体生成も,それぞれ1.35 eV, 1.31 eV不利となった.これら経路の反応活性への寄与はあまり見込めないので,NO-NO二分子反応を検討した.
Figure 5にNO-NO反応のエネルギープロファイル及び中間体構造を示す.この反応は三つのステップからなる.まず,電子供与を受けてN端の正電荷が弱まったNO二分子がN-N結合して,二量体ONNOを形成する.これに伴い,N位とカチオンサイトの結合が伸長して切断しやすくなる.二本の結合のどちらかが切断されると,ONNOが回転してONNOに変化する.今度はカチオンサイトに接したN-O結合が伸長するので,容易に切断してN2Oを生じ,表面にはOが残る.NO-NO反応全体での障壁はTiO2/Agで0.29 eV,ZrO2/Cuで0.39 eVとなり,どちらの系でも容易な反応である.
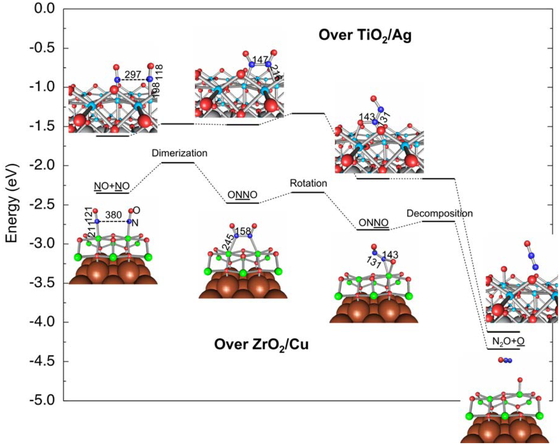
NO + NO → N2O + O reaction over TiO2/Ag and ZrO2/Cu. Energies are referenced to gaseous 2NO. Distance in (pm).
二つの接合系におけるNO-NO反応を比較すると,細部において相違点が認められる.第一に,TiO2/AgよりもZrO2/CuがNOにより多く電子を供与するので,始状態におけるN端の電荷がTiO2/Ag上で+0.11 eであるのに対し,ZrO2/Cu上では-0.07 eとなっている.ただし,大きさとしてはどちらも中性に近く,二量化の反応障壁も同程度となる.第二に,TiO2/Ag上ではONNOのNとOが隣り合うTiサイトに吸着しているのに対し,ZrO2/Cuでは同じZrサイトに吸着している.これは,カチオン間隔がTiO2では300 pmであるのに対し,ZrO2では364 pmと大きいことと対応している.しかしながら,どちらもONNO部分の構造は類似しており,回転ステップの反応障壁も同程度である.このように,二つの接合系は細部において差があるものの,構造や電子供与性の差を吸収する要因が働くため,同じようなNO-NO反応が可能となる.この柔軟性は,接合系の金属や金属酸化物を他の物質に置き換える余地があることを示唆しており興味深い.
3.5 N2O分解前節のNO-NO反応ではN2Oが生成する.N2Oは温暖化係数265の温室効果ガス [26]なので,除去するのが望ましい.TiO2/Ag及びZrO2/Cu上でのN2O分解反応の遷移状態をFigure 6に示す.どちらの系でも,N2Oは両端で二つのカチオンサイトと相互作用して折れ曲り,N2とOに分解する.N2は容易に脱離するが,Oはカチオンサイトに吸着したまま表面に残る.TiO2/Agでの反応障壁は0.51 eVであるが, N2O吸着が弱く(−0.14 eV),高い分解活性は期待できない.ZrO2/CuでもN2O吸着はそれほど強くない(−0.24 eV)が,障壁が0.06 eVと小さいので,分解活性が期待できる.

Transition states of N2O decomposition over (a) TiO2/Ag and (b) ZrO2/Cu.
NO-NO反応及びN2O分解反応により表面に残された酸素原子は,TiO2/AgのTiサイトに-2.17 eV,ZrO2/CuのZrサイトに-2.52 eVで強く吸着している(O2分子のエネルギーの半分を基準とする).この酸素原子は接合系から電子を受容して,それぞれ-0.79 e, −1.01 eの負電荷を帯びてカチオンサイトに吸着している.これからわかるように,接合系の酸素を引きつける力,つまり還元力がこれらNOx還元反応の駆動力となっている.よって触媒サイクルを完結させるためには,CO等の還元剤により接合系を還元しなければならない.この意味で,TiO2/AgやZrO2/Cuはredox触媒である.
COによる接合系の還元反応,即ちCO酸化反応O + CO → CO2の遷移状態をFigure 7に示す.反応障壁はTiO2/Ag上で0.51 eV,ZrO2/Cu上で0.36 eVとなった.また,CO吸着はTiO2/Agで-0.36 eVに対し,ZrO2/Cuで-0.47 eVとなる.よってこの反応についても,ZrO2/Cuの方が活性が高いと予想される.反応障壁が低いのは,COの非共有電子対がカチオンサイトにより反対側に引き離されて,Oとの反発が軽減されるからである(原論文 [11]のFigure 6d参照).

Transition states of O + CO reaction over (a) TiO2/Ag and (b) ZrO2/Cu. Distance in (pm).
本稿では,二つの酸化物/金属接合系(TiO2/AgとZrO2/Cu)のNO-CO反応に対する触媒活性を平面波基底DFT計算により検討した研究 [10,11]を紹介した.NOやOは,金属層からの電子供与を受けてアニオン化し,酸化物表面のカチオンサイトに強く吸着する.そのため,NO + NO → ONNO → N2O + O, N2O → N2 + O反応により,接合系にOを渡す形でNOxが還元される.ここで酸化された接合系は,O + CO → CO2反応により還元され,NO-CO redoxサイクルが完結する.TiO2/AgではN2O分解やCO酸化がやや律速になるのに対し,ZrO2/Cuは還元力が高いにもかかわらずCO酸化反応障壁が低いので,NO-CO反応触媒として優れていると予想される.物質間の差を生じさせる要因として,カチオンサイト正電荷の差や,カチオン間距離の差が挙げられる.
本稿でみたような電子供与作用は,他の酸化物/金属接合系でも重要な役割を果たす.我々はAu@NiOコアシェル型触媒 [27]によるメタクリル酸メチル合成反応のメカニズムを明らかにするため,NiO/Au接合に対するDFT計算を行っている [28].この系では,接合界面のO-Au結合に反結合性があるため,界面から電子を取り出しやすくなっている.そのため,O2吸着やNiサイト欠損などのNiO酸化状態が安定化される.Ni欠損サイトに隣接する表面格子酸素は塩基点となり,触媒反応に関与する.
金属酸化物を経由した電子供与は,通常の担持触媒でも重要になることがある.TiO2に担持した金ナノ粒子のCO酸化触媒活性に関するDFT計算によると,O2は金からの電子供与を受けてアニオン化し,Tiサイトに吸着して,COと反応する [29,30].この場合,O2は金に直接吸着している必要はない.我々のDFT計算によると,金から1.6 nm離れたTiサイトでもO2は吸着活性化する [31].ただし,金に吸着したCOの方がTiサイトに吸着したO2との反応性が高いので,CO酸化反応は主に接合界面直近で起きる.
本稿で見たように,金属表面に担持した酸化物超薄膜は優れた触媒活性を発揮する可能性を持っている.このような新規触媒を開拓する上で,比較的低コストで一定の精度を与え,電子的機構について有用な知見を与えることができる平面波基底DFT計算は,今後とも重要な役割を果たすと考えられる.
本研究は,文部科学省触媒・電池元素戦略プロジェクトにおいて行われた.計算の一部には,京都大学情報環境機構及び九州大学情報基盤研究開発センターのスーパーコンピューターを用いた.TiO2/AgとZrO2/CuのDFT計算は古賀,NiO/AuのDFT計算は林,スピン混入誤差評価は多田が主に担当した.