2013 Volume 99 Issue 11 Pages 651-658
2013 Volume 99 Issue 11 Pages 651-658
Electrochemical hydrogen permeation tests of pure Fe sheets rusted by cyclic corrosion test (CCT) and atmospheric exposure were carried out under controlled temperature and humidity to investigate the influence of atmospheric corrosion on the hydrogen entry behavior. The hydrogen entry into the Fe specimens rusted by CCT increased under wet condition, and the hydrogen entry was increased with the CCT cycle number. During drying process after the wetting, hydrogen entry was further enhanced and a peak of hydrogen current was observed. The peak hydrogen permeation current tended to increase with the growth of rust layer, and the peak value of the hydrogen permeation current became remarkably higher than that at the highest humidity when the rust layer was relatively thick. Similar enhancement of hydrogen entry into an outdoor-exposed specimen was also observed during drying. Drying process after CCT resulted in an increase in hydrogen content of 5 mm-thick steel specimens measured by means of thermal desorption analysis, indicating the enhancement of hydrogen entry during drying process and showing a good agreement with the electrochemical hydrogen permeation test results. It is required to take into consideration the enhanced hydrogen entry to estimate concentration of hydrogen from the environment.
高強度鋼の遅れ破壊特性の研究は,高強度鋼の安心・安全な使用や,更に強度レベルの高い鋼の開発にとって重要である。遅れ破壊限界拡散性水素量(HC)は遅れ破壊感受性評価のための1つの重要なパラメータとして考えられており1,2,3),水素をチャージした試験片の定荷重試験1,2,3,4),低ひずみ速度引張試験(SSRT)5,6,7,8,9),あるいは通常の引張試験(conventional strain rate test(CSRT)10,11,12,13,14))と,昇温脱離法(TDA)による水素量測定とを組み合わせてHCや破断応力と拡散性水素量の関係が求められている。
その一方で,HCと比較されるべき環境から侵入する水素量(HE)の把握も遅れ破壊感受性評価にとって重要であり,例えば建築に用いられる高強度鋼の場合,大気腐食による水素侵入の理解が必要である。筆者らはこれまでに,大気腐食させた後の環状切欠き付き丸棒試験片を用いてSSRTを行い,HEの影響を直接反映させた遅れ破壊特性評価を行った15,16,17,18)。表面に生成した錆層の影響を反映した腐食とそれによる水素侵入を再現するため19),SSRTの間は試験片表面を湿潤環境に保った14,15,16)。温湿度などの環境因子が経時変化する実環境においては水素濃度も経時変化すると考えられる20)。そこで,室外で大気暴露した試験片を用いて同様のSSRTを行う場合には,大気暴露環境での比較的活性な腐食とそれによる水素侵入を再現するとともに,試験片内の水素濃度を均一化することを目的とし19),SSRTに先立って試験片を湿潤環境に1日保持した15,16)。これらの腐食した試験片を用いたSSRTの場合,水素侵入は湿潤環境で促進されているものと仮定しているが,実際の水素侵入は錆層の構造や取り込まれた汚染物質,温湿度等の環境因子の影響を受け複雑であると考えられ21,22),定量的なHEの把握のためには,より詳細な検討が必要である。
電気化学的水素透過試験23,24)は水素侵入の経時変化をモニターするのに有効な方法であり,大気腐食環境下での水素侵入挙動の研究に用いられている15,21,22,25,26,27,28)。著者らの研究でもこの方法を用い,大気腐食によって生成した錆層が水素侵入を促進することを報告している15,28)。本研究では,さらに詳細に錆層と湿度が水素侵入に及ぼす影響を明らかにするために,サイクル腐食試験(CCT)および大気暴露に供したFe板試料を用い,温湿度制御下での電気化学的水素透過試験を行った。さらに,水素侵入に及ぼす腐食速度の効果を検討するため,同条件のCCTに供した大気腐食モニタリング(ACM:Atmospheric corrosion monitoring)センサーを用いた湿度による腐食速度変化の検討も行った。加えて,電気化学的水素透過試験により求めた水素透過電流から推定される水素濃度の定量性を検討するために,昇温脱離法により分析した水素濃度との比較を行った。
購入ままの市販の純Feシート(The Nilaco Corporation, 99.5%)をCCTの後の温湿度制御下の電気化学的水素透過試験に用いた。初期の厚さは0.5mmで水素透過試験に用いた実効面積は20cm2である。シートの両面を#800のSiC研磨紙で研磨した後,片面(水素引き抜き側)にNiめっきを施した。Niめっきはワット浴(NiSO4・6H2O 250g/l, NiCl2・6H2O 45g/l, H3BO3 40g/l)中60ºC,3mA/cm2で180s行った22)。計算上のめっき厚は約180nm28)である。Niめっき面と反対の水素侵入面を後に述べるCCT条件で腐食した後,恒温恒湿槽中の温湿度制御下で電気化学的水素透過試験を行った。
沖縄の屋外で暴露したFeシート試料およびつくばの屋外で暴露したSCM435H鋼の試料14)も用いた。SCM435H鋼の化学組成はTable 1に示す。
| Steel | C | Si | Mn | P | S | Cu | Ni | Cr | Mo | B |
|---|---|---|---|---|---|---|---|---|---|---|
| SCM435H | 0.37 | 0.14 | 0.77 | 0.02 | 0.015 | − | − | 1.06 | 0.14 | − |
| Boron-bearing steel | 0.20 | 0.08 | 0.97 | 0.011 | 0.015 | 0.01 | 0.02 | 0.15 | Tr* | 0.0011 |
*Tr: Trace amount
丸棒を輪切りにしたディスク状のボロン鋼を腐食後の昇温脱離分析(TDA)による水素量測定に用いた。ディスク状試料の直径は20mmで厚さは5mmである。ボロン鋼試料の化学組成はTable 1に示した。ボロン鋼の焼入れ焼戻し熱処理条件はそれぞれ,880°C,60min,水,および290°C,90min,水で,熱処理後の引張強度は1340MPaであった。
2・2 サイクル腐食試験(CCT)と大気暴露試験純Feシート試料は電気化学透過試験前にCCTによって腐食させた。CCTの間,水素引き抜き側のNiめっき面は腐食を防止するためマスキングした。CCTの1サイクルは乾燥(50%RH, 5.75h),湿潤(98%RH, 1.75h)および塩水噴霧(0.5%NaCl 水溶液,0.5h)のステージからなる。CCT全行程で温度は30°Cに保った。CCT後,腐食したFeシート試料は温湿度制御下での電気化学的水素透過試験に供した。腐食試料の表面は走査電子顕微鏡(SEM)で観察した。
実環境で生成した錆層の水素侵入に及ぼす影響を検討するため,Feシート試料を2ヶ月間琉球大学の構内(北緯26.248,東経127.765)にて暴露した。環境は亜熱帯かつ海浜で,環境の腐食性は比較的厳しい。腐食環境としては比較的穏やかな,つくばの物質・材料研究機構構内(北緯36.075,東経140.122)で2年間暴露したSCM435H鋼試料も同様に水素透過試験に用いた。
2・3 電気化学的水素透過試験CCTおよび屋外での大気暴露によって腐食させたシート試料を用いて電気化学的水素透過試験を行った。試験の模式図をFig.1に示す。片面が腐食した試料を改造型のDevanathanセルに固定した。水素引き抜き側のNiめっき面はセル内の1M NaOH水溶液に向け,セル内にはHg/HgO参照電極およびPt対極を設置した。セルは恒温恒湿槽中に入れ,試料および各電極は恒温恒湿槽のポートを通じて外部に置いたポテンショスタットと接続した。

Schematic drawing of electrochemical hydrogen permeation test carried out under controlled temperature and relative humidity.
水素引き抜き側は+0.1V(Hg/HgO)で分極し,水素透過電流を5秒毎にデータロガーで記録した。透過試験に先んじて,Niめっき面は同条件で24時間以上分極し,水素透過電流に対してバックグラウンドとなる不働態保持電流密度を0.1µA/cm2以下となるようにした22)。恒温恒湿槽内の温度は30°Cに保ち,相対湿度を段階的に50, 70, 80, 98%RHの順で増加させた。50-70%RHのそれぞれの湿度には約2時間保った。98%RHまで上昇させた後,その湿度で10h保持し,その後相対湿度を段階的に低下させた。
2・4 大気腐食モニタリング(ACM)センサーFig.2に示すFe基盤とAg電導ペーストからなるACMセンサー29)を用いて腐食挙動をモニターした。ACMセンサーは30サイクルのCCT(CCT条件は前述のとおり)により腐食させ,これを恒温恒湿槽内に設置し,Fe部とAg部の間に流れるACM電流の相対湿度による変化を電流計で測定し,10min毎にデータロガーで記録した。相対湿度の変化は電気化学的水素透過試験の場合と同様で,槽内の温度は30°Cに保った。

Schematic drawing of an ACM sensor30).
CCTによって腐食させた試料の水素量はTDAにより求めた。ハンドリング中の水素の逃散の影響を減らすため,5mmの厚さのボロン鋼試料(直径20mm)を用いた。150サイクル目のCCTの,乾燥(50%RH),湿潤(98%RH)および塩水噴霧(0.5%NaCl aqueous solution)の各ステージ終了後に試料を取り出し,試料内の水素量を分析,比較した。また,150サイクル目の各ステージの条件を24時間継続した後の水素分析も行い,各ステージの腐食条件の水素侵入に及ぼす影響を調べた。
水素のTDAはプログラム昇温炉と四重極質量分析形計を用いた昇温脱離分析装置(アールデック社製)によって行った。昇温速度は100°C/hとした。水素昇温脱離曲線は室温から800°Cの範囲で求め,約300°Cまでに放出される水素を,室温で拡散する拡散性水素と見なした30)。TDA前にはサンドブラストにより錆層の除去を行った。
CCTに供したFeシート表面の例として,30サイクルのCCT後の試料表面のSEM像をFig.3に示す。本研究で用いた比較的厳しいCCTの腐食条件では,30サイクルまでにはほぼ試料全面が錆に覆われた。

60サイクルのCCTで腐食した純Fe試料の湿度変化に伴う水素透過電流密度の変化をFig.4に示す。恒温恒湿槽内の実測の湿度も図中に示した。初期に50%RHまで湿度を上げた際に水素透過電流密度が上がったのを除くと,80%RHの相対湿度まで水素透過電流密度に大きな変化はなかった。しかし,98%RHに相対湿度を上げると水素透過電流は顕著な上昇を見せた。この水素透過電流密度の増加は,恒温恒湿槽内の湿度の上昇よりも明らかに遅く,最大値でほぼ安定になるまでに約8時間を要した。また,この98%RHでの水素透過電流の立ち上がりは,カソード分極による水素チャージによって水素侵入させた水素透過試験における水素透過電流の立ち上がり28)よりも明らかに遅い。したがって,この水素透過電流の立ち上がりの遅れは,表面水素濃度が時間とともに増加し,一定になるまでに時間がかかっていることを示唆している。これは,CCTによって生成した比較的厚い錆層中の水の浸透とそれによる水素侵入の促進に時間がかかったためと思われる。

Representative change in hydrogen permeation current density with the change in relative humidity. The Fe specimen was corroded by 60 cycles of CCT prior to this electrical hydrogen permeation measurement.
相対湿度を98%RHに保持した後に80%RHまで低下させると水素透過電流は初期に低下した後に増加を見せた。更に湿度を70%RHに低下させた場合も同様の水素透過電流の変化が見られた。相対湿度を50%RHまで低下させ,その湿度で長時間保持すると,水素透過電流は初期の低下の後に増加し,約3hの後にピークを示し,その後徐々に低下した。ピークの水素透過電流密度は98%RHでの最大値と同程度であった。
Fig.5に種々のサイクル数のCCTで腐食させたFe試料試料の水素透過電流密度の相対湿度による変化を示す。比較のため,CCTでの腐食の無い作製ままの試料の水素透過電流も示す。この作製ままで腐食していない試料では有意な水素透過電流が見られなかったことから,水素侵入の促進には表面錆層の生成が必要であると考えられる。
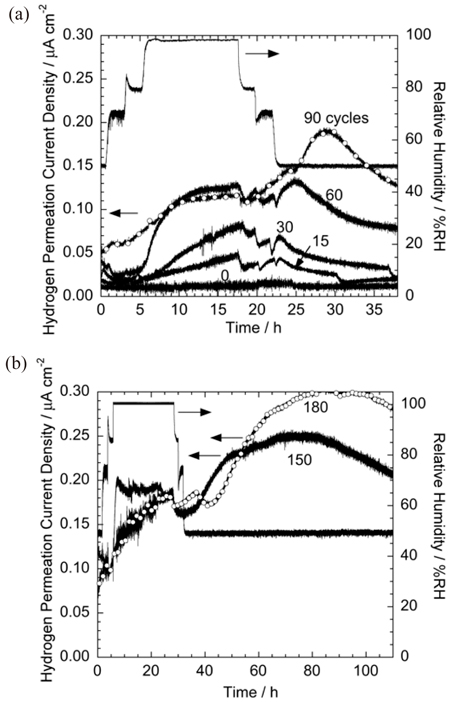
Comparison of the changes in hydrogen permeation current density with relative humidity of pure Fe rusted by varied cycles of CCT. (a) 0-90 cycles; (b) 150 and 180 cycles.
98%RHでの水素透過電流はCCTサイクルの増加にしたがって増加した。この増加は,CCT中で継続的にモニタリングした水素透過電流がCCTサイクルとともに増加したという先の報告の結果28)と一致している。98%RHの湿潤環境に保った後に50%RHまで下げて現れる水素透過電流密度のピークもまた,CCTサイクル数とともに著しく大きくなった。ことにCCTのサイクル数が90以上では,そのピークの値は98%RHでの最大値より明らかに大きくなった。98%RHでの水素透過電流密度の最大値と50%RHでのピーク値のCCTサイクル数による変化をFig.6に示す。それぞれの相対湿度での水素透過電流密度の最大値はCCTサイクル数の増加とともに増加し,98%RHでの最大値は120サイクル以降で概ね一定となる。一方,50%RHでの水素透過電流密度の最大値は180サイクルまで増加し続けた。

Changes in the highest hydrogen permeation current density at 98%RH and 50%RH of pure Fe specimens corroded by 150 cycles of CCT prior to the electrochemical hydrogen permeation measurement.
この比較的厳しいCCT環境では純Fe試料の腐食減量はほぼ時間に比例して増加し,腐食速度はほぼ一定である28)。試料の厚さの減少は拡散性水素の拡散距離を小さくし,水素透過電流の増加を引き起こすと考えられるが,厚さの減少の効果は水素透過電流の増加を説明出来る程大きくない。したがって,98および50%RHでの水素透過電流の増加は腐食速度の変化や試料の厚さが主な原因になっているのではなく,試料表面錆層の成長によるものと考えられ,錆内層のpHの低下による水素還元反応の促進などが寄与しているものと思われる28)。著者らは,W/WO3電極プローブを用いて測定した錆内層のpHがCCTサイクル数に伴い低下することを報告している15)。このpHの低下は下記のような溶出Fe2+の反応によると考えられる21)。
| (1) |
| (2) |
短周期での錆内層のpHの変化をモニタリングは実験的に困難で確認は出来ないが,同様の錆内層のpH低下が錆層の乾燥過程で起こり,水素侵入を促進している可能性も考えられる。また,乾燥過程でのCl−の濃縮による腐食速度の増加や表面電位の低下21)も水素侵入の影響因子になっていると思われる。
相対湿度を90%RHから50%RHに低下した後に水素透過電流のピークが現れるまでの時間をCCTサイクル数に対してプロットするとFig.7のようになる。ここでは,設定相対湿度を98%RHから80%RHに変更した時点を時間0とした。CCTサイクル数の増加にともない,水素透過電流のピークが現れるまでの時間が長くなる。このピーク出現の遅れは,CCTサイクル数にともない錆層が厚くなると,その錆層の乾燥のための時間が長くなることと関係していると考えられる。

Change in the time to the peak of hydrogen permeation current density during drying process of pure Fe specimens corroded by 150 cycles of CCT. The time 0 corresponds to the end of wetting at 98%RH.
沖縄県琉球大学および茨城県つくば市の物質・材料研究機構で屋外暴露した試料を用いて,前述の電気化学的水素透過試験と同様の試験を行った。Fig.8aは沖縄で2ヶ月間暴露した純Fe試料の相対湿度変化による水素透過電流密度の変化を示している。水素透過電流密度は相対湿度とともに増加し,98%RHでほぼ一定の値を示した。この水素透過電流密度はCCTにより腐食した試料と比較すると明らかに小さいが,その後に湿度を下げると,90サイクル以上CCTを行った試料と同様に水素透過電流に顕著な増加が見られた。

Changes in hydrogen permeation current with changing relative humidity of (a) a pure Fe specimen exposed at Okinawa for 2 months and (b) a SCM435H steel specimen exposed at Tsukuba for 2 years.
腐食環境としては比較的穏やかなつくばで2年間屋外暴露したSCM435H鋼試料の場合,98%RHでの水素透過電流密度は先に示した沖縄暴露試料と同程度であったが,その後の乾燥過程で現れるピーク値は98%RHでの値より小さく,また沖縄暴露試料のピークよりも小さかった(Fig.8b)。なお,この測定の場合,主に乾燥過程での水素侵入に着目したため,相対湿度を上げる際には50から98%RHまで一度に引き揚げた。
屋外暴露環境で行った水素透過試験で,湿度が下がる際に水素透過電流が増加する現象については報告がある14,31)。この実環境での水素透過試験の場合,湿度の低下は温度の上昇と連動しているため,温度の上昇が水素の拡散を促進し水素透過電流を増加させた影響も考えられる。一方,本研究では温度は30°Cに保っているため,乾燥過程そのものに水素侵入を促進する効果があることが示された。以上の様に,腐食した試料の電気化学的水素透過試験によって,乾燥過程で水素侵入が促進される可能性があることが示されたことから,遅れ破壊発生限界拡散性水素量HCと比較するべき環境からの侵入水素量HEの最大値を見積もるためには注意深い検討が必要であると言える。
3・3 ACMセンサーを用いた腐食挙動のモニタリング水素侵入に及ぼす腐食速度の効果を検討するために,CCTによって腐食させたACMセンサーのACM電流を温湿度制御下で測定した。Fig.9は30サイクルのCCTによって予備腐食させたACMセンサーのACM電流の相対湿度に伴う変化を示している。ACMセンサーの寿命上の制限から,これ以上長期のCCTによって腐食させたセンサーは用いられなかった。

Change in ACM current with relative humidity for an ACM sensor rusted by 30 cycles of CCT.
ACM電流は相対湿度の上昇とともに増加し,98%RHで10時間以上保持したところ,概ね安定な比較的高い値を保った。この相対湿度に伴う腐食速度の増加は,相対湿度に伴う水素透過電流の増加と対応していると考えられる。相対湿度を80%RHから98%RHに低下させた際にACM電流は急峻な立ち上がりを見せ,そのピーク値は98%RHの場合の倍程となった。このACM電流の増加は,水膜厚さの減少に伴う酸素還元反応の促進によって腐食が加速されたことによるものと思われる32,33,34)。酸素還元反応の促進による腐食速度の増加は直接に水素侵入を促進するものではないが,腐食速度の増加に伴う溶出Fe2+イオンの増加とその加水分解によるpHの低下が水素還元反応の効率を高め,水素侵入の促進に寄与する可能性が考えられる。
3・4 水素透過電流密度と昇温脱離法(TDA)で測定した水素量の関係Fig.10はボロン鋼試料を150サイクルのCCTで腐食した後に測定した水素の昇温脱離曲線である。一方の試料はCCTの後に50%RHの相対湿度,30°Cで24h保持した後に,もう一方の試料はCCT後すぐにTDAを行った。50%RHで保持した試料の水素昇温脱離曲線の方が,保持しない試料よりも明らかに高くなっており,50%RHでの保持の間に水素侵入が加速されたことが示唆される。このことは,150サイクルのCCTで腐食した純Fe試料を用いた電気化学的水素透過試験で,湿潤保持後に50%RHで乾燥した際に水素透過電流が上昇したことと対応している(Fig.5b)。

Representative hydrogen desorption curves of boron-bearing steel specimens with and without keeping at 50%RH and 30 ºC after 150 cycles of CCT.
それぞれの条件で求めた水素量をFig.11に示す。CCTを各ステージ直後で止めて求めた水素量(図中●)を比較すると,塩水噴霧のステージ直後で止めて測定した場合は,他のステージと比較してやや高い水素量が測定された。腐食条件として厳しい塩水噴霧での水素侵入が他のステージよりも促進されていることが示唆される。CCT後の水素量は0.01-0.02wppm(重量ppm)であったが,これに対し,CCT後に各ステージの条件を24時間保持した後に測定した水素量はいずれの条件でも高くなった。24時間保持の条件は,水素量の多い順に,塩水噴霧>乾燥>湿潤であった。

Diffusible hydrogen content measured by means of TDA for disc-shaped boron-bearing steel specimens corroded by 150 cycles of CCT. CCT was stopped at each constituent stages of CCT (solid marks) or each constituent stage condition was continued for 24 h prior to TDA.
以前に報告したCCT環境下での継続的な水素透過電流のモニタリングでは,100サイクル目のCCTでは水素透過電流は,湿潤とそれに続く塩水噴霧時に高かった。水素透過電流は塩水噴霧から乾燥過程に移行した直後に小さなピークを示したが,その後徐々に減少した27)。本論文の実験に用いたCCT後に水素分析を行ったボロン鋼試料への水素侵入挙動も同様であったと考えると,湿潤および塩水噴霧のステージで表面水素濃度は高くなっていると考えられる。しかしCCTの湿潤ステージは1.75h,塩水噴霧ステージは1.5hとそれぞれ短時間であるため,表面の水素濃度が高まっても,試料内部の水素濃度が同様に高まるのには時間が十分でない。24hそれらの条件下に保持した場合には,試料内部の水素濃度も表面に対応して高くなり全体の水素量も増加するため,TDAで求めた水素量が,CCT直後の測定量よりも高くなったものと考えられる。
塩水噴霧,湿潤条件を24h保持した場合だけでなく,乾燥条件を24h保持した場合にも,水素量はCCT直後に測定したよりも高くなった。CCTの乾燥ステージは5.75hと短く,前述のようにこの比較的短時間では水素侵入は低下する傾向を示すが,Fig.5bのCCT後の試料を用いた電気化学的水素透過試験の結果で見られたように,水素侵入はより長時間のスケールでは著しく促進される。24h乾燥保持の試料がCCT直後よりも高い水素量を示したのは,この乾燥過程での水素侵入の促進によると考えられる。
このように,水素量は試料の置かれる環境やその時間により大きく影響を受けるために,腐食により環境から侵入する水素量をTDAなどにより求める場合には注意が必要である。
3・5 水素透過電流密度からの水素量の推定150サイクルのCCTで腐食したFe試料の最大の水素透過電流密度は,98%RHおよび50%RHでそれぞれ0.18µA/cm2および0.25µA/cm2であった(Fig.6)。定常的な水素透過条件でのEq.3が適用出来ると仮定すると35),水素侵入側の表面直下の金属中の水素濃度C0を求めることが出来る。
| (3) |
ここで,Lは試料厚さ,iは水素透過電流密度,Dは試料中の水素の拡散係数,Fはファラデー定数である。本試験で用いた圧延した純Feシート中の水素のDは6.0×10−11m2/sであった28)。
150サイクルのCCTで腐食し,98%RHおよび50%RHに24hおいたFe試料のC0を水素透過電流から求めると,それぞれ0.016および0.022wppmである。ここで,Feの密度は7.86g/cm3とした。試料厚さの初期値は0.5mmであるが,150サイクルのCCTで腐食した厚さを考慮して,Lは0.4mmとした。Kushidaらは,同じ水素侵入環境では水素透過係数(水素透過係数を試料厚さで割った値)が鋼種に限らずほぼ等しいと報告している36)。そこで,TDAに用いたボロン鋼の水素透過電流密度が水素透過試験に用いた純Fe試料と等しいと仮定し,以前に求めたボロン鋼中の水素拡散係数4.5×10−11m2/s8,37)を用いると,ボロン鋼の場合のC0を推定することが出来る。150サイクルのCCTで腐食したボロン鋼中のC0の推定値は98%RHに24hおいた場合0.021wppm,50%RHの場合で0.029wppmである。上記のような仮定を用いて求めたものではあるが,得られた推定値は,Fig.11に示したボロン鋼のTDAで求めた水素量と良く対応している。したがって,電気化学的水素透過試験による水素量の見積もりには定量性が期待できる。
3・6 水素侵入に及ぼす錆層の効果Fig.12にはFeの腐食表面で起こりうる反応の代表的なものを挙げている。水素の侵入は腐食によって引き起こされる。中性の大気腐食環境ではFeのアノード溶解(Eq.4)に対応して起こるカソード反応のほとんどは酸素還元反応(Eq.5)と考えられる。しかし,部分的には水素還元反応(Eqs7,8)が起こり,水素発生の反応中間体である吸着水素Hadsの一部が金属中に侵入する(Eq.9)と考えられる。全体の還元反応に占める水素還元反応の割合はpHの低下によって増加すると考えられ,このpH低下には溶解したFe2+イオンの加水分解反応などが寄与していると考えられる(Eq.1, Eq.2)。一方,酸素還元反応(Eq.5)はpHの増加に寄与する。中性環境では水素還元反応(Eq.7)が全体のカソード反応に占める割合は低いと考えられるが,この反応もまたpHを増加させる。以上の反応を考慮すると,部分的なばらつきはあると思われるが,系全体のpHは中性に保たれると考えられる。

Schematic drawing of rust layer and possible reactions on the substrate metal surface and in the rust layer.
Fe(OH)2の酸化によりFeOOHが生成(Eq.11)すると,FeOOHの還元反応も還元反応の一部として起こると考えられる(Eq.10)38,39)。このマグネタイト(Fe3O4)を生じる還元反応はpHの変化に寄与しない。したがって,このマグネタイト生成反応がカソード反応全体に占める割合が増せば,pHの低下が起こると考えられる。pHの低下は水素還元反応(Eq.7)の割合を増加させ,水素侵入(Eq.9)を促進すると考えられる。
Fig.5およびFig.6に示したCCTのサイクル数の増加に伴う水素侵入の促進は,錆層の成長にしたがい,その内部のpHが低下することが原因となっていることが示唆される19)。著者らはCCTサイクル数に伴う錆内層のpHの低下をW/WO3電極を用いて確かめているが28),このpH低下の観察は上記のような錆内部のpH低下による水素侵入促進の仮説を支持している。
このような比較的長い時間での錆層の変化と同様に,錆層内のpHやFeのイオン種などの変化は環境の湿度などの因子の変化とともに短周期でも起こっていると考えられる。Fig.5およびFig.6に示したような,湿潤環境保持後の乾燥過程においても,H+の濃縮あるいは錆層に取り込まれたCl−の濃縮などの寄与により水素侵入が促進され,錆層が十分乾燥し腐食が抑制されると水素侵入も抑制されるために,水素透過電流密度のピークが現れたものと考えられる。このピークが現れる時間がCCTのサイクル数の増加とともに長くなるのは,錆層の厚さがCCTサイクル数にともなって厚くなり,錆層の乾燥に要する時間が長くなったためであると考えられる。
また,水素侵入には,電位の効果21)や,例えばFe表面とは水素発生反応の機構が異なると考えられるマグネタイトの生成の影響40,41,42)など錆層の構造変化の効果も考えられる。遅れ破壊感受性評価のための大気腐食環境からの水素侵入の理解には,更により詳細な検討が必要である。
腐食したFeおよび鋼への水素侵入挙動を温湿度制御下での電気化学的水素透過試験により観察した。水素侵入は環境を低湿度から高湿度に変化させた時に上昇し,湿潤環境での水素侵入は,CCTによる錆層の成長に伴って促進された。
湿潤保持後の乾燥過程で,水素透過電流はピークを示した。このピーク値は,CCTによる腐食が長く錆層が厚くなる程高くなり,比較的錆層が厚い場合には湿潤保持中よりも乾燥過程での水素透過電流が大きくなった。さらに,このピークの現れる時間もCCTサイクル数とともに長くなった。この水素透過電流密度の変化は,乾燥過程での錆層の特性の変化によるものと思われ,ピークの現れる時間は錆層厚さに依存したものと思われる。
同様の湿潤保持後の乾燥過程での水素透過電流の変化は,実環境で大気暴露した試料でも見られた。環境からの水素侵入を評価するためには,このような乾燥過程での水素侵入の促進を考慮する必要がある。
電気化学的水素透過試験結果から推定した拡散性水素量は,TDAで求めた拡散性水素量と良い対応を示した。このことから,大気腐食環境下での最大の水素侵入量の見積もりに電気化学的水素透過試験が有効であると考えられる。
高力ボルトの遅れ破壊評価法開発に関するプロジェクト14)で用いた,物質・材料研究機構に暴露したSCM435H試料を提供いただいた日本鋼構造協会に感謝いたします。水素昇温脱離分析およびサイクル腐食試験に協力いただいた物質・材料研究機構廣田ゆり子氏および荒木玲子氏に感謝いたします。