Abstract
大腿静脈ルートでの皮下埋め込み型中心静脈アクセスポート(central venous port;以下,CVポートと略)留置による静脈栄養管理は感染症や血栓症のリスクが高く,通常は推奨されない.2005年空腸デスモイドに対して小腸切除術を施行中に,上腸間膜動脈を損傷し大量小腸切除と空腸ストマ造設を行った.結果的に短腸症候群となりCVポートによる静脈栄養管理を導入したが,カテーテル感染を繰り返し,CVポートの抜去と造設を何度も必要とした.経過中に両側内頸静脈から鎖骨下静脈合流部に狭窄をきたし,上大静脈内へのカテーテル留置が困難となり,大腿静脈ルートでCVポートを造設した.その後,カテーテル閉塞とセプタムの露出はあったが,経路変更や感染症の合併はなく現在まで経過している.ポート留置の工夫と適切な管理により,大腿静脈ルートでもCVポートを用いた長期の中心静脈栄養管理は可能であり,選択肢になり得ると思われた.
緒言
中心静脈アクセスポート(central venous port;以下,CV ポートと略)における長期合併症として,カテーテル関連血流感染(catheter related blood stream infection;以下,CRBSIと略)と静脈血栓が挙げられる.特に大腿静脈に留置されるカテーテルはこれらのリスクが高いとされている1).そのためCVポートを留置する際,通常はアクセスルートとして内頸静脈や鎖骨下静脈が優先的に選択されている.今回,両側の内頸静脈-鎖骨下静脈合流部狭窄のために選択できる一般的なアクセスルートが無くなり,大腿静脈ルートにてCVポートを留置し,栄養管理を行っている1例を経験したため報告する.
症例
60代,女性.2003年に家族性大腸腺腫症(familial adenomatous polyposis;以下,FAPと略)に伴う横行結腸がんにて大腸亜全摘術を施行され,J型回腸嚢-下部直腸吻合を実施された.2005年にはFAP関連疾患である空腸の腸間膜デスモイドに対して小腸切除を施行中,高度癒着の剥離操作に起因する上腸間膜動静脈損傷を起こし血管修復を行った.結果的に血管損傷による血流障害を起こしたことで術後縫合不全となり,縫合不全部を含めて血流障害をきたした腸管の大量切除と空腸ストマ造設が行われた.残存小腸が50 cm程度の短腸症候群となり,補液と栄養管理のために導入された右鎖骨下静脈からのCVポートによる間欠的在宅静脈栄養を開始した.2006年9月にCVポート感染による敗血症を発症し,ポート抜去を行った.敗血症治療後,右内頸静脈ルートにてCVポート再留置を行った.2007年2月MRSA腰椎化膿性脊椎炎にて入院となり,血行性感染が疑われたため留置していたポートは抜去し,治療後に尺側皮静脈ルートの左上腕CVポートを造設して退院となった.2008年,左上腕CVポートの真菌感染にて入院しCVポート抜去後,左鎖骨下静脈ルートにてCVポートを留置し退院となった.2011年7月,CVポート感染による2度目の敗血症にてCVポート抜去と抗菌薬による加療を行い,状態安定後にCVポート再留置を試みた.
その際,様々なアプローチで上大静脈へのカテーテル留置を行うも,困難であり,最終的に左鎖骨下静脈ルートでカテーテルを留置した.カテーテル先端の位置の詳細な確認のために造影CTを撮影したところ,カテーテル先端は左心膜横隔膜静脈に迷入していた(図1a,b).また,左腕頭静脈は狭小化し途絶しており,側副路が発達している状態であった(図2).右内頸静脈,右腕頭静脈,上大静脈については,途絶はしていないものの,狭小化を認めていた(図3a,b).カテーテル先端は左心膜横隔膜静脈に迷入しているものの,左心膜横隔膜静脈から左下横隔膜静脈経由にて下大静脈へ流入しており,その位置で使用することとした(図1b).

図1.a:左心膜横隔膜静脈にカテーテル先端が位置している.b:実線 カテーテル先端,破線 左心膜横隔膜静脈から左下横隔膜静脈を経由して下大静脈へ流入している.

図2.左腕頭静脈の造影効果が消失し,途絶している.
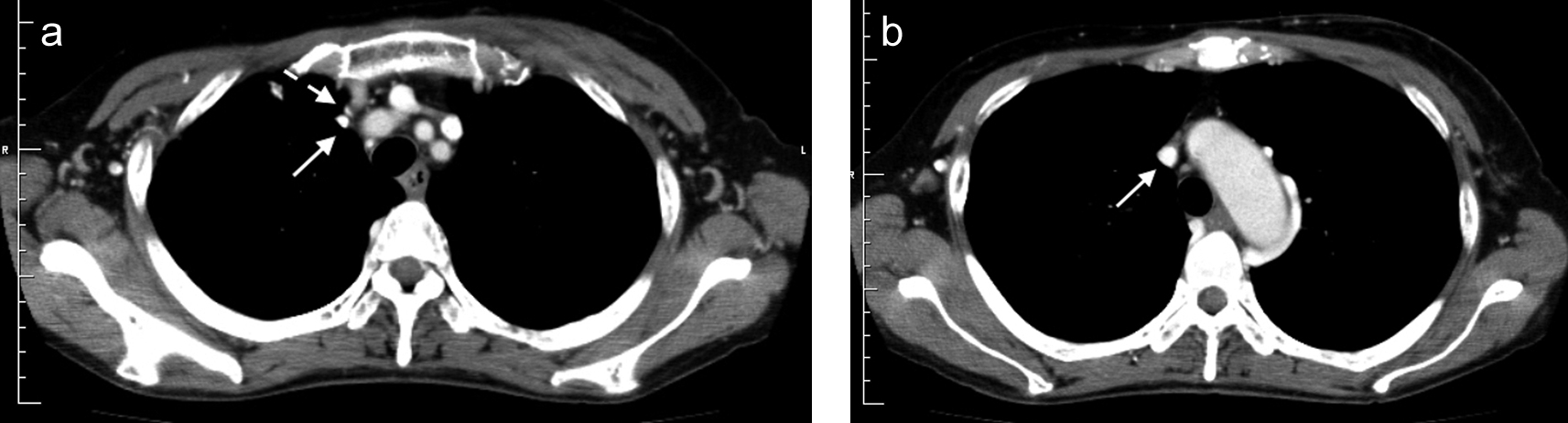
図3.a:実線 右内頸静脈,破線 右鎖骨下静脈.b:上大静脈
その後も2012年,2015年にCRBSIを発症したため,カテーテルを抜去し,同血管に再挿入を行った.2015年9月より,点滴時に左肩~左上肢へ放散痛が出現するようになった.2016年1月に再度入れ替えを行うも,左肩~頸部の疼痛が持続した.これまで大腿静脈ルートはCRBSIや血栓リスクが高いとされていることから避けてきたが,2016年5月に大腿静脈からのCVポート留置を行った.人工肛門が右腹壁に造設されているため,CVポートは左大腿静脈ルートとした.2017年12月には,挿入時には無かったカテーテル刺入部の屈曲が原因と思われるカテーテル閉塞(図4),また2020年9月にセプタムの露出を認め,それぞれ同ルートでのカテーテルとポート交換を実施した.以降2022年3月現在まで,カテーテル感染あるいは感染性合併症を引き起こすことなくCVポートを使用し,患者は安定した生活を送っている(図5).

図4.実線 カテーテル先端部位,破線 静脈刺入部付近でカテーテルの屈曲が強くなっている.

図5.臨床経過
考察
CVポートは,化学療法や長期栄養管理目的に多くの患者に使用されている.中心静脈カテーテルを留置する際に選択する血管についてはCRBSIや静脈血栓を起こしにくいという観点から,多くの場合は内頸静脈や鎖骨下静脈が選択されている1).
本症例でも内頸静脈や鎖骨下静脈ルートにてカテーテルを留置していたが,両側内頸静脈・鎖骨下静脈から腕頭静脈にかけて閉塞や狭窄が発生してしまった.当院においてCVポート造設は,すべて手術室にて透視下で行われている.また,点滴薬剤については,毎日夜間に高カロリー用の糖・電解質・アミノ酸・総合ビタミン・微量元素含有液(エルネオパ®NF2号輸液1,000 mL)+/– で維持液500 mL(薬局のクリーンベンチで混注)が投与されており,在宅栄養管理中にその他薬剤は投与されていなかった.使用していたラインはフィルター一体型のclosed systemを使用しており,毎日交換されていた.穿刺針は3日に1回交換されており,院内で穿刺する際は1%ヘキザックアルコールを使用し,自宅で穿刺する際は80%エタノールを使用した後に10%ポビドンヨードを使用して穿刺しており,穿刺した後にフィルムドレッシング材で保護するよう指導している.また,コネクター部分は80%エタノール綿を使用して付け替えている.当院では,2007年より現在も使用しているフィルター一体型のラインの製品を採用しており,本症例において2005年から2006年にかけては不明であるが,少なくとも2007年以降においては,一般的な中心静脈栄養管理から大きく逸脱した管理はされていなかった.
Lebeaux Dらは,静脈栄養でのCVポート使用時におけるCRBSI発生率は,1,000留置日数あたり0.33~3.20/1,000日と報告している2).本症例と比較すると,2005年のCVポート造設後から大腿静脈ルートに変更となる2016年までにCRBSIが6回発生しているため,発生率は約1.5/1,000日となり,報告よりも高頻度での発症は認めていないと考えられる.これらを踏まえると,本症例のみCRBSIが発生しやすい状態であったわけではなく,長期的に中心静脈栄養を行っていく上で,ある程度避けることのできない合併症であった可能性が考えられる.
本症例では内頸静脈・鎖骨下静脈が使用できなくなった際に,左心膜横隔膜静脈へカテーテルを留置していた.留置時の左心膜横隔膜静脈径は造影CTで測定すると8 mm程度であり,内頸静脈の平均である18.1 mmと比較すると,非常に細い3).2012年から2回のCRBSIを引き起こしたものの,3年程度は左心膜横隔膜静脈を使用することができた.その理由としては,細径ではあるが左腕頭静脈途絶に伴う流出路となっていたため,面積あたりの血流量は比較的多く,流速が速くなっていた可能性が考えられる.
大腿静脈へ留置されている中心静脈カテーテルのCRBSIの頻度が高い理由としては,穿刺部が会陰部に近いため不潔になり易いことや,関節可動部に位置しているため固定やドレーピングが難しく,汚染され易いことが指摘されている4).しかし,多くは中心静脈カテーテルとして留置してある報告であり,CVポート留置について大腿部と他の部位のCRBSI発生率について比較している報告は多くない.ポートが比較的頭側に留置されていれば,前胸部と同じように清潔を保つことができ,CRBSIの発症予防につながる可能性があると考えられる.また,比較的頭側にポートを位置させることは,パンツラインと重なり圧迫することで起こるポート部皮膚の血流障害・潰瘍形成を引き起こすリスクを回避することにもつながると考えられた.実際,CVポート入れ替えの際には患者から「服にポートが当たるため,ポート留置部をもう少し頭側に移動させて欲しい」との申し出があり,左大腿静脈刺入部から頭側へ約17.5 cmの部位にポートを移設している.また,CVポート造設状態でのCRBSIにおいて,ポート部からカテーテル経由での血管内への細菌感染が原因の一つとなるため,CVポート留置部から静脈穿刺部までの距離が長い方が感染率低下に寄与する可能性が考えられる.その反面,CVポート留置部から静脈穿刺部までのカテーテルが長いことで,本症例のように留置時よりもカテーテルの屈曲が強くなること,血栓形成によるCV閉塞のリスクが高まる可能性があることを認識しておく必要があると考える.また,当然ではあるが,感染予防については,穿刺・抜針時に必ずアルコール消毒を行い,ポート周囲の皮膚の清潔を保つよう努める必要がある.
通常,CRBSIや血栓のリスクが高いといわれている大腿静脈ルートを用いたCVポートではあるが,ポート位置の調整,皮下埋没部カテーテルの滑らかな走行を意識すること,穿刺・抜針時の感染予防管理などを徹底することで安全に長期利用することができると思われた.
これまで大腿静脈ルートでのCVポート留置については報告が少なく,我々は現在まで手探りでCVポート管理を行ってきたが,今後も本症例の治療経過を慎重に観察し,そのなかで起こる合併症や問題点を拾い上げ検討し,より良い方法を模索していきたい.
結語
今回,繰り返すCVポート感染のため一般的なアクセスルートがなくなり,大腿静脈ルートにてCVポートを留置している1例を経験した.大腿静脈を使用したCVポートは,他の部位に比べて感染症や血栓症の面でリスクが高いものの,ポート留置位置の最適化,皮下部カテーテルのできる限り屈曲のない滑らかな走行を意識した挿入操作,穿刺・抜針時の十分な感染予防,患者自身へのポートの取り扱い指導などを行うことで長期利用は不可能ではないと思われた.また,上大静脈系のアクセスルートが閉塞等により選択困難である場合は,大腿静脈ルートの選択を今までよりも早期に検討することは患者にとって有益かもしれないと思われた.
なお,今回の症例報告に際しては,岐阜県総合医療センター 倫理審査委員会の承認を得た(承認番号802番).また,患者プライバシー保護に関する指針を十分に遵守することに留意した.
本論文に関する著者の利益相反なし





