2017 Volume 59 Issue 10 Pages 2526-2532
2017 Volume 59 Issue 10 Pages 2526-2532
レーザー経鼻内視鏡EG-L580NWのLCIモードを用いて胃底腺粘膜の近接観察を行い集合細静脈(CV)と腺管構造(GS)の視認性を観察することが,Hpの現感染,除菌後,未感染の診断に有用か否かを後方視的に検討した.CVおよびGS視認性はそれぞれ消失・不明瞭・明瞭の3群に分類した.①現感染ではCVの消失と明瞭なGS視認性,②除菌後では明瞭あるいは不明瞭なCV視認性とGS視認性の消失,③未感染では明瞭なCV視認性,が診断の特異度を上げる所見であった.また,除菌後は2年未満の早期からGS視認性の消失が観察された.LCIモードでは,色調が白色光観察と近似しており違和感なく日常臨床で使用できる点,また,腸上皮化生巣が示唆されるラベンダー色を呈する領域を避けて胃底腺粘膜を観察できる点で有用である.
通常内視鏡によるHelicobacter pylori(以下Hp)の感染診断は様々な内視鏡所見を把握して総合的に行われる.2014年9月に公表された京都分類 1)によると現感染,除菌後,未感染の各感染状態で診断に有用と考えられる所見は,現感染例ではびまん性発赤,粘膜腫脹,白濁粘液,除菌後例では地図状発赤,Hp感染所見はあるが現感染の所見がない場合,未感染では胃角までのregular arrangement of collecting vesels(以下RAC)である.しかしながら,これらの所見は各感染状態で必ずしも出現するわけではない.
一方,本来どの胃にも存在する指標が現感染,除菌後,未感染の各状態に応じて一定の変化を示すのであれば,その変化を所見として捉えることにより感染診断に役立てることが出来ると推測される.拡大内視鏡を用いた八木ら 2),3),大久保ら 4)の報告を基にすると,集合細静脈視認性とpits形態がHp感染状態を判断する共通の指標として有用であると考えられる.経鼻内視鏡は細径であるがゆえに焦点距離が短く3mmまでの近接観察でもピントのあった画像を得ることができる.近接観察により約30倍前後の弱拡大が可能である 5).さらに最近の経鼻内視鏡は様々な画像強調のモダリティーを備えている.これらの特性を応用することにより経鼻内視鏡を用いた近接観察で集合細静脈やpits形態を反映する腺管構造(窩間部と八木ら 2)の言うwhite zoneを合わせた構造)の観察が可能と考えられる.
そこで,レーザー経鼻内視鏡EG-L580NW(富士フイルムメディカル)のLinked Color Imaging(以下LCI)モードを用いた近接観察により集合細静脈(collecting vessels,以下CV)と腺管構造(glandular structure,以下GS)の視認性を観察することが,Hpの現感染,除菌後,未感染の診断に有用か否かを後方視的に検討した.
①対象:2014年8月~2016年10月までの間,経鼻内視鏡EG-L580NWによる近接観察が可能であったHp感染診断が確定した235例238回(男123・女112例,平均年齢62.7±13.2歳)の内視鏡所見である.このうち3例が現感染から除菌後への経過観察例である.内視鏡施行時のHp感染診断は現感染77回,除菌後108回,未感染53回である.除菌後の中で除菌療法後の経過年数が明確な75回の経過年数別の内訳は2年未満17回,2年以上5年未満34回,5年以上10年未満15回,10年以上9回である.
②Hp感染診断:血清抗Hp抗体価(Eプレート栄研H.ピロリ抗体Ⅱ),UBT,内視鏡的萎縮(L580NWによる観察)の組み合わせで行った.(1)Hp抗体価<3で,内視鏡的萎縮なしの場合は未感染,内視鏡的萎縮ありの場合は除菌後とした.(2)3≦Hp抗体価<10でUBT陰性の場合は,内視鏡的萎縮なしは未感染,内視鏡的萎縮ありは除菌後とした.一方,3≦Hp抗体価<10でUBT陽性の場合は現感染とした.(3)10≦Hp抗体価で,UBT陰性の場合は除菌後,UBT陽性の場合は現感染とした.
③機器の設定と判定:近接観察は光量をピークに設定して行い,ピントの合う最近接のreal timeの画像で判断した.判定は一人の同一の内視鏡医によって行われた.内視鏡医は被検者のHp感染についての情報は知らされないで検査を実施した.
④観察部位:血管透見像を認める領域性を伴った萎縮粘膜の大彎側2カ所の胃底腺粘膜を近接観察した.領域性を伴った萎縮粘膜を認めない場合は体中部前壁および体中部大彎の胃底腺粘膜を観察した.隆起や陥凹を呈する領域,あるいは,LCIモードでラベンダー色を呈する領域は観察対象から除いた.
⑤観察項目:⑴CV視認性:LCIモードで観察し,視認性を以下の3群に分類した.明瞭(Figure 1):CVのヒトデ状形態における腕の部分も鮮明に見えるもの.分布が均一・不均一にかかわらず明瞭とした.不明瞭(Figure 2):ヒトデ状形態の腕の部分が一部欠損しているもの,腕のすべてが欠損しdot状に見えるもの,血管の輪郭が鮮明でないもの.消失(Figure 3~6):CVが観察されないもの.⑵GS視認性:LCIモードで観察し,視認性を以下の3群に分類した.消失(Figure 1,2,4):GSが見えない場合,あるいは,分別困難なGSが密に観察される場合.不明瞭(Figure 5):溝状のwhite zoneが観察され,窩間部の発赤が軽度である場合.明瞭(Figure 3,6):溝状のwhite zoneの観察が容易であり,窩間部の発赤が高度である場合.観察部位によって所見が異なる場合は,CV視認性はより不良なもの,GS視認性はより明瞭なものを所見とした.

集合細静脈(CV)視認性 明瞭,腺管構造(GS)視認性 消失.
Hp未感染例.ヒトデ状の形態を示す明瞭な集合細静脈を認める.僅かに腺管構造を認めるが,その分別は難しい.

集合細静脈(CV)視認性 不明瞭,腺管構造(GS)視認性 消失.
Hp除菌後例.一部にヒトデ状の集合細静脈も認められるが,矢印で示すように,血管の輪郭は不鮮明で腕の欠落したドット状のものが多い.僅かに腺管構造を認めるが,その分別は難しい.

集合細静脈視認性 消失,腺管構造視認性 明瞭.
Hp現感染例.集合細静脈は認められない.
溝状のwhite zoneの観察が容易で,窩間部の発赤が高度である.

集合細静脈(CV)視認性 消失,腺管構造(GS)視認性 消失.
Hp除菌後例.やや遠景からの画像である.腸上皮化生巣が示唆されるラベンダー色の領域が認められる.ラベンダー色以外の領域では,集合細静脈や分別可能な腺管構造は認められない.
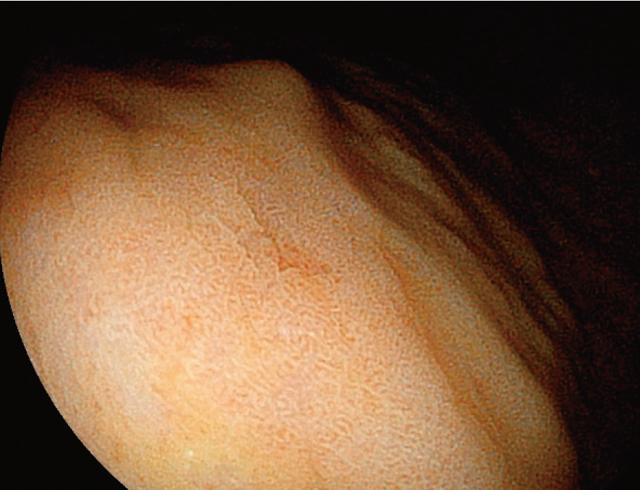
集合細静脈(CV)視認性 消失,腺管構造(GS)視認性 不明瞭.
Hp除菌後例.集合細静脈は認められない.溝状のwhite zoneは認められるが,窩間部の発赤は軽度である.

集合細静脈(CV)視認性 消失,腺管構造(GS)視認性 明瞭.
Hp現感染例.集合細静脈は認められない.溝状のwhite zoneが明瞭に観察され,窩間部の発赤が高度である.
①CV視認性(Figure 7):現感染では消失が88.3%,未感染では明瞭が92.5%を占めた.除菌後では不明瞭が55.6%,次いで明瞭が28.7%であった.

Hp感染状態別にみた集合細静脈(CV)視認性.
現感染では消失が,未感染では明瞭がほとんどを占めた.除菌後では不明瞭,次いで明瞭が多かった.
②GS視認性(Figure 8):現感染では明瞭が84.4%,除菌後では消失が78.7%を占めた.未感染では全例が消失であった.

Hp感染状態別にみた腺管構造(GS)視認性.
現感染では明瞭,除菌後では消失が多かった.未感染では全例が消失であった.
③除菌後の経過年数別 ⑴CV視認性(Figure 9):2年未満では3群は同等の頻度であったが,年数が経過するに伴い消失例が減り5年以上経過した例には消失例は認められなかった.一方,明瞭例が経年的に増える傾向を認め,不明瞭例は経過年数にかかわらず一定の割合を占めた.⑵GS視認性(Figure 10):消失が2年未満から64.7%を占め,さらに,経年的に増加する傾向を認め10年以上経過した例では全例が消失であった.明瞭は2年以上経過した例では認められず,不明瞭も経年的に減少し10年以上経過した例では認められなくなった.

除菌後の経過年数別にみた集合細静脈(CV)視認性.
2年未満では3群は同等の頻度であったが,年数が経過するに伴い消失例が減り明瞭例が増える傾向を認めた.一方,不明瞭例は経過年数にかかわらず一定の割合を占めた.
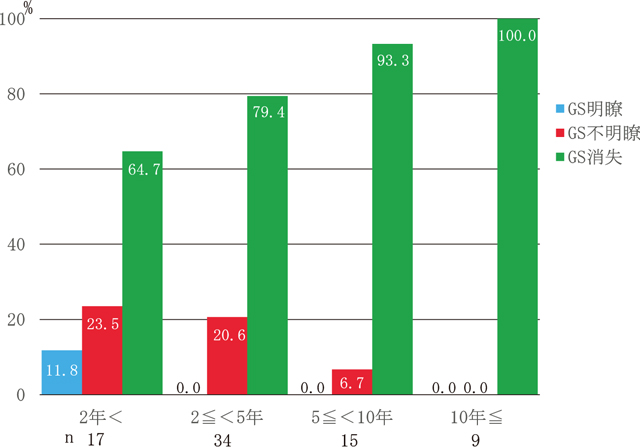
除菌後経過年数別にみた腺管構造(GS)視認性.
消失が2年未満から多くを占め,さらに,経年的に増加する傾向を認めた.10年以上経過した例では全例が消失であった.
八木ら 2)は非萎縮胃底腺粘膜領域の拡大内視鏡所見をCVやpits周囲の毛細血管網およびpits形態の観点からB-0~B-3に分類し,B-0がHp未感染,B-1~B-3がHp現感染の状態と述べている.また,八木ら 3)は,除菌1年後25例の体中部前壁~大彎の拡大内視鏡による観察で,pits間の発赤や浮腫の消失が100%,white pitsからpinhole-like pitsへの変化が96%,CVの視認性の回復が32%に認められたと報告している.また,大久保ら 4)は除菌12週後30例の体部大彎を拡大観察し,enlarged or elongated pitsからsmall oval or pinhole-like pitsへの変化とfine irregular vesselesの減少が高度萎縮や腸上皮化生がない24例では100%に認められたと報告している.除菌後では炎症の消退により窩間部の微細血管増生や浮腫が軽減すると伴に上皮の再構築が起こりpitsの小型化やpinhole状のpitsが出現すると推測される.しかしながら,経鼻内視鏡による近接観察では,このような除菌後の変化に伴ったpinhole状のpitsや,Hp未感染例に観察される八木ら 2)が提唱するB-0で認められるpinhole状のpitsを必ずしも明瞭に観察できるとは限らない.そこで,今回の検討では,white zoneと窩間部を合わせた構造をGSとし,GSが見えない場合や分別困難なGSが密に観察される場合をGS視認性消失として,pinhole状あるいは小型のpitsを示唆する所見とした.
未感染ではCV視認性が明瞭である所見は,未感染と感染(現感染と除菌後)との鑑別において感度92%,特異度82%,正診率84%であった.一方,CV視認性が明瞭で同時にGS視認性が消失である所見は,感度93%,特異度83%,正診率85%であり,GS視認性の上乗せ効果は認められなかった.
現感染ではCV視認性が消失している所見は,現感染とその他(未感染と除菌後)との鑑別において感度88%,特異度89%,正診率89%であった.また,CV視認性が消失し同時にGS視認性が明瞭である所見は,感度79%,特異度97%,正診率91%であり,GS視認性の評価を加えることにより特異度の改善を認めた.
内視鏡でHp感染診断を行う際に最も判断に難渋するのは現感染と除菌後の鑑別である.胃粘膜に萎縮や腸上皮化生巣は存在するが,現感染に特徴的とされる内視鏡所見に乏しい場合やRACを認める場合には除菌後を疑わせる所見と捉えることが多い.しかしながら,除菌後のCVを詳細に観察すると未感染の時に見られる明瞭なヒトデ状形態を示すものは少ない.ヒトデ状形態の腕の部分が一部欠損しているもの,腕のすべてがほとんど欠損しdot状に見えるもの,血管の輪郭が鮮明でないものなど,多様な所見を呈するものが多い.今回の検討ではこのような形態を示すCVを不明瞭としたが,除菌後の55.6%が不明瞭であり,明瞭の28.7%よりも多かった.CV視認性が明瞭である所見は,現感染と除菌後の鑑別において感度29%,特異度97%,正診率67%であったが,不明瞭に明瞭を加えると感度84%,特異度88%,正診率86%であった.したがってCV視認性不明瞭は除菌後の診断に有用な所見であると考えられる.一方,GS視認性については除菌後で消失としたものが78.7%と最も多かったが,GS視認性消失である所見は,現感染と除菌後の鑑別において感度77%,特異度99%,正診率87%であった.さらに,CV視認性が明瞭あるいは不明瞭で同時にGS視認性消失である所見は,現感染と除菌後の鑑別において感度66%,特異度99%,正診率80%であった.除菌後と現感染の鑑別にCV視認性の観察の他にGS視認性を加えることにより特異度は88%から99%に改善した.
症例数が少ないという問題点はあるが,除菌後の経過年数別に所見を検討した.CV視認性は2年未満では3群でほぼ同等の頻度であったが,GS視認性は消失例が64.7%を占め,除菌後早期の感染診断にはGS視認性の評価が重要と考えられた.また,CV視認性は年数が経過するに伴い消失例が減り明瞭例が増える傾向を認めたが,不明瞭例は経過年数にかかわらず一定の割合を占めた.一方,GS視認性の消失例は経年的にさらに増加し10年以上経過した例では全例が消失であった.したがってCV視認性不明瞭である場合にはGS視認性の評価が診断に有用であると考えられる.
胃底腺粘膜のCVやGS視認性を近接観察する場合には腸上皮化生巣を避けて観察する必要がある.LCIモードにおけるラベンダー色を呈する領域 6)は腸上皮化生巣と考えられており,Figure 4に示すように,ラベンダー色の領域を避けつつ注意深く近接観察を行うことが大切である.
経鼻内視鏡の短波長レーザー光による画像強調を近接観察で,胃底腺粘膜の集合細静脈と腺管構造の視認性を評価することによりHp感染診断が可能であった.除菌後と現感染の鑑別において,非典型的な形態を示す集合細静脈を捉えることで正診率が改善し,腺管構造の消失を加味することで特異度の改善が認められた.
本論文内容に関連する著者の利益相反:なし