要旨
2012年の「抗血栓薬服用者に対する消化器内視鏡診療ガイドライン」発刊後,3種類の直接経口抗凝固薬(DOAC)が登場し,ワルファリンとDOACに対する対応を明示するため,2017年に「直接経口抗凝固薬(DOAC)を含めた抗凝固薬に関する追補2017」が発刊された.本追補版では,出血高危険度消化器内視鏡施行時の抗凝固薬休薬は重篤な転帰を辿る血栓塞栓症の発症リスクとなるため,抗凝固薬の継続下,あるいは代替治療下(ワルファリン;ヘパリン置換およびDOAC置換,DOAC:ヘパリン置換)で行うことが推奨されている.ただし,抗凝固薬は高い出血リスクを有する薬剤であることに留置する必要がある.また,ワルファリンは旧来から行われてきたヘパリン置換によって出血リスクが増強すること,DOACは薬効のモニタリングができないデメリットがある.今後,本ガイドラインの有用性の評価を行うとともに,抗凝固薬内服症例における安全な内視鏡診療を提供するシステム作りが重要である.
Ⅰ 緒 言
超高齢化社会の到来に伴う抗血栓薬治療の普及により,抗血栓薬服用者に対して消化器内視鏡検査を行う機会が増加している.抗血栓薬服用者に対して内視鏡検査を行う際には抗血栓薬による消化管出血のリスクと休薬に伴う血栓塞栓症リスクに配慮した対応が必要となるが,従来日本消化器内視鏡学会(JGES)が示していた内視鏡指針では抗血栓薬服用下の消化器内視鏡診療に伴う出血予防に重点が置かれていた.しかし,欧米諸国のガイドラインと同様に抗血栓薬の休薬に伴う血栓塞栓症のリスクに配慮がされるようになり,2012年にJGESから「抗血栓薬服用者に対する消化器内視鏡診療ガイドライン」
1)が発刊された.
抗血栓薬は抗血小板薬と抗凝固薬に大別されるが,それぞれの特徴および対応は大きく異なる.抗血小板薬は,ガイドライン発刊後の8年の間にチエノピリジン誘導体であるプラスグレル(エフィエントⓇ)やチカグレロル(ブリリンタⓇ)が新たに上市されたが,他の薬剤に大きな変化はない.また,抗血小板薬,特に低用量アスピリンを単剤で内服している場合には,内服を継続して侵襲を伴う内視鏡処置を行うことがガイドラインで提唱され,抗血小板薬を継続して内視鏡的粘膜切除術(EMR)や内視鏡的粘膜下層剝離術(ESD)などの高危険度内視鏡処置を行うことが日常診療でも一般的となった.一方,抗凝固薬内服時の対応はガイドライン発刊後,大きな転換期が訪れている.2012年時点では経口抗凝固薬はワルファリンと直接トロンビン阻害薬であるダビガトランの2剤に限られていたが,その後,新たにリバーロキサバン,アピキサバン,エドキサバンの3種類の直接経口抗凝固薬(direct oral anticoagulants[DOAC])が登場し,その対応が必要となったため,2017年に「直接経口抗凝固薬(DOAC)を含めた抗凝固薬に関する追補2017」
2)が発刊された.
抗凝固薬の適応疾患は心房細動や深部静脈血栓症など,塞栓症の発症が重篤となりうる疾患である.血栓塞栓症が生じれば重篤かつ不可逆的な障害,さらには死に至る可能性もあり生命予後が悪いことが重大な問題である.一方で,抗血栓薬非服用者や抗血小板薬服用者と比較して高い内視鏡処置後の後出血率を有することから,抗凝固薬服用者の消化器内視鏡診療においては塞栓症のリスクと出血のリスクの狭間でジレンマが生じている
3)~5).今回の総説では,昨今の高齢化社会の進行に伴う消化器内視鏡診療に密接に関与する抗凝固薬服用者に対する内視鏡診療の現状についてガイドラインおよびガイドライン追補版を交えながら解説するとともに,内視鏡治療術後消化管出血のリスク管理における今後の対策について概説する.
Ⅱ 抗凝固薬の概略
抗凝固薬は,抗血小板薬とは異なり,フィブリン形成および塞栓が主体となる心房細動や深部静脈血栓症,肺塞栓症の治療時に使用される(Table 1).

血液凝固カスケードのビタミンK依存性凝固因子である第Ⅱ,Ⅶ,Ⅸ,Ⅹ因子を阻害して抗凝固作用を発揮するビタミンK拮抗薬であるワルファリンは,2010年までは唯一の経口抗凝固薬であった.しかし,使用時には頻回の薬効のモニタリングが必要で,用量設定が煩雑であること,ビタミンKを含む食事を制限する必要があること,薬物代謝酵素(主としてCYP2C9やVKORC1)
6),7)による個人間差が大きいことなど使用時の制約が非常に多いことが問題であった
8).その欠点を補うため他の作用機序を有する経口抗凝固薬開発の研究が進められ,4種類の直接作用型経口抗凝固薬(direct oral anticoagulants;DOAC)の有用性と安全性を調査するために大規模な前向きランダム化比較試験(RE-LY試験;ダビガトラン
9),ROCKET AF試験;リバーロキサバン
10),ARISTOTLE試験;アピキサバン
11),ENGAGE AF-TIMI48試験;エドキサバン
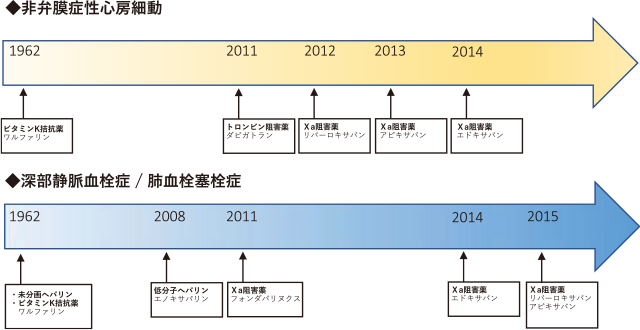
12))が行われた.その後,2011年に直接トロンビン阻害薬であるダビガトラン(プラザキサⓇ)が非弁膜症性心房細動に対して保険適用となり,それに続くように選択的Ⅹa阻害薬であるリバーロキサバン(イグザレルトⓇ),アピキサバン(エリキュースⓇ),エドキサバン(リクシアナⓇ)が非弁膜症性心房細動や深部静脈血栓症に対して保険適用を取得した(Figure 1).これらはあわせて新規非ビタミンK阻害経口抗凝固薬(Novel oral anticoagulants:NOAC)と呼ばれていたが,その普及とともにDOACと呼称されることとなった.DOACがワルファリンよりも優れた特徴は,①用量反応性に優れる,②抗凝固活性の個人間差が少ない,③ビタミンKを含む食事の影響が少ない,④薬物相互作用が少ないなどが挙げられ,近年,非弁膜症性心房細動や深部静脈血栓症の患者においては急速に使用頻度が増加している.DOACはそれぞれ適応疾患や効果が類似しているが,Table 1で示すように各薬剤で異なるため注意を要する.その中でダビガトランは,DOACの中で唯一拮抗薬であるイダルシズマブが存在するといった利点があるが
13),酸性の酒石酸を含むカプセルが食道壁に付着してダビガトラン起因性食道炎を発症するリスクがあること
14),生体利用率が低く消化管内に薬効が蓄積して消化管出血をきたしやすい可能性が指摘され,他の3種類の選択的Ⅹa阻害薬と比較して使用時には注意が必要である
15).
また,「抗血栓薬服用者に対する消化器内視鏡診療ガイドライン」
1)では,抗凝固薬療法中の血栓塞栓症は一度発症すると重篤となる可能性が高いため,抗凝固療法中の症例は全例,血栓塞栓症発症高危険群として対応することが推奨されている(Table 2).また,非弁膜症性心房細動患者の塞栓症リスクはCHADS2スコア(Table 3)と強く相関するため(Figure 2)
16),「心房細動治療(薬物)ガイドライン(2013年改訂版)」
17)や「脳卒中治療ガイドライン2015」
18)でもCHADS2スコアを参考にして抗凝固療法を行うことが推奨されている.われわれ消化器内視鏡医も心房細動に対して抗凝固療法を施している患者に対しては,個々の症例に応じた血栓塞栓症リスクを念頭に置き診療を行っていくことが必要である.
Ⅲ ワルファリン服用者に対する消化器内視鏡診療
ワルファリンの薬効はPT-INRによるモニタリング評価が可能であり,血栓塞栓症予防および出血リスクの観点から至適用量が定められている.実際に非弁膜症性心房細動患者ではPT-INRが2.0を下回ると脳梗塞の発症リスクが上昇し,1.6未満になると大梗塞の発症リスクが上昇するため
5),70歳未満ではPT-INRを2.0-3.0で,70歳以上では出血リスクを考慮して1.6-2.6で調整することが推奨されている
19).ワルファリンを服用している心房細動症例を対象とした検討では,継続内服をしたまま内視鏡検査を施行した438例では塞栓症の発症はなかったものの,休薬や減量を行った987例では1.06%で脳梗塞を発症したと報告された
3).また,ワルファリン休薬時にはリバウンド現象により一過性の過凝固状態となり,血栓塞栓症のリスクが上昇する可能性も示唆され
20),内視鏡検査時にワルファリンを血栓塞栓症の高リスクの症例に対して単純に減量・休薬することは血栓塞栓症の高リスクとなるため避けるべきである.
そこで,即効性かつ半減期が40~90分とワルファリンよりも短い注射用抗凝固薬である未分画ヘパリンで置換するいわゆる “ヘパリン置換” が代替治療として考案された.ヘパリン置換は高い有用性が示されていたため,ワルファリン内服者は積極的にヘパリン置換で内視鏡診療や内視鏡治療が行われてきた
21).しかし,最近の報告では,ヘパリン置換は血栓症発症の危険性を軽減する作用は乏しく,むしろ出血のリスクのみを高めることが証明された
22),23).同様に,胃ESD施行時でも術後出血の頻度はワルファリン休薬群と比較し,ヘパリン置換群で有意に高いことが示された(Risk Ratio=2.99,95%CI:1.51-5.92,P=0.002).大腸腫瘍に対するEMR施行症例を対象としたメタ解析
24)でも,ヘパリン置換群が休薬群と比較して後出血の頻度が有意に高いことが報告された(OR=8.29,95%CI:4.96-13.87,P<0.01).さらに,Mabeら
25)は多施設共同の前向き観察研究で抗血栓薬服用者5,250例の内視鏡的処置後の後出血について検討し,高危険度内視鏡処置(OR=19.2,95%CI:9.8-37.6,P<0.001),ヘパリン置換(OR=4.1,95%CI:1.6-10.5,P=0.003),腎不全・透析(OR=5.7,95%CI:1.7-19.5,P=0.005)が独立した有意な後出血リスク因子であることを報告した.このようにヘパリン置換は抗血栓薬非服用者やワルファリン休薬症例と比較して,消化管出血リスクを著しく増加させる.そのため,現在ではワルファリン内服者に対する内視鏡処置時においてヘパリン置換を行う意義が問われており,それらの結果を踏まえた形で,追補版
2)では,ワルファリン服用者に対する出血高危険度の消化器内視鏡は,PT-INRで3.0以下の治療域であればワルファリン継続下,あるいは非弁膜症性心房細動の場合にはDOACに一時的の変更のいずれかの方法での内視鏡処置も行うことも認められた(Table 4).

治療内視鏡検査時にワルファリン継続時とヘパリン置換時の安全性や有効性を比較した報告は少ないが,Yanagisawaら
26)は,大腸polypectomy後の術後消化管出血率を検討した後方視的研究で,ヘパリン置換群の術後出血率が21.7%(18/83)であるのに対して,ワルファリン継続群で4.3%(2/43,P=0.013)と,ヘパリン置換群で出血の危険性が有意に高いことを報告した
26).ただし,ワルファリン服用者に対する高危険度内視鏡処置のヘパリン置換時とワルファリン継続下,あるいはDOAC変更時との有効性と安全性を検討したランダム化比較試験は未だ報告されておらず,エビデンスは不十分であることに変わりはない.
Ⅳ DOAC服用者に対する消化器内視鏡
前述のガイドライン改訂版
2)では,出血高危険度の消化器内視鏡処置時には,DOACは前日まで継続内服して処置当日の朝から中止するとともに,出血の徴候がない場合には翌日の朝から内服を再開することを推奨している.ただし,血栓塞栓症を発症する危険性の高い症例では処置後より翌日朝のDOAC内服再開時までヘパリン投与を対応することも認可している(Table 4).
非弁膜症性心房細動症例に対するDOAC4剤の有害事象を評価したメタ解析では,DOACはワルファリンに比較し消化管出血のリスクを約25%増加させる(Risk Ratio=1.25,95%CI:1.01-1.55,P=0.043)
27).DOACの消化管出血のメカニズムとして,ワルファリンと異なり経口投与されたDOACが血中に吸収されずに消化管内に残存し,直接消化管内で止血機序を阻害することで,出血を助長する可能性も考えられている
15).すなわち,DOACを使用している時点で,ワルファリン以上に高い消化管出血のリスクを伴うことを前提として対応することが重要である.
DOAC服用者に対する消化器内視鏡診療は,諸外国のガイドラインでも対応が明記されている.米国では高危険度内視鏡処置においては1-4日間の事前の休薬が腎機能や薬剤の種類に応じて定められている
28).また,英国(BSG)/欧州(ESGE)のガイドライン
29)では,高危険度内視鏡処置時には,少なくとも2日前から休薬し,処置1-2日後[超高危険度処置(EMR/ESD):3日後以降]から再開することが明記され,本邦のガイドラインよりも長い休薬期間を設けているのが特徴である.実際にBSG/ESGEガイドラインの妥当性を検討した前向きコホート研究
30)では,高危険度内視鏡処置時にはDOAC服用者の11.9%(95% CI:7.8-17.2%)に術後消化管出血が発症した.また,休薬期間別の検討では,ガイドラインに遵守した休薬群で後出血率が6.6%であるのに対し,休薬延長群で7.7%と両群間で明らかな差は認めず(P=0.76),高危険度内視鏡処置後の休薬期間は処置1-2日後が適切と思われる.
抗血栓薬非服用者とDOAC服用者との高危険度消化器内視鏡時の術後消化管出血率についての比較検討をTable 5に示す
26),31)~35).高危険度消化器内視鏡時のDOAC服用者の術後消化管出血率は7.9%-22.2%であり,抗血栓薬非服用者の0.5%-3.4%と比べて高危険度消化器内視鏡の種類や対象臓器にかかわらず,一様に高い術後消化管出血率を示した.ただし,Table 5の研究はエビデンスレベルが低い後方視的観察研究のみであり,今後前向き研究で明らかにしていく必要がある.
DOAC内服者におけるヘパリン置換は,ワルファリンと同様にDOAC継続内服時と比較して術後消化管出血の危険性は有意に高い(OR=1.52,95%CI:1.25-1.85,P<0.001)
36).さらに血栓塞栓症の発症を抑制せず,後出血のリスクが増強すると報告している
30).DOAC内服症例でもヘパリン置換は高い術後の消化管出血の危険性を持ち,さらに血栓塞栓症の抑制効果がないことから,治療内視鏡時にはヘパリン置換を選択すべきではない.
「直接経口抗凝固薬(DOAC)を含めた抗凝固薬に関する追補2017」
2)では様々な背景を基に臨床の場において多くの可能性のある選択肢を提示されており,それらの方法の妥当性について今後の臨床データの蓄積や臨床研究によって検証し,エビデンスを蓄積していくことが必要である.
Ⅴ DOACの今後の展望;薬理学的個人間差の可能性
抗血栓薬服用者の消化器内視鏡後の消化管出血のリスク因子は患者側因子(年齢,既往歴,透析歴,遺伝学的背景等),処置関連因子(腫瘍の大きさ,占拠部位,処置内容,処置時間等),および薬剤側因子(抗血栓薬の種類,内服量等)により規定されている
25).以前より患者側因子や処置関連因子においてDOAC内服症例における内視鏡処置後の消化管出血の高危険群の絞り込みを試みる検討は多く行われているが
37),DOAC自体の薬剤種の特性,薬物動態,薬物代謝の個人間差について検討した報告は未だ十分ではない.
日常臨床の現場ではワルファリン内服者が消化管出血で受診した際にPT-INRが3.0以上と治療域を超えている場合もあり
4),消化管出血の原因としてワルファリンの過投与による過抗凝固状態であった症例も存在する.実際に,ワルファリンの処方医は薬効をモニタリングするためにPT-INRを定期的に測定し,評価を行っている
17),18).一方,DOACは頻回のモニタリングが不要である反面,日常診療で測定できる簡便なモニタリングする指標が存在しないことが臨床上の大きな問題である.現在,トロンビン阻害薬ではAPTTが,他の選択的Ⅹa阻害薬ではPT-INRが薬効をモニタリングする候補マーカーとなっているが,測定結果は使用試薬により大きく乖離することが知られており,APTTやPT-INRのみではDOACの薬効をモニタリングする指標としては不十分である
38)~40).
DOACの抗凝固作用は濃度依存性であり,大規模ランダム化比較試験では3種類の選択的Ⅹa阻害薬とも最低血中薬物濃度(トラフ濃度)と血栓塞栓症の発症リスクは負の相関を,有害事象である大出血エピソード(頭蓋内出血や消化管出血等)の発症率とは正の相関を認めた(Figure 3)
41)~43).すなわち,DOACのトラフ濃度が上昇すると,大出血の有害事象のリスクが上昇することとなる.そのため,DOAC服用者の消化器内視鏡処置後の消化管出血もトラフ濃度は重要なリスク因子である可能性が考えられる.
DOACの血中濃度は内服用量,年齢,体重,腎機能などに影響される
9)~12).特に年齢,体重,腎機能はDOACの薬理学的個人間格差に影響を及ぼすため,多くのDOACでは用法用量設定の重要な因子である(Table 1).また,一般的に欧米人と比較し日本人の血中濃度は高値を示すことが報告され,人種間差も存在することが明らかとなっている
44).DOACの薬物代謝に関与する薬物代謝酵素(CYP3A4,5)やトランスポーター(P-glycoprotein,APT-binding cassette transporter G2[ABCG2])をコードする遺伝子には遺伝的多型性があり,DOACの血中濃度や抗凝固作用に影響を及ぼすことが示されている
45),46).実際にアピキサバン内服時にはCYP3A5*1/*1型と比較して*3の保持者で,ABCG2 421C/C型と比較してABCG2 421A/A型で薬物血中濃度/用量比が有意に高くなることが報告されている
46).DOACは日常臨床の現場で固定用量にて投与されているが,上記のようにDOACの血中濃度を規定する因子の影響により,実際のトラフ濃度に個人間差が存在し,消化管処置後出血のリスクにも個人間差が存在する可能性が考えられる.
現時点ではDOACの薬物血中濃度を日常診療で簡易に測定することはできない.一方,抗Ⅹa活性は選択的Ⅹa阻害薬の血中濃度を良好に反映し,トラフ時の薬物血中濃度と正の相関を示すことから選択的Ⅹa阻害薬の体内での治療効果や薬物血中濃度を推定する代替の指標として有用となる可能性が考えられている(Figure 4)
47)~49).
以上のように,DOAC服用者の内視鏡施行症例において消化器内視鏡処置後の出血リスクに影響する因子と考えられるDOACの薬物血中濃度や抗Ⅹa活性,そして薬物血中濃度を規定する因子と実際の術後消化管出血イベントとの関連についての前向きの検討は未だない.現在,多施設共同の前向き研究にて「抗血栓薬服用者に対する消化器内視鏡診療ガイドライン(追補2017)」に準拠して高危険度消化器内視鏡である内視鏡的大腸ポリープ切除術やESDを受けたDOAC内服症例の薬物血中濃度や抗Ⅹa活性,遺伝子多型などの薬理学的因子が術後消化管出血発症をきたす高危険群を抽出する予測因子の同定を目的とした探索的研究が行われている(UMIN;000031930,000032017).本研究の研究結果によって,DOAC服用者における臨床上問題となる高危険度消化器内視鏡後の消化管出血と関連している因子が明らかとなることで,薬理学的な側面からDOAC服用者に対する消化器内視鏡における個別化治療の可能性が秘められており,その結果が待たれる.
Ⅵ おわりに
抗凝固薬服用者に対する内視鏡診療の現状についてガイドラインおよび追補版を交えながら概説した.抗凝固薬は消化器内視鏡において高い術後消化管出血のリスクを有し,その対応はガイドラインでも十分なエビデンスが確立しているとは言えない.特に,DOAC服用者の薬効モニタリング等,術後消化管出血に関わるリスク管理の観点から現行のガイドラインの検証を進めるとともに,多方面からの検討を行うことで安全な消化器内視鏡診療を提供していくシステムを構築していく必要がある.
文 献
- 1. 藤本 一眞, 藤城 光弘, 加藤 元嗣ほか.抗血栓薬服用者に対する消化器内視鏡診療ガイドライン.Gastroenterological Endoscopy 2012;54:2073-102.
- 2. 加藤 元嗣, 上堂 文也, 掃本 誠治ほか.抗血栓薬服用者に対する消化器内視鏡診療ガイドライン 直接経口抗凝固薬(DOAC)を含めた抗凝固薬に関する追補2017.Gastroenterological Endoscopy 2017;59:1549-58.
- 3. Blacker DJ, Wijdicks EF, McClelland RL. Stroke risk in anticoagulated patients with atrial fibrillation undergoing endoscopy. Neurology 2003; 61:964-8.
- 4. Choudari CP, Rajgopal C, Palmer KR. Acute gastrointestinal haemorrhage in anticoagulated patients:diagnoses and response to endoscopic treatment. Gut 1994; 35:464-6.
- 5. Yasaka M, Minematsu K, Yamaguchi T. Optimal intensity of international normalized ratio in warfarin therapy for secondary prevention of stroke in patients with non-valvular atrial fibrillation. Intern Med 2001; 40:1183-8.
- 6. Aithal GP, Day CP, Kesteven PJ et al. Association of polymorphisms in the cytochrome P450 CYP2C9 with warfarin dose requirement and risk of bleeding complications. Lancet 1999; 353:717-9.
- 7. Rost S, Fregin A, Ivaskevicius V et al. Mutations in VKORC1 cause warfarin resistance and multiple coagulation factor deficiency type 2. Nature 2004; 427:537-41.
- 8. Birman-Deych E, Radford MJ, Nilasena DS et al. Use and effectiveness of warfarin in Medicare beneficiaries with atrial fibrillation. Stroke 2006; 37:1070-4.
- 9. Connolly SJ, Ezekowitz MD, Yusuf S et al. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009; 361:1139-51.
- 10. Patel MR, Mahaffey KW, Garg J et al. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med 2011; 365:883-91.
- 11. Granger CB, Alexander JH, McMurray JJ et al. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2011; 365:981-92.
- 12. Xu H, Ruff CT, Giugliano RP et al. Concomitant Use of Single Antiplatelet Therapy With Edoxaban or Warfarin in Patients With Atrial Fibrillation:Analysis From the ENGAGE AF-TIMI48 Trial. J Am Heart Assoc 2016; 5:e002587.
- 13. Pollack CV Jr, Reilly PA, Eikelboom J et al. Idarucizumab for Dabigatran Reversal. N Engl J Med 2015; 373:511-20.
- 14. Okada M, Okada K. Exfoliative esophagitis and esophageal ulcer induced by dabigatran. Endoscopy 2012; 44(Suppl 2 UCTN):E23-4.
- 15. Desai J, Granger CB, Weitz JI et al. Novel oral anticoagulants in gastroenterology practice. Gastrointest Endosc 2013; 78:227-39.
- 16. Gage BF, Waterman AD, Shannon W et al. Validation of clinical classification schemes for predicting stroke:results from the National Registry of Atrial Fibrillation. Jama 2001; 285:2864-70.
- 17. 日本循環器学会.循環器病の診断と治療に関するガイドライン2013:心房細動治療(薬物)ガイドライン(2013 年改訂版). http://www.j-circ.or.jp/guideline/pdf/JCS2013_inoue_h.pdf.
- 18. 日本脳卒中学会脳卒中ガイドライン委員会.脳卒中治療ガイドライン2015.協和企画,東京,2015.
- 19. Kodani E, Atarashi H, Inoue H et al. Use of warfarin in elderly patients with non-valvular atrial fibrillation--subanalysis of the J-RHYTHM Registry. Circ J 2015; 79:2345-52.
- 20. Palareti G, Legnani C, Guazzaloca G et al. Activation of blood coagulation after abrupt or stepwise withdrawal of oral anticoagulants--a prospective study. Thromb Haemost 1994; 72:222-6.
- 21. Constans M, Santamaria A, Mateo J et al. Low-molecular-weight heparin as bridging therapy during interruption of oral anticoagulation in patients undergoing colonoscopy or gastroscopy. Int J Clin Pract 2007; 61:212-7.
- 22. Douketis JD, Spyropoulos AC, Kaatz S et al. Perioperative Bridging Anticoagulation in Patients with Atrial Fibrillation. N Engl J Med 2015; 373:823-33.
- 23. Siegal D, Yudin J, Kaatz S et al. Periprocedural heparin bridging in patients receiving vitamin K antagonists:systematic review and meta-analysis of bleeding and thromboembolic rates. Circulation 2012; 126:1630-9.
- 24. Jaruvongvanich V, Assavapongpaiboon B, Wijarnpreecha K et al. Heparin-bridging therapy and risk of post-polypectomy bleeding:Meta-analysis of data reported by Japanese colonoscopists. Dig Endosc 2017; 29:743-8.
- 25. Mabe K, Kato M, Oba K et al. A prospective, multicenter survey on the validity of shorter periendoscopic cessation of antithrombotic agents in Japan. J Gastroenterol 2017; 52:50-60.
- 26. Yanagisawa N, Nagata N, Watanabe K et al. Post-polypectomy bleeding and thromboembolism risks associated with warfarin vs direct oral anticoagulants. World J Gastroenterol 2018; 24:1540-9.
- 27. Ruff CT, Giugliano RP, Braunwald E et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation:a meta-analysis of randomised trials. Lancet 2014; 383:955-62.
- 28. Acosta RD, Abraham NS, Chandrasekhara V et al. The management of antithrombotic agents for patients undergoing GI endoscopy. Gastrointest Endosc 2016; 83:3-16.
- 29. Veitch AM, Vanbiervliet G, Gershlick AH et al. Endoscopy in patients on antiplatelet or anticoagulant therapy, including direct oral anticoagulants:British Society of Gastroenterology(BSG)and European Society of Gastrointestinal Endoscopy(ESGE) guidelines. Endoscopy 2016; 48:385-402.
- 30. Radaelli F, Fuccio L, Paggi S et al. Periendoscopic management of direct oral anticoagulants:a prospective cohort study. Gut 2019; 68:969-76.
- 31. Niikura R, Yasunaga H, Yamada A et al. Factors predicting adverse events associated with therapeutic colonoscopy for colorectal neoplasia:a retrospective nationwide study in Japan. Gastrointest Endosc 2016; 84:971-82.e6.
- 32. Sanomura Y, Oka S, Tanaka S et al. Taking Warfarin with Heparin Replacement and Direct Oral Anticoagulant Is a Risk Factor for Bleeding after Endoscopic Submucosal Dissection for Early Gastric Cancer. Digestion 2018; 97:240-9.
- 33. Yamashita K, Oka S, Tanaka S et al. Use of anticoagulants increases risk of bleeding after colorectal endoscopic submucosal dissection. Endosc Int Open 2018; 6:E857-64.
- 34. Ono S, Ishikawa M, Matsuda K et al. Clinical impact of the perioperative management of oral anticoagulants in bleeding after colonic endoscopic mucosal resection. BMC Gastroenterol 2019; 19:206.
- 35. Yasuda R, Yoshida N, Murakami T et al. Multicenter Study of the Hemorrhage Risk after Endoscopic Mucosal Resection Associated with Direct Oral Anticoagulants. Gastroenterol Res Pract 2019; 2019:5743561.
- 36. Nagata N, Yasunaga H, Matsui H et al. Therapeutic endoscopy-related GI bleeding and thromboembolic events in patients using warfarin or direct oral anticoagulants:results from a large nationwide database analysis. Gut 2018; 67:1805-12.
- 37. Terasaki K, Dohi O, Naito Y et al. Effects of Guidelines for Gastroenterological Endoscopy in Patients Undergoing Antithrombotic Treatment on Postoperative Bleeding after Endoscopic Submucosal Dissection for Early Gastric Cancer:A Propensity Score-Matching Analysis. Digestion 2019:1-9.
- 38. Perzborn E, Strassburger J, Wilmen A et al. In vitro and in vivo studies of the novel antithrombotic agent BAY 59-7939--an oral, direct Factor Xa inhibitor. J Thromb Haemost 2005; 3:514-21.
- 39. Douxfils J, Mullier F, Robert S et al. Impact of dabigatran on a large panel of routine or specific coagulation assays. Laboratory recommendations for monitoring of dabigatran etexilate. Thromb Haemost 2012; 107:985-97.
- 40. Barrett YC, Wang Z, Frost C et al. Clinical laboratory measurement of direct factor Xa inhibitors:anti-Xa assay is preferable to prothrombin time assay. Thromb Haemost 2010; 104:1263-71.
- 41. Reilly PA, Lehr T, Haertter S et al. The effect of dabigatran plasma concentrations and patient characteristics on the frequency of ischemic stroke and major bleeding in atrial fibrillation patients:the RE-LY Trial(Randomized Evaluation of Long-Term Anticoagulation Therapy). J Am Coll Cardiol 2014; 63:321-8.
- 42. Ruff CT, Giugliano RP, Braunwald E et al. Association between edoxaban dose, concentration, anti-Factor Xa activity, and outcomes:an analysis of data from the randomised, double-blind ENGAGE AF-TIMI 48 trial. Lancet 2015; 385:2288-95.
- 43. Leil TA, Feng Y, Zhang L et al. Quantification of apixabanʼs therapeutic utility in prevention of venous thromboembolism:selection of phase Ⅲ trial dose. Clin Pharmacol Ther 2010; 88:375-82.
- 44. Tanigawa T, Kaneko M, Hashizume K et al. Model-based dose selection for phase Ⅲ rivaroxaban study in Japanese patients with non-valvular atrial fibrillation. Drug Metab Pharmacokinet 2013; 28:59-70.
- 45. Herink MC, Zhuo YF, Williams CD et al. Clinical Management of Pharmacokinetic Drug Interactions with Direct Oral Anticoagulants(DOACs). Drugs 2019; 79:1625-34.
- 46. Ueshima S, Hira D, Fujii R et al. Impact of ABCB1, ABCG2, and CYP3A5 polymorphisms on plasma trough concentrations of apixaban in Japanese patients with atrial fibrillation. Pharmacogenet Genomics 2017; 27:329-36.
- 47. Hinder M, Frick A, Jordaan P et al. Direct and rapid inhibition of factor Xa by otamixaban:a pharmacokinetic and pharmacodynamic investigation in patients with coronary artery disease. Clin Pharmacol Ther 2006; 80:691-702.
- 48. Frost C, Song Y, Barrett YC et al. A randomized direct comparison of the pharmacokinetics and pharmacodynamics of apixaban and rivaroxaban. Clin Pharmacol 2014; 6:179-87.
- 49. Mendell J, Noveck RJ, Shi M. A randomized trial of the safety, pharmacokinetics and pharmacodynamics of edoxaban, an oral factor Xa inhibitor, following a switch from warfarin. Br J Clin Pharmacol 2013; 75:966-78.
- 50. De Caterina R, Husted S, Wallentin L et al. New oral anticoagulants in atrial fibrillation and acute coronary syndromes:ESC Working Group on Thrombosis-Task Force on Anticoagulants in Heart Disease position paper. J Am Coll Cardiol 2012; 59:1413-25.
- 51.
ワーファリン添付文章.2019年1月改訂(第23版);エーザイ株式会社
- 52.
プラザキサカプセル添付文章.2019年11月改定(第11版);日本ベーリンガーインゲルハイム株式会社
- 53.
イグザレルト錠添付文章.2020年2月改定(第2版);バイエル薬品株式会社
- 54.
エリキュース錠添付文章.2020年1月改定(第1版);ブリストル・マイヤーズスクイブ株式会社,ファイザー株式会社
- 55.
リクシアナ錠添付文章.2020年1月改定(第1版);第一三共株式会社





