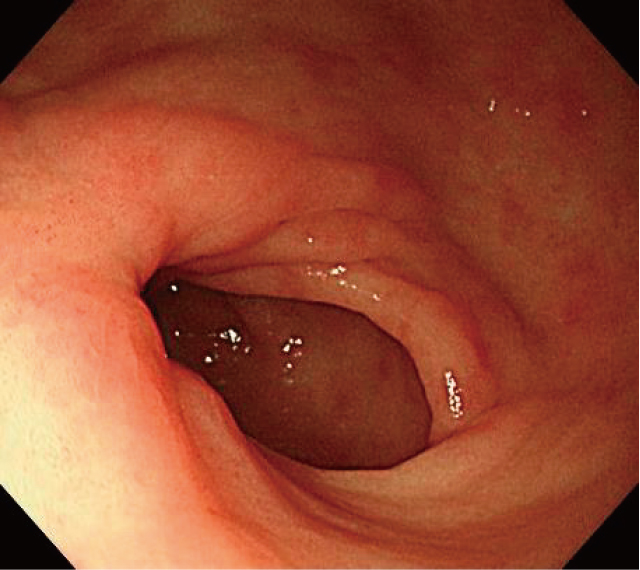
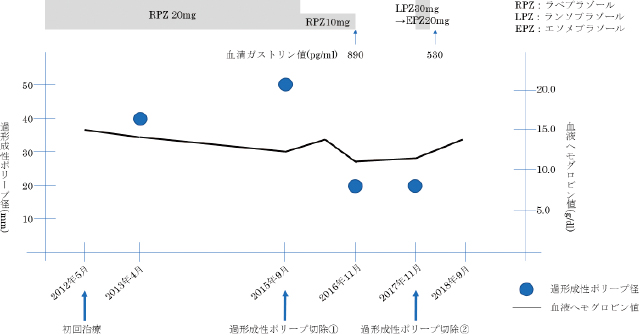
要旨
症例は69歳男性.前庭部大彎の胃腺腫に対して内視鏡的粘膜下層剝離術(以下ESD)を施行した.病理結果はtubular adenomaであり,病理組織学的に治癒切除であった.ESD時に認めたH. pylori感染は経過の中で自然除菌されたものの,ESD瘢痕部に過形成性ポリープが発生し,1年後に40mm大,3年後に50mm大へと増大傾向を示したため同腫瘍をESDにて切除した.しかし同部位に過形成性ポリープの再発を認め,悪性疾患が否定できないため再度ESDを行うとともに,再発予防のためにトリアムシノロンアセトニド80mgの局注療法を施行した.その後は1年8カ月の経過観察で再発は認めず,胃ESD後瘢痕部に生じる過形成性ポリープに対して,ステロイド局注療法が有用である可能性が示唆された.
Ⅰ 緒 言
現在,胃の上皮性腫瘍に対して内視鏡的粘膜下層剝離術(endoscopic submucosal dissection:ESD),内視鏡的粘膜切除術(endoscopic mucosal resection:EMR)などの低侵襲な内視鏡的切除術が普及しているが,まれに切除後の瘢痕部分に原疾患の遺残とは異なる良性の隆起性病変を認めることがあり,多くは過形成性ポリープであると報告されている
1)~13).その発生機序についてはさまざまな原因で潰瘍底の肉芽組織の過度な増生や上皮の過形成が起こることによると考えられているが
13)未だ不明であり,確立された治療法がないのが現状である.
一方,広範な病変に対する食道や胃のESD後の狭窄予防としてステロイド局注の有効性が報告されており
14),15),ステロイドによって線維組織の増生が抑制されるためと考えられているが,内視鏡的切除後の過形成性ポリープ発生を抑制する目的でのステロイド局注の有効性についての報告はこれまでにない.
今回著者らは,胃腺腫に対して施行したESD後の瘢痕に繰り返し発生する過形成性ポリープに対して,切除後潰瘍にステロイドを局注したことでその後の過形成性ポリープの発生を予防し得た1例を経験したため若干の文献的考察を加え報告する.
Ⅱ 症 例
患者:69歳,男性.
主訴:右側腹部違和感.
既往歴:大腸腺腫,高脂血症.
家族歴:特記すべきことなし.
現病歴:2010年7月,腹部膨満感を主訴に当院受診.上部消化管内視鏡検査(esophagogastroduodenoscopy:EGD)で前庭部前壁に10mm大の平坦隆起性病変を認めた(Figure 1-a).生検診断はtubular adenoma, Group3であり,経過観察としていた.2012年5月のEGDで病変の形態に変化はなかったが,本人から治療の希望があったため内視鏡的切除目的に入院した.
入院時現症:身長161.3cm,体重66.5kg,体温36.0℃,血圧156/88mmHg,脈拍76回/分.意識清明.眼瞼結膜に貧血なし・眼球結膜に黄染なし.表在リンパ節触知せず.胸部に異常所見なし.腹部平坦,軟で圧痛なし.肝脾触知せず.下腿浮腫認めず.
入院時検査所見(Table 1):血液検査所見では脂質異常症以外に特記すべき異常所見は認めなかった.

臨床経過:2012年5月,胃腺腫に対してESDを施行した(Figure 1-b).切除標本の病理診断はtubular adenomaで大きさ9mm×9mm,断端陰性であった.使用したデバイスはFlexKnifeⓇ(Olympus Corporation,Tokyo,Japan),ITknife2Ⓡ(Olympus Corporation,Tokyo,Japan)で,局注液は生理食塩水を使用した.術後経過は順調で,ラベプラゾール(RPZ)20mgを内服とし,経過観察を行っていた.なお,ESD前の血清Helicobacter pylori(Hp)抗体価は29U/mlと高値であった.2013年4月,1年後の初回EGDにてESD瘢痕部に40mm大の山田Ⅲ型ポリープを認めた.生検ではhyperplastic polypの病理診断であったため経過観察としていた.Hp除菌治療は行っていなかったがこの時血清Hp抗体価は9U/ml,尿素呼気試験は0.3‰でともに陰性であった.2013年6月に脳梗塞を発症しシロスタゾールの内服が開始された.2014年3月,2015年3月のEGDでは形態,大きさに著変はなかったが,2015年9月のEGDではポリープは約50mmへ増大し形態も山田Ⅳ型へ変化を認めた(Figure 2-a).さらに初回ESD前の血液検査ではHb 15.0g/dlであったが,Hb 12.6g/dlと緩徐に低下しており,抗血小板薬を内服していたことによる同部位からの出血が懸念された.胸腹部CTや下部消化管内視鏡検査では他に貧血の原因を認めなかった.また上腹部痛症状を訴えるようになりball valve syndromeを来している可能性も考慮され,これらの理由より切除が必要と判断した.腫瘍径が大きく,瘢痕部の線維化が予想されたこととからEMRによる一括切除は困難であると考え,また増大傾向があることから悪性腫瘍の可能性を完全には否定できなかったため,2015年9月に2回目となるESDを施行した.切除標本の病理診断はhyperplastic polypで悪性所見はなく,大きさ45mm×33mm,断端陰性であった(Figure 2-b).術後はRPZ 20mgを8週間内服後,10mgを継続とした.2015年11月,2カ月後のEGDでは潰瘍面に再生上皮が出現していたがポリープの形成は認めず,貧血はHb 13.8g/dlへ改善していた.2016年11月,1年後のEGDでは以前と同様に瘢痕部に25mm大の過形成性ポリープの出現を認めた(Figure 3-a).この時までRPZを継続して内服しており血清ガストリン値(SGL)が890pg/mlと高値であったことから,プロトンポンプ阻害薬(PPI)による腺窩上皮の過形成が影響している可能性を考慮しRPZは中止して経過観察としていた.2017年10月のEGDでは病変の大きさに著変はなかったが,上腹部痛症状が再燃しており,Hb 12.9g/dlと貧血が再度進行していたことから2017年11月に3回目となるESDを施行した(Figure 3-b).ESD直後の潰瘍部に,肉芽組織の過剰な増生を抑える目的でトリアムシノロンアセトニド80mgの局注を行った.切除標本の病理診断はhyperplastic polypで大きさ23mm×19mm,断端陰性であった.術後はランソプラゾール30mgを2週間,その後エソメプラゾール20mgを8週間内服してPPIを中止とした.2018年2月,3カ月後のEGDでは潰瘍面に再生上皮の出現を認めたが,縦走する潰瘍底が一部残存していた.2019年7月,1年8カ月後の上EGDではESD後潰瘍瘢痕のみを認め,明らかなポリープの形成は認めず経過している(Figure 4,5).

Ⅲ 考 察
胃潰瘍の治癒過程において隆起性病変が発生することは古くから報告されているが
16),胃の上皮性腫瘍に対する内視鏡的切除後の潰瘍にも,遺残再発とは異なる同様の隆起性病変が発生することが報告されている.医学中央雑誌(1983年~2017年)で検索したところ本邦での症例報告としては18例であった(Table 2).症例の特徴としては男性,前庭部に多く,いずれも組織型は過形成性ポリープであり,今回の症例でも同様の特徴がみられた.ポリープに対する治療は,ポリペクトミーやESDによる切除を選択している例が10例,経過観察が6例,Hp除菌療法を行った例が2例であった.切除を選択した症例では,経過を確認できた5例中4例が切除後に再増大を来しており,高い確率で再発を来す可能性が示唆された.また,多数例の検討では,広瀬ら
5)は胃EMR後に抗潰瘍薬を使用した症例で,術後1年以上の経過で50例中11例(22%)に瘢痕隆起が発生すると報告している.河合ら
17)は,術後使用薬剤は不明だが3~6カ月の時点で34例中12例(35.3%)に認めるとしている.また稲葉ら
13)は術後2カ月の時点で77例中16例(20.8%)に認めたが,抗潰瘍薬の中止により14例は半年以内に平坦化したと報告している.いずれの報告でもL領域に有意に多いとされている.胃粘膜切除後のポリープの発生機序としては,①切除による粘膜損傷の修復過程において胃粘膜上皮が過剰再生するという機序,②H2ブロッカーやPPIにより胃粘膜の過形成が引き起こされるという機序,③胃蠕動運動による物理的な刺激の関与,④多発性ポリープを有し背景粘膜にポリープを生じやすい素因があること,⑤Hp感染状態による影響などが示唆されている
1),2),4),11).良性潰瘍の治癒過程では,血管透過性が亢進して炎症細胞浸潤が起き,線維芽細胞の増生により肉芽組織が形成され,その後再生上皮が潰瘍底を覆い治癒が得られる
18).この過程において①~⑤のいずれか,または複数の要因が影響して肉芽組織や上皮の過形成が起きることでポリープが発生するのではないかと推測される.本症例では病変部位と内服薬を考慮すると①~③が主に関与していたと考えられる.Hpについては,本症例では初回ESDの時点ではHp抗体価が陽性であり,その後除菌治療をしていないにもかかわらず2回目のESDの時点では陰性であった.これは,過去に自然除菌され抗体価が下がっていく経過を見ていたのかもしれないが,Hp抗体価が陰性となった後も過形成性ポリープは再発していたため,本症例の過形成性ポリープに関してはHp感染の影響は大きくなかったと推測される.

PPIについては,PPIによるSGLの上昇とHp未感染者に発生する過形成性ポリープの関連性が指摘されている
19).ガストリンは粘膜増殖作用があるため
20),PPI内服者ではその作用が亢進し過形成を引き起こすと考えられている.本症例でもSGLが高値であったことからガストリン刺激の関与が考えられるが,3回目のESD後はPPIを短期間で終了したことがポリープの発生に対して抑制的に影響した可能性がある.
胃粘膜切除後のポリープに対する治療方針に関して,Arantes Vらの検討では,胃ESDを施行された2,275人のうち28人に過形成性ポリープが発生したが,いずれも生検で腫瘍性変化を認めなかったことから経過観察でよいと報告している
21).そのため基本的には治療は要さないが,過形成性ポリープの中でも出血リスクがあるものやball valve syndromeの原因と疑われるものでは治療が検討されることがあり
22),23),本症例でも同様の理由から治療適応と考え切除を行う方針とした.しかし切除から1年後に再発を認めたため,再切除を行ってもさらに再発を繰り返す可能性が懸念された.
一方で,胃や食道の全周性に近いESD後潰瘍に対するステロイド局注が狭窄予防に効果的であると近年報告されており
14),15),ステロイドが炎症細胞浸潤や線維芽細胞の増生を抑制することで線維組織の増生を抑制して狭窄予防に働くと考えられている.われわれは,胃粘膜切除後潰瘍においてもステロイドにより炎症細胞浸潤や線維芽細胞増殖を抑制することで治癒が遷延して過度な肉芽組織の増生を予防する効果が期待できると考えた.既報において胃ESD後潰瘍に対するステロイド局注により術後出血や穿孔の頻度が増加したという報告はなく,安全性についても許容されると考えたため,十分なInformed ConsentのもとでESD後の潰瘍面にステロイド局注を行った(倫理委員会未承認).内視鏡治療後の過形成性ポリープに対して内視鏡的切除後にステロイド局注を行った報告は未だなく,今後同様の症例に対する治療方針を決定する上で興味深い症例と思われた.
Ⅳ 結 語
胃腺腫に対して施行したESD後に繰り返し生じた過形成性ポリープの発生を,内視鏡的切除後のステロイド局注にて予防し得た1例を経験した.
文 献
- 1. 大山 隆, 坂田 祐之, 後藤 祐大ほか.胃腺腫およびⅡa型早期胃癌の内視鏡的切除後に生じた過形成性ポリープの2例.胃と腸 1994; 29: 1315-8.
- 2. 石野 祐佐子, 大田 由己子, 熊倉 泰久ほか.急速に発育した胃過形成性ポリープの1例.Gastroenterol Endosc 1994; 36: 986-91.
- 3. 石賀 敬子, 北垣 一成, 安藤 章文ほか.早期胃癌に対する内視鏡的切除後に生じた過形成ポリープの一例.甲南病院医学雑誌 1995; 15: 25-8.
- 4. 今枝 博之, 岩倉 泰, 都築 義久ほか.早期胃癌の内視鏡的切除後に生じた巨大過形成性ポリープの1例.Gastroenterol Endosc 1996; 38: 2853-7.
- 5. 広瀬 昭一郎, 太田 肇, 早川 康浩ほか.早期胃癌,胃腺腫の内視鏡的切除後の瘢痕部に生じた良性の隆起性病変の検討.Gastroenterol Endosc 1996; 38: 846-50.
- 6. 萩谷 一男, 川崎 恒雄, 海山 智隆ほか.内視鏡的粘膜切除術後の切除瘢痕部に山田Ⅲ型ポリープを形成した未分化型早期胃癌の1例.消化器内視鏡の進歩 1997; 51: 178-9.
- 7. Yoshikane H, Asai T, Sakakibara A et al. Gastric hyperplastic polyp occurring at the resection site of gastric adenoma. Endoscopy 1999; 31: 563-5.
- 8. 七条 公利, 飯利 孝雄, 柳沢 介ほか.早期胃癌の内視鏡的切除後に瘢痕部に生ずる過形成性ポリープの検討.ENDOSCOPIC FORUM for digestive disease 1999; 15: 6-13.
- 9. 小尾 龍右, 藤本 誠, 岡 洋志ほか.内視鏡的粘膜切除術による瘢痕部に生じた胃過形成性ポリープの1例.ENDOSCOPIC FORUM for digestive disease 2007; 23: 33-6.
- 10. 上原 慶太, 加藤 信彦, 橋本 建夫ほか.ESD瘢痕部に認めた胃過形成性ポリープの1例.Progress of Digestive Endoscopy 2008; 73: 134-5.
- 11. 松井 文美, 青木 信也, 古土 井明ほか.早期胃癌の内視鏡的治癒切除後に生じた過形成性ポリープに対してHelicobacter pylori除菌療法が成功した1例.Gastroenterol Endosc 2009; 51: 207-12.
- 12. 下山 省二, 藤城 光弘, 矢作 直久ほか.胃腺腫の内視鏡切除後に発生し,Helicobacter pylori除菌療法とプロトンポンプ阻害剤投与期間の相違により異なる経過を示した2個の過形成性ポリープの1例.Gastroenterol Endosc 2010; 52: 2938-45.
- 13. 稲葉 知己, 石原 茂直, 水川 翔ほか.胃ポリープの自然史とmalignant potential EMR/ESD後に発生するポリープ.胃と腸 2012; 47: 1235-45.
- 14. Shoji H, Yamaguchi N, Isomoto H et al. Oral prednisolone and triamcinolone injection for gastric stricture after endoscopic submucosal dissection. Ann Transl Med 2014; 2: 22.
- 15. Nonaka K, Miyazawa M, Ban S et al. Different healing process of esophageal large mucosal defects by endoscopic mucosal dissection between with and without steroid injection in an animal model. BMC Gastroenterol 2013; 13: 72.
- 16. 伊東 進, 石川 公, 岸清 一郎ほか.隆起型胃潰瘍瘢痕について.Gastroenterol Endosc 1976; 18: 420-7.
- 17. 河合 隆, 川上 浩平, 武井 和夫ほか.内視鏡的粘膜切除(EMR)後潰瘍瘢痕部の内視鏡形態の検討.新薬と臨床 2004; 53: 1009-11.
- 18. 寺野 彰, 太田 慎一, 平石 秀幸ほか.消化管粘膜障害とその修復.Mebio 1994; 11: 16-23.
- 19. Miyamoto S, Kato M, Matsuda K et al. Gastric Hyperplastic Polyps Associated with Proton Pump Inhibitor Use in a Case without a History of Helicobacter pylori Infection. Intern Med 2017; 56: 1825-9.
- 20. Bhandari S, Bakke I, Kumar J et al. Connective tissue growth factor is activated by gastrin and involved in gastrin-induced migration and invasion. Biochem Biophys Res Commun 2016; 475: 119-24.
- 21. Arantes V, Uedo N, Morita Y et al. Polypoid nodule scar after gastric endoscopic submucosal dissection:results from a multicenter study. Endosc Int Open 2018; 6:E1198-203.
- 22. 伊東 傑, 山下 允孝, 井上 悌仁ほか.出血を契機に診断し得た胃過形成ポリープの1例.Progress of Digestive Endoscopy 2013; 83: 112-3.
- 23. 青松 直撥, 中村 雅憲, 長谷川 毅ほか.十二指腸に陥入しball valve症候群を来した胃過形成ポリープの1例.Progress of Digestive Endoscopy 2014; 84: 94-5.