2022 Volume 64 Issue 9 Pages 1533-1540
2022 Volume 64 Issue 9 Pages 1533-1540
腺窩上皮型胃腫瘍は腺窩上皮細胞への分化を示す胃型腫瘍である.Helicobacter pylori(H. pylori)未感染胃に発生する場合は,発赤調で表面顆粒状の小隆起として認められることが多く,肉眼像から「ラズベリー様」と呼ばれる.胃体部および穹窿部が好発部位であり,ほとんどが5mm以下で発見される.Narrow band imaging拡大観察では乳頭状/脳回様構造を呈し,窩間部は広く,拡張した異常血管が視認されることが多い.組織学的には腺窩上皮細胞に類似した腫瘍細胞で構成される上皮内腫瘍であり,本邦では胃型腫瘍の潜在的悪性度を考慮されて癌と診断されることが多いが,非浸潤性の上皮内腫瘍であることからWHO分類(2019)ではfoveolar-type gastric adenomaである.内視鏡所見が類似した病変として,H. pylori未感染者の過形成性ポリープや過誤腫があるが,多くは内視鏡所見による鑑別が可能である.
Foveolar-type gastric neoplasia (adenoma/carcinoma) refers to a gastric epithelial neoplasm with an immunophenotype characterized by gastric foveolar cell differentiation. This neoplasm presents as a small, reddish protruded polyp with a raspberry-like appearance in Helicobacter pylori-naïve gastric mucosa. The lesion commonly occurs in the gastric body or fornix and is small in size (≤5 mm). The papillary or gyrus-like microstructure, which typically shows a wide intervening portion and dilated irregular vessels is best viewed using narrow-band imaging with magnification endoscopy. Histopathologically, the lesion appears as an intraepithelial neoplasm with gastric foveolar cell differentiation. This tumor is usually diagnosed as carcinoma in Japan based on its gastric phenotype; however, it is classified as a foveolar-type gastric adenoma by the World Health Organization classification based on its non-invasiveness. The differential diagnosis in cases of H. pylori-naïve gastric mucosa includes a hyperplastic polyp or hamartoma, which shows similar morphological features; however, magnification endoscopy can distinguish between these lesions.
本邦のHelicobacter pylori(H. pylori)感染者数は1980年代の出生で10-20%,1990年代で5%,2000年代では2%以下に低下した 1).これにより,全胃癌の1%以下とされてきたH. pylori未感染胃腫瘍の報告が近年増加している.H. pylori未感染胃腫瘍は大きく5つに分けられ,①未分化型胃癌,②胃底腺由来の腫瘍,③腺窩上皮型胃腫瘍,④前庭部に発生する腸型形質を発現する腫瘍,⑤食道胃接合部に発生する癌が存在する 2).本稿では,H. pylori未感染の腺窩上皮型胃腫瘍について解説する.
腺窩上皮型胃腫瘍は,腺窩上皮細胞への分化を示す胃型形質の上皮性腫瘍である.H. pylori未感染胃に発生したものは,多くが発赤した表面顆粒状の小隆起を呈し,いわゆる「ラズベリー様」腺窩上皮型胃腫瘍と呼ばれる 3).肉眼所見が名称に付いている理由は,白色扁平隆起を呈する腺窩上皮型胃腫瘍が存在するためである.白色扁平隆起型には症候性と特発性があり,前者は家族性大腸腺腫症やその類縁疾患でみられる.両者ともに本邦では胃型腫瘍における潜在的悪性度から癌と診断されることも多いが,非浸潤性の上皮内腫瘍であり,WHO分類ではfoveolar-type adenomaである 4).なお,現行の胃癌取り扱い規約(第15版)には腺窩上皮型胃癌という診断名はないため,われわれはWHO分類の名称に準じて,foveolar-type gastric adenoma with raspberry-like appearance(FGA-RA)と報告しており 5),本稿でもその略称を使用する.
2015年2月~2020年3月に,島根大学医学部附属病院で切除された647例の胃上皮性腫瘍患者のうち,7.7%(50/647)がH. pylori未感染と診断され,その68%(34/50)がFGA-RAと診断された.平均年齢57±23歳,男女比22/12と中年男性に多かった.喫煙率・飲酒率は44.1%(15/34)・38.2%(13/34)であり,本邦の喫煙率(19.8-26.7%)・飲酒率(24.7-28.0%) 6)より高い傾向があった.癌の家族歴・既往はそれぞれ5.9%(2/34)・2.9%(1/34)と低く,また,家族性大腸腺腫症やその類縁疾患も認めなかった(Table 1).

患者背景(文献5から改変引用).
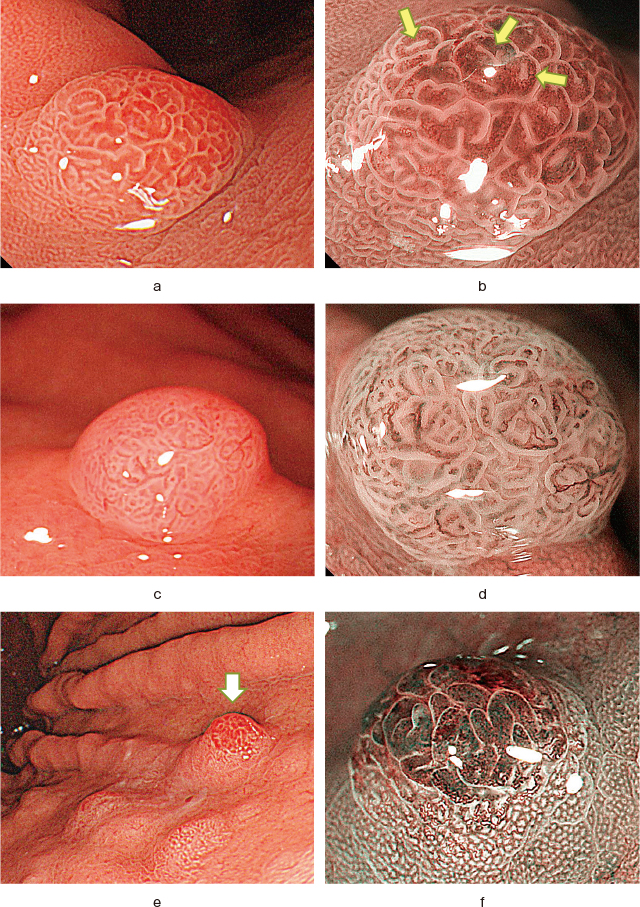
本腫瘍の典型的な内視鏡像をFigure 1に示す.胃体部または穹窿部の萎縮のない胃底腺粘膜に発生することが多く,しばしば多発性に認められる.腫瘍径は5mm以下のものが多く,鮮紅色の小隆起であり,いわゆるラズベリー様外観を呈する.Narrow band imaging(NBI)拡大観察では大小不同のある乳頭状/脳回様の腺構造を呈し,腺窩辺縁上皮を反映するwhite zoneは明瞭で,しばしば菲薄化して認められる.窩間部が広いことも特徴であり,内部に拡張した異常血管が透見されることが多い.半数以上で胃底腺ポリープが併存し,特に多発例で多く認められる 5).
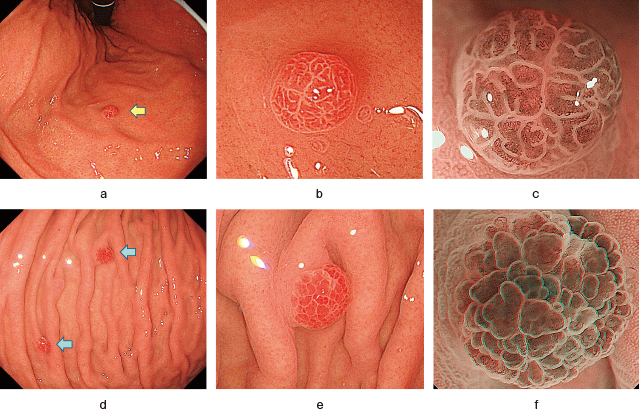
ラズベリー様腺窩上皮型胃腫瘍の内視鏡像.
a:萎縮のない胃体部前壁に約3mmの発赤隆起を認める(黄矢印).
b:近接観察では,粗大な腺構造が視認され,周囲粘膜と境界明瞭である.
c:NBI拡大観察では,窩間部は脳回様で,内部に走行不整を伴う血管が増生し,white zoneは概ね明瞭である.本腫瘍の典型的なNBI拡大像である.
d:胃体部大彎に2つの発赤隆起を認める(青矢印).
e:近接観察では鮮紅色の表面顆粒状の小隆起を呈し,典型的なラズベリー様の外観を呈する.
f:NBI拡大観察では,大小不同の乳頭状構造を呈し,white zoneは菲薄化している.
腫瘍腺管は乳頭状/管状の腺構造を呈し,腺窩上皮細胞に類似した腫瘍細胞が,腺窩上皮を置換しながら増生する.多くがlow-grade dysplasia相当であり,構造異形は弱く,mucin capを有し,核の極性も概ね保たれている.一方,high-grade dysplasia相当の病変では,mucin capが不明瞭化し,核の極性も低下しているが,これまで間質浸潤を認めた症例を経験していない(Figure 2).
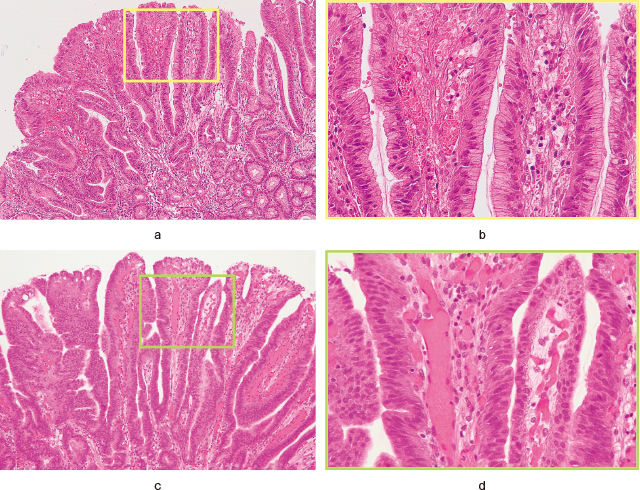
ラズベリー様腺窩上皮型胃腫瘍の病理組織像(文献5から改変引用).
a:軽度の構造異形を伴う管状/乳頭状の腫瘍腺管を認める.
b:腫瘍細胞はmucin capを有し,腺窩上皮細胞に類似し,核は大小不同と形態不整を伴うが,極性は概ね保たれており,FGA-RA(low-grade dysplasia)と診断した.
c:乳頭状に増生する構造異形の強い腫瘍腺管を認める.
d:腫瘍細胞のmucin capは確認できず,核クロマチンは増加し,核の極性は消失している.異形度は強いが,間質浸潤を認めず,FGA-RA(high-grade dysplasia)と診断した.
Figure 3に本腫瘍の免疫組織化学染色を示す.腫瘍細胞はMUC5AC(胃腺窩上皮の分泌型ムチン)が強陽性,MUC6(胃幽門腺・噴門腺,胃副細胞,Brunner腺の分泌型ムチン)はほぼ陰性,MUC2(小腸および大腸の杯細胞の分泌型ムチン)/CD10(a glycosylated transmembrane protein,腸型形質のマーカー)は陰性である.Ki-67は腫瘍表層を除いてびまん性に過剰発現することが多く,胃型腫瘍としての潜在的悪性度を示しており,本邦で癌と診断される理由の1つになっている.なお,p53蛋白はsporadicな発現のみで,これはH. pylori未感染の胃型腫瘍に共通した特徴であると考えている.また,β-cateninは細胞壁に認めるのみであり,核内異常集積は認めない.
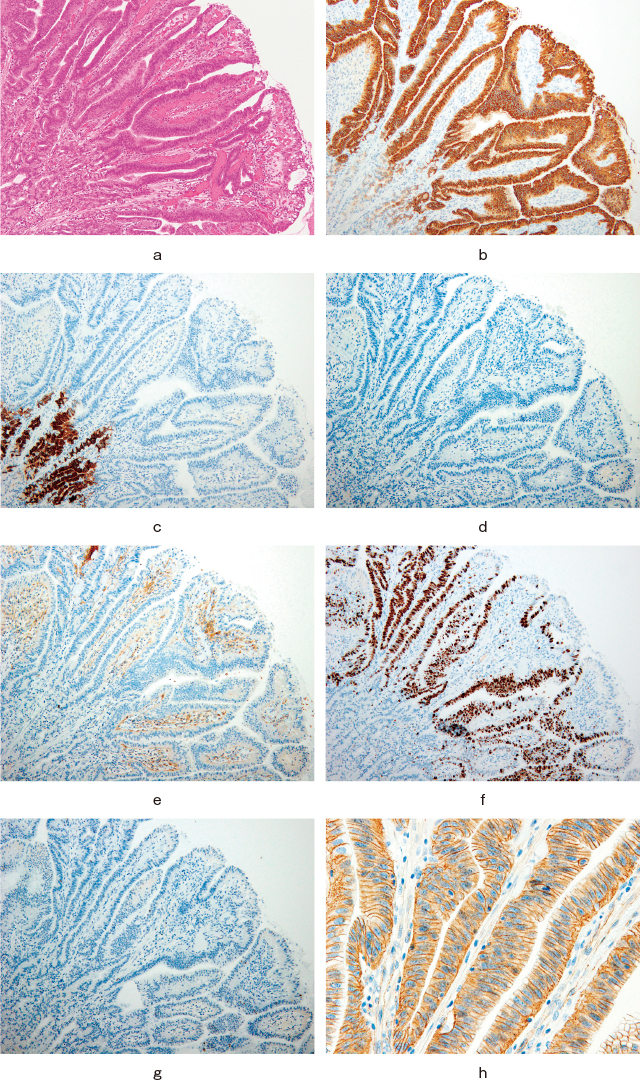
ラズベリー様腺窩上皮型胃腫瘍の病理組織像,免疫組織化学染色(文献9から改変引用).
a:管状/乳頭状に増生する構造異形の強い腫瘍腺管を認める.
b:抗MUC5AC抗体:腫瘍細胞全体に強陽性.
c:抗MUC6抗体:腫瘍細胞はほぼ陰性.
d:抗MUC2抗体:腫瘍細胞は陰性.
e:抗CD10抗体:腫瘍細胞は陰性.
f:抗Ki-67抗体:腫瘍細胞は表層部分を除いてびまん性に過剰発現している.
g:抗p53抗体:腫瘍細胞は陰性.
h:抗β-catenin抗体:細胞壁のみの染色,核の濃染は認めない.
鮮やかに発赤した隆起であり,注意して観察すれば拾い上げは比較的容易である.しばしば襞壁の間隙に隠れるため,胃体部の観察時には十分な送気が必要である.ラズベリー様の発赤隆起を呈する病変はFGA-RA以外にも存在し,未感染胃粘膜では主に過形成性ポリープと過誤腫,既感染胃粘膜では過形成性ポリープと癌などが挙げられる(Figure 4).FGA-RAはH. pylori未感染胃粘膜に発生する腫瘍であり,主な鑑別対象は過形成性ポリープとなる.
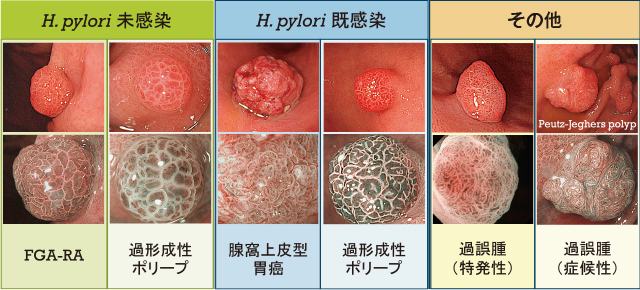
ラズベリー様の形態を呈する胃病変.
過形成性ポリープはH. pylori既感染胃だけでなく,未感染胃にも発生する.未感染胃の過形成性ポリープはFGA-RAと同様に,ほとんどがUM領域に発生し,5mm以下の発赤調の小隆起であり,一見すると両者は類似した肉眼像を持つ.当初は内視鏡像による鑑別に難渋した時期もあったが,症例を経験するうちに両者の鑑別のポイントも明らかとなってきた.
鑑別点は,色調,構造,white zone,demarcation lineの4つである.FGA-RAはほぼ全例が鮮やかな発赤調であるが,過形成性ポリープは半数で色調が淡い.また,FGA-RAは乳頭状または脳回様の表面構造を呈するが,過形成性ポリープは半数で管状構造を含んだ表面構造を呈し,腺窩辺縁上皮細胞の豊富な細胞質を反映してwhite zoneが厚く,white zoneの肥厚所見としてすでに報告している 7).最後に,FGA-RAは上皮性腫瘍なので全例でdemarcation lineが陽性であるが,過形成性ポリープは半数がdemarcation lineが部分的に不明瞭化する(Figure 5).
H. pylori未感染胃の過形成性ポリープ.
a:発赤したラズベリー様の小隆起を認める.
b:NBI拡大内視鏡では脳回様と管状(黄矢印)の腺構造が混在し,周囲粘膜との境界も不明瞭であり,過形成性ポリープの診断は可能である.
c:色調の淡い発赤隆起を認める.
d:NBI拡大観察で脳回様/乳頭状の不整な腺構造を認めるが,white zoneは肥厚している.
e:プロトンポンプ阻害剤内服者の肥厚した胃粘膜にラズベリー様の小隆起を認める(白矢印).
f:NBI拡大観察で脳回様の腺構造を呈し,white zoneも薄いが,周囲粘膜との境界は不明瞭である.
H. pylori既感染胃の胃型形質の腫瘍は,癌であれば脱分化やリンパ節転移率が高く,胃型腺腫(幽門腺腺腫)も癌の合併率が比較的高いことが知られており,ステージに応じた治療が必要である 8).一方,未感染胃に発生する胃型腫瘍(FGA-RA,胃底腺から発生する腫瘍,印環細胞癌)は,いずれも脈管侵襲やリンパ転移をほぼ伴わない.これらの腫瘍は治療介入がなくても予後に関連しない可能性もある.しかし,いずれも本邦では癌と診断される病変であり,自然史がいまだ不明で,内視鏡的切除も容易であるため,現時点では切除せざるを得ない病変と考える.FGA-RAに関しては腫瘍径も小さいため,内視鏡的粘膜切除術で十分である.
H. pylori未感染胃腫瘍は,20-30年後の本邦の胃腫瘍のほとんどを占めることが予想されている.一方,FGA-RAを含め,いずれも比較的稀で,食道胃接合部癌を除ければ悪性度も低いと考えられており,対策型胃癌検診の対象疾患になるかは現時点では疑問である.しかし,いまだ不明な点が多い腫瘍群であり,長期予後の解明には今後の症例集積が必要であろう.内視鏡医はこれらの特徴をよく理解した上で平素の内視鏡診療を行う必要がある.
本論文内容に関連する著者の利益相反:石原俊治(武田薬品工業株式会社,EAファーマ株式会社,田辺三菱製薬株式会社,日本化薬株式会社,株式会社JIMRO,アッヴィ合同会社)