2022 Volume 64 Issue 9 Pages 1579-1587
2022 Volume 64 Issue 9 Pages 1579-1587
食道疾患に対するEUSは,治療方針決定の一助となるためその有用性は高い.診断には技術的要素が大きく関係するため,その精度を高めるためには統一した手技で安定的な検査を行う必要がある.ソフトバルーンを用いてのEUSとジェル充満下のEUSの手技はそれぞれ一長一短があるが,その特徴を理解したうえで実践することで治療方針の決定の一助となる.適応となる病変は食道粘膜下腫瘍と表在型食道癌であり,特に後者においては,T1bが疑われ相対的適応としての内視鏡治療を検討している場合,確実に深部断端陰性で切除が可能かどうかの判断には非常に有用である.ソフトバルーンでは圧排や腫瘍直下でのリンパ濾胞に伴う深読みのリスクがあり,微小浸潤を認識できないことによる浅読みの可能性がある.ジェル充満では安定してできる部位で確実に行うことが重要である.
EUS for esophageal diseases is highly useful for determining treatment strategies. Because the diagnosis of esophageal disease is largely based on technical factors, a well-established examination with a standardized technique is needed to improve the accuracy of findings. Soft balloon EUS and gel immersion EUS have different pros and cons; however, practicing each diagnostic method would be helpful in gaining a working knowledge about each toolʼs characteristics. Esophageal submucosal tumor and superficial esophageal cancer are good candidates for diagnosing with EUS. When T1b cancer is suspected and endoscopic treatment is being considered, EUS can be very useful in determining the possibility of an endoscopic resection with a negative vertical margin. Regarding the soft balloon method, there are some potential risks of both overdiagnosis owing to compression or lymphatic follicles just below the tumor and underdiagnosis owing to microinvasion. In terms of the gel immersion method, importance should be placed on ensuring that the procedure is performed in a completely immerged area.
細径プローブを用いた食道疾患に対する超音波内視鏡検査(EUS)は,手技の特殊性と得られる画像の解釈の観点から敬遠されがちで,保険点数が低いこともあり実際に施行されているケースは少ないと思われる.
食道表在癌において,深達度診断は治療方針に大きくかかわるためその重要性は高い.しかし通常観察像,食道学会分類の拡大観察での血管像を駆使してもいまだ満足のいく成績は得られていないのが現状である.以前からEUSを用いての深達度診断がなされてきたが,その有用性においてはcontroversialである.その大きな要因として術者による格差が大きいことが推測され,またいくつかの手技で施行され統一されていないこと,病変の位置によっては管腔の広がりが得にくくscanが難しくなることなどの技術的要因があげられる.近年石原ら 1)により,食道表在癌における深達度診断において白色光観察や拡大を伴う狭帯域光観察(Narrow band imaging:NBI)にEUSを行うことで診断に上乗せ効果があるかの前向き試験が行われた.結果としてその効果は否定される結果となっている.しかし実臨床においては,EUS以外の診断に信頼がおけずEUSで確信が得られるケースや姑息的な治療における層構造の状態の確認など内視鏡治療を確実に施行するための客観的なデータの一つとして有用であるため,症例によって施行されているのが現状である.
より精度を高めるためには統一した手技で画一的に施行していくこと,さらにその手技の経験を高めることなどが必要と考える.本稿では,われわれが施行してきた方法と近年施行している新たな方法を紹介する.
食道表在癌と粘膜下腫瘍が主たる適応と考えられる.
食道表在癌の診断においては,内視鏡的粘膜下層剝離術(ESD)の適応となる病変であるのかESD以外の外科的手術などを行うべき病変かを判断する基準となる.平坦な病変で拡大観察でB1血管のみの典型的な上皮内病変(Epithelium:EP)もしくは粘膜固有層(Lamina Propria Mucosae:LPM)が想定される病変は積極的な適応からは外していいと考える.白色光観察上少し凹凸が見られる病変,拡大観察で白苔などの付着が見られ血管像での判断が難しい症例,表面に露出している部分の外に粘膜下腫瘍様の盛り上がりが見られる症例などはよい適応と考える.
食道粘膜下腫瘍においては,質的診断とともに病変の主座がどこなのか,どの層由来の病変なのかを判断する材料となる.発見されて初回のケースや治療を想定しているケースが主たる検査適応病変と考えられる.
これまでいくつかの手技が施行されてきている.われわれが推奨する手技としては,ソフトバルーンを用いたEUSとジェル(ビスコクリアⓇ)を充満させてのEUSを施行している.どちらも診断には有用と考えるが,準備の点とコストの点,観察できる部位などにおいて一長一短がある.まずはその準備と実際の手技を紹介し,具体的な症例を通して長所短所の解説を行う.
1.ソフトバルーン前準備が重要であり,基本的には内視鏡技師さんに準備を依存している.その手順を解説する.
①使用するソフトバルーン
市販のコンドームを用いる.生地が薄いものほどいい.中の潤滑油を水で洗浄し,適当な大きさに切る(Figure 1-a).

ソフトバルーンの作成方法.
a:使用するバルーンを作成するため,潤滑剤をきれいに洗い落とし,適切な大きさに切る.
b:鉗子孔口にT字管(MD807Ⓡ)を装着し,黒の鉗子栓とエクステンションチューブを装着する(左).スコープの吸引口から空気を蒸留水が流出してくるまで排出し,特性の栓で吸引孔を閉じる(右).
c:吸引金口もゴム栓で閉じる.
d:スコープの先端に準備したバルーンをEVL用のOリングを用いて装着する(左).余分なバルーンは取り除き,テープで固定する(右).
e:ソフトバルーン内に送水と脱水を繰り返しながら内部の空気を抜き取る.
f:AW洗浄アダプターで送気・送水口を塞ぐ.
g:送水管をゴム栓で塞ぎ,再度バルーンに蒸留水を挿入し,漏れがないことを確認する.
②使用するスコープ
Olympus社製のH290を用いている(これはH260でも可能).鉗子孔口にT字管(MD807Ⓡ)を装着し,その一つは新しい黒の鉗子栓を付け,もう一つにはエクステンションチューブを装着する.このエクステンションチューブから蒸留水を注入し,スコープの吸引口から蒸留水が流出してくるまで注入し,内部の空気の排出を行う.排出できたら特性の栓で吸引孔を閉じる(Figure 1-b).引き続き蒸留水の注入を継続し,吸引金口から蒸留水が出てきた段階でゴム栓で閉じる(Figure 1-c).スコープの先端に準備したバルーンを装着する.蒸留水を注入してバルーンを膨らませることを念頭に置き,スコープの先端からバルーンまでの距離を,少し余裕を持たせた位置で固定する.ここは重要な点で,どこの病変をscanするかにより,バルーンの長さを微調整している.具体的には食道胃接合部の病変をscanする場合は,それ以外の部位の時よりバルーン自体を小さめにしている.固定には内視鏡的静脈瘤結紮療法(Endoscopic variceal ligation:EVL)用のOリングを用いる.Oリングを装着具に取り付け,その中にスコープの先端を挿入してリングをリリースする.余分なバルーンは取り除き,テープで固定する(Figure 1-d).ソフトバルーン内に送水と脱水を繰り返しながら内部の空気を抜き取る(Figure 1-e).AW洗浄アダプターで送気・送水口を塞ぐ(Figure 1-f).送水管をゴム栓で塞ぎ,再度バルーンに蒸留水を挿入し,漏れなどがないことを確認する(Figure 1-g).最後に本体の送気がOFFになっていることを確認してスコープをセットする.
③実際の検査時
作成したソフトバルーン付き内視鏡を挿入する前に,まず観察用の内視鏡スコープを挿入し,病変の観察を行い,同時に病変や病変周囲の唾液などを洗い流す.観察後スコープを抜去して,ソフトバルーン付きの内視鏡を挿入する.この時,ソフトバルーンが薄いため,挿入に必要な視野はバルーン越しに確認できるためゼリーなどの塗布は不要である.病変部まで挿入した段階で装着している50mlのシリンジから蒸留水を送水しバルーンを膨らませる.引き続いて鉗子孔からMiniature probe 20MHzのプローブを挿入しバルーン内でscanできるような位置まで挿入する.
2.ジェルを用いてのEUSの場合①使用するジェル
用いるジェルはビスコクリアⓇで,50mlのシリンジに入れて用意する(Figure 2-a).
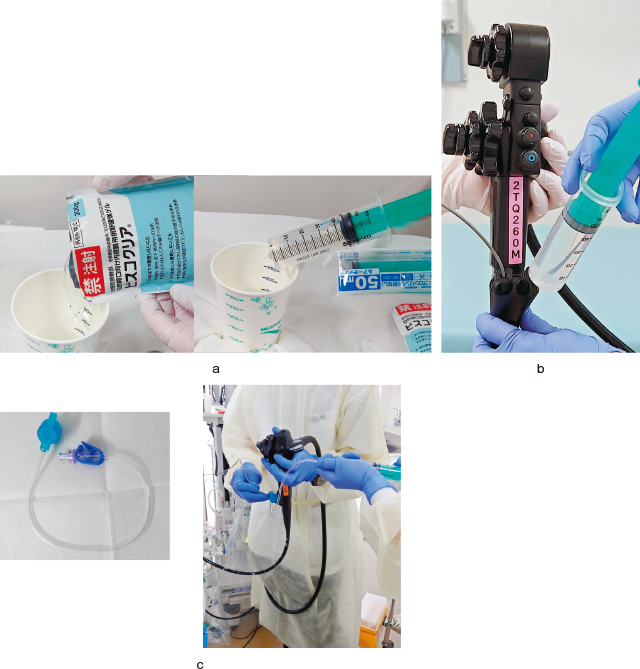
Gel immersion EUS.
a:ジェル(ビスコクリアⓇ)を用意する.紙コップに移し(左),50mlのシリンジで注入できるようにする.
b:2チャンネルのスコープで,片方にプローブを挿入し,もう片方からジェルを注入していく.
c:シングルチャンネルのスコープでは,バイオシールド(左)を装着し,プローブとジェルの注入を行う(右).
②使用するスコープ
スコープは2チャンネルのマルチベンドスコープを用いている.右の鉗子孔からプローブを挿入し,病変近傍に先端を留置したのち,助手が対側の鉗子孔からビスコクリアⓇをゆっくり注入していく(Figure 2-b).病変周囲が充満された段階でscanを開始する.前もって病変を観察する場合は,内視鏡の入れ替えを行うことを患者さんに説明しておく.処置用のスコープ(Q260JやH290T)などシングルチャンネルのスコープを用いる場合は,鉗子孔にバイオシールドⓇ(US endoscopy)を装着してジェルを注入していく(Figure 2-c).細径プローブが挿入された状態であるため,注入には抵抗感があるが,注入は十分可能である.
③実際の検査時
食道の蠕動がジェルの流出を促進して検査の妨げとなるため,あらかじめ検査開始時に抗コリン剤の投与を行う.もちろん使用不可のケースでは使用しないままの検査となる.スコープを挿入して病変の確認を行ったのち,あらかじめ装着しておいたバイオシールドを通して細径プローブをまず挿入する.引き続いてバイオシールドのイリゲーション部分からジェルを注入し食道内病変周囲をジェルで満たす.プローブを病変の位置に合わせscanを行う.
①正常層構造の描出(Figure 3)
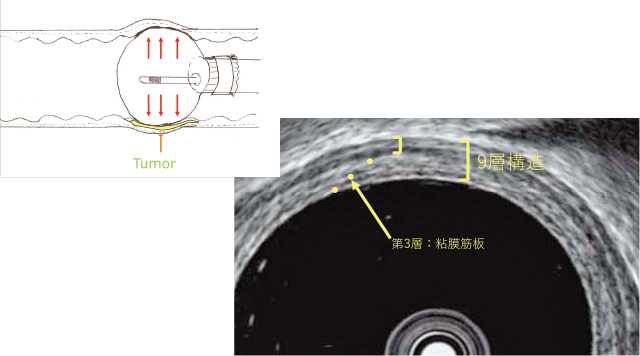
正常層構造のEUSでの描出像.
ソフトバルーンを脱気水で充満させ正常層構造を観察するとFigure 3のように9層構造として描出される.特に第3層が粘膜筋板に相当するhigh echo層であり,これが適切に描出されることで病変の深達度が粘膜内であるのか粘膜下層へ浸潤しているのかが判断できる.
②症例(Figure 4)
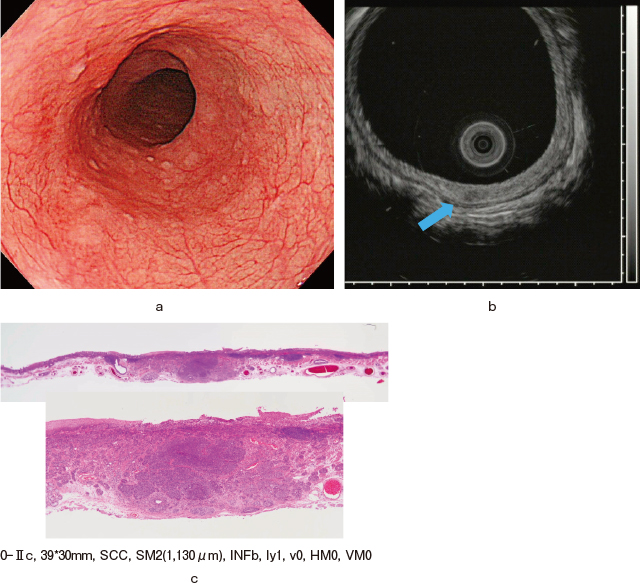
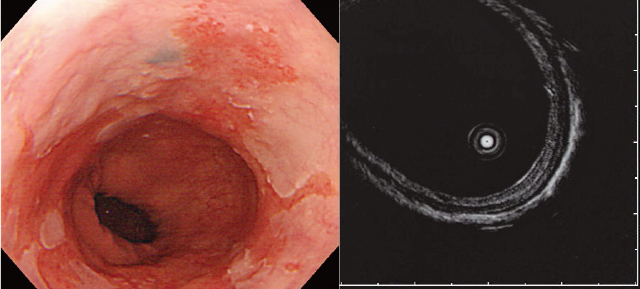
ソフトバルーンでのEUS.
a:左側壁中心の約半周性の病変である.
b:ソフトバルーンを用いてのscanでは,主病変は低エコーを呈する領域として描出され,同部で第3層が途絶している像が見られる.第5層は軽度外側に圧排されているものの菲薄化は見られていない.
c:切除後の組織像では,SM2(1,130μm)までの浸潤が見られた.
胸部中部食道左側壁中心の病変である(Figure 4-a).この病変に対してソフトバルーンを用いた細径プローブでscanを行うと,腫瘍部に一致して低エコーを主体とする限局的な壁肥厚像が描出される.その周囲と比較すると肥厚部で第3層が断裂していることがわかる.第5層のhigh echo層は外側に圧排されながらも菲薄化像などはなく粘膜下層(Submucosal layer:SM)2の深達度と診断できる(Figure 4-b).組織学的にSM2の1,130μmの浸潤であった(Figure 4-c).
2.ジェル充満症例(Figure 5)
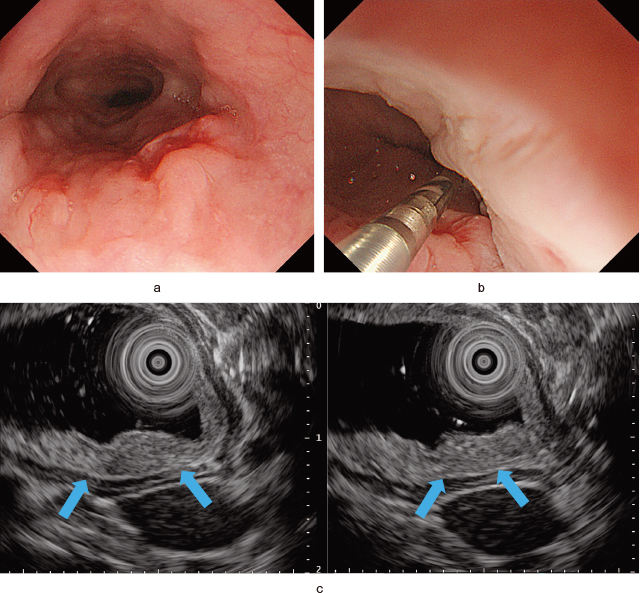
Gel immersion EUS.
a:胸部中部後壁からやや右側壁寄りの陥凹性病変である.
b:ジェルを充満され,細径プローブでscanを行う.
c:病変部で低エコーを呈する腫瘤像により第3層が断裂している像が確認される(左).Scanする部位によっては第3層が保たれている(右).
胸部中部食道後壁右側よりの陥凹性病変である(Figure 5-a).病変部分の唾液を洗い流しすぐscanできるように細径プローべを挿入しておく.ジェルを2チャンネルスコープの場合はもう一つの鉗子孔から,シングルチャンネルのスコープの場合はバイオシールドを通して注入する.空気が押し流され病変がジェルで満たされた段階でscanを開始する(Figure 5-b).Figure 5-cに示すように病変周囲では第3層が描出されているが,病変中心部ではそれが途絶している像がとらえられる.また他の部分をscanすると低エコーを呈する部分が第4層を占め,少し第5層が外側に圧排される像が見られる(Figure 5-c).SM2の深達度と診断できる.
長所
病変の位置にかかわらずscanが可能である.頸部食道や食道胃接合部でもバルーンを膨らませてscanを行うことができる.
Figure 6はBarrett食道癌の症例で同病変をscanした像である.層構造が9層構造として描出されている.
白色光観察(左)で1時から2時方向に病変が存在し,同部をscanする(右)と9層構造が描出され,層構造の乱れが認められなかった.
短所
①準備が煩雑である.技師の手を煩わせる形となるが,経験値が増すと準備には5分以内で可能となる.
②病変とバルーンとの間に空気などが入り込むとair shadowで腫瘍像の一部が観察ができなくなり,病変の評価が難しくなる.
③基本的に病変をバルーンで圧排して得られた像で評価を行うため,それに伴う深読みをしてしまう可能性がある.特に第5層が病変とバルーンで圧排されるため,粘膜下層浸潤癌では深読みしてしまうリスクがある.
以前112病変を対象として検討した結果(Table 1)では,深読みしたのは7.1%で腫瘍の圧排やリンパ濾胞などの存在が主な原因であった(Figure 7).浅読みしたケースは25%であったがこのうちの多くは粘膜筋板が保たれた形での浸潤であった(Figure 8).

ソフトバルーンを用いたEUS深達度診断.
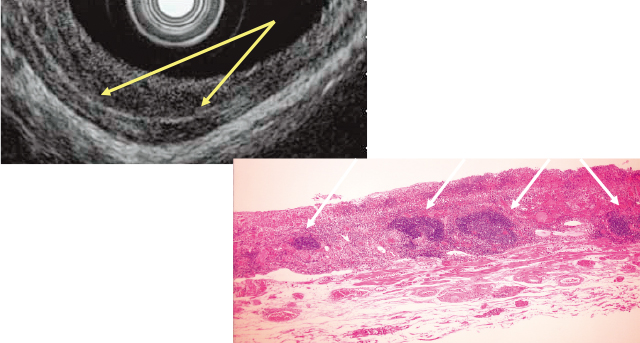
深読み症例.EUS像(左)では低エコーを呈する腫瘤像により第3層が途絶をきたし,粘膜下層までの浸潤が示唆された.組織学的検索(右)では,腫瘍直下にリンパ濾胞を形成する像が見られ,これを腫瘍浸潤像と判断して読影していた.
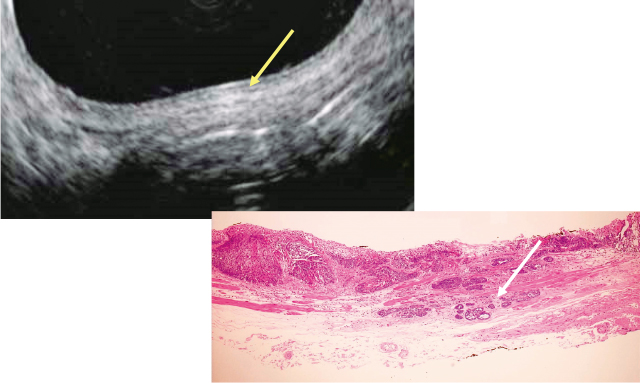
浅読み症例.EUS像(左)では層構造が確認でき深達度EP/LPMと判断したが,組織学的検索(右)では,粘膜筋板の構造を保ちながら粘膜下層まで腫瘍が浸潤している像が見られた.
長所
準備が簡単である.
断続的にジェルを注入してscanができる.病変の形態を認識しながら最深部が病変のどこに相当するのか確認がしやすい.
短所
病変の位置によってはジェルをためておくことが困難でscanができなくなる.特に頸部食道と食道胃接合部では難しくなる.
最近の報告では石原ら 1)が前向きにclinical T1病変に対して,非拡大観察と拡大観察にEUSを追加することでその診断率が向上するかの検討がなされた.それによるとこの時の診断方法においては,脱気水充満,ゼリー充満,バルーン法などで施行されている.EUSを追加することで6.6%深読みが増し,4.5%浅読みが減るという結果であった.また非拡大と拡大観察での深達度正診率が72.9%であるのに対し,EUSを追加しても74%であった.Mizumotoらの報告 2)では,174例で検討し,EUSの深達度正診率は全体で70%,亜分類で見るとEP/LPMの正診率は84%,粘膜筋板(Muscularis mucosae:MM)/SM1では29%,SM2以深では40%であった.結論としてNBI拡大内視鏡検査のほうが有用性が高い可能性があるとしている.May Aら 3)は,前向き試験で100例を対象として,水充満法で20MHzの細径プローブを用いてEUSを施行し,正診率79.6%を得ている.内視鏡観察での深達度診断83.4%と比較して遜色ないデータを出している.診断はT1aとT1bで評価を行っているが,T1aにSM1を加える形で評価すると,正診率がEUSで86%に,内視鏡診断で89%になるとしている.またThosani Nら 4)は19文献でのsystematic reviewを行っている.これによると,日本からの報告か日本以外の国からの報告で診断率に差が生じ,扁平上皮癌で見るとEUSでの深達度正診率はT1aとT1bの鑑別で81%,浅読み15%,深読み4%であった.著者らはEUSの役割は,内視鏡的粘膜切除術(EMR)やESDの治療として適応とならないT2病変の同定にあると述べている.
EUSの有用性は単に正診率などの数字だけでは表せないところにある.数字をあげようとすると,明らかなEP/LPMの割合を増やせば,全体の正診率が上昇する.しかし臨床的に有用な場面は治療方針の決定に影響を及ぼす場面である.特に周囲リンパ節がなく,病変をESDとその後の追加治療で対応しようとする場合などは実際ESDが可能な病変かどうかを判断するには客観的な所見が得られやすく,有用性が高い.T1b病変に対して,ESDを施行しその後追加の化学放射線療法を行う治療が外科的手術の代替治療として認知されてきた 5)現状では,限られた症例においては有用性が高いものと考える.
謝 辞
ソフトバルーン作成画像を提供いただいた今本たか子さんにこの場を借りて謝辞を送らせていただきます.
本論文内容に関連する著者の利益相反:なし