2024 Volume 66 Issue 3 Pages 286-292
2024 Volume 66 Issue 3 Pages 286-292
早期消化管癌に対する内視鏡治療後の粘膜欠損部に対して,後藤らにより内視鏡用軟性持針器と逆戻り防止弁付き縫合糸を用いた内視鏡的手縫い縫合法(endoscopic hand-suturing;EHS)が開発された.当科にて内視鏡用軟性持針器を用いてEHSを施行した5症例(胃3症例,大腸2症例)を検証した.EHSは全例で完遂でき縫合時間も既報と遜色ない結果であった.導入初期には胃症例で創部離開を1例認めたものの,全例で治療後の合併症は認めなかった.各病変の縫縮に要した時間は切除時間と同程度であったが,経験症例数が増えるに従って1針あたりの縫合時間は短縮傾向であった.EHSは様々な臨床応用が期待されるが,新規導入にあたってはトレーニングモデルを活用し十分な準備が必要である.
Goto et al. developed an endoscopic hand-suturing (EHS) technique using a flexible endoscopic needle holder and sutures with anti-reversal barbs for mucosal defects after endoscopic treatment of early-stage gastrointestinal cancers.
We examined five cases, three gastric and two colorectal cancers, in which we performed EHS using EHS devices (SutuArtⓇ) at our hospital. An early phase case showed wound dissection, but EHS was completed in all cases, and no post-procedure complications occurred. The resection and suture times for each lesion were similar, and suture time per stitch may shorten as the number of procedures increase. Although EHS is clinically promising, adequate preparation using a training model is necessary for its new introduction.
本邦において早期消化管癌に対する内視鏡的粘膜下層剝離術(ESD)は標準治療として広く普及している 1).内視鏡医の技術の進歩やESD関連デバイスの性能の向上により病変切除の手技は概ね確立した一方,切除後の創部に対する対応は旧来からほとんど変わっておらず,内視鏡治療後の粘膜欠損部は胃酸や食物,便汁等にさらされ,後出血や創傷治癒遅延が誘発されている可能性がある 2),3).一般的にESDにおける後出血率は1.7~6%と報告されているが 4)~6),抗血栓薬内服中の患者では10~23.3%まで上昇する 7)~11).
近年では後出血や遅発性穿孔等の治療関連合併症のリスクを減らすため様々な縫縮法が試みられているが 12),クリップによる粘膜-粘膜縫合では創部に対する把持力が不十分な場合があり,外科的縫合と同様の強度を持った縫合法の開発が課題とされていた 13).後藤らにより動物臓器を用いた研究やさらにヒトでの臨床試験を経て,軟性持針器と逆戻り防止弁付き縫合糸を用いた内視鏡的手縫い縫合法(endoscopic hand-suturing;EHS)が開発され 14),2022年にEHS専用ディスポーザブル内視鏡用軟性持針器(SutuArtⓇ,オリンパスメディカルシステムズ株式会社)が日本国内で使用可能となった(Figure 1).SutuArtⓇはこれまで内視鏡医が切望していた手縫い縫合を内視鏡のみで実現する革新的なデバイスである.今回当科におけるSutuArtⓇを用いたEHSの導入成績に関して報告する.

ディスポーザブル持針器SutuArtⓇ(オリンパス株式会社).
a,b:SutuArtⓇのラチェットと持針器の先端,ラチェット付き鉗子と逆戻り防止弁付き縫合糸(V-LocTM180クロージャーデバイス,コヴィディエン社).
2022年9月から2023年2月までの期間で当科において胃・大腸ESDを施行した52症例の中から,後述の適格・除外基準に従いEHSを行った.胃症例は3cm未満の早期胃癌を対象とし,噴門・幽門にかかる病変や穹窿部の病変は除外した.大腸症例は5cm未満の早期大腸癌で,技術的難易度を考慮し左側結腸または直腸病変を対象とした 14)~16).EHSを臨床で行うにあたり術者はESD施行経験1,000例以上のエキスパートに固定し,介助者はESD施行経験100例以上の医師2名の合計3名で行った.ESDにて病変を一括切除し,続いてSutuArtⓇを用いてEHSを施行したが,縫合は後藤らの手法に従い,逆戻り防止弁付き縫合糸V-Loc180クロージャーデバイス(コヴィディエン社)を使用した(胃症例では26mm,1/2周,大腸症例では17mm,1/2周) 2).針の通過による粘膜損傷を予防するため,胃症例では全例オーバーチューブを使用し,大腸症例に関しては透明キャップ(MH-588,オリンパス社)を装着し,キャップ内に針を収納した状態で体内に挿入した.胃ESD症例に関しては原則翌日に内視鏡検査を行い創部の縫合維持を確認した.ESDの2日後より胃症例では流動食,大腸症例では5分食から食事を開始しその後全粥まで食上げを行い退院とした.抗血栓薬に関しては消化器内視鏡学会のガイドラインに準じ周術期は休薬とし,再出血がないことを確認した上で治療翌日より再開した.症例・病変毎に局在,切除標本径,切除時間,縫合時間,縫合針数,創部離開の有無,治療関連合併症(後出血/遅発性穿孔)の有無を確認しEHSの導入成績を検証した.
早期大腸癌2病変(2例),早期胃癌4病変(3例)を対象に検討を行った(Table 1).病変の局在は大腸症例でS状結腸,直腸が1病変(平均病変径40.5±4.9mm),胃症例では体上部後壁が2病変,体下部大彎,前庭部小彎が1病変(病変径平均21.6±6.6mm)であった.切除標本長径は大腸病変で平均45.0±7.1mm,胃病変で平均28.8±6.0 mmで,一括切除率,EHS完遂率はいずれも100%であった.ESDでの病変切除時間は中央値56分(27-205),縫合時間は中央値52分(28-72)であった.縫合針数は中央値4針(3-6)で,縫合時間は初回が14.4分/針であったが徐々に短縮し後半の症例では9~10分/針となった(Figure 2).

症例.

1針あたりの縫合時間.
*2病変平均
早期胃癌4病変(3症例)のうち1例でのみ創部離開を認めたが(症例2,Figure 3),残りの全例において縫縮は維持されていた.また高度線維化を伴っていた胃体上部後壁の1例では術中穿孔を生じたが,気腹に対してMcBurney点から18Gの末梢静脈留置針を用いて穿刺し脱気をすることで処置継続可能であったため,病変切除後に引き続きEHSを行った.その後腹痛等の症状はなく術後3日目には食事を再開でき経過良好で10日目に退院となった(症例4,Figure 4).全症例において遅発性穿孔,後出血は生じなかった.
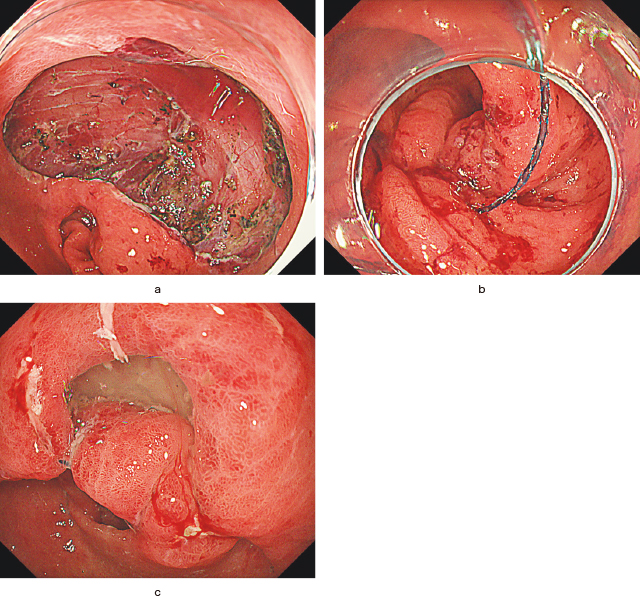
EHS後創部離開症例.
a:ESD後の粘膜欠損部.
b:SutuArtⓇによるEHS施行後(180°反転).
c:翌日の内視鏡検査では創部が離開していた.

術中微小穿孔例に対しSutuArtⓇによるEHSを施行した症例.
a:胃体上部後壁に30mm大の0-Ⅱa+Ⅱc病変を認める.
b:穿孔部(赤矢印),RDIモード.
c:1週間後も創部の縫縮は維持されていた.
当科にてSutuArtⓇによるEHSを施行した計6病変(5例)を検証した.EHSは全例で完遂でき縫合時間も既報と遜色ない結果であった 14)~16).導入初期には胃症例で創部離開を1例認めたものの,全例で治療後の合併症は認めなかった.また術中穿孔例であってもEHSを追加することで治療後の合併症はなく,比較的早期に食事が再開可能であった.手技に関しては経験症例数が増えるに従って1針あたりの縫合時間は短縮傾向であった.
EHS専用処置具の臨床での適用に関しては,後藤らにより2015年から初めてヒトを対象として内視鏡用軟性持針器と縫合糸を用いたEHSの臨床試験が開始され,3cm以下の病変においてESD施行後の粘膜欠損部に対する内視鏡的縫合の実行可能性が証明された 14).その後胃腫瘍を有する患者を対象とした国内3施設での単アーム前向き探索的臨床試験が開始され,EHSの完遂率97%,ESD後3日目における縫合維持率は83%,また術後胃を除いたEHS後縫合維持例においては後出血0例という良好な成績であった 15).また大腸腫瘍に対するEHSについては,阿部らにより単施設共同研究の結果が報告され,大腸ESD後の後出血予防に対する有用性が報告された 16).これらの臨床試験での有望な結果を踏まえ,2022年6月に内視鏡的手縫い縫合専用処置具ディスポーサブル持針器SutuArtⓇが本邦で発売され使用可能となった.
胃EHS症例に関して縫合維持の確認を行ったが,1例を除き全例で縫縮は維持されていた.創部離開を認めた胃前庭部小彎病変は当科でのEHS2例目の症例で,縫合糸の締め込みが不十分であったことが原因と推定した.前庭部では幽門に近づくにつれて管腔が狭くなり,さらに小彎側では反転しても縫合面が正面視となってしまうため針の刺入が難しいとされており,脱気して胃角部をできるだけ鈍化させたり,曲率半径の小さい針を用いたりすることが有用と報告されている 2).
ESD術中に穿孔を生じた1例(症例4)では,穿孔により固有筋層が菲薄化した部位で通常のクリップによる縫縮は逆に創部を広げてしまう懸念もありEHSを行った.1週間後も縫縮は維持されておりEHSが非常に有効な症例であったが,穿孔例に対するEHSの安全性は未だ確立されていない.本症例では,気腹に対して腹腔穿刺を行うことで全身状態が安定していたことや,この時点で数例のEHSを経験し手技が安定してきていたことからEHSを完遂することができたが,経験の少ない施設での術中穿孔例におけるEHSは慎重に判断すべきである.
本検討では,病変切除時間とEHSでの縫縮に要した時間は同程度であったが,1針あたりの縫縮時間は施行毎に短縮していった.EHSには適切な位置と角度での縫合針の把持が必要不可欠であるが,縫合針を垂直につかむためには針を消化管内の安定する位置に移動させ,軽く把持した状態でダウンアングルをかけ押し付けるようにしながら鉗子を閉じるのが肝要である 2).実際当科でSutuArtⓇによるEHSを臨床で開始する前には,事前にEHSの解説動画( https://www.olympus-medical.jp/gastroenterology/et/sutuart)を視聴した後,EHSトレーニングモデル(オリンパス社より貸与)を用いて複数回ハンズオントレーニングを行った.通常の外科の手縫い縫合は2つの手で行われるが,SutuArtⓇは内視鏡1本のみで行う手縫い縫合である.そのため初回は適切に針を把持するだけでも容易ではなかったが,繰り返すことで徐々にコツをつかむことができた.また,管腔内でのスムーズな運針にはSutuArtⓇの操作を担う介助者も含め操作に習熟する必要があるため,EHSの新規導入にあたってはモデルを用いたハンズオントレーニングから開始することが望ましい.
SutuArtⓇによるEHSはESD後出血の予防や将来的に全層縫合への臨床応用が期待されているが,技術的な課題も多く残されている 15)~17).今回の検討で導入期のラーニングカーブを示すことができた.しかし,単一術者の少数例の検証であり,さらに検討を重ね術者別の導入成績の解析等も必要である.また内視鏡によるEHSの手技の普及には,より簡便に施行可能なデバイスへの改良が期待される.
SutuArtⓇによるEHSは通常のクリップのみでは縫縮困難な症例に有用と考えられるが,内視鏡的手縫い縫合の新規導入にあたっては,トレーニングモデルを活用し十分な準備が必要である.
本検討の内容の一部は第126回日本消化器内視鏡学会北海道支部例会で報告し優秀演題賞を受賞した.
本論文内容に関連する著者の利益相反:山野泰穂(オリンパスマーケティング株式会社(内視鏡機器の図の無償提供))