抄録
There have been few epidemiological data on gastroenteropancreatic neuroendocrine tumors (GEPNETs) in Japan. First, we reported the epidemiology of pancreatic endocrine tumors (PNETs) and gastrointestinal neuroendocrine tumors (GI-NETs) in Japan in 2005. Next, we conducted the second survey regarding with GEPNETs patients who received treatment in 2010. A total of 3,379 individuals received treatment for PNETs in 2010. The number of patients in 2010 was an increase of about 1.2 times as compared to that in 2005. Non-functioning tumor (NF)-PNET constituted 64.5%, followed by insulinoma (20.9%) and gastrinoma (8.2%). On the other hand, an estimated 8,088 patients received treatment for GI-NETs. The number of patients in 2010 was an increase of about 1.8 times as compared to that in 2005. The locations of GI-NETs varied: foregut, 26.1%; midgut, 3.6%; and hindgut, 70.3%. The frequency of carcinoid syndrome in GI-NETs was only 3.2%. The results show that the number of Japanese patients with GEP-NET in 2010 was an increase compared in 2005.
はじめに
通常,neuroendocrine tumors(NETs)は比較的希な腫瘍で,進行も緩徐と考えられているが[1],米国の疫学データベースであるSEER(the Surveillance, Epidemiology, and End Results)studyによるとNET患者数は増加傾向にあり,1973年の発症率が1.09/100,000人であったのに対し,2004年では5.25/100,000人と約5倍に増加していた[2]。疾患の認識が普及したこと,診断技術の向上が寄与していると考えられ,患者数の動向については継続的なデータを集積し確認していく必要がある[3,4]。
一方,我が国における膵内分泌腫瘍(PNETs)および消化管神経内分泌腫瘍(GI-NETs)の実態は,2005年に受療した膵消化管NETs(GEPNETs)患者を対象に全国疫学調査が初めて施行され[5],徐々に欧米との相違などが明らかになった。欧米との大きな相違は,日本では非機能性PNETsにおけるmultiple endocrine neoplasia type 1(MEN-1)の合併率が欧米より低率であること,GI-NETsで中腸NETが少なく,カルチノイド徴候合併も少ないことであった[5]。本稿では新たに施行された第2回全国疫学調査[6]を基に,日本におけるGEPNETsの疫学の推移について総説する。
1.第2回GEPNETs全国疫学調査
2010年に受療したGEPNETs患者を対象に層化無作為法に疫学調査を6,339施設で施行し,3,366(PNETs 1,273,GINETs 2,093)症例が集積された。症例はWHO分類2010を用い[7],NET G1/G2およびNECに分類された。Mixed adenoneuroendocrine carcinoma(MANEC)およびhyperplastic and preneoplastic lesionsは今回の調査では対象外とした。症候性で血中ホルモン高値の患者は機能性に,無症候性および組織免疫染色やmRNAレベルで発現があっても血中のホルモン値が正常の場合は非機能性と定義した。
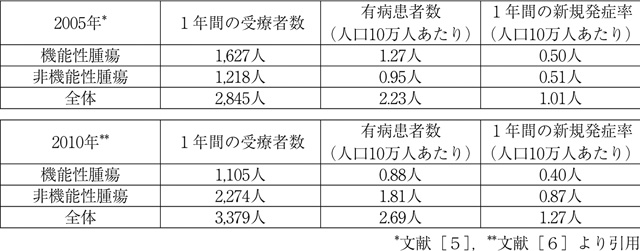
a.疫学(表1)
2010年に受療したPNETs症例は約3,379人と推定された。年間有病率は人口10万人あたり2.69人と推定され,2005年に比べ約1.2倍に増加していた。機能性PNETsは年間受療者数1,105人で,非機能性PNETsは2,274人であった。興味あることには,2005年では機能性PNETsの患者が多かったのに対し,2010年では非機能性のPNETsの患者が機能性に比し多かった。一方,2010年の新規発症数は人口10万人あたり1.27人であった。非機能性PNETsでは新規発症数が増えており,2005年の約1.7倍であった。
b.2010年におけるPNETs疾患分布およびWHO分類
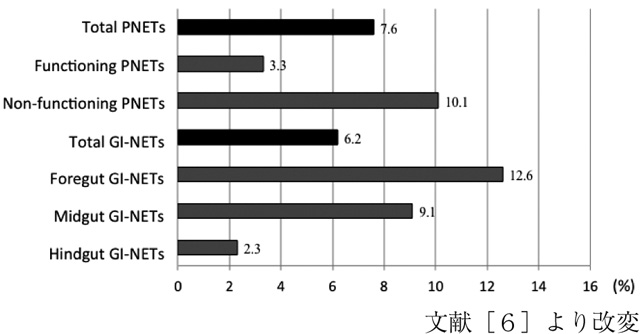
非機能性PNETsはPNETs全体の65.5%,機能性PNETsは34.5%を占めていた。機能性ではインスリノーマが最も多く20.9%,次にガストリノーマの8.2%であった。ついで,グルカゴノーマ,VIPオーマ,ソマトスタチノーマであり,それぞれ3.2%,0.6%,0.3%であった。また,PNETs全体におけるNECの割合は7.6%であった(図1)。非機能性PNETsではNECが10.1%と高頻度であった。
c.遠隔転移およびMEN―1合併率
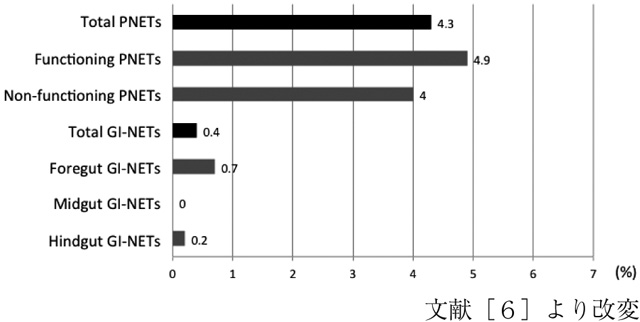
診断時に遠隔転移を認めた症例は19.9%であり,機能性で16.9%,非機能性で21.3%であった。機能性ではガストリノーマが30.2%と高率で,インスリノーマは9.3%であった。一方,MEN-1の合併はPNETs全体で4.3%であり(図2),機能性で4.9%,非機能性で4.0%であった。ガストリノーマはMEN-1の合併が高率で16.3%に認めたのに対し,インスリノーマでは0.8%であった。
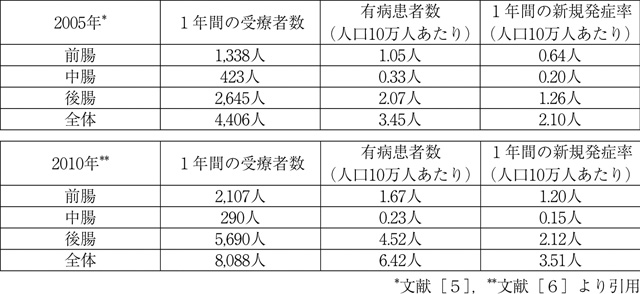
a.疫学(表2)
2010年に受療したGI-NETs症例は約8,088人と推定された。部位別では前腸約2,107人,中腸約290人,後腸約5,690人であった。年間有病率は人口10万人あたり6.42人と推定され,2005年に比べ約1.8倍に増加していた。2005年と同様に日本では中腸NETsの比率が低率であった。一方,2010年の新規発症数は人口10万人あたり3.51人であった。明らかに,前腸および後腸の発症率は2005年に比較し増加していたが,中腸の発症率に変化は認めなかった。
b.2010年におけるGI―NETsのWHO分類
GI-NETs全体におけるNECの割合は6.2%であった(図1)。前腸NETsでの割合は12.6%と最も高率であった。次いで,中腸NETsの9.1%,後腸NETsの2.3%であった。
c.遠隔転移,MEN―1およびカルチノイド徴候合併率
診断時に遠隔転移を認めた症例はGI-NETs全体で6.0%であった。部位別では前腸で8.6%,中腸9.8%,後腸NETs3.5%であり,中腸で最も高率であった。一方,MEN-1合併はGI-NETs全体で0.7%であり(図2),部位別では前腸で0.7%,中腸で0%,後腸0.2%であり,日本ではGI-NETsのMEN-1合併は希であった。さらに,カルイノイド徴候はGI-NETs全体の3.2%しか認めなかった。部位別では前腸4.2%,中腸17.1%,後腸1.1%であり,中腸で高率に認めた。
4.考察
第2回全国疫学調査で,日本における2010年のPNETsの年間受療者数は5年間で約1.2倍,GI-NETsでは約1.8倍に増加していた。興味あることに,2005年では非機能性PNETsの占める割合は42.8%であったのが,2010年では65.5%と増加しており,欧米の頻度に近づいていた[2]。この理由として,NETという疾患概念が一般臨床家に浸透してきたこと,つまりNETも念頭において診療を行うことが啓発されてきたことが推察される。さらに,超音波内視鏡(EUS)の普及により[8,9],経過観察されていた腫瘍に対してもEUS-FNA(EUS-guided fine needle aspiration)が容易に施行されるようになり,GEPNETsの病理診断が正確に行われるようになったためと考えられる[10,11]。
現在まで,日本におけるGEPNETsにおけるNECの頻度は明らかでなかった。日本に於けるGEPNETs全体でのNECの割合は6.7%であったが,韓国での報告[12]では,2.8%と報告されている。
現在までに,MEN-1,von Hippel-Lindau病(VHL),von Recklinghausen病,およびtuberous sclerosisの4つの遺伝子異常疾患が神経内分泌腫瘍と関連が示唆されている。MEN-1[13,14]およびVHL病[15]に合併するPNETsにおいては,サーベーランス方や治療方針も異なるため,必ず診断時にスクリーニングを施行する必要がある。MEN-1では非機能性PNETsを約80%に合併し,ガストリノーマまたはインスリノーマをそれぞれ約50%,約20%合併すると報告されている。一方,ガストリノーマの20~25%,インスリノーマの4~5%にMEN-1を合併すると報告されている[16]。今回の調査では,機能性PNETsでのMEN-1合併頻度は4.9%と欧米と変わりなかったが[16,17],非機能性PNETsでは4.0%と欧米に比しかなり低率であり,さらにGI-NETsのMEN-1合併も0.7%と低率であり人種の相違と考えられる[6]。
一方,GI-NETsに関して,2005年の調査同様に日本では中腸NETは少なく,部位別では前腸26.1%,中腸3.6%,後腸70.3%であった。欧米では30~60%が中腸由来であり[2,18,19],日本と大きな相違を認めた。最近Taiwan[20],中国[21],韓国[12,22]などのアジア諸国からもGEPNETsの疫学の報告がなされているが,日本と同様に中腸の患者の比率は低い。これはアジア人と欧米人との人種差によるものと考えられる。
5.今後の展望
進行性切除不能GEPNETsに対する抗腫瘍薬に関して,日本では未だ化学療法のコンセンサスがなく,保険適応外レジメンが殆どであった。近年,GEPNETsに対する様々な分子標的薬を用いた国際臨床試験の結果,mTOR阻害薬であるエベロリムス[23,24]とマルチキナーゼ阻害薬であるスニチニブ[25,26]が進行性PNETs(NET G1/G2)に有効であることが示され,さらに,2009年に中腸由来の転移性高分化型NETに対するオクトレチドLARの抗腫瘍効果が示され(PROMID study)[27],日本でも抗腫瘍薬として保険適用となった。NETでは腫瘍の機能性,進達度,転移の有無を正確に評価し,腫瘍の分化度および悪性度に合わせた治療が必要である[4,28~30]。外科的切除による全摘を目指すのが標準であるが,根治治療が困難な場合でも,原発巣や肝転移巣に対する減量手術が症状緩和や予後改善に有効とする報告もある[4,28,31]。一方,切除不能進行例では,腫瘍増殖を抑制し生命予後を改善させることと,臨床症状の改善の両方を目的とした治療が必要であるが[16],そのためには患者背景,特に疫学を十分に把握し欧米との相違を知ることは重要であり,特に5年間のGEPNETsの推移を調査した第2回全国疫学調査は有用であったと思われる。今後は新たに設立された日本神経内分泌腫瘍研究会(JNETS)で,症例登録制度が開始されることが決定しており,今後日本の疫学を世界に発信できることが期待される。
【文 献】
- 1. Metz DC, Jensen RT: Gastrointestinal neuroendocrine tumors. Gastroenterology 135: 1469-1492, 2008
- 2. Yao JC, Hassan M, Phan A, et al.: One hundred years after “carcinoid” :epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States. J Clin Oncol 26: 3063-3072, 2008
- 3. Modlin IM, Oberg K, Chung DC, et al.: Gastroenteropancreatic neuroendocrine tumours. Lancet Oncol 9: 61-72, 2008
- 4. Ito T, Igarashi H, Jensen RT: Therapy of metastatic pancreatic neuroendocrine tumors (pNETs):recent insights and advances. J Gastroenterol 47: 941-960, 2012
- 5. Ito T, Sasano H, Tanaka M, et al.: Epidemiological study of gastroenteropancreatic neuroendocrine tumors in Japan. J Gastroenterol 45: 234-243, 2010
- 6. Ito T, Igarashi H, Nakamura K, et al.: Epidemiological trends of pancreatic and gastrointestinal neuroendocrine tumors in Japan:a nationwide survey analysis. J Gastroenterol. 2014 Feb 6. [Epub ahead of print]
- 7. Bosman FT, Carneiro F, Hruban RH, et al.: WHO World Health Organization classification of tumors and genetics of the digestive system, IARC press, Lyon, 2010.
- 8. Ishikawa T, Itoh A, Kawashima H, et al.: Usefulness of EUS combined with contrast-enhancement in the differential diagnosis of malignant versus benign and preoperative localization of pancreatic endocrine tumors. Gastrointest Endosc 71: 951-959, 2010
- 9. Itokawa F, Itoi T, Sofuni A, et al.: EUS elastography combined with the strain ratio of tissue elasticity for diagnosis of solid pancreatic masses. J Gastroenterol 46: 843-853, 2011
- 10. Haba S, Yamao K, Bhatia V, et al.: Diagnostic ability and factors affecting accuracy of endoscopic ultrasound-guided fine needle aspiration for pancreatic solid lesions:Japanese large single center experience. J Gastroenterol 48: 973-981, 2013
- 11. Hosoda W, Takagi T, Mizuno N, et al.: Diagnostic approach to pancreatic tumors with the specimens of endoscopic ultrasound-guided fine needle aspiration. Pathol Int 60: 358-364, 2010
- 12. Gastrointestinal Pathology Study Group of Korean Society of Pathologists, Cho MY, Kim JM, et al.: Current Trends of the Incidence and Pathological Diagnosis of Gastroenteropancreatic Neuroendocrine Tumors (GEP-NETs) in Korea 2000-2009:Multicenter Study. Cancer Res Treat 44: 157-165, 2012
- 13. Ito T, Igarashi H, Uehara H, et al.: Causes of death and prognostic factors in multiple endocrine neoplasia type 1:a prospective study:comparison of 106 MEN1/Zollinger-Ellison syndrome patients with 1613 literature MEN1 patients with or without pancreatic endocrine tumors. Medicine (Baltimore) 92: 135-181, 2013
- 14. Niina Y, Fujimori N, Nakamura T, et al.: The current strategy for managing pancreatic neuroendocrine tumors in multiple endocrine neoplasia type 1. Gut Liver 6: 287-294, 2012
- 15. Igarashi H, Ito T, Nishimori I, et al.: Pancreatic involvement in Japanese patients with von Hippel-Lindau disease:results of a nationwide survey. J Gastroenterol 49: 511-516, 2014
- 16. Jensen RT, Cadiot G, Brandi ML, et al.: ENETS Consensus Guidelines for the management of patients with digestive neuroendocrine neoplasms:functional pancreatic endocrine tumor syndromes. Neuroendocrinology 95: 98-119, 2012
- 17. Oberg K, Eriksson B: Endocrine tumours of the pancreas. Best Pract Res Clin Gastroenterol 19: 753-781, 2005
- 18. Pavel M, Baudin E, Couvelard A, et al.: ENETS Consensus Guidelines for the management of patients with liver and other distant metastases from neuroendocrine neoplasms of foregut, midgut, hindgut, and unknown primary. Neuroendocrinology 95: 157-176, 2012
- 19. Oberg K: Diagnosis and treatment of carcinoid tumors. Expert Rev Anticancer Ther 3: 863-877, 2003
- 20. Tsai HJ, Wu CC, Tsai CR, et al.: The epidemiology of neuroendocrine tumors in taiwan:a nation-wide cancer registry-based study. PLoS One 8: e62487, 2013
- 21. Wang YH, Lin Y, Xue L, et al.: Relationship between clinical characteristics and survival of gastroenteropancreatic neuroendocrine neoplasms: A single-institution analysis (1995-2012) in South China. BMC Endocr Disord 12: 30, 2012
- 22. Lim T, Lee J, Kim JJ, et al.: Gastroenteropancreatic neuroendocrine tumors:incidence and treatment outcome in a single institution in Korea. Asia Pac J Clin Oncol 7: 293-299, 2011
- 23. Yao JC, Shah MH, Ito T, et al.: Everolimus for advanced pancreatic neuroendocrine tumors. N Engl J Med 364: 514-523, 2011
- 24. Ito T, Okusaka T, Ikeda M, et al.: Everolimus for advanced pancreatic neuroendocrine tumours:a subgroup analysis evaluating Japanese patients in the RADIANT-3 trial. Jpn J Clin Oncol 42: 903-911, 2012
- 25. Raymond E, Dahan L, Raoul JL, et al.: Sunitinib malate for the treatment of pancreatic neuroendocrine tumors. N Engl J Med 364: 501-513, 2011
- 26. Ito T, Okusaka T, Nishida T, et al.: Phase Ⅱ study of sunitinib in Japanese patients with unresectable or metastatic, well-differentiated pancreatic neuroendocrine tumor. Invest New Drugs 31: 1265-1274, 2013
- 27. Rinke A, Müller HH, Schade-Brittinger C, et al.: Placebo-controlled, double-blind, prospective, randomized study on the effect of octreotide LAR in the control of tumor growth in patients with metastatic neuroendocrine midgut tumors:a report from the PROMID Study Group. J Clin Oncol 27: 4656-4663, 2009
- 28. Ito T, Igarashi H, Jensen RT: Pancreatic neuroendocrine tumors:clinical features, diagnosis and medical treatment:advances. Best Pract Res Clin Gastroenterol 26: 737-753, 2012
- 29. Tsutsumi K, Ohtsuka T, Mori Y, et al.: Analysis of lymph node metastasis in pancreatic neuroendocrine tumors (PNETs) based on the tumor size and hormonal production. J Gastroenterol 47: 678-685, 2012
- 30. Ito T, Tanaka M, Sasano H, et al.: Preliminary results of a Japanese nationwide survey of neuroendocrine gastrointestinal tumors. J Gastroenterol 42: 497-500, 2007
- 31. Imamura M: Recent standardization of treatment strategy for pancreatic neuroendocrine tumors. World J Gastroenterol 16: 4519-4525, 2010