2018 Volume 67 Issue 5 Pages 734-739
2018 Volume 67 Issue 5 Pages 734-739
福岡地区の病院における血液培養の検査状況をアンケート調査した。回答項目は,病床数,2015年度の血液培養検査実施状況,使用機器,使用ボトル,培養日数,陰性ボトルのサブカルチャーの有無,採取時の皮膚消毒方法,血液接種時のホルダー使用の有無,陽性ボトルから直接菌液を調整した感受性試験の実施の有無,時間外に提出された血液培養検査の対応等である。18施設から回答が得られたアンケートの結果,陽性ボトルから直接菌液を調整した感受性試験の実施や,陰性ボトルのサブカルチャー,血液培養ボトルへの接種時のホルダーの使用は多くの施設で実施していなかった。血液培養の精度管理および質評価の観点から一般的に用いられている指標,採取時の消毒方法,時間外の対応等は施設によって異なり,血液培養検査の実態を把握することができた。
血液培養検査は,感染症診療において迅速正確な診断と適切な抗菌薬選択のために最も重要な検査である。血液培養検査における採取や検査方法,結果報告から解釈の仕方について,米国微生物学会(American Society for Microbiology; ASM)の血液培養ガイドライン(Cumitech 1C: Blood Cultures IV 2005; CUMITECH)1)や,日本臨床微生物学会の血液培養検査ガイド(以下,血液培養検査ガイド)2)などが公開されている。一方で,国内における血液培養検査の実施状況については施設間差があることが報告されており3),採取や手順,報告までのプロセスも同様に各施設によって異なることが予想される。そこで,今回,福岡地区の病院における血液培養の実施状況および時間外の対応について確認することを目的にアンケート調査を行ったので報告する。
2016年12月に福岡県臨床検査技師会福岡支部微生物部門から福岡地区の病院24施設にアンケートを配布し,回答があった18施設(75%)の結果を集計した。
1. 調査項目病床数,2015年度の血液培養検査実施状況,使用機器,使用ボトル,培養日数,陰性ボトルのサブカルチャーの有無,採取時の皮膚消毒方法,血液接種時のホルダー使用の有無,陽性ボトルから直接菌液を調整した薬剤感受性試験の実施の有無,時間外に提出された血液培養検査の対応等について情報を収集した。
2. 血液培養実施状況の指標についての定義指標の定義はCUMITECHおよび血液培養検査ガイドを参考とした。
総採取セット数は,好気・嫌気ボトル1セットを1件とし,好気ボトルのみ,または嫌気ボトルのみの場合も1件とカウントした。
1,000 patient-daysあたりの採取セット数は,総採取セット数÷在院患者延べ数×1,000)とした1)
複数セット採取率は,(総採取セット数-1セット採取数)÷総採取セット数×100(%)2)とした。
陽性率は,陽性セット数÷総採取セット数×100(%)とし,汚染率は,汚染と判定されたセット数÷総採取セット数×100(%)とした。汚染の判定基準は,コアグラーゼ陰性ブドウ球菌,Propionibacterium acnes,Micrococcus属,緑色連鎖球菌,Corynebacterium属,Bacillus属が2セット以上採取されたうち1セットのみ陽性となったものとした4)。
アンケート調査結果を,Table 1, 2,及びFigure 1に示す。
| 回答数 | 中央値 | 最小値 | 最大値 | |
|---|---|---|---|---|
| 病床数 | 18 | 359.5 | 135 | 1,275 |
| 総採取セット数 | 17 | 2,375 | 134 | 8,572 |
| 1,000 patient-daysあたりの採取セット数 | 12 | 17.95 | 4.6 | 43 |
| 複数セット採取率 | 13 | 80.5 | 1.3 | 99 |
| 陽性率 | 14 | 11.35 | 6.1 | 18.1 |
| 汚染率 | 12 | 1.75 | 1 | 5.3 |
アンケート調査結果
| 使用機器 |
|---|
| バクテアラート10 バクテック5 用手法2 バーサトレック1 |
| 使用ボトル(複数回答あり) |
| ビーズ有り10 ビーズ無し9 抗酸菌ボトル5 |
| 培養日数 |
| 7日10 6日5 5日3 |
| 陰性ボトルのサブカルチャーの有無 |
| 未実施16 培養液混濁時等,陰性が疑わしい時1 Helicobacter cinaedi等の特殊菌が目的の時1 |
| 消毒方法 |
| アルコールとヨード製剤9 アルコールとクロルヘキシジングルコン酸塩4 アルコールのみ2 |
| アルコールとヨード製剤,アルコールとクロルヘキシジングルコン酸塩の使い分け2 |
| アルコールのみ,アルコールとヨード製剤,アルコールとクロルヘキシジングルコン酸塩の使い分け1 |
| ホルダー使用の有無 |
| 未使用14 使用3 採取する医師によって使い分け1 |
| 陽性ボトルから直接菌液を調整した感受性試験実施の有無 |
| 未実施15 実施3 |
| 時間外に提出された血液培養検査の対応 |
|---|
| 装置にセットまで15 室温保存3 |
| 陽性時対応 |
| Gram染色の結果まで報告7 Gram染色・同定・感受性試験まで実施3 対応しない2 培地の接種まで2 |
| 陽性ボトル取り出しまで1 日勤帯は同定・感受性試験まで実施し夜勤帯はボトル取り出しまで1 |
| Gram染色の確認まで(結果報告は行わない)1 土曜午前中のみGram染色の結果報告まで1 |
| 陽性時の連絡体制 |
| 主治医・主治医不在時は病棟連絡9 連絡なし3 病棟に連絡2 主治医の携帯1 |
| 主治医・ICT・感染症科医師に報告し主治医不在時は病棟に連絡1 ICDに連絡1 |
| 主治医および病棟・主治医不在時は病棟のみに連絡1 |
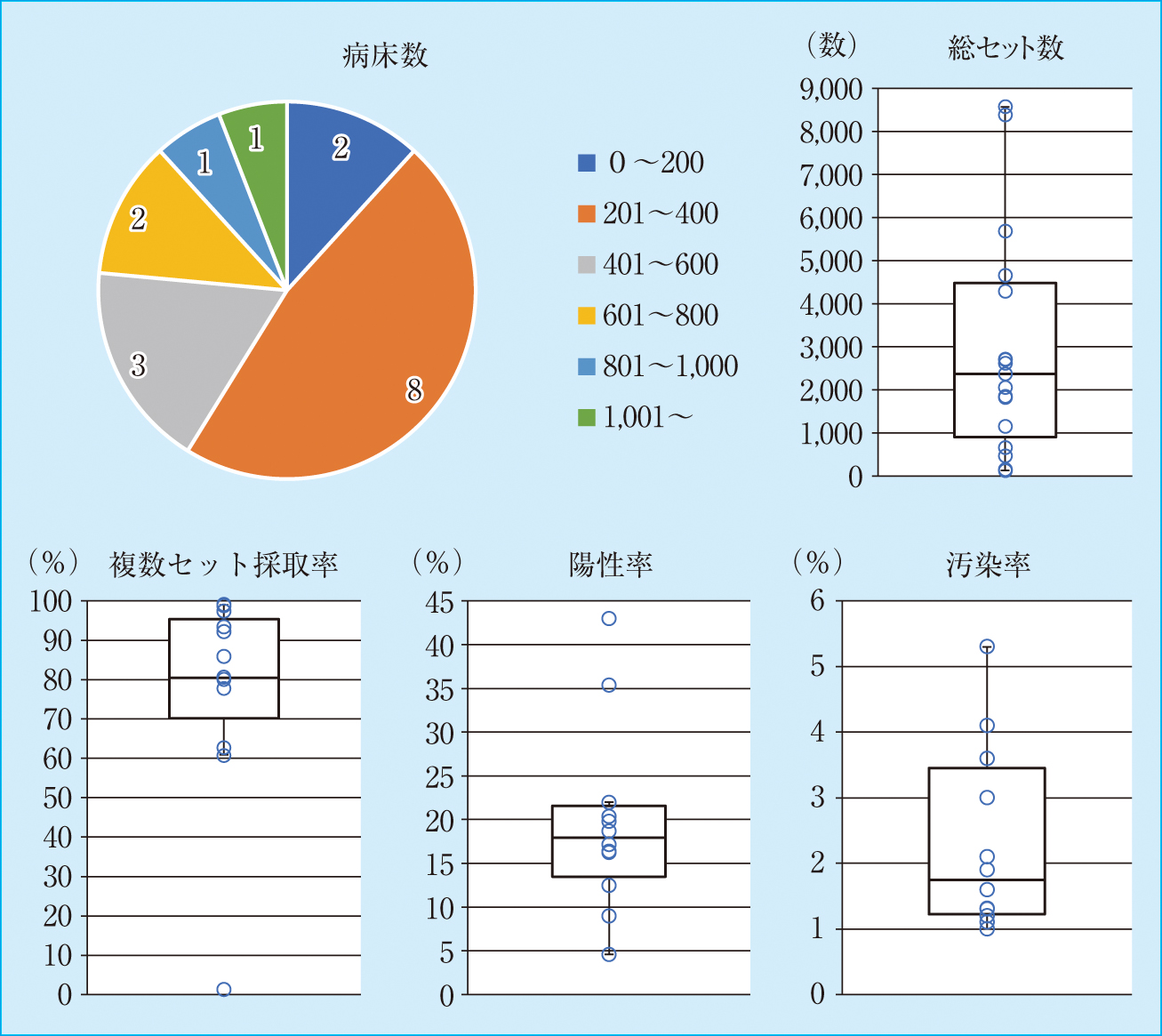
血液培養検査実施状況の詳細
病床数,総セット数,複数採取セット数,陽性率,汚染率の詳細を示した。
血液培養実施状況の集計値の中央値(範囲)は,病床数359.5(135~1,275),総セット数2,375(134~8,572),1,000 patient-daysあたりの採取セット数17.95(4.6~43),複数セット採取率80.5(1.3~99),陽性率11.35(6.1~18.1),汚染率1.75(1~5.3)であった。
2. 使用機器バクテアラート(ビオメリュー・ジャパン)10施設,バクテック(日本ベクトン・ディッキンソン)5施設,バーサトレック(コージンバイオ)1施設,用手法2施設であった。
3. 使用ボトル吸着ビーズ無し9施設,吸着ビーズ有り10施設であった。小児用ボトル併用施設が5施設あった。
4. 培養日数7日間10施設,6日間5施設,5日間3施設であった。
5. 陰性ボトルのサブカルチャーの有無未実施16施設,培養液混濁時等,陰性が疑わしい時に実施1施設,Helicobacter cinaedi等の特殊菌が目的の場合に実施1施設であった。
6. 消毒方法および汚染率との関係アルコールとヨード製剤9施設,アルコールとグルコン酸クロルヘキシジン4施設,アルコール消毒のみ2施設,アルコールとヨード製剤・アルコールとクロルヘキシジングルコン酸塩の併用2施設,アルコールのみ・アルコールとヨード製剤・アルコールグクロルヘキシジングルコン酸塩の使い分け1施設であった。消毒方法別による汚染率の集計値の中央値(範囲)は,アルコールのみが1.1%,アルコール+ヨード製剤3.6%(2.1~5.3%),アルコール+クロルヘキシジングルコン酸塩1.4%(1~1.9%)であった。
7. ホルダー使用の有無ホルダー使用3施設,未使用14施設,採取する医師によって使い分け1施設であった。
8. 陽性ボトルから直接菌液を調整した薬剤感受性試験の実施の有無実施3施設,未実施15施設であった。
9. 夜間休日帯(時間外)に提出された血液培養検査の対応検体受付時の対応として,室温保存3施設,装置にセット15施設であった。培養陽性時の対応は,Gram染色の結果まで報告7施設,Gram染色・同定・感受性試験まで実施3施設,何も対応しない2施設,培地への接種まで2施設,陽性ボトル取り出しまで1施設,日勤帯は同定・感受性試験まで実施し夜勤帯はボトルの取り出しまで1施設,Gram染色による鏡検確認まで実施し,結果報告はしない1施設,土曜午前中のみGram染色の結果報告まで実施1施設であった。培養陽性時の連絡体制は,主治医または主治医不在時は病棟に連絡が9施設,連絡しないが3施設,病棟に連絡が2施設,主治医の携帯が1施設,主治医・ICT・感染症科医師に報告し主治医不在時は病棟に連絡が1施設,ICDに連絡が1施設,主治医および病棟・主治医不在時は病棟のみに連絡が1施設であった。
今回のアンケート調査の目的は,福岡地区における血液培養検査実施状況の確認である。
総セット数,1,000 patient-daysあたりの採取セット数,複数セット採取率などは施設間差が多く見られた。国内における血液培養採取状況および検出率に関する全国規模のパイロットスタディにおいても,血液培養の施設間差が指摘されている3)が,今回の結果も同様であった。複数セット採取率が1.3%の施設があったが,特定医師のみが複数セット採取を依頼しているのとの回答であった。
陽性率は,6.1~18.1%とばらつきが見られた。CUMITECHにおける陽性率の適正範囲として,5%以下に低下したり,15%以上に上昇したりしている場合は,医師が適切に血液培養検査をオーダーしているか調査を開始しなければならないとしている1)。今回のアンケートではオーダーの実施状況については確認ができなかったが,概ね適正範囲内であった。採取時の消毒方法はアルコールとヨード製剤が9施設と最も多く,アルコールとクロルヘキシジングルコン酸が4施設と続いた。アルコールのみの消毒を行っている施設や,消毒方法を使い分けている施設も見られた。
汚染率の算出は,多くの施設が参考としているCUMITECHや血液培養検査ガイドに記載されている算出方法を採用した。本方法はベンチマークを得るものではなく,汚染率の算出方法として分母を述べ症例数としてカウントする方法が適切であるとの報告がある5)。従って,本アンケート調査の結果から汚染率を比較することは困難であると思われるが,消毒方法別による汚染率については,アルコールとクロルヘキシジングルコン酸塩による消毒が比較的低い傾向にあった。
採血時に抗菌薬を投与されていた患者では陽性率が低いことが報告されており6),血中の抗菌薬を吸着する性質をもつ合成樹脂(レズン)や活性炭,ポリマービーズが含有されている血液培養ボトルが市販されている。今回の調査ではやや吸着ビーズ有りの施設が多かった。
CUMITECHでは,全自動血液培養装置を用いた場合の培養日数は5日間としている1)。一方で,Helicobacter cinaediなどの一部の菌では発育に5日以上を要したとの報告があり1),7),血液培養検査ガイドではこれらの菌の検出を可能とするには培養日数は7日間が必要である3)とされている。今回のアンケート調査では7日間が10施設と最も多かったことは,この点を考慮しての結果と考える。
血液をボトル内に注入する際は針刺し事故のリスクがあるため,安全装置付きシリンジや,各社から販売されている専用の分注器具(BDバキュティナブラッドトランスファーデバイス,バクテアラート用血液培養ボトルセーフティーホルダー等)の使用が推奨されている。今回のアンケート調査では13施設と半数以上の施設でホルダーは未使用であり,今後の普及が望まれる。
血液培養ボトル内容液から菌液を調整し,直接薬剤感受性試験を行う方法(以下直接法)が報告されている8)~10)。米国Clinical and Laboratory Standard Institute(CLSI)標準法による結果と80%以上が一致するとされているが,標準法による結果が得られるまでの暫定的な結果であり,結果報告時には医師にそのことが理解できるコメントを付記するよう記載されている2)。分離菌の薬剤感受性試験の迅速な報告として,直接法は暫定的ではあるが有効な手段である。今回の調査では3施設が実施していた。
時間外に血液培養が陽性時となった際,Gram染色を実施している施設は18施設中11施設であり,結果報告まで行っている施設は7施設,Gram染色に加えて同定・感受性検査まで実施している施設は3施設,Gram染色による鏡検確認まで実施し,結果報告はしない施設は1施設であった。一方でGram染色を行っていない施設は5施設であった。日勤帯や夜勤帯,曜日によって対応を変えている施設も2施設見られた。Gram染色の判別による起炎菌の推定は,適切な抗菌薬の選択に繋がり患者予後の改善と在院日数短縮に結び付く。血液培養2セット採取の浸透に伴い,今後ますます血液培養陽性件数は増加することが考えられる。今回のアンケート結果では,Gram染色を実施していない理由は確認できていないが,可能な限りGram染色まで実施・報告できる体制が整備されることが望まれる。
血液培養の精度管理および臨床指標として一般的に用いられている指標,および採取時の消毒方法,時間外の対応等は施設によって異なっているが,陽性ボトルから直接菌液を調整した薬剤感受性試験の実施や,陰性ボトルのサブカルチャー,血液培養ボトルへの接種時のホルダーの使用は多くの施設で実施していない傾向にあった。施設によって病床数やマンパワー及び設備の違い,血液培養採取過程の質管理に対する取り組みの違いがあるとは思われるが,可能な範囲で対応していた。
今回のアンケート結果によって,福岡地区の病院における血液培養検査の実施状況が把握できた。施設によって取り組み可能な範囲は異なるが,CUMITECHや血液培養検査ガイド等を参考として,より適切な血液培養検査が実施されることが望まれる。
本論文の要旨は,第52回日本臨床検査技師会九州支部医学検査学会(2017年,長崎)で発表した。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。