2019 Volume 68 Issue 3 Pages 525-532
2019 Volume 68 Issue 3 Pages 525-532
登録衛生検査所における検体集荷業務は,検体受領・保管・輸送の重要な役割を担っており,検査目的に応じた適正な検体の取り扱いが要求される。特に微生物検査対象検体は生物を含んでいることから特別な制約があり,その取り扱いに苦慮する場合も少なくない。そこで我々は検体集荷者へ微生物検査に関する疑問や不安要素の聞き取りをおこなうとともに,1年半における微生物検査室からの確認作業内容を集計した。その結果,検体量の確認,検査材料の確認,依頼項目の確認の3項目で88.0%を占めた。この問題を解消するために,専用の微生物検査マニュアルを作成し,資料配布とともに集荷者に対する研修会を実施した。この取り組みを2013~2017年の5年間継続し,成果検証を目的に微生物検査室から集荷者に確認した作業件数を集計した。その結果,依頼項目に関する確認作業,検査材料に関する確認作業,共に件数が半減し成果を証明できた。さらに微生物検査室と集荷者との連携強化を目的に両者で利用するための2種類の「連絡用紙」を考案して運用した。これらの連絡用紙を活用した件数の推移も取り組みによる成果を示していた。研修会の実施のみならず集荷者からの問い合わせ電話に常時応対している微生物検査室スタッフの努力と集荷者の微生物検査を理解しようとする意欲と取り組みの継続が成果に繋がったと考える。
The receipt, storage, and transport of laboratory samples are important tasks for sample collection services in registered clinical laboratories. Among various types of sample, microbiological samples are particularly difficult to handle because they contain potentially harmful microorganisms, and specific restrictions on their handling are established. We conducted a survey by face-to-face interview on the concerns of the sample collection staff with regard to the handling of microbiological samples. The results showed that three major issues, namely, sample volume, sample confirmation, and requested test, accounted for 88% of all concerns. To resolve these issues, we prepared a microbial inspection manual and conducted workshops for the staff. We continued the workshops for five years from 2013 to 2017 and investigated the number of inquiries from the microbiology laboratory staff to the sample collection staff concerning sample confirmation and requested items. Because of this, the number of inquiries was successfully reduced by half. Furthermore, to strengthen the collaboration between the microbiology laboratory staff and the sample collection staff, a contact form was devised to share important information on both sides. In conclusion, through these efforts, understanding of the sample collection staff has been considerably improved and practical problems have significantly diminished. In addition, we would like to report also the efforts of the microbiology laboratory staff who always supports customers’ inquiries.
感染症の診断治療を目的とした微生物検査は,医師による臨床診断(予測)に即した適正検査が大切であり,迅速性,確実性が求められる。特に採取された検体は経時的に変化し,細胞変性や微生物死滅の可能性があることから,その取り扱いには十分な配慮が必要である。故に,ベッドサイド検査ができない登録衛生検査所では,新鮮材料を少しでも早く入手し目的別検査に供することを念頭に日々努力している。具体的には,検体の種類に応じた採取方法と専用容器の指示,保存と輸送に関する注意点などを依頼者側に説明し協力を得ている。しかし,検体受付時に不適検体であった場合は,受付保留となり再提出となるなど,依頼者に迷惑(患者に不利益)をかけることとなる。この鍵を握るのが検体集荷者である。集荷者は採用時とその後の定期研修を受けているものの,大多数が検査に卓越しておらず,さらに広域検査(血液・生化学・免疫血清・一般・病理・微生物など)に対応したあらゆる種類の検体を取り扱っている。このことから検体集荷時に困惑することもしばしばである。特に微生物検査では検体の種類が多く,検体適否の判断に苦慮し,医師や看護師からの質問に答えられず不安を抱えているのが実情である。そこで,この問題を解消し,不適検体数の軽減を目的に微生物検査室と集荷者との連携を密にする活動に着手し,成果を得たので報告する。
2013年に九州圏内営業所の集荷者を対象として微生物検査に対する疑問や不安要素などの聞き取りをおこない,回答内容を抽出した。
2. 事前調査微生物検査室から集荷者に作業確認をした内容と件数を,検体受付時の不備事項を記録している引継ぎノートより事前調査し分析した。期間は2012年5月から2013年10月までの1年半分を集計した。
1検体で複数の確認内容があった場合,内容毎に集計した。
3. 微生物検査マニュアルの作成聞き取りや事前調査の分析を基に,集荷者に理解でき,検査依頼者側への説明にも活用できるようにガイドライン1),ハンドブック2),および総合案内3)を参考に微生物検査マニュアルを作成した。
特に,喀痰の依頼項目数に対する検体の必要量と優先順位の必要性は写真と図表で明記し,専門知識であるグラム(Gram)染色は実際の顕微鏡写真を掲載し,微生物の染色性による区別は説明や注意点などを含め具体的に示した4)。
さらに,医師からの情報(感染症の種類や目的菌など)の入手の大切さや代表的な微生物の読み方(カタカナ表示),微生物検査手順のフローチャートなどを提供した。
4. 検体集荷者への研修会作成した微生物検査マニュアルを用いて集荷者向けの研修会を開き,検査の実情と注意点の理解を求めるとともに,依頼項目と検査材料の確認作業を重視するよう伝えた。また,集荷者からの意見を聞き出すことにも努め,「担当病院で困っていることはないですか?」など具体的に話しかけた。そして最後には必ず「とにかく,分からなければ何でも微生物検査室に電話してください!」と伝えた。
5. 微生物検査室から集荷者に確認を要した件数研修会の成果を見守るために開始から5年間(2013~2017年),微生物検査室から集荷者に確認(検査材料と依頼項目に関する内容)を要した件数を調査した。これは検体受付時の不備事項を記録している引継ぎノートより検査材料の確認件数と依頼項目の確認件数を各々集計し,検査材料の確認件数は依頼検体件数に対する割合,依頼項目の確認件数は依頼項目数に対する割合で示した。
6. ヒヤリ・ハット対策微生物検査室と集荷者の連携開始とともに,検体量不足の確認や依頼内容の連絡などの聞き間違いによる検査過誤防止を目的に,ヒヤリ・ハット対策として2種類の「連絡用紙」の運用を開始した。ひとつは検体が微生物検査室到着後に量不足と判断した際に「検体受付保留連絡用紙」に記入し集荷者にFAX送信するものであり,集荷者から依頼者側の指示を仰ぐために利用した。もうひとつは集荷先で検体量不足と判断した集荷者が依頼項目の優先順位を依頼者に確認し,それを「優先順位連絡用紙」に記入し検体と共に微生物検査室に提出するものである。これら連絡用紙の活用件数も研修会の成果として,依頼検体件数に対する割合で調査した。
集荷者の微生物検査に対する疑問や不安は,依頼項目数に応じた必要量がわからず検査可能な項目数が判断できない,検体の状態による検査可否が判断できない,検体種類別や依頼項目別の保存輸送条件がわからない,嫌気・微好気培養状態で提出された培地の輸送方法がわからない,報告までの日数がわからない,目的菌の指示があるが依頼方法がわからない,微生物名や専門用語を言われたが意味がわからない,検体が漏れていた時の対処法を教えてほしい,など多岐にわたった(Table 1)。
| 分類 | 内容 |
|---|---|
| 検査不可条件 | 1.依頼項目数に応じた検体の必要量がわからない |
| 2.どのような状態が検査不可能なのかわからない | |
| 3.検体採取日が3日前だが検査が可能かわからない | |
| 検体種類別の保存輸送条件 | 1.冷凍・冷蔵・室温など保存条件がわからない |
| 2.専用容器の保存輸送条件がわからない | |
| 3.嫌気・微好気培養状態で提出された培地の輸送方法がわからない | |
| 検査所要日数 | 1.報告までの日数がわからない |
| 2.抗酸菌検査の報告日がわからない | |
| 3.遺伝子検査の報告日がわからない | |
| 依頼方法 | 1.目的菌の指示があるが依頼方法がわからない |
| 2.皮膚真菌培養の依頼方法がわからない | |
| 3.環境材料の依頼方法がわからない | |
| 総合的 | 1.微生物名が書いてあるが意味がわからない |
| 2.微生物の専門用語がわからない | |
| 3.一連の微生物検査手順が知りたい | |
| 感染予防 | 1.感染予防はどうすればいいのかわからない |
| 2.検体が漏れていた時の対処法を教えてほしい |
集計総数は851件であり,最も多かったのは検体量不足の369件(43.4%)で約半数であった。次いで検査材料の確認が227件(26.7%),依頼項目の確認が152件(17.9%)と上位3項目だけで全体の88.0%を占めた(Figure 1)。尚,この3項目の具体的内容をTable 2に示した。検体量不足に関しては喀痰についての確認がほとんどであり,369件中337件(91.3%)を占めた。検査材料の確認227件の内訳は,材料不明であった件数が87件(38.3%),ポリメラーゼ連鎖反応(polymerase chain reaction; PCR)法や皮膚の真菌学的観察法である水酸化カリウム(KOH)法がスワブ検体で依頼されており検査に適していなかった件数が84件(37.0%),依頼項目は喀痰培養であるにもかかわらず気管支洗浄液が提出されているなど材料確認をおこなった件数40件(17.6%)の順であった。依頼項目の確認152件の内訳は,真菌や病原大腸菌などは検出に専用選択培地の追加が必要となるが,目的菌として明確な指示がされておらず主治医に確認が必要であったものが152件中92件(60.5%),嫌気性菌の目的菌があるにもかかわらず嫌気培養の依頼がないものが20件(13.2%),採取容器が期限切れであったため参考値で検査を継続するか再提出するかを確認したものが17件(11.2%),動静脈血でのPCR法と抗酸菌培養検査は各々採血管が必要であるが1本しか提出されなかったため各々採血管が必要であることを伝えた件数が14件(9.2%)の順であった。
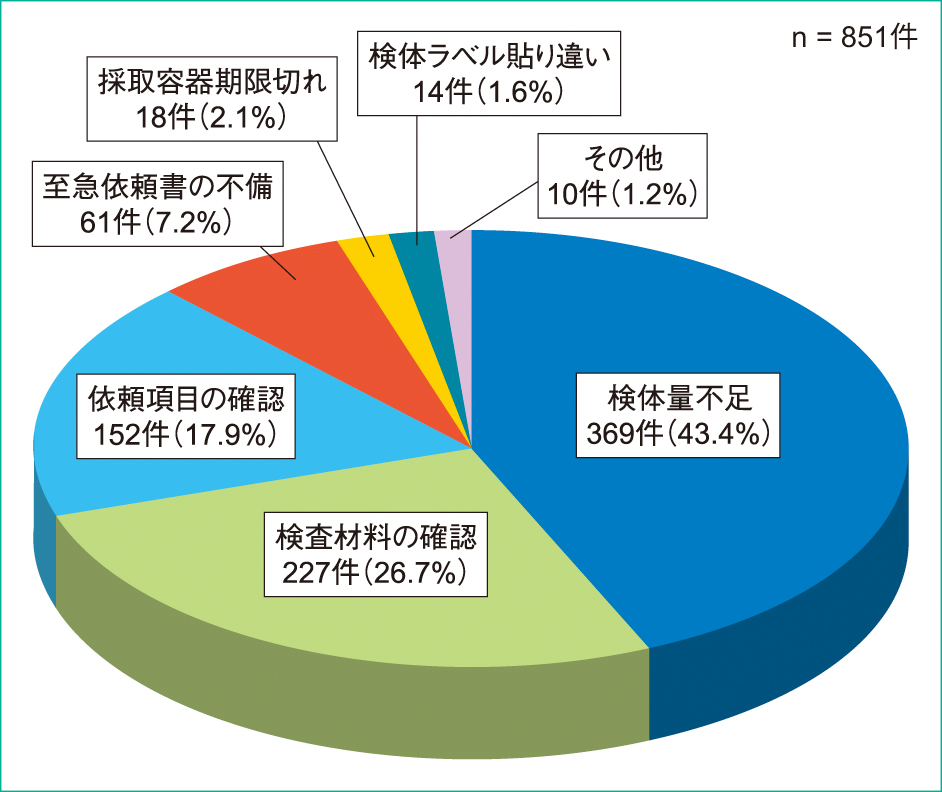
2012年5月~2013年10月の期間中に微生物検査室から集荷者に確認した内容を集計した。
| 項目 | 内訳 | 件数 | (%) |
|---|---|---|---|
| 検体量不足 (n = 369) |
喀痰 | 337 | 91.3 |
| 検体なし | 12 | 3.3 | |
| 尿 | 10 | 2.7 | |
| 膿 | 4 | 1.1 | |
| 糞便 | 3 | 0.8 | |
| 穿刺液 | 3 | 0.8 | |
| 検査材料の確認 (n = 227) |
材料不明 | 87 | 38.3 |
| PCR法や水酸化カリウム法はスワブでは不適のため確認 | 84 | 37.0 | |
| 依頼内容と材料が不一致のため材料を確認 | 40 | 17.6 | |
| 環境検査の材料が不明のため確認 | 9 | 4.0 | |
| 血液培養ボトルに記載された採取日が依頼書と不一致 | 7 | 3.1 | |
| 依頼項目の確認 (n = 152) |
真菌や病原大腸菌など目的菌の追加依頼が必要 | 92 | 60.5 |
| 嫌気培養の追加依頼が必要 | 20 | 13.2 | |
| 採取容器が期限切れのため参考値で継続か中止か確認 | 17 | 11.2 | |
| 動静脈血でPCR法と抗酸菌培養の依頼で採血管は1本 | 14 | 9.2 | |
| 耐性菌が目的であるが感受性の依頼がない | 4 | 2.6 | |
| 環境検査の目的を確認 | 3 | 2.0 | |
| その他 | 2 | 1.3 |
ポリメラーゼ連鎖反応(polymerase chain reaction; PCR)
作成した微生物検査マニュアルの概要をTable 3に示す。微生物検査マニュアルには,微生物検査が感染症を治療する目的でおこなわれることを明記して,微生物の種類と目的菌一覧も掲載した。また,材料によって検査実施料が異なることを説明するために依頼書の書き方も掲載した。さらに,材料別注意事項として事前調査より得られた材料毎の問題が解決できるような内容を掲載した。例えば,喀痰の量不足の解決には着色水を検体に見立て採取容器に必要量を分注したものや,血液培養ボトルや嫌気性菌の適正保存輸送の注意事項を記載し,尿定量培養は菌数把握のために必要であること,皮膚を材料とした時のKOH法と一般に用いられるGram染色との違いなどである。加えて,喀痰検査において,材料が微生物検査に適しているか否かを肉眼的観察(外観)評価ができるように唾液性喀痰と膿性喀痰の違いを写真で示した。また,微生物名をわかりやすく和名やカタカナで表記した。さらに,検査手順は各依頼項目についてどの様に検査を実施しているのか動画撮影をおこない,写真やフローチャートも示し研修会を実施した(Figure 2)。
| 分類 | 項目 | 要点 |
|---|---|---|
| I.検査依頼 | 一般細菌 | 1.微生物検査とは |
| 結核菌 | 2.微生物の種類 | |
| 真菌 | 3.目的菌一覧 | |
| 4.依頼書は材料と検査実施料にご注意を! | ||
| II.材料別注意事項 | 呼吸器 | 1.喀痰を預かったら! |
| 泌尿器 | 2.血液培養ボトルを預かったら! | |
| 穿刺液 | 3.尿定量培養とは? | |
| 皮膚 | 4.皮膚の真菌学的観察には水酸化カリウム(KOH)法には皮膚が必要! | |
| 5.材料別・菌種別適正保存輸送温度 | ||
| III.検体量 | 必要量 | 必要量と品質評価による肉眼的判断 |
| IV.微生物名 | 主な感染症原因微生物 | 和名またはカタカナ表記で一覧表を作成 |
| V.検査手順 | 塗抹 | 写真・フローチャート・動画で解説 |
| 培養 | 1.塗抹検査とは(一般細菌・抗酸菌) | |
| 感受性 | 2.培養検査とは(一般細菌・抗酸菌) | |
| 遺伝子 | 3.感受性検査とは(一般細菌・抗酸菌) | |
| 4.耐性菌とは | ||
| 5.遺伝子検査とは(PCR法・LAMP法) |
PCR; polymerase chain reaction
LAMP; loop-mediated isothermal amplification
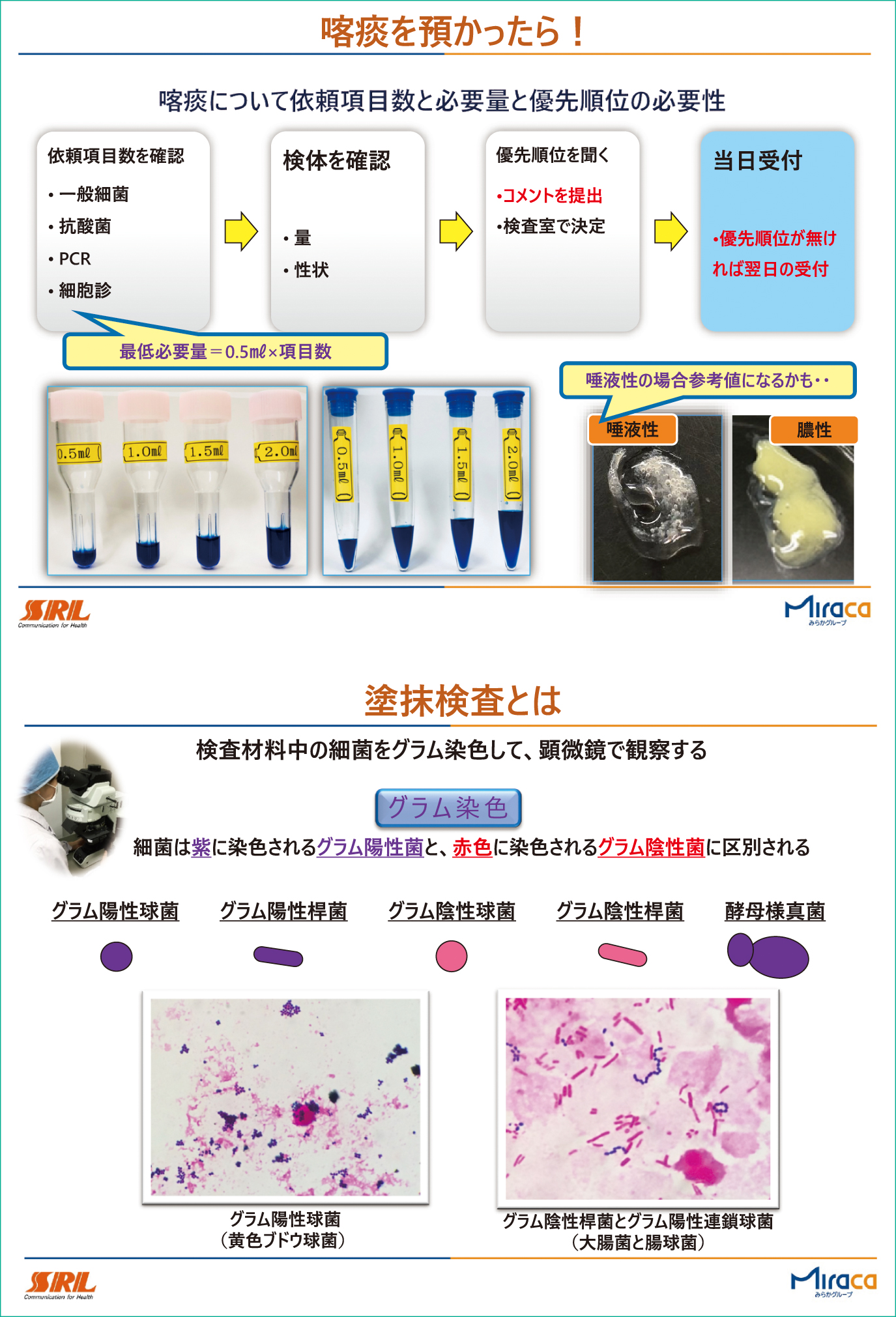
集荷者や検査依頼者への説明に活用できるように作成した「微生物検査マニュアル」のうち2枚を抜粋
●「喀痰を預かったら!」
喀痰を提出されたら依頼項目数と必要量と優先順位の必要性を図解したもの
●「塗抹検査とは」
実際のGram染色写真と細菌の染色性による区別を記載したもの
検体集荷者への研修会で特に入念に伝えた内容は,①喀痰について(膿性の良質な痰であること,唾液性では検査不可能と判断することもある),②最低必要量(一般細菌培養・抗酸菌培養・遺伝子検査,各々の必要量),③検体量不足時の優先順位の重要性(受付保留となり検査開始が遅れる),④検査実施料は材料によって異なる,⑤微生物検査専用材料コードによるシステム入力の徹底(他分野の材料コードは使用しない),⑥一般細菌培養・抗酸菌培養・真菌培養は培養日数や培養方法が異なる,⑦その他,CAPD(持続携帯式腹膜透析,continuous ambulatory peritoneal dialysis)排液などの専門用語や MRSA(メチシリン耐性黄色ブドウ球菌,methicillin-resistant Staphylococcus aureus)・ESBL(基質拡張型β-ラクタマーゼ,extended-spectrum β-lactamase)産生菌・CRE(カルバペネム耐性腸内細菌,carbapenem-resistant Enterobacteriaceae)・MDRP(多剤耐性緑膿菌,multiple drug-resistant Pseudomonas aeruginosa)などの耐性菌や感染予防についても解説した(Table 4)。これらは営業拠点毎に集荷者へ研修会を実施するとともに営業担当者へも研修会を定期的におこない,検査・集荷・営業の連携強化を図った。集荷者への研修会開始から5年間(2013~2017年)に,微生物検査室から集荷者へ確認した作業件数を「検査材料の確認」と「依頼項目の確認」別に集計し年次推移を示した(Figure 3)。このうち「検査材料の確認」件数は,2013年に161件(0.073%)2014年に171件(0.082%)であったが,2017年には83件(0.045%, p < 0.05)と半減した。また,「依頼項目の確認」件数は2013年に128件(0.028%)であったものが2017年には60件(0.016%, p < 0.05)と減少した。
| 項目 | 内容 |
|---|---|
| ① 喀痰について | 膿性の良質な痰であること,唾液性は検査不可になるかも |
| ② 最低必要量 | 一般細菌・抗酸菌・遺伝子検査 各々の必要量 |
| ③ 検体量不足時の優先順位の重要性 | 受付保留となった場合は検査開始が遅れる |
| ④ 材料系統と検査実施料の問題 | 検査実施料は材料によって異なる |
| ⑤ 微生物検査専用材料コードによる依頼の徹底 | 病理・細胞診など,他分野の材料コードは使用不可 |
| ⑥ 一般細菌培養・抗酸菌培養・真菌培養の相違点 | 培養日数や培養方法が異なる |
| ⑦ その他 | CAPD排液などの専門用語について解説 MRSA・ESBL産生菌・CRE・MDRPなど解説 感染予防について解説 |
CAPD;持続携帯式腹膜透析,continuous ambulatory peritoneal dialysis
MRSA;メチシリン耐性黄色ブドウ球菌,methicillin-resistant Staphylococcus aureus
ESBL;基質拡張型β-ラクタマーゼ,extended-spectrum β-lactamase
CRE;カルバペネム耐性腸内細菌,carbapenem-resistant Enterobacteriaceae
MDRP;多剤耐性緑膿菌,multiple drug-resistant Pseudomonas aeruginosa
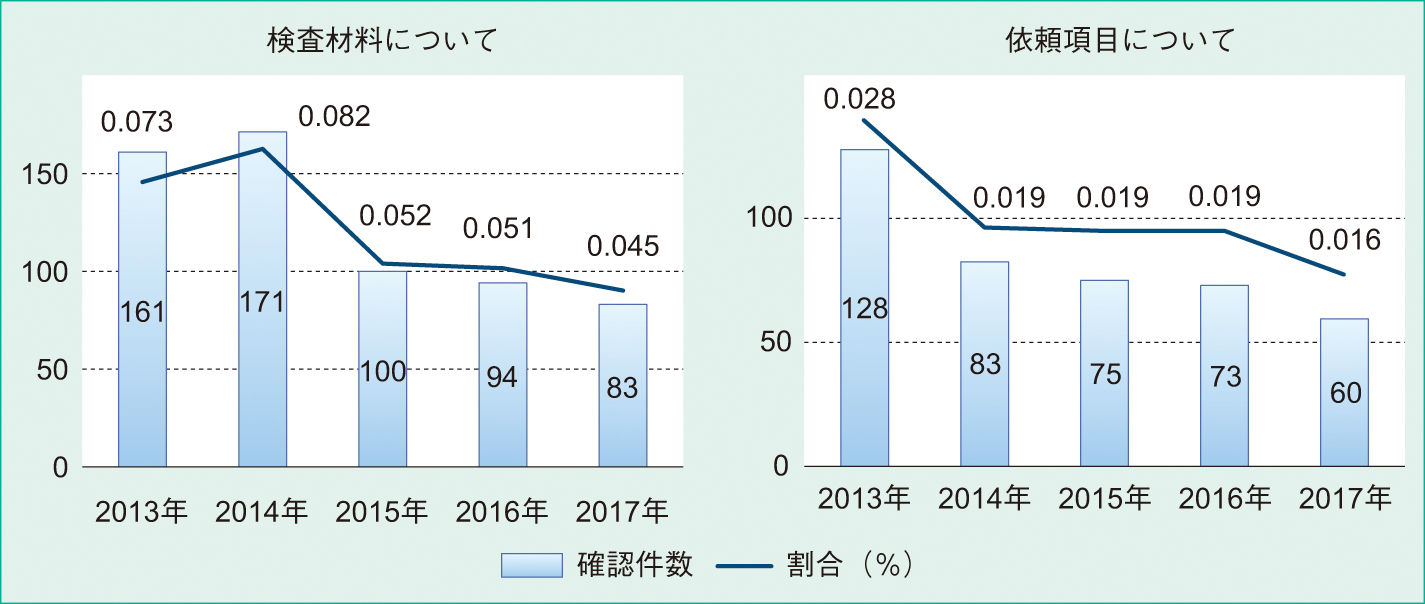
5年間(2013~2017年)に微生物検査室から確認作業をおこなった件数を「依頼項目」と「検査材料」別に集計した。
2013~2017年のあいだに微生物検査室から集荷者へFAX送信した「検体受付保留連絡用紙」と集荷者から微生物検査室へ提出された「優先順位連絡用紙」の2種類の連絡用紙の活用件数を集計し年次推移を示した(Figure 4)。
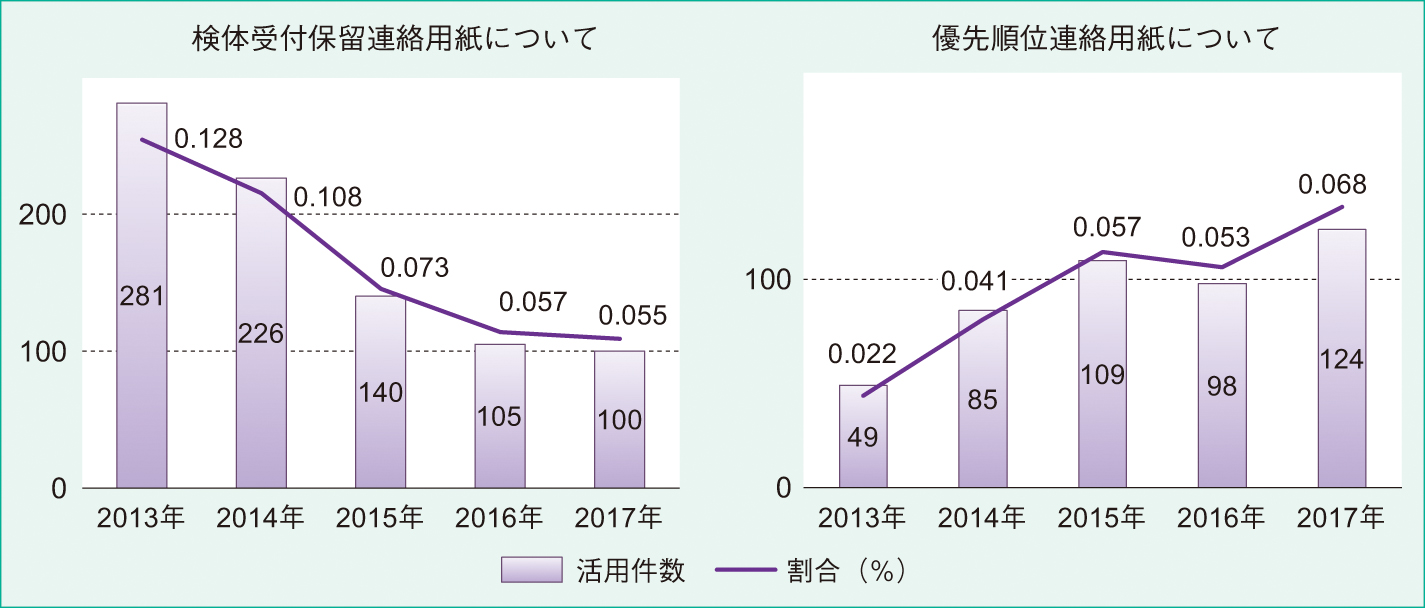
5年間(2013~2017年)に2種類の連絡用紙「検体受付保留連絡用紙」と「優先順位連絡用紙」を使用した件数を集計した。
「検体受付保留連絡用紙」を活用した件数は,2013年に281件(0.128%)であったが,2017年には100件(0.055%, p < 0.05)と大幅に減少した。また,「優先順位連絡用紙」を活用した件数は,2013年に49件(0.022%)であったものが,2017年には124件(0.068%, p < 0.05)と3倍に増えた。
登録衛生検査所における検査と病院施設内検査の根本的違いは,検査に取り掛かるまでの時間差であり,適正検体の受領と短時間輸送に十分な配慮が要求される。この厳正な役割を担っているのが検体集荷者であり,広域な種類の検体取り扱いに熟知し,適正材料かどうかを短時間で判断後,目的に応じた保存状態で輸送するよう教育されている。
特に微生物検査については検体の種類や原因微生物に応じた取り扱いが指示されている4)。しかし,集荷者の多くは特別な教育を受けていないことから,多くの微生物検査独特の専門用語に困惑しているのが実情である。
今回の取り組みは,微生物検査に関する集荷者からの「微生物検査は難しい,先生や看護師さんからの質問に答えられず不安だ。」という声がきっかけとなり,その不安要素を取り除くには何をするべきかを考えたことから始まった。九州全域300人を超える検体集荷者に微生物検査を浸透させることは容易ではないと判断し,まずは集荷者へ微生物検査に対する疑問や不安要素の聞き取り調査から開始した。その結果,検体受領時にどの程度の量が必要なのか苦慮していること,必要量以外の検査不可条件や検体種類別の保存輸送条件がわからない,検査所要日数がわからない,さらに,一般細菌と真菌の検査法の違いや感染管理目的の環境検体と臨床検体の目的の違いなど専門性の高い内容を理解している集荷者は少なく,その悩みは多岐にわたっていた。これらの内容はFigure 1とTable 2で示す,事前調査した微生物検査室から集荷者へ確認した851件の集計結果にも表れており,検体量の確認,検査材料の確認,依頼項目の確認の3項目が88.0%を占めたことは,問題点解決に向けての参考となった。
これらを踏まえて集荷者,および営業担当に利用してもらうために作成したのが微生物検査マニュアルであり,Table 3の概要に沿ったFigure 2のようなビジュアル表現と塗抹標本作製・染色・顕微鏡観察・培地への塗布から同定と感受性など一連の作業を撮影した動画を供覧することで普段見る機会の少ない実務検査の説明に,参加者からは再認識できたとの声が聴けた。さらに材料系統毎にまとめたシステム入力用の材料コード表や目的菌一覧表も配布したことで,集荷時に携帯でき依頼書と検体の照合に役に立つと集荷者から高評価を受けた。また,分からなければ何でも微生物検査室に電話で質問するように伝えた。このことにより微生物検査室への電話本数が増加したが,検査室スタッフに協力を求め丁寧な応対を心掛けた。その際,検査業務に支障をきたすことも懸念されたが,微生物検査室から集荷者へおこなう確認電話の件数減少を期待した。電話応対の具体例として,目的菌に関する場合は「目的菌一覧表はそこにありますか?」と配布した目的菌一覧表を活用して説明をすることで集荷者の理解が素早く得られ,目的菌に関する質問は減少していった。この効果は微生物検査室から集荷者に確認した内容のうち検査材料に関する確認作業,依頼項目に関する確認作業,共に件数が半減したことに反映されていると考える。
同時に実施したヒヤリ・ハット対策の2種類の「連絡用紙」の効果も如実であり,微生物検査室から集荷者へFAX送信した検体受付保留連絡用紙の活用件数の減少,および集荷者から微生物検査室へ提出された優先順位連絡用紙の活用件数の増加は,集荷者の知識向上による順当な検査実務遂行と受付保留の削減を表しており微生物検査マニュアルを用いた研修会の成果と考えられた。
今回の取り組みで最も重要であったのは連携であり,微生物検査室・検体集荷者・営業の三位一体で成り立つことを実感した。検査スタッフの理解と日常検査の中でいつでも応対する姿勢と取り組み,集荷者の微生物検査を理解したいという意欲,これらの連携があったからこその成果であり,受付保留の削減が実現できたと言える。
今回の取り組みで集荷者の問題が解消でき,円滑に検査開始できた件数が増加した。これからも検体集荷者の入れ替わりや新入社員の教育に対応するべく微生物検査研修会の継続は必要不可欠と考えている。また,検査室内でもより分かりやすく説明できるように,研修会講師の質の向上と意識統一を図っていきたい。集荷者を通して,より直接的に診療現場との接点を増やし診療現場とも連携をとることで感染症診断への貢献を模索していきたい5)。
本報告は患者の個人情報に関することを含んでいないため,倫理委員会の承認を得ていない。
尚,本報告は日本臨床衛生検査所協会第24回学術研究発表会全国大会で発表した。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。