2019 Volume 68 Issue 4 Pages 683-690
2019 Volume 68 Issue 4 Pages 683-690
Dimensionシリーズを用いたタクロリムス測定は,ACMIA法を測定原理とし,その特徴は前処理の除蛋白操作が自動化されていることである。今回我々は,抗体や磁性粒子へのタクロリムス結合法の変更,代謝産物との反応性の改良などが成された試薬が開発されたため,試薬の性能を評価する目的で検討を行った。基本性能として再現性(併行精度,室内再現精度),希釈直線性試験,共存物質の影響,ブランク上限(limit of blank; LoB),検出限界(limit of detection; LoD),定量限界(limit of quantification; LoQ),相関性について検討した結果,室内再現精度において低濃度で若干ばらつきが認められた。相関性ではARCHITECTとの相関はy = 1.146x − 0.951相関係数r = 0.988,Cobas8000との相関はy = 1.094x − 0.947相関係数r = 0.986とDimensionが10%程度高め傾向であった。その他は概ね良好な結果であった。また,採血容器に抗凝固剤として含まれるEDTA-2K濃度が測定値に与える影響についても検討した。その結果,規定量採血されていない場合,EDTA-2K濃度の上昇により測定値が低くなる傾向が認められたが,さらなる試薬の改良によりその影響は軽減された。しかしまだ改善の余地が残されており,現状では規定量採血することが必要である。
The principle of tacrolimus measurement using the Dimension series is based on the ACMIA method, with which the pretreatment deproteinization operation is automated. We evaluated the performance of the tacrolimus reagent with modification of the method to improve tacrolimus binding to antibodies and magnetic particles, as well as improve tacrolimus reactivity with metabolites. As a result of investigating reproducibility (simultaneous, within-day difference), dilution linearity, effect of coexisting substances, limit of blank, limit of detection, limit of quantification and correlation, we found that results varied with low reproducibility (within-day difference). Moreover, Dimension showed about 10% higher correlation than ARCHITECT and Cobas8000. When the blood collected did not reach the specified amount, the measured value tended to be low owing to the increase in the concentration of EDTA-2K, but this effect was reduced by further improvement of the reagent. However, because the improvement remains incomplete, it is necessary at present to collect the specified amount of blood.
タクロリムスは,1993年に肝臓移植における拒絶反応の抑制として使用され,その後腎臓,心臓,肺などの移植にも用いられてきた。また,移植に留まらず,関節リウマチや重症筋無力症,ループス腎炎など自己免疫性疾患の治療薬としても用いられるようになっている1)~4)。当院検査部における依頼件数は2011年度に12,876件だったものが,2017年度には21,178件と,6年間で約1.6倍になっており,臨床からのニーズも高まっている。しかしその一方で,2014年に発行された「免疫抑制薬TDM標準化ガイドライン」によると,現在タクロリムス測定にはLC-MS/MS法,CLIA法,ACMIA法,EMIT法,ECLIA法などが用いられているが,測定方法により測定値に誤差が生じているとの指摘があり,報告もある5)。また,大部分が赤血球中に存在するため前処理として除蛋白操作が必要であり,操作者による測定結果のばらつきなども問題点として指摘されており6),今後の課題も多い。
今回我々は,Dimensionシリーズのタクロリムス測定試薬において,抗体や磁性粒子へのタクロリムス結合法の変更や代謝産物との反応性の改良などが成されたため,試薬の性能について評価した。また,採血容器に抗凝固剤として含まれているEDTA-2K濃度が,測定値に与える影響について確認することを目的として検討を行った。性能を評価するにあたり,一般社団法人TDM品質管理機構が主催するTDM外部精度管理調査結果についても報告する。
2017年8月~12月に当院検査部にタクロリムス検査の依頼があった検体の残余血液を用いた。
2. 測定機器および試薬検討機器は臨床化学自動分析装置Dimension EXL200[シーメンスヘルスケア・ダイアグノスティクス(株):以下Dimension],検討試薬はフレックスカートリッジタクロリムスTAC[シーメンスヘルスケア・ダイアグノスティクス(株):以下改良試薬-1および改良試薬-2]を用いた。
改良試薬-1はACMIAクロム粒子コーティング法を測定原理とし,磁性粒子へのタクロリムス結合方法を変更したことにより安定性が向上した試薬である。また,代謝産物との交差性は測定値へ影響を与える要因の1つであるが7),抗体の変更により代謝産物との交差反応が改善されている8)。
さらに,前処理液を界面活性剤から新界面活性剤+カオトロープ試薬+シロリムスに変更したことにより非特異反応が軽減されている。なお,タクロリムス濃度が20 ng/mLを超える場合は,前処理液を変更し測定対象物であるタクロリムス以外の物質により生じたシグナルを反映させることで,初検と再検の結果の差から非特異反応を自動的にチェックする機能が追加されている。測定時間は従来法と変わらず15分である8)。
改良試薬-2は改良試薬-1のロット変更として前処理液の濃度を変更した試薬であり,現在市販されているのは改良試薬-2である。
なお,以下の基礎検討および相関については改良試薬-1の結果である。
3. 基礎検討 1) 再現性併行精度は3濃度の管理血清を用いて10回測定した。室内再現精度は3濃度の管理血清を用いて10日間測定した。
2) 希釈直線性試験低濃度と高濃度の患者検体を用い,0濃度キャリブレータで10段階希釈したものを2重測定した。
3) 共存物質の影響干渉チェックAプラスおよびRFプラス[共にシスメックス(株)]を用いて,抱合型ビリルビン(20.7 mg/dL),遊離型ビリルビン(19.1 mg/dL),乳び(1,650 FTU),RF(450 IU/mL)について確認した。
4) ブランク上限(limit of blank; LoB),検出限界(limit of detection; LoD)および定量限界(limit of quantification; LoQ) ① LoB0濃度キャリブレータ,2件のタクロリムスを投与されていないことを確認した患者検体(それぞれ2重測定)を午前と午後1回ずつ5日間測定し,日本臨床化学会より公表されているバリデーション算出プログラム9)より求めた。
② LoD2.5 ng/mL濃度のキャリブレータを用いて調整した5種類の低濃度試料を午前と午後1回ずつ5日間測定し,前述の算出プログラムより求めた。
③ LoQ15件の低濃度患者検体を午前と午後1回ずつ5日間測定し,前述の算出プログラムより求めた。
4. 相関100件の患者検体を用いて相関性を確認した。
対象機器としてARCHITECT i2000SR[アボットジャパン(株):以下ARCHITECT]とその専用試薬であるタクロリムス・アボット[アボットジャパン(株)],およびCobas8000[ロシュ・ダイアグノスティックス(株)]とその専用試薬であるエクルーシス®試薬タクロリムス[ロシュ・ダイアグノスティックス(株)]を用いた。
5. EDTA-2K濃度が測定値に与える影響タクロリムス測定には,採血容器としてEDTA-2K管を用いるが,改良試薬-1において,規定量採血されていない場合,EDTA-2K濃度の上昇により測定値が低くなる傾向があることが報告されているため10),11),この現象に対しさらに試薬を改良(改良試薬-2)し,その前後で測定値に与える影響について検討した。方法は,5件の患者検体を用い,規定量採血された状態をEDTA-2K濃度1倍とし,2倍,4倍,8倍に調整した検体を2重測定し,その平均値を用いて比較した。検体の濃度は改良試薬-1において検体1:4.00 ng/mL,検体2:7.20 ng/mL,検体3:10.25 ng/mL,検体4:19.20 ng/mL,検体5:25.20 ng/mL,改良試薬-2において検体1:3.55 ng/mL,検体2:6.55 ng/mL,検体3:8.65 ng/mL,検体4:12.95 ng/mL,検体5:18.40 ng/mLである。
6. 外部精度管理調査一般社団法人TDM品質管理機構が主催するTDM-QC研究会での3年間の推移について評価した。
なお本検討については東京女子医科大学倫理委員会の承認を得て行った【承認番号:4349】。
併行精度は2.40~5.17%,室内再現精度は4.66~9.04%となり,室内再現精度において低濃度で若干ばらつきが大きかった(Table 1)。
| Sample | MORE1 | MORE2 | MORE3 |
|---|---|---|---|
| mean | 4.67 | 12.12 | 24.14 |
| min | 4.4 | 11.6 | 22.9 |
| max | 5.2 | 12.8 | 24.8 |
| SD | 0.241 | 0.406 | 0.579 |
| CV (%) | 5.17 | 3.35 | 2.40 |
| Sample | MORE1 | MORE2 | MORE3 |
|---|---|---|---|
| mean | 4.41 | 11.87 | 23.62 |
| min | 3.7 | 10.5 | 21.3 |
| max | 5.0 | 12.7 | 25.1 |
| SD | 0.399 | 0.694 | 1.101 |
| CV (%) | 9.04 | 5.85 | 4.66 |
測定範囲内において原点を通る直線性が得られた(Figure 1)。

全てにおいて最終濃度まで変化率は±10%以内であり,影響は認められなかった(Figure 2)。

ノンパラメトリック法で0.023 ng/mLとなった。mean:0.002 ng/mL,SD:0.009 ng/mLであった。
② LoDノンパラメトリック法で0.275 ng/mLとなった。理論濃度0.25 ng/mLに対してmean:0.12 ng/mL,理論濃度0.50 ng/mLに対してmean:0.32 ng/mL,理論濃度0.75 ng/mLに対してmean:0.62 ng/mL,理論濃度1.00 ng/mLに対してmean:0.85 ng/mL,理論濃度1.25 ng/mLに対してmean:1.07 ng/mL,合成標準偏差:0.153 ng/mLであった。
③ LoQCV20%のとき0.963 ng/mLとなった(Figure 3)。
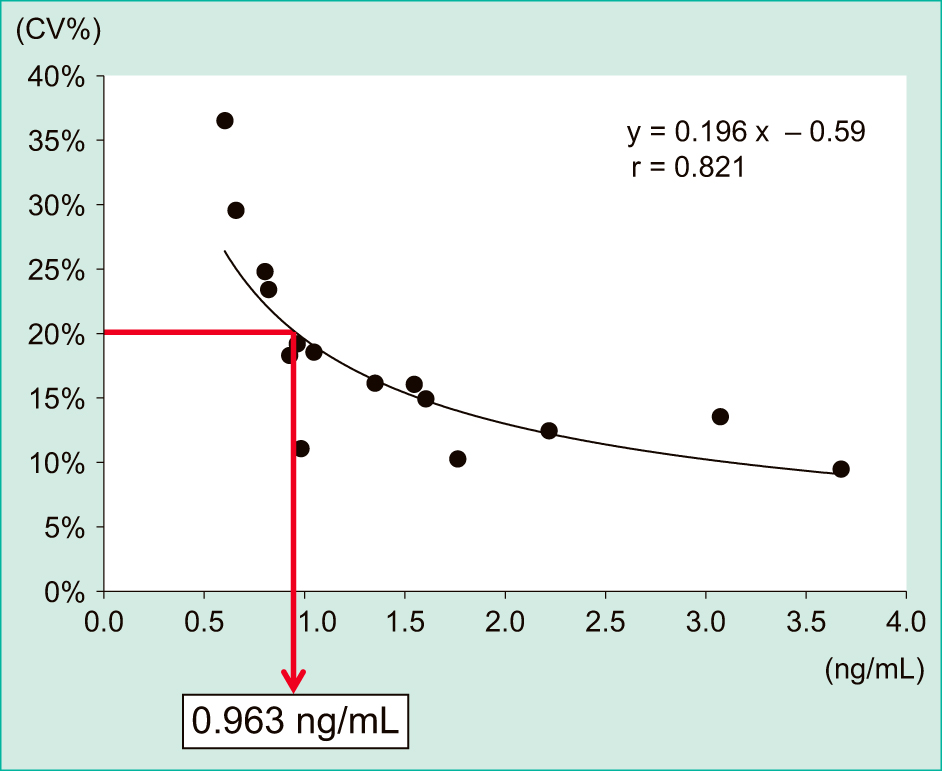
From the validation calculation program published by the Japanese Society of Clinical Chemistry
ARCHITECTとの相関は,回帰式y = 1.146x − 0.951,相関係数r = 0.988,Cobas8000との相関は,回帰式y = 1.094x − 0.947,相関係数r = 0.986となり,2法に比べDimensionが10%程度高め傾向であった(Figure 4)。

Left: Correlation between Dimension and ARCHITECT
Right: Correlation between Dimension and Cobas8000
2法のうちより傾きの大きかったARCHITECTとの相関性を5 ng/mL未満,5~10 ng/mL,10 ng/mL以上の濃度別で確認した(Figure 5)。結果は5 ng/mL未満では回帰式y = 0.951x − 0.208,相関係数r = 0.897,5~10 ng/mLでは回帰式y = 1.036x − 0.393,相関係数r = 0.908,10 ng/mL以上では回帰式y = 1.132x − 0.519,相関係数r = 0.962(いずれもy:Dimension,x:ARCHITECT)となり,10 ng/mL以上の高値域でDimensionが高め傾向であった。

Left: Correlation of less than 5 ng/mL between Dimension and ARCHITECT
Center: Correlation of 5~10 ng/mL between Dimension and ARCHITECT
Right: Correlation of more than 10 ng/mL between Dimension and ARCHITECT
改良試薬-1(Figure 6左図)ではEDTA-2K濃度が2倍から測定値の低下が認められ,最大で13.7%まで低下することを確認した。改良試薬-2(Figure 6右図)では2倍での変化率は5%以内,最大でも7.3%の低下に留まり改善が認められた。

Left: Before improvement of EDTA-2K concentration
Right: After improvement of EDTA-2K concentration
Dimension群は第1回の2016年度に比べ,第3回の2018年度ではCV%にはまだ改善の余地があるものの,理論値(試料作製時に薬剤を添加し,計算された理論濃度として算出された数値)との差は小さくなっていた(Table 2)。
| 2016 (n = 21) | 2017 (n = 16) | 2018 (n = 14) | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Sample | Theoretical value | Measured value | CV (%) | Theoretical value | Measured value | CV (%) | Theoretical value | Measured value | CV (%) |
| 1 | NA (0) | 1.0 ± 1.00 | 96.0 | 1.5 | 1.2 ± 0.37 | 32.4 | 6.0 | 5.9 ± 0.54 | 9.2 |
| 2 | 13.8 | 9.80 ± 1.40 | 14.1 | 16.5 | 15.9 ± 1.40 | 9.0 | 2.0 | 2.2 ± 0.32 | 14.7 |
| 3 | 1.7 | 1.4 ± 0.60 | 44.6 | 6.0 | 5.6 ± 0.49 | 8.8 | 2.0 | 2.4 ± 0.45 | 19.0 |
Excerpt from external survey results carried out “TDM Quality Control Organization of the General Association”
従来試薬では併行精度においてmean:6.54 ng/mL,14.70 ng/mL,21.67 ng/mLに対してCV:7.88%,3.92%,4.39%,室内再現精度においてmean:6.03 ng/mL,13.67 ng/mL,20.77 ng/mLに対してCV:7.56%,6.75%,5.14%(導入時検討データより)であったが,改良試薬では併行精度で改善が認められた。感度においても従来試薬の2.6 ng/mL10)に比べ改良試薬の方が低値まで測定可能であった。
ARCHITECTとの相関性において,10 ng/mL以上の高値域でDimensionが高め傾向であったため,値付けとキャリブレーションカーブについて確認した。値付けに関しては,キャリブレータのクロス測定(n = 2)を行った。DimensionのキャリブレータをARCHITECTで測定したときの回収率は97.5~116.7%,ARCHITECTのキャリブレータをDimensionで測定したときの回収率は90.0~110.2%と双方共に大きな差はなく,値付けに起因するものではないと考える。次に,10 ng/mL以上のキャリブレータのポイントを比較してみると,ARCHITECTは12.0 ng/mL,20.0 ng/mL,30.0 ng/mLであるのに対し,Dimensionでは10.4 ng/mLの次が30.0 ng/mLであるため,この付近のキャリブレーションカーブに起因している可能性があると考える。Dimensionの較正は0~10 ng/mLまでは直線的であるため歪みは少ないが,10 ng/mL以上では曲線的であるためロット固有に,もしくは装置の状態により発生する多少の歪みが測定値に影響している可能性が示唆された。この点についてはロット間差など更なる検討が望まれる。
EDTA-2K濃度が測定値に与える影響に関しては,測定値の低値化は改善されたが,まだ改善の余地が残るため,現状では規定量採血することが必要と考える。この現象については従来試薬では確認されておらず,試薬の改良に伴い発生しているため,変更箇所に原因があると推測されるが,未だ特定には至っていない。検体によっては上昇しているものもあり,これらに関しては再現性に起因する要素も含まれていると考える。検体の前処理の除蛋白操作が自動化されていることで業務の効率化,除蛋白操作を行うための教育が不要,TATの短縮といった大きなメリットがあるだけに再現性も含め更なる改良が期待される。
外部精度管理調査の結果では,年度によりターゲットとする値に差があるため単純に比較することは難しいが,改善の兆しが見られ,試薬が改良されたことに起因するところが大きいと考える。測定方法により測定値に誤差が生じているとの指摘に対する解決策の一助となり得ると考える。
ISO15189では要求事項として外部精度評価プログラムに参加することを求めている。また,2018年12月1日より施行された医療法等の一部を改正する法律(平成29年法律策57号12))の一部の施行に伴う厚生労働省関係省令の整備に関する省令(平成30年厚生労働省令第93号13))にも外部精度管理調査の受検が努力義務として定められている。シーメンスヘルスケア・ダイアグノスティクス(株)によると,2016年度には改良試薬の割合はほぼ無かったが,2017年度から徐々に移行し,2018年度では改良試薬のみとなっているとのことであり,この3年間の推移は外部精度管理調査結果にも反映されていた。
この様に第三者機関による評価を受けることは,機器・試薬・測定法により結果が異なることの多い免疫項目において,現状を認識する機会になる。今回のような試薬の改良に繋げる試みは有意義であり,また,検査室の品質を保証し患者に質の高い医療を提供するためにも必要と考える。
Dimension EXL200を用いたタクロリムスの改良試薬-1は,室内再現精度において低濃度域で若干のばらつきが認められたが,それ以外の基本性能は概ね良好であった。規定量採血されなかった場合,EDTA-2K濃度の上昇により測定値の低値が認められたが,さらなる試薬の改良(改良試薬-2)により影響は軽減された。しかしまだ改善の余地が残されており,現状では規定量採血することが必要である。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。