2020 Volume 69 Issue 4 Pages 570-576
2020 Volume 69 Issue 4 Pages 570-576
乳酸脱水素酵素(LD)活性測定は2020年4月1日よりJSCC法からIFCC法に変更される。そこで,LタイプワコーLD・IF試薬(富士フイルム和光純薬)を用いたLD活性測定の基礎的検討を行った。併行精度及び再現精度は,いずれの管理試料においても変動係数C.V.は1.2%以下と良好であった。LD高値活性検体を用いて10段階の希釈直線性試験を行ったところ,2,470 U/Lまで測定可能であった。干渉物質はビリルビンF,ビリルビンCおよび乳ビは測定値に影響を認めなかったが,ヘモグロビンは正誤差を受けた。現行試薬との相関は,相関係数r = 0.994と良好で,回帰式はy = 0.923x + 9.8と現行試薬とほぼ同等な成績が得られた。一方,回帰直線よりも低値に乖離したと考えられた5検体に関して,クイックジェルLD試薬(ヘレナ研究所)を用いたLDアイソザイム分析結果はLD5分画値が59%以上とMサブユニット優位な検体であった。健常者におけるLD活性値の基準範囲は108~202 U/Lと算出された。LタイプワコーLD・IF試薬は日常の臨床検査に十分な性能を有していた。
The lactate dehydrogenase (LD) activity test was converted from the JSCC method to the IFCC method on 1 April 2020. We conducted a basic evaluation of LD activity using “L-type Wako LD·IF” manufactured by Fujifilm-Wako. Parallel-run precision and reproducibility for all control materials were good with a C.V. below 1.2%. The detection limit determined using 10 dilution series of high-activity LD samples was 2,470 U/L. There was no interference by bilirubin F, bilirubin C or chyle, but hemoglobin caused a false positive result. The correlation between currently used reagents was good with similar results, that is, correlation factor r = 0.994 and regression equation y = 0.923x + 9.8. Isozyme analyses of five samples using “Quick Gel LD” manufactured by Helena showed a small divergence from the regression line and indicated that the LD5 fraction was over 59%, which means that the M subunit was dominant in the five samples. The normal LD activity range was calculated as 108–202 U/L. The results showed that L-type Wako LD·IF reagent has sufficient performance for routine testing.
現在,国内の乳酸脱水素酵素(LD)活性測定に用いられているLDアイソザイムの反応性を見るとJSCC法はLD5がLD1よりも高めに測定されている。一方,海外ではLD1とLD5の反応性がほぼ同等に測定されるIFCC法を用いている1)。
2020年4月1日,国内ではLD活性測定法がJSCC法からIFCC法に変更される予定であり,現在はJSCCの酵素・試薬専門員会LDプロジェクトが主体となって測定法変更の準備が進められている。健常者を対象としたJSCC法とIFCC法との相関から,LD活性値は許容誤差範囲内に収まりほぼ同等なLD活性値を示したことから現在の共用基準範囲(124~222 U/L)については変更しないことが報告されている2)。しかし,肝疾患患者ではLD5が優位となるため,LD活性測定法の変更に伴い,LD活性値はJSCC法に比べてIFCC法では10~20%低値傾向となることに留意する必要があると言われている3)。
今回われわれは,LD活性測定法のJSCC法とIFCC法の比較検討を行った成績と職員健診検体を用いてLD活性値の基準範囲を求めたので報告する。
1)LタイプワコーLD・IF(LD・IF)(富士フイルム和光純薬)
酵素キャリブレーター(IFCC表示値 436 U/L)(富士フイルム和光純薬)
2)LタイプワコーLD・J2(LD・J2)(富士フイルム和光純薬)
3)タイタンジェルS-LD試薬(S-LD試薬)(ヘレナ研究所)
2. 測定機器1)JCA-BM 8060型自動分析装置(日本電子)
2)全自動電気泳動装置エパライザ2(ヘレナ研究所)
3. 測定原理試料中のLDの作用により,β-ニコチンアミドアデニンジヌクレオチド酸化型(NAD)の存在下で乳酸はピルビン酸に酸化される。この時NADはβ-ニコチンアミドアデニンジヌクレオチド還元型(NADH)に還元され340 nmの吸光度が上昇する。このNADHの増加速度を測定することにより試料中のLD活性値を求める。
緩衝液は次のとおりである。
JSCC法:ジエタノールアミン(DEA),pH 8.8(30℃)
IFCC法:N-メチル-D-グルカミン(NMG),pH 9.4(37℃)
なお,本検討に用いたJCA-BM 8060型自動分析装置における分析条件(分析パラメータ)をTable 1に示す。
| Items | LD·IF & LD·J |
|---|---|
| Main wave length (nm) | 410 |
| Analysis method | RRA |
| Speciment volume (μL) | 7.5 |
| Reagent (R1) volume (μL) | 60.0 |
| Reagent (R2) volume (μL) | 15.0 |
| Calibration method | STD |
低濃度(L)は液状コントロール血清IワコーC&C(富士フイルム和光純薬),中濃度(M)はLiquichek Unassayed Chemistry Control (Human) 2(バイオラッドラボラトリーズ),高濃度(H)はL-コンセーラII EX「ニッスイ」(日水製薬)をそれぞれ20回測定し,変動係数(CV%)を算出した。
2. 室内再現精度4)併行精度の検討に用いた高濃度(H)を,それぞれ5重測定し,15日間のCV%を算出した。統計ソフトJMP ver. 14(SAS)を用いて,15日間5重測定のコントロールデータの解析を行った。
3. 正確さ4)常用参照標準物質:JSCC常用酵素(CRM-001d)を用いて,10回測定して平均値,標準偏差および変動係数を求め,CRM-001dの実測値がその95%信頼区間の上限値と下限値に表示値が含まれていることを確認した。
4. 希釈直線性リニアチェックEnzyme(非売品:富士フイルム和光純薬)を生理食塩水にて10段階希釈して試料を調製し,2重測定した。
5. 共存物質の影響自社管理検体(ゴールデンウェスタンバイオ)9容に干渉チェックAプラス(シスメックス)のビリルビンF(遊離型)およびビリルビンC(抱合型),ヘモグロビン,乳ビ成分をそれぞれ1容添加し,LD活性値に及ぼす影響を検討した。添加0濃度の検体はサンプル9容に生理食塩水1容を添加した。なお,添加0濃度のLD活性値の10重測定の平均値を100%とした場合,±5%以内を測定値に影響がないと判断した。
6. 検出限界LD活性値として約10 U/Lに調整した血清試料を生理食塩水にて10段階希釈した試料を作製した。作製した試料を各10回測定し,測定値の平均値と標準偏差(SD)を算出した。生理食塩水の測定値の平均値 +2SDと試料の測定値の平均値-2SDが重ならない最小濃度を検出限界とした。
7. 相関性試験当社で受託した血清検体を匿名化した206例を用いて,LタイプワコーLD・IF試薬と比較対照としてのLタイプワコーLD・J試薬との相関性を検討した。
8. LDアイソザイム分析相関性試験で乖離していると考えられた5検体について,S-LD試薬と全自動電気泳動装置エパライザ2を用いて,15℃の温度条件下240 V,13分電気泳動後,酵素活性染色を行い,LDアイソザイム分画値を求めた。
9. 健常者の基準範囲社内の健康診断で肝機能,腎機能,脂質異常を認めず且つ同意書が得られた社員348名(男:155名;女:193名)の血清検体を用いてLD活性値の基準範囲を求めた。なお,統計ソフトはJMP ver. 14(SAS)を用いてノンパラメトリック法で計算した。
低濃度(L),中濃度(M),高濃度(H)ともにC.V.は0.4~0.5%と良好な結果が得られた(Table 2)。
| LD·IF | L | M | H |
|---|---|---|---|
| Mean (U/L) | 151.7 | 372.8 | 410.3 |
| S.D. (U/L) | 0.81 | 1.53 | 2.00 |
| C.V. (%) | 0.5 | 0.4 | 0.5 |
(n = 20)
室内再現精度のC.V.は1.2%と良好な結果が得られた(Table 3)。
| Item | Average (U/mL) | S.D. (U/mL) | C.V. (%) |
|---|---|---|---|
| Intermediate precision | 406.5 | 4.94 | 1.2 |
| Diurnal precision | 406.5 | 4.59 | 1.1 |
| Repeatability precision | 406.5 | 1.83 | 0.5 |
CRM-001dを10回測定した平均値は434.3 U/Lであり,CRM-001dの表示値(430 ± 11 U/L)以内であった(Table 4)。
| Certified value (U/L) | 430 ± 11 |
| n | 10 |
| Average (U/L) | 434.3 |
| S.D. (U/L) | 1.56 |
| C.V. (%) | 0.4 |
| Relative error | 4.3 |
| 95% confidence interval | 431.3–437.4 |
リニアチェックEnzymeを用いた検討では2,470 U/Lまでは良好な希釈直線性が得られた(Figure 1)。

Control serum was diluted 2 times with physiological saline to prepare samples and confirmed. As a result, good linearity was confirmed.
ビリルビンFは20.2 mg/dL,ビリルビンCは20.7 mg/dL,乳ビは3,000 FTUまではLD活性値に影響は認められなかった。しかし,ヘモグロビンは濃度依存性に高値となりLD活性値に影響した(Figure 2)。
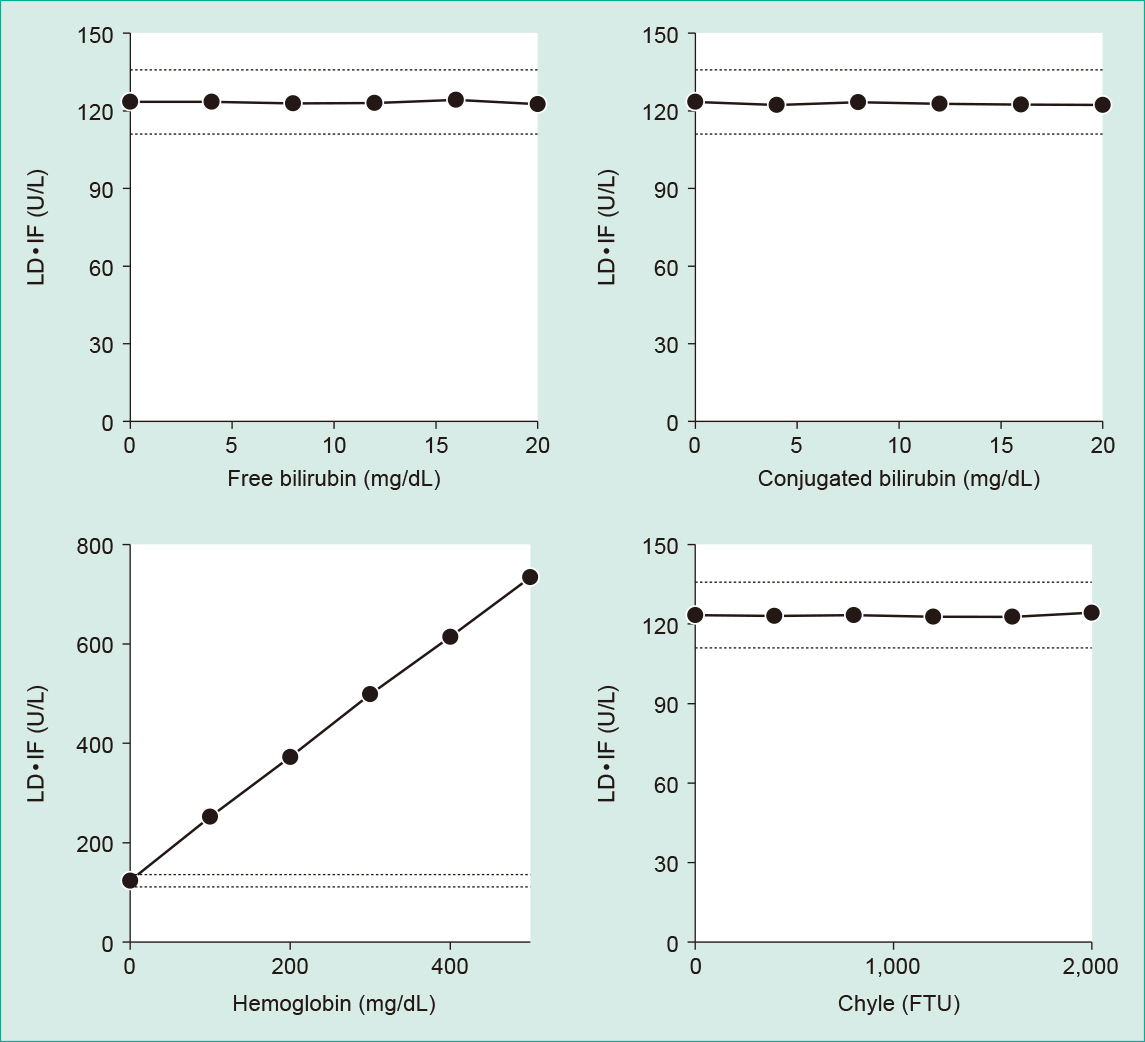
Dotted line: untreated mean value ±5%.
Control serum were used to confirm the effects of free bilirubin, conjugated bilirubin and chyle. As a result, no influence was observed up to the concentration shown in the figure. But Hemoglobin had a positive error.
LD活性値の検出限界は1.9 U/Lであった(Figure 3)。

Dotted line: mean value of physiological saline + 2SD.
Serum were diluted 10 times with physiological saline to prepare samples and confirmed. As a result, the detection limit was LD activity concentration 1.9 U/L.
206検体を用いたLD・J2試薬とLD・IF試薬との回帰式はy = 0.923x + 9.8,相関係数r = 0.994と良好な結果であった(Figure 4)。なお,乖離していると考えられた5検体(〇)を除いた201検体の回帰式はy = 0.977x + 2.2,相関係数r = 0.999であった。

Correlation of measured values between ‘LD·IF’ and ‘LD·J2’ using clinical serum samples. As a result, correlation is good (y = 0.923x + 9.8, r = 0.994, n = 206).
●: Specimens close to the regression line, ○: Specimens with deviation from the correlation line.
Figure 4に示す相関で低値に乖離していると考えられた5検体(〇)のLDアイソザイム分析結果は,LD5分画値が59%以上とMサブユニット優位な検体であった(Table 5)。
| No. | JSCC (U/L) | IFCC (U/L) | IFCC/JSCC | LD1 (%) | LD2 (%) | LD3 (%) | LD4 (%) | LD5 (%) |
|---|---|---|---|---|---|---|---|---|
| 1 | 356 | 318 | 0.89 | 11.7 | 13.3 | 7.8 | 7.2 | 60.0 |
| 2 | 244 | 223 | 0.91 | 8.3 | 11.7 | 8.4 | 8.7 | 62.9 |
| 3 | 334 | 278 | 0.83 | 2.6 | 4.9 | 5.9 | 10.2 | 76.4 |
| 4 | 250 | 220 | 0.88 | 8.8 | 12.1 | 10.1 | 9.9 | 59.1 |
| 5 | 372 | 320 | 0.86 | 8.1 | 10.9 | 8.4 | 6.2 | 66.4 |
| Reference range of LD isozyme | 20–32 | 28–35 | 21–27 | 6–13 | 4–14 | |||
当社職員検診で健常と判定されたLD測定値の基準範囲のパーセンタイル値(95%範囲)はJSCC法で108~203 U/L,IFCCでは108~202 U/Lと算出された。なお,Figure 5にLD活性値のヒストグラムを示した。

The standard range was calculated with 202 from 108 than the activity level of healthy persons (n = 348).
IFCC法試薬であるLD・IFの基礎的検討を行ったところ,精度(併行精度および再現精度)はC.V. 1.2%以内,検出限界は1.9 U/L,希釈直線性も約2,470 U/Lと良好な結果であった。比較対照試薬であるLD・J2との相関性も良好であり,LD・IF試薬は日常検査に十分利用可能な試薬性能を示した。また,赤血球はLD活性を有しており溶血検体は注意を要する。
LD・IF試薬の緩衝液のpHは9.4とLD・J2試薬のpH 8.8よりもアルカリ性であることから自動分析機上で試薬の装置内保存による測定(オンボード測定)する場合,二酸化炭素の吸収によりpHが低下することが考えられ,LD活性値の変動が懸念されるが,今回は検討を行っていないのでこの点は今後の課題としたい。ただし,当社総合研究所では1日当たりの受託検体数が多いために1~2日以内に試薬交換をするために試薬変更を行ってもこの点については問題ないと考えられた。
相関試験でJCSS法のLD・J2試薬よりもIFCC法のLD・IF試薬で低値に乖離した5検体についてLDアイソザイム分析を行った結果,LD5分画が59%以上と高値を示す検体であることが確認できた。従って,肝疾患の患者はLD5が優位となるため試薬の変更後の測定は低値傾向になるものと考えられた3)。また,乖離した5検体を除いた回帰式はy = 0.977x + 2.2,相関係数r = 0.999であったことよりIFCC法のLD・IF試薬はLDアイソザイムのHサブユニットに対してはLD・J2試薬とほぼ同等の値を示すことが確認された。一方,LD・IF試薬はMサブユニット優位な検体においてはLD・J2試薬よりもLD活性は低下することから,JSCC法からIFCC法に試薬変更する場合は臨床医への説明と注意喚起を十分に行う必要があると考えられた。
健常者の基準範囲をノンパラメトリック法で算定したところ,LD・J2試薬は108~203 U/L,LD・IF試薬は108~202 U/Lと両試薬から求めた基準範囲は許容誤差範囲内(検定で有意差なし)であったことから現行の基準範囲を変更する必要はないことが確認できた2),5)。ただし,現行法の共用基準範囲である124~222 U/L5)に比べると今回われわれが求めた基準範囲は約10%程度低値であったが,この点に関しては年齢や男女などの母集団の違いと考えられた。
以上の結果から,LD・IF試薬は日常的な臨床検査に用いることができる十分な試薬性能を有していた。今後,国際的な治験にも対応できる試薬と考えられるため,海外との測定値が共有化でき利便性が高くなることが期待できる。
LタイプワコーLD・IF試薬は今回の基礎的検討において良好な成績が得られたことから,日常検査に問題なく対応できる試薬である。また,基準範囲は現行の共用基準範囲よりもやや低値であったが,JSCC法試薬とIFCC法試薬に差が認められないことを確認した。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。