2022 Volume 71 Issue 4 Pages 638-643
2022 Volume 71 Issue 4 Pages 638-643
目的:SARS-CoV-2の新しい検査法は開発・普及が急速に進んでいる。当院では鼻咽頭ぬぐい液を検体とする検査は自動遺伝子解析装置のGeneXpertシステムを用いて実施していた。2020年7月以降より唾液検体が新型コロナウイルス核酸検出における正式な検体として認められたことから検体採取時における医療従事者への2次感染の防止などを考慮し,唾液検体での検査を要望された。これを受け新たにGENECUBEモデルC(東洋紡)を導入し,ジーンキューブ® HQ SARS-CoV-2(東洋紡)にて唾液検体での検査を実施することとなった。導入にあたり,唾液検体からの核酸抽出についても検討を進めることとなり,自動核酸抽出法であるmagLEAD(PSS,magLEAD法)とヒートブロックを使用する加熱抽出法について3つの検討を行った。方法:①擬似ウイルス管理試料で希釈系列を作成し,両核酸抽出法の検出能を検証した。②陰性確認済みの唾液検体に擬似ウイルス管理試料を加えた疑似検体を用いて両核酸抽出法への阻害物質の影響を検証した。③magLEAD法にて陽性であった臨床検体を加熱抽出法でも確認した。結果:magLEAD法の検出能は0.25コピー/μL,加熱抽出法で1コピー/μLであった。一方で加熱抽出法では検出ができなかった。結論:唾液検体を用いる場合は阻害物質の影響を考慮して検査をする必要があると思われた。
Purpose: Nucleic acid amplification assays for SARS-CoV-2 have been developed rapidly. Our laboratory has been testing for SARS-CoV-2 with Xpert Xpress using nasopharyngeal swab samples. However, the clinical staff requested that saliva samples be tested to prevent secondary infections of the medical staff. Therefore, we introduced GENECUBE® Model C and GENECUBE® HQ SARS-CoV-2. We evaluated the heat extraction and magLEAD methods. Methods: ① We prepared a dilution series with AccuPlex and evaluated the results of the two detection methods. ② We added saliva to AccuPlex to prepare a dilution series and examined the effects of the inhibitors on the two methods. ③ We compared the results of the two methods using clinical samples. Results: The LOD of the magLEAD method was 0.25 copies/μL and that of the heat extraction method was 1 copy/μL. From verification ②, the magLEAD method was found to have the same sensitivity as the heat extraction method even when saliva was added, but SARS-CoV-2 could not be detected by the heat extraction method. When verifying the illness days and fluorescence values of 40 clinical samples, the heat extraction method had a significant difference between 1–3 illness days and 4 illness days (p < 0.05). The magLEAD method had no significant difference between them. Conclusion: When using saliva samples, it seems necessary to consider the effects of inhibitors.
中国武漢市を発生源とする新型コロナウイルス感染症は2021年11月時点で,感染者数は全世界で2億5,000万人以上,500万人以上の死亡が報告されており1),国内での感染者数は170万人を超えている2)が,多くの市民や事業者の感染対策への協力やワクチン接種率の向上で,2回接種完了者が70%を超えるなどの甲斐があり3),10万人あたり1感染者と2020年の夏以降最も低い水準で推移している。しかし小規模なクラスターは絶えず発生しており,感染伝搬はなお続いているため4),引き続き積極的疫学調査が重要であると思われる。そのような中で,SARS-CoV-2の新しい検査法は開発・普及が急速に進んでいる。機種によっては感度特異度や測定時間や使用検体が異なる5)。当院のSARS-CoV-2検査は,鼻咽頭ぬぐい液を検体としてGeneXpertシステム(ベックマン・コールター株式会社,GeneXpert)で行っていたが,臨床側から医療従事者への感染のリスクを減らすために患者自ら採取可能な唾液検体での測定が望まれた。そして2021年5月より唾液検体で測定可能なGENECUBE(モデルC)(東洋紡,GENECUBE)と核酸抽出精製装置であるmagLEAD 6gC(プレシジョン・システム・サイエンス,magLEAD)を新たに導入することになった。今回,これらの機器を使用してGENECUBEの2つの核酸抽出法の検出能を比較し,SARS-CoV-2陽性患者検体の検出を検証したため報告する。
対象は2021年7月~2021年9月までの当院を受診されたSARS-CoV-2検査陽性患者の唾液検体40例とした。
2. 材料 1) GENECUBEによるSARS-CoV-2核酸検出本装置は核酸検出検査における作業工程を自動化した自動遺伝子解析装置である。専用試薬を組み合わせて使用することにより,新型コロナウイルス(SARS-CoV-2)核酸検出など,さまざまな感染症の検査に利用できる。増幅した標的核酸に対して,QProbeをハイブリダイズさせ,融解曲線解析によって蛍光のピーク温度を解析することでSARS-CoV-2 RNA検出を行う6)。検討には専用試薬であるジーンキューブ® HQ SARS-CoV-2(東洋紡)を使用した。本試薬の核酸抽出については,事前の処理を行う必要があり,2通りの核酸抽出を採用し,GENECUBEで測定した。
2) ヒートブロックを使用した核酸抽出後,GENECUBEで測定する方法(以下,加熱抽出法)プロテイナーゼKによって検体中の核酸合成酵素阻害物質を65℃で分解し,95℃でウイルスと同時にプロテイナーゼKを失活させる。その後溶解液と混合し,GENECUBEで測定を行う。測定結果は本試薬の場合,標的遺伝子の蛍光値が10を超えると陽性と判定され,検体受付から約50分で結果を出すことができる。
3) magLEADによる核酸抽出後,GENECUBEで測定する方法(以下,magLEAD法)magLEADは磁性粒子を担体として核酸の抽出・精製を行っている「Magtration法」を用いて行っている。Magtration法では,分注チップの側面に磁石をあてて磁性粒子を分注チップ内で捕獲・分散させる。この工程で検体を4倍まで濃縮することができる。試薬は全てカートリッジ内にあらかじめ封入されており,前処理後,magLEADで核酸抽出を行い,GENECUBEで測定を行う。加熱抽出法と同様,蛍光値が10を超えると陽性と判定され,検体受付から約70分で結果を出すことができる7)。各測定法の特徴をTable 1に示す。
| 測定機器 | GENECUBE (magLEAD法) |
GENECUBE (加熱処理法) |
| 測定原理 | QProbe-PCR | QProbe-PCR |
| 抽出法 | magLEADを使用 | ヒートブロックを使用 |
| 測定時間 | 約70分 | 約50分 |
| 標的RNA | N1及びN2 | N1及びN2 |
| コスト | 2,500円 | 2,000円 |
| 試薬供給 | 300/月 | 300/月 |
| 値 | 蛍光値 | 蛍光値 |
加熱抽出法は1.5 mLチューブにプロテイナーゼK(関東化学)10 μLを分注し,検体100 μLを加えて,混合した。混合後,ヒートブロックで65℃,5分間加温後,更に95℃,5分間で加温した。加温後,遠心(13,000 × g,2分間),冷却した検体を専用溶解と等量混合しGENECUBEで測定した。
一方,magLEAD法は検体とセミアルカリプロテアーゼ(極東製薬工業)を等量加え,十分に攪拌した後15分間インキュベーションした。その後,上清150 μLとPrep Buffer A(プレシジョン・システム・サイエンス)を混合し,5分間インキュベーションした後,magLEADで核酸抽出したものをGENECUBEで測定した。
4. 検討方法 1) 検討①各方法の感度を調べるためにウイルス量がわかる擬似ウイルス管理試料を用いた検討を行った。対象は疑似ウイルス管理試料AccuPlex SARS-CoV-2(seracare, AccuPlex)を使用した。AccuPlex(原液5コピー/μL)を滅菌精製水(大塚製薬)で0.125~1コピー/μLまでの希釈系列を作成し検体として,3重測定を実施した。
2) 検討②各方法の唾液の影響をみるためにAccuPlexに唾液(SARS-CoV-2陰性確認済み)を混合したものを検体として希釈系列を作り,3重測定を実施した。
3) 検討③SARS-CoV-2陽性患者検体を用いて,各方法で測定を行い,結果一致率,発症病日と,各機器の測定値について比較を行った。
3重測定により全て陽性となった最終濃度を検出感度とすると,加熱抽出法の検出感度は1コピー/μLであった。また,magLEAD法の検出感度は0.25コピー/μLであった(Table 2, Figure 1)。
| 原液 5,000/mL(5/μL) |
5倍希釈 1,000/mL(1/μL) |
10倍希釈 500/mL(0.5/μL) |
20倍希釈 250/mL(0.25/μL) |
40倍希釈 125/mL(0.125/μL) |
|
|---|---|---|---|---|---|
| magLEAD法 | (+)53.82 | (+)21.29 | (+)24.33 | (−)3.44 | |
| (+)50.77 | (+)42.94 | (+)11.87 | (−)9.17 | ||
| (+)50.23 | (+)40.37 | (+)21.29 | (−)5.29 | ||
| 加熱抽出法 | (+)31.01 | (+)11.56 | (−)8.50 | NT | |
| (+)36.79 | (−)1.80 | (−)1.65 | NT | ||
| (+)28.85 | (−)1.39 | (−)3.56 | NT |
(判定結果)数値は蛍光値,赤字は陽性を示す。(NT: not tested)
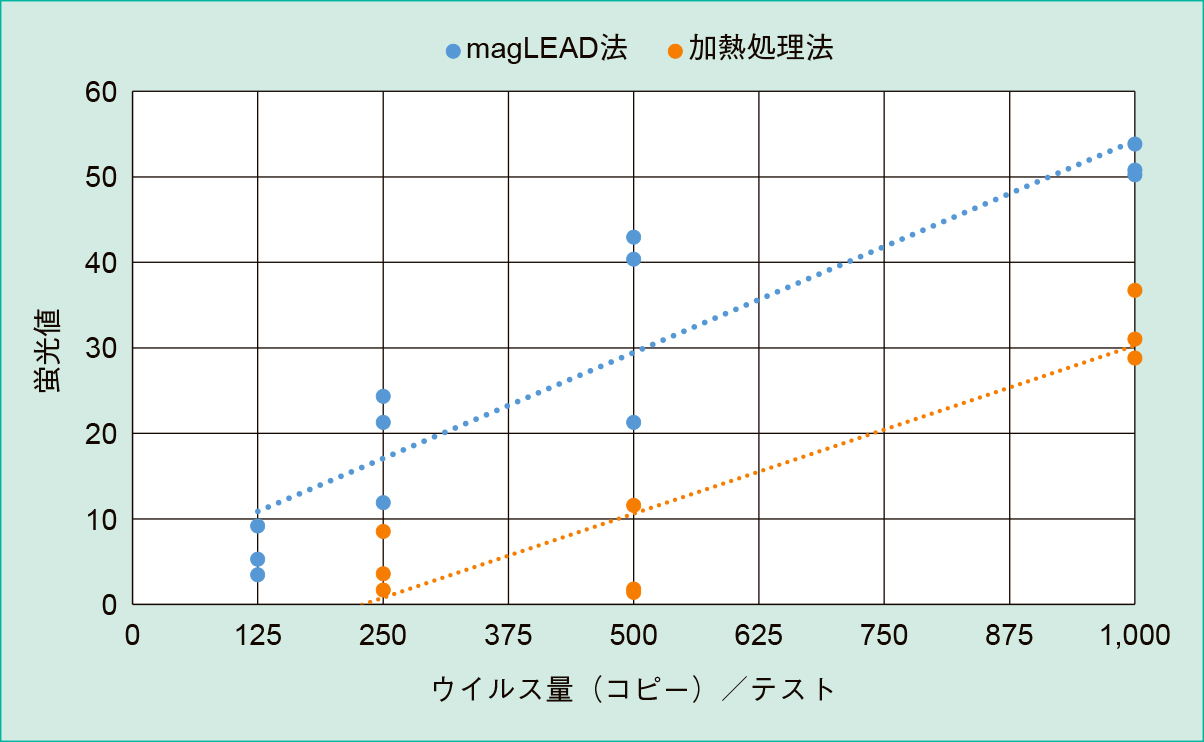
正の相関を認める。
3重測定により全て陽性となった最終濃度を検出感度とすると,加熱抽出法では検出できなかった。magLEAD法の検出感度は0.25コピー/μLと検体阻害の影響の有無にかかわらず同様の結果であった(Table 3, Figure 2)。
| 5倍希釈 1,000/mL(1/μL) |
7倍希釈 714/mL(0.714/μL) |
10倍希釈 500/mL(0.5/μL) |
20倍希釈 250/mL(0.25/μL) |
40倍希釈 125/mL(0.125/μL) |
|
|---|---|---|---|---|---|
| magLEAD法 | (+)40.97 | (+)52.07 | (+)13.24 | (+)10.55 | |
| (+)42.55 | (+)41.85 | (+)18.38 | (−)0.00 | ||
| (+)44.35 | (+)26.38 | (+)10.56 | (−)3.27 | ||
| 加熱抽出法 | (−)0.00 | NT | NT | NT | NT |
| (−)1.92 | NT | NT | NT | NT | |
| (−)1.45 | NT | NT | NT | NT |
(判定結果)数値は蛍光値,赤字は陽性を示す。(NT: not tested)

正の相関を認める。
判定結果は1例不一致があった(Table 4)。また,magLEAD法の蛍光値では有意差が認められなかったが,加熱抽出法は4病日目に有意な差があった(p < 0.05)(Figure 3, 4)。
| GENECUBE (magLEAD法) |
|||
|---|---|---|---|
| (+) | (−) | ||
| GENECUBE(加熱処理法) | (+) | 39 | 0 |
| (−) | 1 | 0 | |
| 合計 | 40 | 0 | |
陽性一致率 97.5%

1~3病日と4病日目で差を認める(p < 0.05)。

1~3病日と4病日目で差が見られない。
検討①の結果より,加熱抽出法の検出感度は1コピー/μLであり,検査にはおよそ4 μL使用しているため4コピー/テストとなる。これはKiyasuらの報告8)や,添付文書上の最低検出感度(10コピー/μL)よりも良好な結果が得られた。また,magLEAD法の検出感度は0.25コピー/μLであり,検査にはおよそ4 μL使用しているため1コピー/テストとなる。これは添付文書上の最低検出感度(10コピー/μL)の10倍高い感度が得られた。magLEADで核酸抽出するプロセスで,精製と4倍まで濃縮することができ,検出感度の向上が可能である。検討①のように既知濃度のウイルスを測定する場合,阻害物質の影響がなければ理論上4倍検出感度が向上する。magLEAD法は加熱抽出法の4倍感度が向上しているため正しく操作ができていることが確認できた。
また検討②のように唾液を混合させると阻害物資等が混じることになるが,加熱抽出法では1コピー/μLでは検出しなかった。加熱抽出法の阻害物質の除去は規定量のプロテイナーゼKを一定時間反応で分解させるが,唾液の阻害物質の量は検体によって一定ではないため,多少阻害物質の残留が予想される。これが影響して低コピー数では検出しなかったことが考えられる。一方,magLEAD法の感度は0.25コピー/μLであった。magLEAD法は阻害物質を洗浄除去しながら核酸だけを抽出する工程があるが,検討①と同感度であったことから,ほぼ除去できていると考えられる。
検討③より,加熱抽出法で1例陰性となった患者は9病日目となったため,ウイルス量が少なかったことが考えられる。1コピー/μL以下のようなごく微量のウイルスが含まれる検体の場合,核酸精製工程の有無で差が認められた。
数値で検証すると加熱抽出法は発症病日1日目と4日目の蛍光値に有意な差がみられたが,magLEAD法では見られなかった。これはmagLEADが検体の核酸を濃縮精製しているため感度が向上していることがわかる。本検討期間での陽性となった患者背景は,発熱を機に受診された患者と濃厚接触者の方がほとんどで,98%が発病日数4日以内と早い段階で受診されているため発症早期のデータ検証となっている。5病日以降のデータが集まっていれば同じようにmagLEAD法でも有意差が見られた可能性がある。
今回の結果を受けて,検査体制や臨床の要望に合わせて,検査法(特に核酸抽出)と検体種を選択して検査することが望ましい。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。