2023 Volume 72 Issue 2 Pages 306-312
2023 Volume 72 Issue 2 Pages 306-312
症例は40代の男性。主訴は悪寒,発熱,呼吸困難,胸部違和感。経胸壁心臓超音波検査(transthoracic echocardiography; TTE)では,左室は壁運動のびまん性高度低収縮と対称性左室肥大を認めた。また,右室にも壁運動低下を認めた。劇症型心筋炎(fulminant myocarditis; FM)と診断され,他院へ治療目的で紹介となった。他院搬送後,血行動態が悪化したため,経皮的心肺補助法(percutaneous cardiopulmonary support; PCPS),大動脈内バルーンパンピング(intra aortic balloon pumping; IABP)の導入となった。冠動脈造影検査では冠動脈に有意狭窄はなく,右室より心筋生検が施行された。組織学的に心内膜下および心筋内にリンパ球,形質細胞主体の炎症細胞浸潤を認めた。5日後にはPCPSおよびIABPから離脱し,再度行ったTTEでは左室肥大および壁運動低下,右室壁運動低下は改善が認められた。FMの超音波所見として左室の対称性壁肥厚やびまん性壁運動低下が特徴的とされており,右室壁運動低下を合併した報告は少ない。本症例は,左室のびまん性肥厚と壁運動低下に加え,右室の壁運動低下も認めた稀な1例であった。
The patient was a male in his 40s. He suffered from breathing difficulty, as well as chest discomfort, chills, and fever. Advanced diffuse hypocontraction and left ventricular hypertrophy (LVH) were confirmed in the left ventricle by transthoracic echocardiography (TTE). Furthermore, hypocontraction in the right ventricle was confirmed as well. He was diagnosed as having fulminant myocarditis (FM) and referred to another hospital for treatment. Once transferred to the other hospital, his hemodynamics declined and he required percutaneous cardiopulmonary support (PCPS), and intra-aortic balloon pumping (IABP) was introduced. There was no significant coarctation in the coronary artery upon coronary angiography, so a myocardial biopsy was conducted from the right ventricle. Subendocardium and intramyocardial lymphocytes, as well as plasma-cell dominant inflammatory cell infiltrate, were histologically confirmed. Five days later, we were able to remove the PCPS and IABP. Improvements of the wall motion in both the left and right ventricles and the LVH were observed upon repeat TTE. LVH and left ventricular diffuse hypocontraction determined by ultrasound examination are said to be characteristic symptoms of FM, with only a few cases reported in which complications occurred in the right ventricle abnormal wall motion. In this case, we confirmed a decline in the right ventricle wall motion along with left ventricular hypocontraction and LVH. We encountered a rare case in which we were able to observe by ultrasound exams the course of FM in both the left and right ventricles due to an infection.
心筋炎は心筋を主座とした炎症性疾患であり,その中でも血行動態の破綻を急激に来たし,致死的経過をとる急性心筋炎を劇症型心筋炎(fulminant myocarditis; FM)と定義される。この病態の超音波所見としては,左室の全周性求心性壁肥厚とびまん性壁運動低下が特徴とされている。われわれは,左室の肥厚および壁運動異常に加え,右室壁運動異常も来たしたFMの1例を経験したので報告する。
患者:40代,男性。
主訴:悪寒,発熱,呼吸困難,胸部違和感。
既往歴:特記すべき事項なし。
家族歴:特記すべき事項なし。
現病歴:某年2月に悪寒と38℃の発熱で近医を受診し,抗菌薬内服で経過観察されていた。3日後に呼吸困難や胸部違和感が出現し,当院内科へ紹介となった。
来院時現症:身長は173 cm,体重は76.5 kg,体温は36.5℃であった。血圧は収縮期血圧は80 mmHg,拡張期血圧は計測不可であった。眼球結膜の黄染や眼瞼結膜の貧血は認めなかった。心拍数は100 bpm,SpO2は98%であった。心音は整で心雑音はなく,呼吸音は清であった。
血液検査は,トロポニンT,CRP,NT-proBNPの上昇を認めた。また肝機能および腎機能障害を認めた(Table 1)。
| 血算 | 凝固 | 生化学 | |||||
|---|---|---|---|---|---|---|---|
| WBC | 7.34 × 103/μL | APTT | 29.7秒 | TP | 6.7 g/dL | Na | 130 mmol/L |
| RBC | 5.03 × 106/μL | PT | 71% | AST | 111 U/L | K | 4.7 mmol/L |
| Hb | 15.3 g/dL | PT-INR | 1.19 | ALT | 83 U/L | Cl | 91 mmol/L |
| Ht | 44.6% | D-dimer | 1.7 μg/mL | LDH | 536 U/L | CRP | 25.53 mg/dL |
| MCV | 88.7 fL | CK | 214 U/L | NT-proBNP | 33,866 pg/mL | ||
| MCH | 30.4 pg | CK-MB | 20 U/L | フェリチン | 1,087 ng/mL | ||
| MCHC | 34.3 g/dL | BUN | 90 mg/dL | プロカルシトニン | 1.040 ng/mL | ||
| PLT | 223 × 103/μL | CRE | 2.32 mg/dL | トロポニンT | 3.24 ng/mL | ||
心電図検査は,洞調律,心拍数は101/分であった。四肢誘導で低電位,I・aVL・V5・V6誘導で軽度ST上昇を認めた(Figure 1)。

洞調律で,心拍数は101/分であった。四肢誘導にて低電位,I・aVL・V5・V6誘導にて軽度ST上昇を認めた。
胸部X線では,CTRは58%,右肺炎像と少量の胸水貯留を認めた(Figure 2)。

CTRは58%,右肺炎像と軽度胸水貯留を認めた。
単純CTでは,右肺に軽度の肺炎像と少量の両側胸水及び少量の心嚢水を認めた(Figure 3)。

右肺に軽度の肺炎像と両側少量胸水,少量の心嚢水を認めた。
経胸壁心臓超音波検査(transthoracic echocardiography; TTE)では,左室壁運動はびまん性高度低収縮で左室駆出率(left ventricular ejection fraction; LVEF)は24%,左室長軸方向収縮期ストレイン(left ventricular global longitudinal strain; LVGLS)は−5.8%と低値を示した。また,対称性左室肥大(中隔および後壁厚12 mm)と少量の心嚢水貯留を認めた。右室内腔面積変化率(right ventricular fractional area change; RVFAC)は15%,三尖弁輪収縮期移動距離(tricuspid annular plane systolic excursion; TAPSE)は7 mmであり著明な右室壁運動低下を認めた。右室長軸方向収縮期ストレイン(right ventricular global longitudinal strain; RVGLS)は−6.7%,右室自由壁長軸方向収縮期ストレイン(right ventricular free wall longitudinal strain; RVFWSL)は−6.4%と低下していた。三尖弁逆流は軽度~中等度で三尖弁圧較差(transtricuspid pressure gradient; TRPG)は15 mmHgであった(Figure 4 使用機器:GEヘルスケアジャパン社製VividE90 使用プローブ:M5Sc-Dプローブ)。

左室壁運動はびまん性高度低収縮,左室後壁~下壁側に軽度の心嚢水貯留を認めた。左室右室共に長軸方向のストレイン値は低下していた。傍胸骨左室長軸像;拡張期(A)収縮期(B),傍胸骨左室短軸像;拡張期(C)収縮期(D),心尖部四腔像;拡張期(E)収縮期(F),左室長軸方向ストレイン(G)右室長軸方向ストレイン(H)
臨床所見および各種検査所見より劇症型心筋炎と診断され,他院へ治療目的で紹介となった。他院搬送後,血行動態の悪化を認め,経皮的心肺補助法(percutaneous cardiopulmonary support; PCPS),大動脈内バルーンパンピング(intra aortic balloon pumping; IABP)の導入となった。冠動脈造影検査では冠動脈に有意狭窄はなく(Figure 5),右室より心筋生検を実施した。組織学的に,心内膜下や心筋細胞間にリンパ球,形質細胞を主体とする高度な炎症細胞浸潤を認め,急性心筋炎に合致した所見であった(Figure 6)。好酸球性心筋炎や巨細胞性心筋炎を示唆する特異な所見はみられなかった。外注検査で血清中のウイルス抗体価を検査したところ,明らかな陽性所見は得られなかったが(Table 2),上記病理所見よりウイルス感染に伴うFMが最も考えられた。5日後にはPCPSおよびIABPから離脱し,再度施行されたTTEで左室肥大および壁運動低下,右室壁運動低下の改善が認められた(Figure 7)。20日後には退院し,現在外来にてフォロー中である。

有意な冠動脈病変は認めなかった。

心内膜下や心筋細胞間にリンパ球,形質細胞主体の炎症細胞浸潤を認め,好中球,少量の好酸球も混在してみられた。急性心筋炎に合致する像であった。A:×100(対物レンズ10×),B:×400(対物レンズ40×)
| 病原体 | 抗体価 |
|---|---|
| アデノウイルス | 検出せず |
| SARS-COV2 | 検出せず |
| ヒトニューモウイルス | 検出せず |
| インフルエンザウイルス | 検出せず |
| パラインフルエンザウイルス | 検出せず |
| RSウイルス | 検出せず |
| ライノウイルス | 検出せず |
| エンテロウイルス (コクサッキーウイルス,エコーウイルス含む) |
検出せず |
| B型肝炎ウイルス | 検出せず |
| C型肝炎ウイルス | 検出せず |
| パラ百日咳 | 検出せず |
| クラミジア | 検出せず |
| マイコプラズマ | 検出せず |
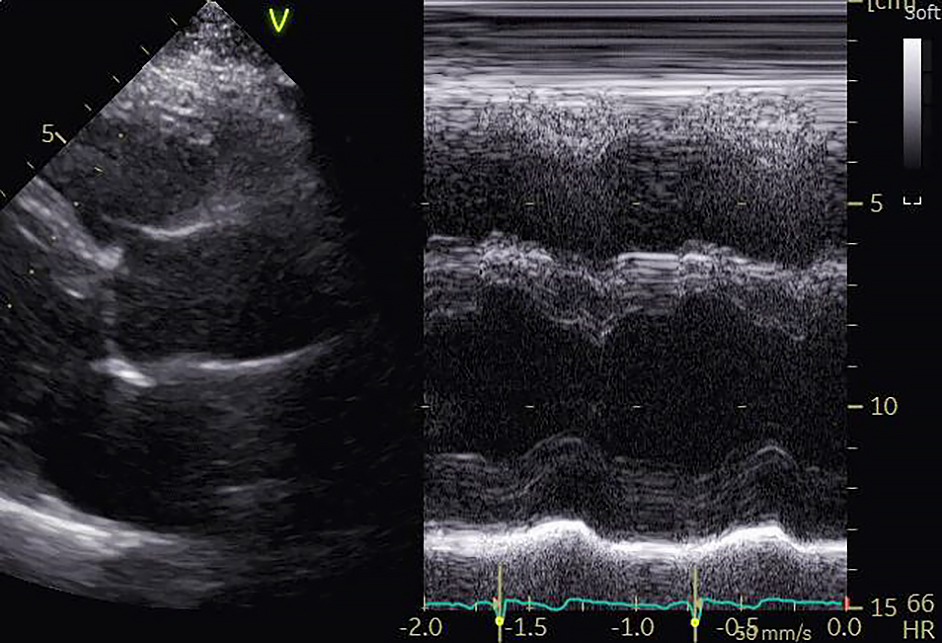
左室壁の肥厚および収縮能は改善した。
急性心筋炎は心臓が炎症過程の状態にあり,それに引き続いて心筋細胞の壊死や変性を来たす疾患である。心筋炎は組織学的特徴から,リンパ球性心筋炎,巨細胞性心筋炎,好酸球性心筋炎,肉芽腫性心筋炎に分類され,リンパ球性心筋炎はウイルス感染によるものが多いとされている。原因ウィルスには,コクサッキーウイルスB群1–6型,およびA群4・9・16型,アデノウイルス,サイトメガロウイルス,エコーウイルス9・11・14・16・22型,パルボウイルスB19,ヒトヘルペスウイルス6型,インフルエンザAおよびBウイルスなどがよく知られている1),2)。本症例では,Table 2に示す13種類のウイルスの血清抗体価を検査したが,原因となるウイルスを特定するには至らなかった。しかし,検査できた抗体価の種類は原因となるウイルスのごく一部に過ぎないことや,心筋生検が施行され,組織学的に心内膜下や心筋細胞間にリンパ球および形質細胞を主体とする高度な炎症細胞浸潤を認めたことから,本症例はウイルス感染に伴う心筋炎とするのが妥当と考えられた。
FMは一般的に「血行動態の破綻を急激に来たし,致死的経過をとる急性心筋炎」と定義され,体外循環補助を必要とした重症度を有する心筋炎を指す3)。FMの機械的循環補助としてPCPS,IABPが第一選択となるが,より重篤なFMの場合は,IABPやPCPSの短期補助では救命できず補助人工心臓(ventricular assist device; VAD)による長期間の循環補助や心移植に至る症例もあり,その中には,左心のみならず右心不全も合併した重篤な両心不全を呈することも報告されている4)。本症例はこの報告例と同様に左心だけでなく右心不全を伴うFMの1例であったが,比較的予後は良好でPCPSおよびIABP導入により救命できVADへの移行には至らなかった。このように右心不全を合併したFMの予後について本症例と過去の報告例を比較してみても一定の傾向はみられなかったが,稀な病態であるため十分な解析がなされているとはいえない。
急性心筋炎の超音波所見として,心膜液貯留に加えて,炎症部位に一致した一過性の壁肥厚と壁運動低下が特徴的とされ,典型例では左室の全周性求心性壁肥厚とびまん性壁運動低下,心腔の狭小化を認める5),6)。FMにおいても同様に左室のびまん性の壁肥厚および壁運動低下がみられ,このような左室を中心とした特徴的な超音波所見はFMを含めた急性心筋炎を診断する上で極めて重要である。急性心筋炎のうちおおよそ3割がFMを引き起こすとされているが7),このような症例ではLVEFが40%未満に低下していることが多いと報告されている8)。本症例においても心膜液の軽度貯留と左室の求心性壁肥厚,LVEFは24%と左室壁運動の著明な低下を認め,FMに典型的な超音波所見が得られた。しかし,LVEFが40%未満であっても劇症化に至らなかった例9)~11)や,逆にLVEFが40%以上であっても劇症型心筋炎となった例12)も少なからず認められることから,LVEFだけでは劇症化の予測は困難である。一方,本症例と同様にFM症例で右心不全を合併した場合はより重篤であるとする報告がみられることから,右心機能の評価が劇症化予測の新たな指標となる可能性を否定できない。TTEにて右室の収縮機能を評価する方法としてTAPSE,組織ドプラ法による三尖弁輪収縮期最大移動速度(S’),RVFAC,RVGLS,RVFWSLがあり,異常値はTAPSE < 17 mm,s’ < 9.5 cm/s,RVFAC < 35%,RVGLSおよびRVFWSL −20%とされている13)。本症例では,RVFACは−15.6%,TAPSE 7 mm,RVGLS −6.7%,RVFWSL −6.4%と明らかな異常値を示し,右心収縮機能の著しい低下を裏付けることができた。従って,FMで右室に壁運動の低下がみられた場合には積極的に超音波検査を施行し,客観的な数値によって右室を評価することは重要と考えられた。しかし,本症例のようにFMにおいて超音波検査で右心機能の詳細な解析がなされた報告はわれわれが調べた限りでは過去にみられないため,急性心筋炎の劇症化予測と右心機能との関連については今後のデータの積み重ねが必要であると思われる。
本論文の要旨は,第55回中四国医学検査学会(2022年10月,広島)において発表した。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。