2012 Volume 45 Issue 7 Pages 732-739
2012 Volume 45 Issue 7 Pages 732-739
症例は70歳の男性で,心窩部痛を主訴に近医を受診,肝腫瘤を指摘され当院紹介となった.肝炎ウイルスマーカーは陰性,血清CA19-9は上昇していた.造影CTで肝内側区域を主座とし,辺縁から内部に向かって不均一に造影される6 cm大の腫瘍と,臍部から左枝に至る門脈腫瘍栓,左葉肝内胆管の拡張を認めた.腫瘤形成型肝内胆管癌の診断で,拡大肝左葉切除術を施行した.病理組織学的検査所見では腫瘍は主に中分化型腺癌,充実性増殖部,および紡錘形細胞の3成分からなり,互いに移行像を認めた.また門脈腫瘍栓は肉腫様の紡錘形細胞で構成されていた.術後8か月で肝内多発転移および縦隔リンパ節転移を認めたが,化学療法を施行し,術後27か月生存中である.肉眼的に明らかな門脈腫瘍栓を伴う肝内胆管癌の切除報告は少なく,中でも門脈腫瘍栓が肉腫様成分からなるものは本症例のみとまれである.その臨床病理組織学的特徴について,文献的考察を加え報告する.
肝内胆管癌の中でも肉腫様変化を伴う症例は少なく,急激な進行・転帰を呈し予後不良とされる1).また肝内胆管癌で画像上明らかな門脈腫瘍栓を伴うことはまれである.今回,肉腫様成分を含み,臍部から左枝に至る門脈腫瘍栓を伴った肝内胆管癌の1例を経験したので,文献的考察を加え報告する.
患者:70歳,男性
主訴:心窩部痛
既往歴:尿路結石症
家族歴:特記すべきことなし.
現病歴:心窩部痛で近医を受診し,精査の結果,肝左葉の腫瘍を指摘され,当院へ紹介された.
現症:身長172 cm,体重80 kg,腹部は平坦,軟で腫瘤は触知せず.心窩部に軽度圧痛を認めたが,反跳痛は認めなかった.
入院時検査所見:ALP値404 IU/l, γ-GTP値131 IU/lと胆道系酵素の軽度上昇を認めた.腫瘍マーカーはCA19-9のみ301 U/mlと高値であったが,CEA, AFPやPIVKA-IIは正常範囲内であった.またB型・C型肝炎ウイルスマーカーは陰性であった.
腹部超音波検査所見:肝左葉に6 cm大の比較的境界明瞭で内部不均一な腫瘍と左葉肝内胆管の拡張を認めた.腫瘍近傍の門脈臍部は不明瞭で,内部血流は確認できず,腫瘍進展が疑われた.また中肝静脈は下大静脈合流部から末梢側5 cmの範囲で腫瘍により圧排され軽度狭小化していた.
腹部造影CT所見:肝内側区域を主座として,動脈相で辺縁から造影され,平衡相で淡く不均一に造影される6 cm大の腫瘍と(Fig. 1a),腫瘍から連続して臍部,左枝に至る門脈内の欠損像,および左葉肝内胆管の拡張を認めた(Fig. 1b).また左および中肝静脈は腫瘍による浸潤を受けていた.
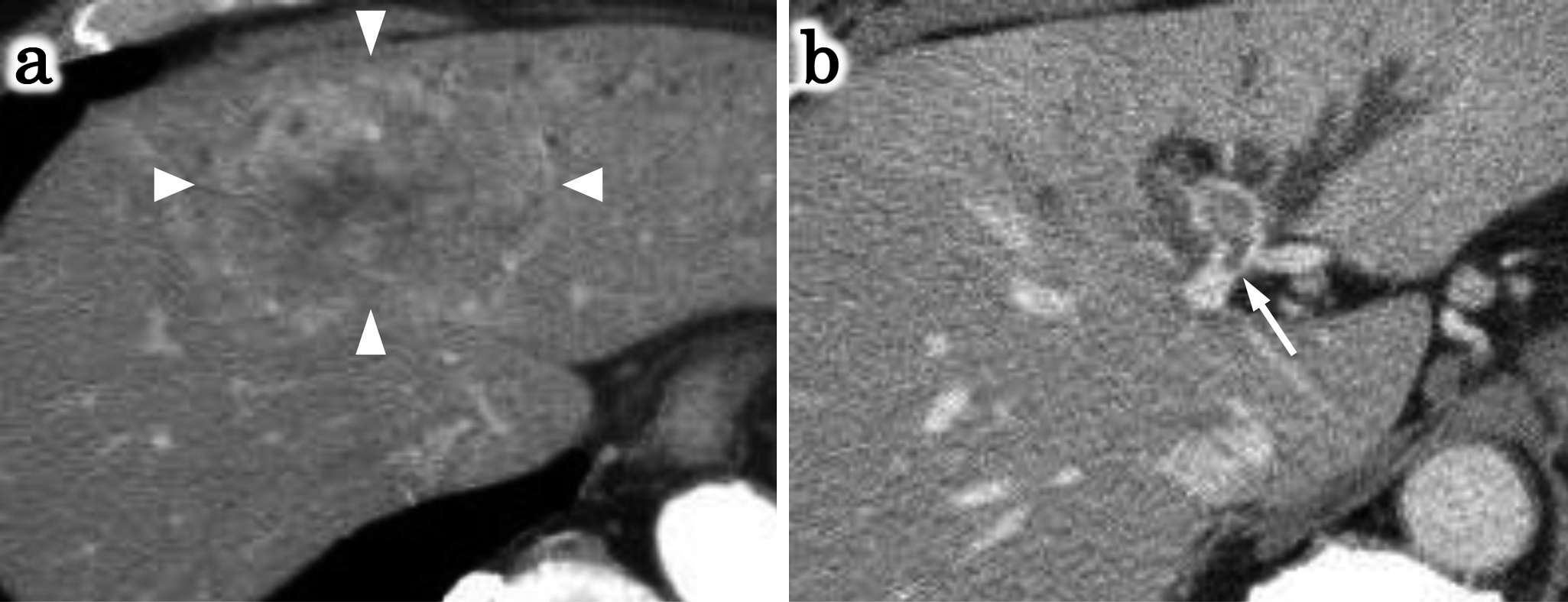
Contrast-enhanced CT scan revealed an irregularly-shaped tumor in the medial segment of the liver with peripheral enhancement in the arterial phase (a: arrowheads). Axial image demonstrated the presence of tumor thrombus in the umbilical portion and the left portal vein (b: arrow).
以上の所見から,門脈腫瘍栓を伴う腫瘤形成型の肝内胆管癌,ないし混合型肝癌,St-ML,6.0 cm,S0,N0,Vp3,Vv2,B2,P0,M0,T3N0M0,Stage IIIと診断し,手術を行った.
手術所見:肝内転移,腹膜播種なし.肝内側区域表面に腫瘤を触知した.術中迅速病理組織学的診断にて,8a, 16b1intリンパ節いずれも転移陰性で,肝十二指腸間膜内に腫大したリンパ節を認めなかったことより,リンパ節郭清は不要と判断した.術中超音波検査で腫瘍は中肝静脈に接していたため,腫瘍が露出しないように前区域の一部と中肝静脈を含む拡大左葉切除術を施行した.術中迅速診断で左肝管断端は腫瘍進展陰性,また門脈については,術中超音波検査で腫瘍栓が門脈左枝内に留まっていることを確認の上,腫瘍栓より中枢側の門脈左枝根部で結紮切離した.
切除標本肉眼所見:腫瘍は肝内側区域から外側区域にかけて存在する6 cm大の境界明瞭な充実性腫瘍であった.腫瘍割面は黄白色で軽度膨隆を認める弾性軟の部分と,その周囲の灰白色で膨隆を認めない弾性硬の部分から構成されていた.また内側区域門脈枝から門脈臍部,左枝に腫瘍栓を認めた(Fig. 2).腫瘍より切離面までの肉眼的距離は最短5 mmであった.
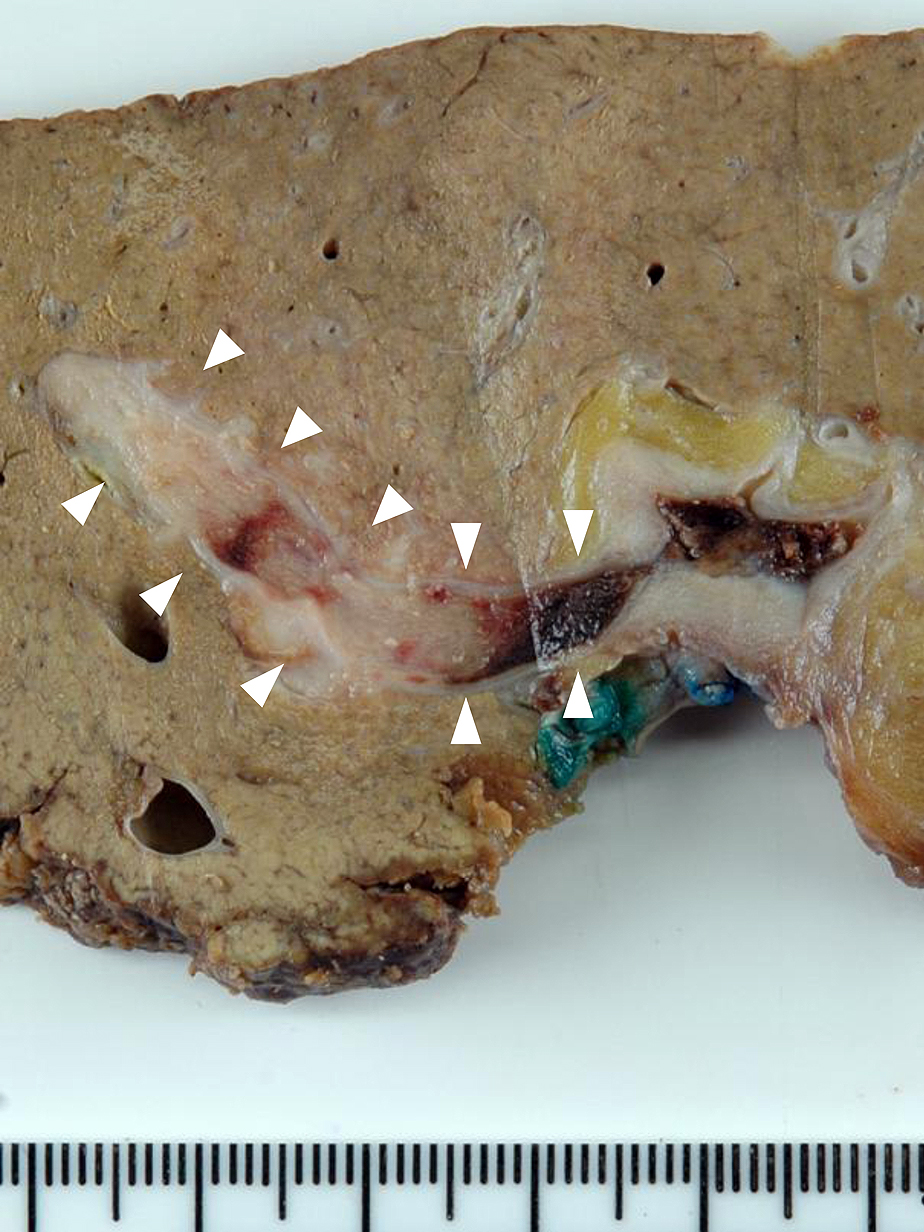
Macroscopic finding of the resected specimen. Tumor thrombus (arrowheads) was seen in the medial segmental portal branch and the left portal vein.
病理組織学的検査所見:組織像は主に3種に分類でき,占める割合が多い順に,1)充実性増殖部(60%);小型類円形不整核と好酸性胞体を有する腫瘍細胞が充実性に増殖する領域(Fig. 3a),2)紡錘形細胞(肉腫様)(30%);肉腫に類似した紡錘形の腫瘍細胞が著明な線維間質の増生を伴い増殖する領域(Fig. 3b),1)と2)の間に3)中分化型腺癌(10%);不整な癒合腺管や篩状構造を有する中分化型腺癌が散在する領域(Fig. 3c),から構成され,これら3成分には移行像を認めた.また門脈腫瘍栓は組織学的には紡錘形細胞から形成されていた.免疫染色検査では充実性増殖部は上皮系のマーカーであるcytokeratin(以下,CKと略記)7陽性,epithelial membrane antigen(以下,EMAと略記)陽性,間葉系のマーカーであるvimentin陽性,紡錘形細胞はCK7陰性,EMA陰性,vimentin陽性,中分化型腺癌はCK7陽性,EMA陽性,vimentin陰性であり,いずれの腫瘍も抗肝細胞抗体は陰性であった(Fig. 4).以上より,病理組織診断はcholangiocellular carcinoma with sarcomatous differentiation,mass forming type,6.0×6.0×5.0 cm,ig,fc(–),sf(–),s0,n0,vp3,vv2,va0,b2,p0,sm(–),im(–),T3N0M0,Stage IIIであった.

Histological findings of the tumor. The hepatic tumor was composed of the solid proliferative component with small oval nuclei and eosinophilic cytoplasm (a), the spindle-shaped sarcomatous component with abundant fibrous stroma (b) and the moderately differentiated adenocarcinoma component with distorted tubular glands with cribriform formation (c).

Histological findings of the transitional regions between the solid component (*) and the adenocarcinoma component (***) (a, b), and between the sarcomatous component (**) and the adenocarcinoma component (***) (c, d). Immunohistochemical stainings for CK-7 and vimentin (a–d). The solid component showed positive reactions for CK-7 and vimentin. The sarcomatous component was negative for CK-7 and positive for vimentin. The adenocarcinoma component was positive for CK-7 and negative for vimentin.
術後経過:術後第15病日に退院した.術後8か月のCTで肝内多発転移および縦隔リンパ節転移を認めたため,gemcitabineによる全身化学療法を開始した.術後16か月頃よりCA19-9の上昇および再発巣の増大を認め,progressive disease(以下,PDと略記)と判定,化学療法をgemcitabine+cisplatinへ変更したが,5か月間でPDとなり,その後S-1投与するもPDのため緩和医療へ移行した.術後27か月現在生存中である.
肝内胆管癌は肝細胞癌と比較し切除成績は不良で,診断された時点で切除不能である症例も少なくない.肝内胆管癌の治療成績が不良である要因としては,早期発見が困難であること,血管侵襲傾向が強く肝動脈および門脈に高頻度に浸潤すること,リンパ管・神経周囲侵襲,リンパ節転移および腹膜播種が多いこと2),などが挙げられる.
本邦における原発性肝癌に占める肝内胆管癌の割合は,4.4%と報告されている3).中でも肉腫様変化を伴う胆管癌は肝内胆管癌の4.5%とまれである1).肉腫様変化とは,病理組織学的には「いわゆる癌肉腫」に相当し,以前より「真の癌肉腫」との区別に混乱が生じていた.最近では「真の癌肉腫」は上皮由来の癌腫と間葉系細胞由来の肉腫が混在し,肉腫成分に骨や軟骨などの明らかな特異的間葉系腫瘍成分が含まれるものと定義され,「いわゆる癌肉腫」は一見肉腫様に見えるが特定の肉腫の特徴をもたず,癌腫と肉腫間に移行部が存在し,癌腫が肉腫様に分化したものと定義されている4)5).本症例では肉腫様部分に特定の分化を認めず,さらに,癌腫と肉腫様成分の間に移行像を認めることから,「いわゆる癌肉腫(肉腫様変化)」に相当すると考えられた.
肉腫様変化を伴った肝内胆管癌の切除報告例は,医学中央雑誌で1983年から2011年9月までの期間で「肝内胆管癌」,「胆管細胞癌」,「肉腫様」をkey wordに検索した結果,会議録を除いて8例,またPubMedで「intrahepatic cholangiocarcinoma」,「cholangiocellular carcinoma」,「sarcomatous」,「sarcomatoid」をkey wordに検索した結果,27例あり,自験例を含め36例であった1)6)~24).報告例の臨床的特徴として,平均年齢65歳(37~87歳)で,男性21例,女性15例と男性にやや多く,初発症状は腹痛や発熱が多く,これらは出血,壊死像や腫瘍増大速度に関連していると考えられる.また,腫瘍径は平均8.5 cm(2.5~22 cm)で,診断時にはすでに大きな腫瘍となっており,増殖能が高いことを示唆する結果であった.肝内胆管癌では一般的にCEAやCA19-9が上昇することが多いが,肉腫様変化を伴う肝内胆管癌では,腫瘍マーカーの陽性率はCEA 16%, CA19-9 48%とそれほど高くない.また画像診断でも特徴的な像はなく,通常の肝内胆管癌と鑑別困難である15).治療法は手術による完全切除が唯一長期予後を期待できる方法とされ,化学療法や放射線療法の有効性は明らかではない.病理組織学的検査所見では85%の症例で肉腫様成分が優勢で,vimentin陽性率85%,CK陽性率86%,EMA陽性率65%であった.Nakajimaら1)は肉腫様成分でCKやEMA陽性の症例は上皮系の特徴を有し,陰性症例はより未分化に近い脱分化を示していると報告している.
予後については,過去報告例で予後判明33例中19例は術後あるいは診断後5か月以内に死亡しており,非常に不良である.診断時にすでに肝内転移,リンパ節転移,腹膜播種を来し根治手術が不可能な症例や,術後再発時に進行が早く,全身状態不良で化学療法や放射線療法を施行できない症例が多くみられた.また,転移巣判明12例中,肉腫様成分を含んだ11例の予後は特に不良であったが1)6)9)17)21),腺癌成分のみの転移を示した症例の予後は良好であった1).術後再発に対する治療の報告はMalhotraら24)の1例のみと少なく,術後5週間で多発肝転移および腹膜播種を来したが,gemcitabine+cisplatin投与により部分寛解を示し,術後29か月再発生存中と報告されている.
本症例では腫瘍は病理組織学的検査所見では中分化型腺癌,充実性増殖部,紡錘形細胞の3成分からなり,互いに移行像を認めた.さらに,免疫染色検査で充実性増殖部と中分化型腺癌はkeratin AE1/3,CK7,CK19陽性を示し,紡錘形細胞は陰性,一方,充実性増殖部と紡錘形細胞はvimentin陽性を示し,中分化型腺癌は陰性であったことから,充実性増殖部は低分化型腺癌に相当し,中分化型腺癌が脱分化して,充実性増殖部さらに,紡錘形細胞へと肉腫様変化を来していったとする機序が考えられた.またその肉腫様成分もCK陰性,EMA陰性で,より未分化に近い形質を有していると考えられた.
原発性肝癌追跡調査報告書3)によると,肝内胆管癌の7.7%にVp3以上の組織学的門脈侵襲が確認されているが,通常,肝内胆管癌の門脈侵襲は周囲からの浸潤による狭窄や閉塞が特徴であり,肝細胞癌のように肉眼的に明らかな門脈腫瘍栓を認めることはまれである25).なお,山本ら26)によると肝内胆管癌で門脈腫瘍栓を認めた症例は全て腫瘤形成型であった.
Vp3以上の門脈腫瘍栓を伴った肝内胆管癌の切除報告例は,医学中央雑誌で1983年から2011年9月までの期間で「肝内胆管癌」,「胆管細胞癌」,「門脈腫瘍栓」をkey wordに検索した結果,会議録を除いて7例の報告があり,PubMedで「intrahepatic cholangiocarcinoma」,「cholangiocellular carcinoma」,「portal vein tumor thrombus」をkey wordに検索した結果,2例の報告があり,計9例であった27)~35).男性6例,女性3例で,腫瘍径は平均8.6 cm(4~15 cm),病理組織学的検査所見では中分化型腺癌4例,高分化型腺癌2例,低分化型腺癌1例で,いずれも主腫瘍と門脈腫瘍栓は同じ組織像を示し,門脈腫瘍栓と肝内胆管癌の間に特徴的な病理組織学的特徴は認めなかった.山本ら26)は門脈腫瘍栓を認めた症例では術後の残肝再発率が高く,長期生存例はみられていないと報告しており,門脈腫瘍栓が重要な予後因子としている.また治療法に関して,龍野ら35)は門脈本幹に突出するように進展した腫瘍栓合併例で,術後に残肝再発が高率に起きる危険性を考慮して肝動注化学療法を先行させたが,腫瘍栓が片側の門脈枝内に留まっている場合には,術中の癌細胞の揉み出しの危険性は少ないため術前肝動注化学療法の必要性はないとしている.
肝内胆管癌は,本邦での規約上,原発性肝癌の一つとして取り扱われているが,その生物学的特性は胆管癌に近いとされ,国際的には胆道癌の一つとして扱われることが多い.肝内胆管癌を含む胆道癌切除後の補助化学療法に関しては,明確に有効性が示された無作為化比較試験の結果はいまだ報告されておらず,標準的治療として確立されていないのが現状である.一方,切除不能・再発胆道癌に対しては一般的にgemcitabine36)やS-137)による化学療法が行われてきたが,最近ではgemcitabine単剤療法とgemcitabine+cisplatin併用療法を比較した英国の大規模第III相試験(ABC-02試験)38)の結果,gemcitabine+cisplatin併用療法群で,gemcitabine単剤療法群と比較して有意な生存期間の延長が確認され(生存期間中央値11.7か月vs. 8.3か月),gemcitabine+cisplatin併用療法が国際的な標準治療として位置づけられるようになっている.
本症例はVp3門脈腫瘍栓を有し,かつ肉腫様変化を伴う肝内胆管癌であったため,予後は不良と思われたが,比較的長期の生存が得られている.本症例が長期生存している要因としては,手術で門脈腫瘍栓を含めて一括に切除できたこと,組織像で腫瘍内の肉腫様成分の占める割合が約30%と比較的少なかったこと,肝内胆管癌の予後不良因子である肝内転移やリンパ節転移が切除した時点で認められなかったこと,元来腺癌が脱分極して肉腫様変化を来した腫瘍のため再発後のgemcitabineやgemcitabine+cisplatinによる化学療法で一定期間stable diseaseの状態が得られたこと,などが考えられた.Vp3門脈腫瘍栓や肉腫様変化を伴い,予後不良とされる肝内胆管癌の中にも,本症例のように化学療法が有効な症例もあることから,遠隔転移や肝内多発転移,リンパ節転移など,他の予後不良因子を認めない場合には積極的に切除を行い,術後再発が見られた場合には化学療法による集学的治療を行っていくことが,長期生存を得るためには重要と考えられる.
利益相反:なし