Abstract
膵頭十二指腸切除(pancreatoduodenectomy;以下,PDと略記)術後に生じた腹腔内出血に対し,開腹止血術による総肝動脈血流消失を認め,門脈部分動脈化(arterioportal shunting;以下,APSと略記)を施行することで救命し,後日Longmire法による胆管空腸吻合術を施行した1例を経験したので報告する.症例は76歳の男性で,胆道系酵素の上昇を認め,精査の結果中部胆管癌を疑い,PD術を施行した.術後膵液漏と腹腔内感染を生じ,第17病日に腹腔内出血による出血性ショックで緊急手術となった.胆管空腸吻合部を切り離して術野を確保し,出血源であった総肝動脈を縫合止血した.肝動脈の血行再建が不可能であったため,回結腸動静脈シャント術を施行しAPSを行った.胆管の再吻合は行わず,胆管内にドレナージチューブを留置し,完全外瘻化した.後日,Longmire法による胆道再建を行った.術後24か月経過しているが,現在無再発生存中である.
はじめに
膵頭十二指腸切除(pancreatoduodenectomy;以下,PDと略記)術後の合併症発生率は他の消化器切除術と比べ高く,20~45%とされている1).なかでも,胃十二指腸動脈断端や仮性瘤化した総肝動脈の破裂による腹腔内出血は重篤な状態に陥ることがある.今回,我々はPD術後の総肝動脈出血に対し,再建不可能であった総肝動脈を縫合止血し,肝動脈の血流回復を目的に門脈部分動脈化を行い,さらに二期的にLongmire法で胆道再建した症例を経験したので若干の文献的考察を加えて報告する.
症例
患者:76歳,男性
主訴:肝機能障害
既往歴:甲状腺機能低下症(慢性甲状腺炎),高血圧
現病歴:2012年10月に近医で行った血液生化学検査で肝機能異常を指摘され,腹部超音波検査と腹部造影CTにて肝内胆管の拡張を認めた.胆管炎のため内視鏡的逆行性胆道ドレナージチューブが留置され,2013年1月に精査加療目的で当科転院となった.
入院時現症:身長159 cm,体重51 kg.眼球結膜に黄染なし.腹部は平坦,軟であった.
入院時検査所見:アルブミン3.5 g/dl,クレアチニン1.00 mg/dl,AST 28 U/l,ALT 25 U/l,血清アミラーゼ98 U/l,総ビリルビン0.6 mg/dl,直ビリルビン0.4 mg/dl,CEA 0.7 ng/ml,CA19-9 36 U/ml.
腹部MRI所見:中部胆管で胆管壁の肥厚,内腔閉塞,上部胆管の拡張を認めた.
内視鏡的逆行性胆管造影検査所見:中部胆管に2 cmにわたる狭窄を認めた(Fig. 1).
胆管擦過細胞診でclass II,生検でatypical cellで悪性所見は得られなかったが,中部胆管癌が強く疑われたため,転院1か月後に手術を行った.
手術所見:肝転移,腹膜播種,リンパ節転移を認めなかった.腫瘍は中部胆管に認められたが,術中迅速検査に提出した上部胆管断端の上皮内に癌細胞を認めたため,肝門部胆管まで追加切除して,断端陰性を確認した.亜全胃温存膵頭十二指腸切除を施行し,再建はChild変法Roux-en Y法とした.追加切除の結果,右肝管と左肝管と尾状葉胆管枝が分離された状況になったため,右肝管と尾状葉胆管枝を形成して1穴とし,左肝管と2穴で胆管空腸吻合を行った.また,膵管に3 mmの膵管チューブを挿入し,膵腸吻合は膵管粘膜吻合および膵実質-空腸漿膜筋層吻合(柿田式)を行った.手術時間は447分,出血量は810 gであった.
切除標本病理組織学的検査所見:Bm,平坦浸潤型,中分化型管状腺管癌,ss,Hinf0,Ginf1,Panc0,Du0,PV0,A0,N0,HM0,DM0,EM0,p-Stage II,CurAであった.
術後経過:術後3日目の膵空腸吻合部ドレーンの排液中のアミラーゼが4,575 U/lと高値であったが,7日目には 239 U/lまで低下した.炎症反応が高値で持続し,ドレーン排液の培養検査でEnterococcus faecalisを認め,腹腔内感染に対して抗生剤とドレナージを継続し,16日目にはCRP 0.92 mg/dl,白血球8,900/μlと改善していた.しかし,17日目の夜間に膵空腸吻合部ドレーンより大量の出血を認め,ショック状態となり,緊急再開腹止血術を施行した.
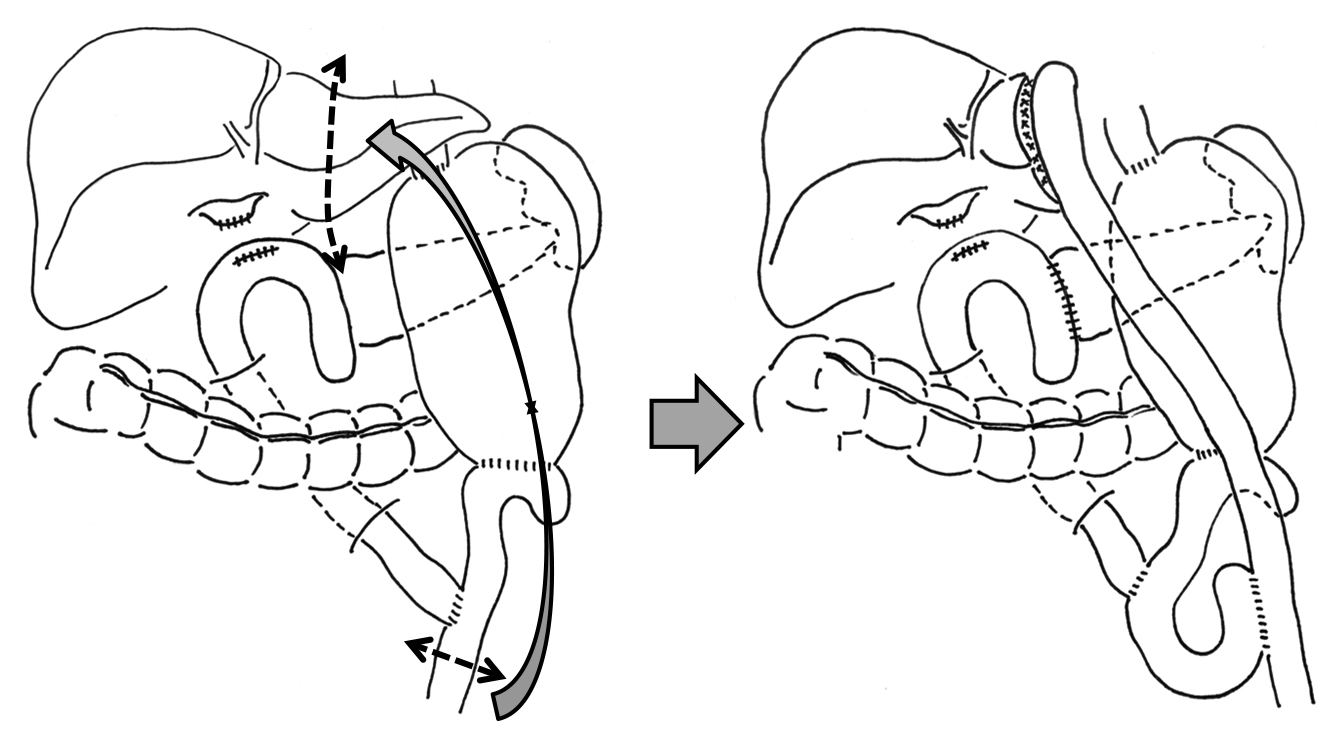
再手術所見:開腹すると腹腔内は大量の血液と凝血塊で満たされていたため,可及的に除去した.胆管空腸吻合部背側から血液の湧出があったため,胆管空腸吻合を切離して術野を確保し,総肝動脈壁の破裂部から噴出性の出血を確認した.出血部を縫合止血し,その後に施行したカラードプラエコーでは,肝動脈の血流が確認できなかった.肝動脈再建は周囲組織の膵液漏による鹸化と感染,炎症性癒着により困難であった.そこで門脈部分動脈化(arterioportal shunting;以下,APSと略記)を施行することとした.直径約5 mmの回結腸動脈・静脈を露出し,7-0ポリプロピレンによる連続縫合で回結腸動脈と静脈を側々吻合してAPSを行った.切離した胆管と空腸の吻合孔はそれぞれ閉鎖し,胆管内にretrograde transhepatic biliary drainage(以下,RTBDと略記)tubeを留置し,完全外瘻化した.手術時間は245分,出血量は5,000 gであった.
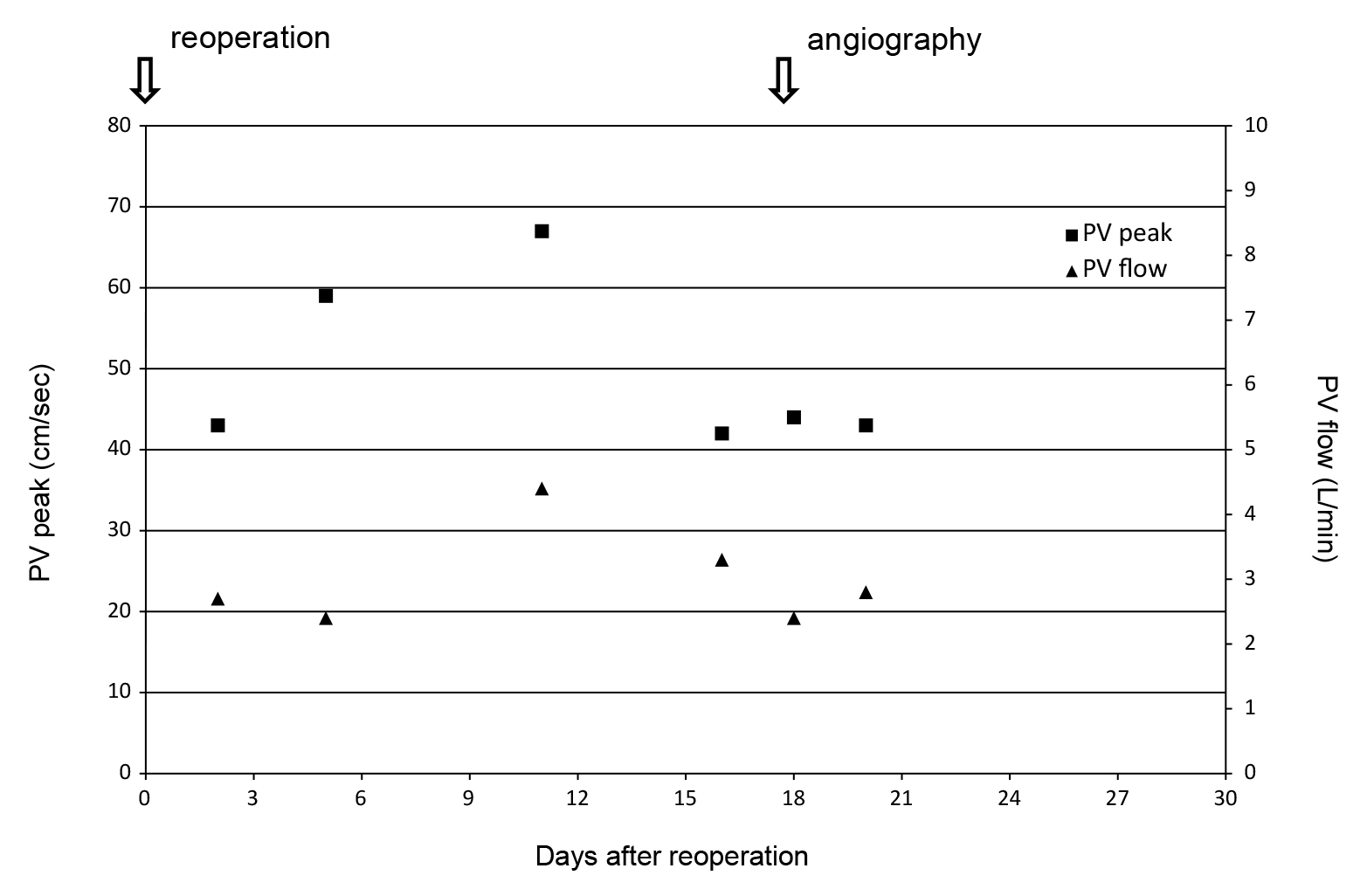
再手術後経過:術後再出血はなく,全身状態は安定した.深部SSIのためドレナージは必要としたが,感染のコントロールは良好であった.再手術翌日のドプラー超音波検査で計測した門脈本幹の血流速度(以下,PV peakと略記)は43 cm/秒,門脈本幹の血流量(以下,PV flowと略記)は2.7 l/分と高値であり,部分動脈化の影響と考えられた(Fig. 2).再手術後9日目に施行した造影CTでは,動脈相で門脈が明瞭に濃染されており,動脈化によりシャント血流が確保できていることが予想された(Fig. 3).その後,PV peak,PV flowはさらに上昇し,再手術後11日目に最高値(PV peak 67 cm/秒,PV flow 4.4 l/分)となったが,同日の血液検査では AST 649 U/l,ALT 400 U/lと肝機能障害が認められた.一旦落ち着いたものの,再手術後16日目に再度悪化(AST 398 U/l,ALT 422 U/l)したため,再手術後18日目に血管造影を行ったところ,回結腸動静脈吻合部は確認できなかった.この時期のPV peakは44 cm/秒,PV flowは2.4 l/分と低下していた.その後,肝機能障害は徐々に改善し,膵管チューブを再手術後33日目に抜去し,胆管を完全外瘻化したまま再手術後88日目に退院した(Fig. 4).5か月後に胆管空腸再吻合目的で入院したが,強固な癒着および肝門部周辺の側副血行路を理由に,肝門部での胆管空腸再吻合は困難であると判断した.そのためLongmire法による胆管空腸再建を予定した.
再手術所見:開腹すると予想通り高度な癒着により肝門部への到達は困難であった.再建する胆管は最も太いS3の1本のみとし,肝S3の2本,S2の1本の胆管は結紮し,外側区域切除を施行した.Y脚より下流で挙上空腸を離断し,末梢の空腸とB3を吻合し,中枢の空腸と挙上空腸を側々吻合した(Fig. 5).術後24日目にRTBDを抜去し,術後42日目に退院となった.術後24か月経過した現在も無再発生存中である.
考察
膵頭部領域癌に対する標準術式であるPDは,近年比較的安全に行えるようになってきているが,合併症発生率は20~45%とほかの消化管手術に比べ依然高率である1).重篤な合併症としては,腹腔内動脈性出血があげられ,2~18%を占めると報告されている2).原因としては膵消化管吻合縫合不全による膵液漏,感染による腹腔内膿瘍による侵襲,リンパ節郭清時の血管内,外膜損傷が考えられ,いったん発生すると止血に難渋するため,死亡率は30~60%と非常に高い3).茂垣ら4)の報告では出血部位は10例中総肝動脈3例,胃十二指腸動脈2例,脾動脈,右左肝動脈が各1例で,発症までの期間は平均16.3日(5~41日)であったと報告している.自験例においても,膵液漏と腹腔内感染により術後17日目に総肝動脈が破綻したことが原因であったと考えられた.
PD術後出血に対する処置法としては,開腹止血術と血管塞栓術に大別される.近年のinterventional radiologyの進歩により,出血に対する止血手段として経カテーテル的血管塞栓術の有用性が報告されている5).児玉ら6)は開腹止血術と血管塞栓術を行った各6名の救命率はそれぞれ16.6%と60%であり,血管塞栓術のほうが良好な転帰であったと報告している.さらに,最近では肝血流の温存が可能なカバードステントによる止血例が散見されるようになってきており,出血した場合の処置は,血管塞栓術が第一選択となることが多い7).しかし,自験例のように夜間に突然発生し,かつ出血性ショックを呈している状況であれば,救命のため迅速確実な開腹止血術を選択せざるをえなかった.
本例の如く,膵液漏や腹腔内感染により肝動脈壁が脆弱化し再建不能な場合には,縫合止血せざるをえないことがある.PD術後は胆管切除やリンパ節郭清により肝十二指腸間膜内の側副血行路は全て遮断され,胆道再建術後に胆管空腸吻合部腸間膜や下横隔動脈から肝臓への側副血行路が完成するまでに約3~4週間が必要である8).したがって,総肝臓動脈の血流遮断が起こると肝臓への血流は門脈血主体となる.肝臓への血液供給は25%前後が動脈性,75%前後が門脈性といわれている9).肝動脈は肝血流量維持としてより酸素供給量保持としての意義が高く,必要酸素供給量の約50%が肝動脈由来である10).そのため門脈血流が保たれても完全な肝動脈血流遮断が起こると肝細胞壊死は起こりうるので,自験例においてもPD術後の側副血行路が完全に消失した状態での肝動脈血流途絶による肝壊死が危惧された.
APSは門脈下大静脈吻合後の肝不全予防対策として古くから研究されてきたが,近年では肝動脈再建が困難な肝切除などに臨床応用されている11).また,肝動脈再建後の血栓性閉塞,仮性動脈瘤破裂に対する肝動脈結紮や塞栓術後の低酸素による肝不全予防対策に緊急避難的にAPSが施行された報告が散見される6)12).鈴木ら8)は,側副血行路を遮断した状態で肝動脈が閉塞すると胆道系の酸素飽和度は28%まで低下したが,APSによって57%に回復したと報告している.シャント作成部位は,総肝動脈-門脈本幹や腸間膜内の動脈-静脈が考えられるが,術後出血の際には出血源から離れており血管壁が正常でアプローチが容易な腸間膜内シャントが適していると考える.自験例においては総肝動脈が損傷のため使用できず,回結腸動静脈でシャント作成した.術直後には虚血を疑う肝機能障害は認められず,また術後から施行していたドプラー超音波検査ではPV peak,PV flowが増加していることから,肝臓への酸素供給は十分であったと考えられた.また,再手術後17日目の肝機能障害出現時の上腸間膜動脈造影では,シャント血流は確認できなかったが,腹腔動脈造影では,左肝動脈の血流が確認できた.今回の肝機能障害の原因がシャントによるものかは断定できなかったが,APS後に食道静脈瘤や腹水などの門脈圧亢進症が認められた報告もあり13),側副血行路の発達する3~4週ぐらいでシャントは塞栓する必要があるといわれている.医学中央雑誌(1977年~2013年)およびPubMed(1976年~2013年)で「出血」,「門脈部分動脈化」,「hemorrhage」,「arterioportal shunting」をキーワードとして検索したところ,会議例を除く報告例は3例のみであった.そのうち,シャント閉鎖に1か月以上要した2例はシャント関連の合併症(静脈瘤や肝不全)を生じていた12)14).
術野確保のために切り離した胆管空腸再吻合は,縫合不全や腹腔内膿瘍などの合併症を引き起こすことが予想されたため,一期的再建は行わずに完全外瘻化しておいた.胆道バイパス手術として,1948年にLongmireら15)による外側区域の部分切除後に肝内胆管空腸吻合を行った報告があり,その後Soupault ら16)も報告している.肝切除を伴うLongmireに対して,Soupaultの方法は肝円索左側で肝臓を離断してB3胆管を露出,胆管側壁に空腸を吻合する方法であり肝切除を伴わない利点がある一方,より中枢での吻合が必要となる.自験例では肝門付近に高度な癒着,側副血行路の存在が予想されたため末梢での吻合が適しており,Longmire法を選択した.癒着剥離も不要で,側副血行路や他臓器を損傷することなく胆道再建を行い,術後経過も非常に順調であったことから,二次的な合併症を回避するための有効な手段であった.
利益相反:なし
文献
- 1) 高松 督, 五関 謹秀, 寺元 研一.膵頭十二指腸切除後の縫合不全および腹腔内出血に対しソマトスタチンアナログが有効であった1例.外科.2002;64:1347–1350.
- 2) Miedema BW, Sarr MG, van Heerden JA, Nagorney DM, McIlrath DC, Ilstrup D. Complication following panacreatico-duodenectomy. Current management. Arch Surg. 1992;127:945–949.
- 3) Yeo CJ, Cameron JL, Sohn TA, Lillemoe KD, Pitt HA, Talamini MA, et al. Six hundred fifty consecutive pancreatico-duodenectomies in the 1990s: pathology, complications, and outcomes.. Ann Surg. 1997;226:248–260.
- 4) 茂垣 雅俊, 藤井 秀樹, 松田 政徳, 松本 由朗.膵頭十二指腸切除術後に発生した腹腔内大量出血症例の検討.手術.2000;54:987–991.
- 5) 金井 道夫, 近藤 成彦, 梛野 正人, 栗木 浩, 向山 博夫, 浅野 昌彦,ほか.腹部大量出血に対する緊急経カテーテル的動脈塞栓術の有効性について.日本消化器外科学会雑誌.1988;21:1301–1307.
- 6) 児玉 孝仁, 木下 壽文, 原 雅雄, 西村 一宣, 青柳 成明.膵頭十二指腸切除術後の腹腔内出血に対する治療の検討.日本腹部救急医学会雑誌.2003;23:883–889.
- 7) Roulin D, Cerantola Y, Demartines N, Schäfer M. Systematic review of delayed postoperative hemorrhage after pancreatic resection. J Gastrointest Surg. 2011;15:1055–1062.
- 8) 鈴木 温, 近藤 哲, 平野 聡, 田中 栄一, 原 敬志, 齋藤 克憲,ほか.胆道癌血管浸潤例の諸問題,血管浸潤例の術前処置の問題点―門脈動脈化の有効性は?―.胆と膵.2005;26:631–635.
- 9) Charles H, Joseph P. Experimental subtotal ligation of the arteries supplying the liver. Arch Surg. 1937;35:878–886.
- 10) Conolly WB, Belzer FO, Dunphy JE. Safe hepatic artery occlusion in dogs. Surgery. 1969;66:772–774.
- 11) 向谷 充宏, 平田 公一, 桂巻 正, 木村 康利, 本間 敏男, 古畑 智久.門脈部分動脈化を利用した2期手術の適応と手技の実際.手術.2001;55:1855–1860.
- 12) 渡邉 健次, 加藤 岳人, 柴田 佳久, 鈴木 正臣, 吉原 基, 安藤 晴光.膵頭十二指腸切除後総肝動脈破綻出血に対し肝動脈結紮と門脈部分動脈化が有効と考えられた1例.日本臨床外科学会雑誌.2007;68:410–414.
- 13) Ko S, Nakajima Y, Kanehiro H, Aomatsu Y, Yoshimura A, Taki J, et al. Successful management of portal hypertension following artificial arterioportal shunting: report of a case. Surg Today. 1995;25:557–559.
- 14) 新藏 信彦, 光吉 明, 大田 豊承, 中村 健一, 財間 正純.腸間膜動・静脈シャントによる門脈部分動脈化を行い救命しえた術後肝動脈破裂の2例.手術.2009;63:1081–1084.
- 15) Longmire WP Jr, Sanford MC. Intrahepatic cholangiojejunostomy with partial hepatectomy for biliary obstruction. Surgery. 1948;24:264–276.
- 16) Soupault R, Couinaud C. New procedure for intrahepatic biliary shunt: left cholangiojejunostomy without hepatic sacrifice. Presse Med. 1957;65:1157–1159.