2020 Volume 53 Issue 10 Pages 817-825
2020 Volume 53 Issue 10 Pages 817-825
症例は75歳の男性で,排尿障害,前立腺特異抗原(prostate specific antigen;以下,PSAと略記)高値にて針生検を施行したところ前立腺癌と診断され,精査中に下部直腸(Rb)前壁に1/3周性Type 2病変を認めた.骨盤MRIで前立腺癌は肛門管直上で直腸壁に接しており,直腸癌とも近接していた.直腸間膜リンパ節(mesorectal lymph node;以下,MLNと略記),側方および鼠径部に多数のリンパ節腫大,および複数の骨転移を認めた.前立腺癌(Stage D)に対しホルモン療法を1サイクル施行後,PSA値の低下,側方リンパ節の縮小を確認し,腹腔鏡下腹会陰式直腸切断術を施行した.直腸癌はtub1,pT2,pN0,pStage Iで,MLN転移は神経内分泌分化を伴う前立腺癌の転移であった.前立腺癌のMLN転移の報告はごくまれであるが,本症例のように浸潤傾向の強い前立腺癌において,直腸間膜内へのリンパ行性転移を来しうることを念頭に置くべきと思われた.
A 75-year-old man who suffered from dysuria with elevated serum prostate specific antigen (PSA) level was diagnosed as having prostate carcinoma by needle biopsy. Upon further examination, Type 2 rectal carcinoma was found in the anterior wall of the lower rectum concurrently. MRI imaging of the pelvis revealed that the prostate carcinoma was adjacent to the anterior wall of the rectum above the anal canal and also close to the rectal carcinoma. CT revealed multiple lymph node metastases of mesorectal, lateral and inguinal lesions and PET-CT showed metastases to some bones. After one cycle of anti-androgen therapy for Stage D prostate carcinoma, the PSA level was normalized and shrinkage of the metastatic lateral lymph node (LLN) was assessed, followed by laparoscopic abdominoperineal resection for the rectal carcinoma. Pathological findings of the rectal cancer showed well-differentiated adenocarcinoma, pT2, pN0, pStage I and the origin of the mesorectal lymph node (MLN) metastasis was prostate carcinoma with neuroendocrine differentiation. Metastatic prostate carcinoma to the MLN is very rare but it is important to keep this unsuspected pattern of lymphatic spread in mind, especially in case of infiltrative high-risk prostate carcinoma.
直腸癌と神経内分泌分化型(neuroendocrine differentiation;以下,NEDと略記)前立腺癌の同時性重複癌の1例を経験した.本症例は複数の遠隔転移とともに直腸間膜リンパ節(mesorectal lymph node;以下,MLNと略記)転移を伴った極めてまれな症例であった.前立腺癌のMLN転移はごく少数の報告例を散見するのみであり1)~4),直腸-前立腺領域間のリンパ流を介した転移形式について考察を加え報告する.
患者:75歳,男性
主訴:排尿困難
既往歴:高血圧,糖尿病,心筋梗塞(ステント留置後)
生活歴:喫煙12本/日×15年
現病歴:7,8か月前より排尿困難を自覚し近医で前立腺特異抗原(prostate specific antigen;以下,PSAと略記)高値を指摘された.当院泌尿器科で経会陰的前立腺針生検を施行し腺癌と診断された.その際の骨盤MRIで前立腺癌に近接する直腸壁肥厚,および側方,直腸間膜,鼠径部にリンパ節腫大を多数認め当科紹介となった.
来院時現症:直腸診にて前立腺は過胡桃大,石様硬で,口側の直腸前壁に腫瘤を触知した.
血液検査所見:末梢血,生化学検査には異常値を認めず,腫瘍マーカーはCEA 5.3 ng/ml,PSAは91 ng/mlと高値であった.
下部内視鏡検査所見:肛門縁から4 cm,前壁に1/3周性Type 2病変を認めた(Fig. 1).生検の結果は高分化型腺癌であった.
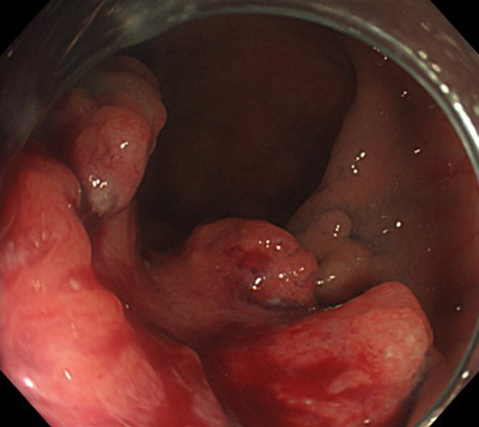
Colonoscopy showed a Type 2 tumor in the anterior wall of the rectum, 4 cm from the anal verge.
腹部造影CT所見:前立腺径は51×48 mmと腫大し,不均一な造影効果を伴っていた.前立腺に接した直腸前壁に壁肥厚を認めた.
骨盤MRI所見:前立腺癌はほぼ全体がT2強調像低信号域であり,近接する直腸前壁に壁肥厚を認めた.恥骨直腸筋付着のレベルで前立腺との境界が一部不明瞭であった.MLN,両側内外腸骨動脈領域,右鼠径部にリンパ節腫大を多数認めた(Fig. 2).
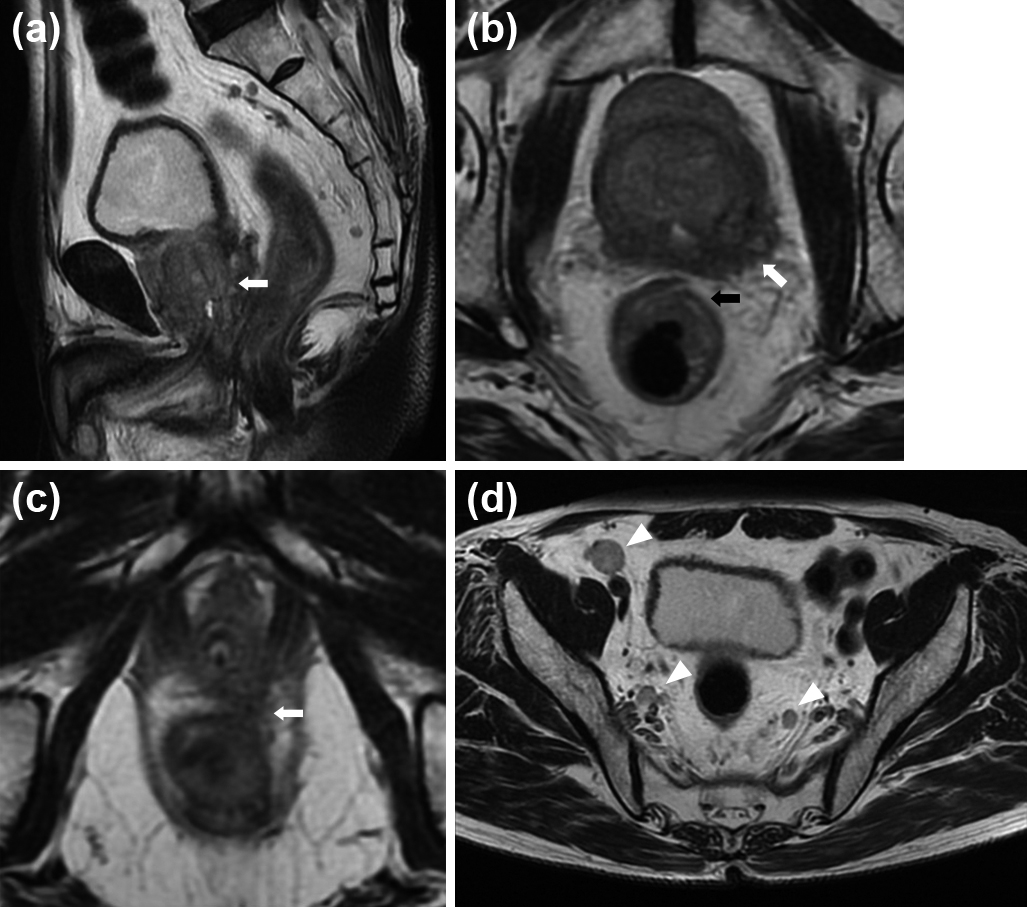
(a) Sagittal T2-weighted MRI showed hetero-intensity signal in the prostatic tumor (arrow). (b) Axial T2-weighted images showed thickening of the anterior wall of the lower rectum (black arrow) and prostatic tumor (white arrow). (c) There was unclear delineation between the apex of the prostatic tumor and the lower rectum at the level of the puborectal sling (arrow). (d) The mesorectal, inguinal and lateral lymph nodes were grossly positive (arrowheads).
PET/CT所見:直腸壁肥厚部にFDGの集積を認めた(Fig. 3).また,外腸骨リンパ節,MLNに複数のFDG集積を認めた.
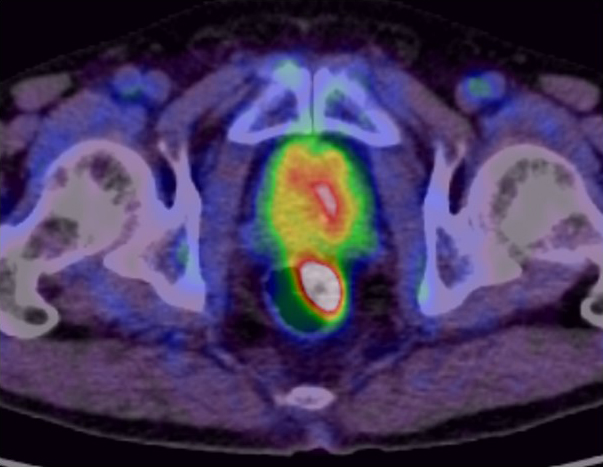
FDG-PET/CT showed accumulation in the lower rectum and prostate.
骨シンチグラフィ所見:左第2胸椎,第9肋骨に高集積を認めた(Fig. 4).
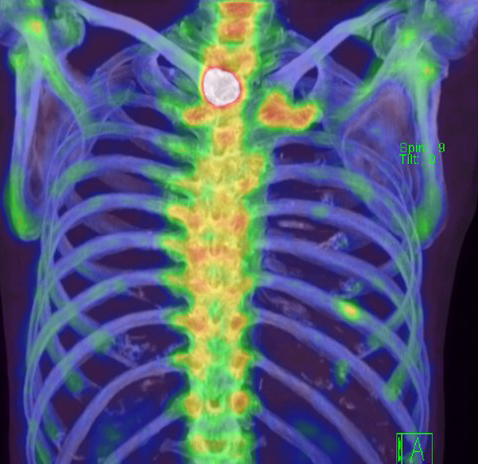
A bone scintigram showed accumulation in the left 9th rib and 2nd thoracic vertebra.
前立腺針生検所見:adenocarcinoma,Gleason score 4+4=8(Fig. 5).
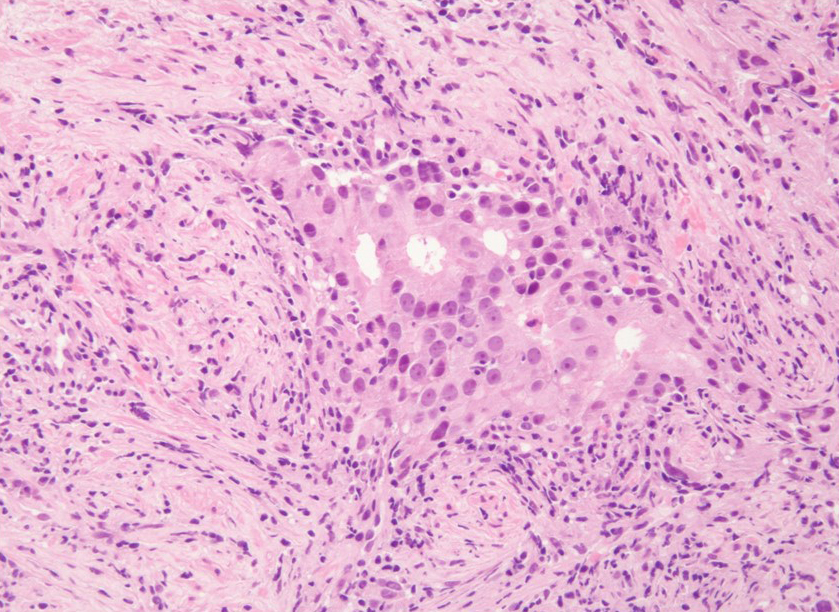
Microscopic findings of the needle biopsy specimen (HE stain) showed adenocarcinoma, Gleason score 4+4=8.
以上より,骨転移,多発リンパ節転移を伴う前立腺癌(cT3b,N1,M1,cStage D)と下部直腸癌(cT2,N2a,M0,cStage IIIb)の重複癌と診断した.近傍の腫大した複数のMLNは直腸癌の転移と判断した.前立腺癌は内分泌療法の方針とし,抗アンドロゲン製剤およびLH-RH agonistを1コース施行後に前立腺癌,側方リンパ節の縮小傾向を確認し,直腸癌に対し腹腔鏡下腹会陰式直腸切断術を施行した.
手術所見:腹腔鏡下で経腹的に total mesorectal excision(TME)を進め,背側は尾骨寄りでhiatal ligamentを処理し,前方は剥離可能な前立腺尖部までを全周性に剥離したところで会陰操作に移った.会陰操作の最終局面で,直腸尿道筋に相当する組織が腫瘤様に硬く前立腺下縁との境界が不明瞭であったため,剥離に難渋した.切離ラインが尿道側に近接し,検体摘出時に尿道背側組織の菲薄化を認めたため,遅発性尿道損傷のリスクを考えて術中に膀胱瘻を造設した.
病理組織学的検査所見:直腸癌は高分化型腺癌,pT2,pN0,INFb,Ly0,V0,pPM0,pDM0,pRM0,pStage Iであった(Fig. 6a).MLN組織内にはNEDを疑わせるロゼット様構造を認めたため免疫染色検査を追加したところ,synaptophysin一部陽性,chromogranin-A(以下,CGAと略記)陰性であった(Fig. 6b, c).小細胞癌成分は認めなかった.ホルモン療法前の前立腺針生検を再検しsynaptophysin一部陽性で組織像が類似するため,NEDを伴う前立腺癌の転移と診断された.郭清リンパ節13個中#251,6/8;#252,1/2で全て前立腺癌の転移であり,術前MRIで腫大を認めた間膜内リンパ節と一致した.術中の切離ラインと病理組織所見との関係をシェーマで表示した(Fig. 7a).前立腺癌は直腸癌下縁より1 cm肛側にあたるHermann線のレベルで,直腸前壁の縦走筋,直腸尿道筋から壁外の横紋筋線維の交錯する境界まで,線維化を伴って浸潤していた.切離断端の横紋筋は尿道括約筋に近接する恥骨直腸筋に相当すると思われ,近傍に神経周囲浸潤を複数認めた(Fig. 7b, c).前立腺癌浸潤部でのリンパ管侵襲,静脈侵襲は確認できなかった.前立腺癌は壁外浸潤と領域外リンパ節転移の所見が加わり,T4,N1,M1bの診断となった.
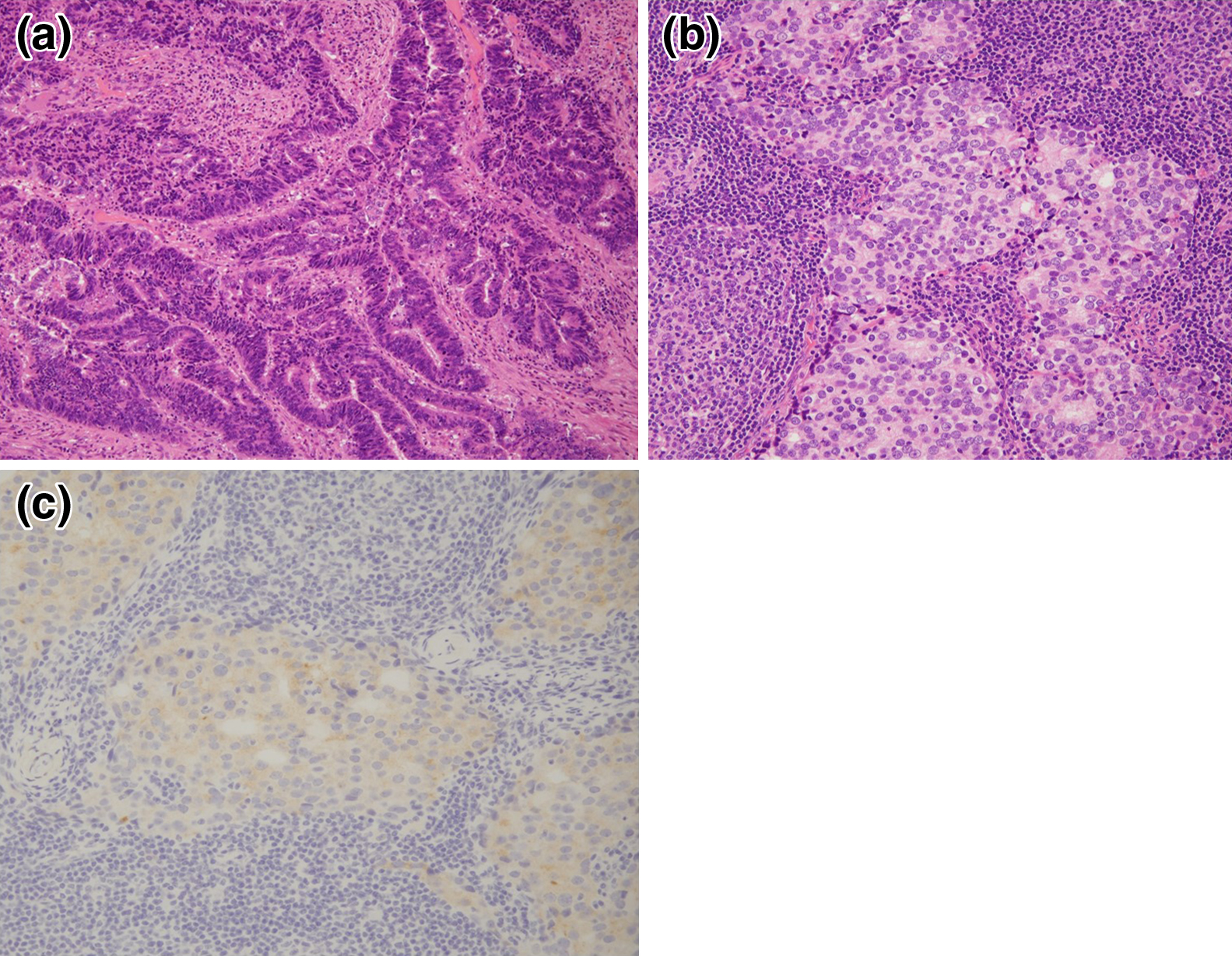
(a) Histopathology revealed well-differentiated rectal adenocarcinoma. (b) Metastatic prostatic carcinoma in MLN. (c) Synaptophysin positive NED cells.

(a) A schema of the abdominoperineal resection line and pathological findings of the lesion of extramural invasion of prostate cancer (arrows). (b) Prostate cancer with perineural invasion (arrow) was seen near the boundary of the recto-urethral muscle and puborectal muscle (arrowhead). (c) Prostate cancer involving the fibrotic recto-urethral muscle.
術後経過:術後は11日目に尿道カテーテルを抜去後も症状を認めず25日目に退院したが,術後33日目に外来で施行した膀胱瘻造影にて前立腺部尿道背側に造影剤の漏出を認めた.経過観察中8か月後の再検で造影剤の漏出なく,尿道損傷部の治癒を確認した.現在術後15か月経過し,ホルモン療法を継続中で新出病変は認めていない.
前立腺癌は精囊,尿道,膀胱への直接浸潤,および骨盤内リンパ節転移,骨,肺への血行性転移がしばしば認められる.しかしながら,本症例で見られた直腸への浸潤は比較的まれであり5)6),さらに,MLN転移の報告例はごく少数である1)~4).隣接臓器である直腸への浸潤はDenonvillier筋膜(Denonvilliers’ fascia;以下,DVFと略記)の存在が障壁となり少ないと考えられているが7),一旦DVFを越えると次にバリアとなる直腸固有筋層周囲を全周性に広がりながら浸潤する形式をとり,臨床像としては全周性狭窄像を呈することが多いと指摘されている6)8).
Winter9)は前立腺癌の直腸浸潤・転移様式につき32例で検討し,I型:直腸前壁の粘膜下浸潤,II型:直腸全周性の粘膜下浸潤,III型:直腸粘膜までの浸潤,IV型:前立腺と離れた直腸やS状結腸壁への転移,V型:直腸浸潤と直腸癌の合併の5型に分類した.I~III型は直接浸潤の経過を示し,IV型はリンパ行性の直腸転移を示している.頻度はII型が41%と最も多く,IV型は9%,V型は1例のみの3%であったと報告している.自験例はV型の重複癌に加え,前立腺癌の直腸壁内浸潤と同時に間膜内へのリンパ行性転移を起こしており,IV型の要素も含まれると考える.直腸浸潤を来す経路としてLaneら10)は①DVFを経由する直接浸潤,②前立腺-直腸間の共通リンパ流を経由するリンパ行性浸潤の他,医原性の③経直腸針生検時のimplantationを挙げている.前立腺からのリンパ液の排出経路については,Yuenら11)によるインドシアニングリーンを用いた報告や,抗desmoplakin抗体を用いたリンパ管造影で前立腺中底部にかけて密集したリンパ流を可視化したFukudaら12)の報告があり,前立腺から内・外腸骨動脈沿い,閉鎖領域,および仙骨前面に沿って走行するリンパ流が確認されている.前立腺癌取扱い規約(第10版)では前立腺の所属リンパ節(N1)を総腸骨動脈分岐以下の骨盤内リンパ節(内外腸骨リンパ節,閉鎖リンパ節),それ以外を遠隔リンパ節(M1a)と定義しており13),郭清に関しては閉鎖領域のみ行うのが一般的であったが,2016年の「前立腺癌診療ガイドライン」では中リスクおよび高リスク群で内外腸骨動脈領域を含めた拡大リンパ節郭清が推奨(GradeB)されるようになった14).さらに,今回の症例で示唆されるように,骨盤内で密集するリンパ流が直腸と前立腺領域間で一部交通し,腸骨動脈系から腸間膜動脈系へのリンパ行性転移を来しうることや,DVFを経由して早期からの微小転移が潜在的に起こっている可能性について少数の文献で指摘されている2)10).しかしながら,実際に前立腺癌でMLN転移を来した症例報告は,PubMed(1950年~2018年)において「prostate carcinoma」,「rectal carcinoma」,「mesorectal lymph node/perirectal lymph node」をキーワードとして検索したかぎり,本症例を加えた5施設の13例のみであった1)~4).そのうちの5例はMurrayら1)が直腸癌で切除しリンパ節転移を認めた全112例をretrospectiveに再検討して確認しえたものである.Mourraら2)は5症例を報告したが,うち1例で一つのリンパ節組織中に前立腺癌と直腸癌成分が併存するまれな“collision phenomenon”を指摘した.前立腺癌でMLN転移を来した13例中,他にも2例にcollision phenomenonの報告があった3)4).本症例は肛門管上縁近傍の直腸尿道筋内で神経線維に沿った前立腺癌の浸潤を認めており,MLN転移は浸潤した直腸壁からのリンパ流由来か,直腸-前立腺間の共通のリンパ流を介したものか,いずれの可能性も考えられる.自験例同様全ての報告例で術前は直腸癌の転移と誤認されており,直腸切除後の病理組織学的診断で判明していた.直腸癌の転移と誤認されたままの症例,前立腺癌単独で手術適応とならず,証明されえなかった症例が潜在する可能性は否定できない.MLN転移を来した前立腺癌の報告例のうち,NEDを伴う前立腺癌は本症例のみであった.前立腺癌は一般的に放射線照射やホルモン療法の効果が期待でき,リンパ節郭清の治療的意義については見解が定まっていないが,浸潤傾向の強い前立腺癌に本症例のような転移形式が存在することを念頭に置く必要があると考えられた.前立腺癌におけるNEDには二つの病態があり,①神経内分泌癌である小細胞癌と②通常型の腺癌の中に部分的にNEDが見られるものに分類される.①はまれであり,PSAを産生しないために進行した状態で診断されることが多く,予後は極めて不良と考えられている15).本症の相当する②は,前立腺全摘術を行った組織の約半数に認められるという報告もあるが,明確な病理学的診断基準は決められていない16).また,治療前からNEDを認める症例だけではなく,新規ホルモン剤を含めた各種ホルモン療法中にNEDを認める症例も散見され17),その病態や治療についても定まった見解はない18)19).
前立腺癌におけるNEDの免疫組織染色検査のマーカーとしてはNSE,CGA,neural cell adhesion molecules(NCAM)などが有用であるが20),Jensenら21)はCGAに比較してsynaptophysinが特異的マーカーとしての感度が高いことを報告しており,本症例もCGA陰性,synaptophysin陽性であった.本症例は直腸癌術後15か月,ホルモン療法継続で新出病変なく経過している.重複癌では直腸癌の手術適応に加えて,前立腺癌の臨床病期,Gleason score,組織型の評価および術後合併症のリスク,機能温存についても十分検討したうえでの治療戦略を要するが,隣接臓器における本症のような予期せぬ転移形式が存在することも念頭に置くべきと思われた.
利益相反:なし