2020 Volume 53 Issue 3 Pages 221-229
2020 Volume 53 Issue 3 Pages 221-229
症例は78歳の男性で,近医で胆囊総胆管結石と急性胆囊炎に対して内視鏡的胆管結石除去術後に開腹胆囊摘出術を施行した.術後の病理検査でpT2胆囊癌の診断となり根治手術目的で当科紹介となった.胆囊摘出術から3週後に胆囊床切除術+肝外胆管切除術を施行した.切除標本では病理組織学的癌遺残およびリンパ節転移は認めなかった.術後S-1による補助化学療法を15か月施行した.胆囊摘出術から2年10か月後に右肋骨弓下斜切開部の腹壁転移に対して腫瘍摘出術を施行した.術後ゲムシタビン+S-1療法を4か月,ゲムシタビン療法を8か月施行した.2年7か月後に腹壁転移の局所再発に対して腫瘍摘出術+右第VIII・IX肋骨切除術を施行した.切離断端が陽性であったため放射線照射50 Gyを施行した.その後GEM+S-1併用療法を14か月,S-1療法を10か月施行し,現在胆囊摘出術から8年5か月(腹壁再発腫瘍摘出術から5年7か月)後の現在,再発の徴候なく生存中である.

Unexpected gallbladder carcinoma was identified in a 78-year-old man after he had undergone a cholecystectomy with right subcostal incision for acute cholecystitis. A resection of the gallbladder bed and the extrahepatic bile duct was performed 3 weeks later. Adjuvant chemotherapy with S-1 was administered for 15 months. Two years and 10 months after the cholecystectomy he underwent a resection of abdominal wall recurrence in the laparotomy scar. Gemcitabine and S-1 therapy and subsequent gemcitabine therapy were performed for 4 and 8 months, respectively. Two years and 7 months later, he underwent a resection of the local recurrence in the surgical scar. Pathological examination revealed cancer invasion in the surgical margin. Radiotherapy was performed with a total dose of 50 Gy. Following radiation therapy, gemcitabine and S-1 therapy and subsequent S-1 therapy were performed for 14 and 10 months, respectively. The patient is currently alive without recurrence at 8 years and 5 months/5 years and 7 months after the cholecystectomy/initial resection of the abdominal wall recurrence.
胆囊癌の腹壁再発はまれな疾患で1),ほとんどの報告が腹腔鏡下胆囊摘出術(laparoscopic cholecystectomy;以下,LCと略記)後のポートサイト部再発である2)3).今回,我々は集学的治療にて長期生存が得られた開腹胆囊摘出術の創部に発生した胆囊癌腹壁再発の1例を経験したので,若干の文献的考察を加えて報告する.
患者:78歳,男性
主訴:右季肋部腫瘤
既往歴:肺気腫,71歳時に脳梗塞,72歳時に副鼻腔炎手術
現病歴:2010年2月近医で急性胆囊炎に対して開腹胆囊摘出術が施行された.術中に胆囊穿孔と胆囊周囲膿瘍を認めた.術後の病理組織学的検査で胆囊癌の診断となった.組織型は乳頭状腺癌で,pT2,ly0,v0,pn2,pCM1,pEM0であった(胆道癌取扱い規約第6版4)).根治手術目的で当科紹介となり,3週後に胆囊床切除術+肝外胆管切除術を施行した.病理組織学的検査では局所の癌遺残とリンパ節転移は認めなかった.術後6週からS-1(120 mg/body/day,隔日内服)による術後補助化学療法を15か月施行した.2012年11月に右季肋部腫瘤を自覚したため2013年1月精査目的で入院となった.
入院時現症:身長165 cm,体重80 kg.貧血,黄疸は認めなかった.右季肋部斜切開創部に鳩卵大の腫瘤を触知した.
血液検査所見:Hb 11.6 d/dl,Ht 36.7%と軽度の貧血を認めた.腫瘍マーカーはCEA 15.2 ng/dl,CA19-9 59.2 U/mlと軽度上昇していた.
腹部造影CT所見:右季肋部腹壁内に4.3 cm大の不整な腫瘍を認めた(Fig. 1).

An irregular abdominal wall tumor (arrow), 4.3 cm in size, was found in the right hypochondrium on CT.
FDG-PET所見:右季肋部腹壁内に異常集積(SUVmax:15.7)を認めた.その他の部位に異常集積は認めなかった(Fig. 2).

PET-CT revealed an increased uptake in the abdominal wall in the right hypochondrium.
以上より,胆囊癌術後腹壁再発と診断し手術の方針とした.
手術所見:紡錘状の皮膚切開で開腹し皮膚を含めて腫瘍摘出術を施行した.肝S4辺縁との癒着を認めたため合併切除を施行した.観察した範囲内には腹膜再発を示唆する所見は認めなかった.腹壁欠損部は左大腿筋膜グラフトを用いて再建した.
切除標本所見:4.5×4.3 cm大の白色調腫瘍を認めた(Fig. 3).
Macroscopic findings of the resected specimen. Macroscopically, a cut section of the resected specimen showed an ill-circumscribed, milky-white tumor measuring 4.5 cm.
病理組織学的検査所見:腹壁内に線維増生を伴い浸潤増殖する高分化型管状腺癌,一部に中分化腺癌を認めた.肝臓には浸潤を認めず切除断端に腫瘍の露出は認めなかった(Fig. 4).胆囊癌は乳頭状腺癌が優勢であったが浸潤部では管状腺癌が主体をなしていたことと,腫瘍細胞の形態が類似していることから,胆囊癌の腹壁転移と診断した.
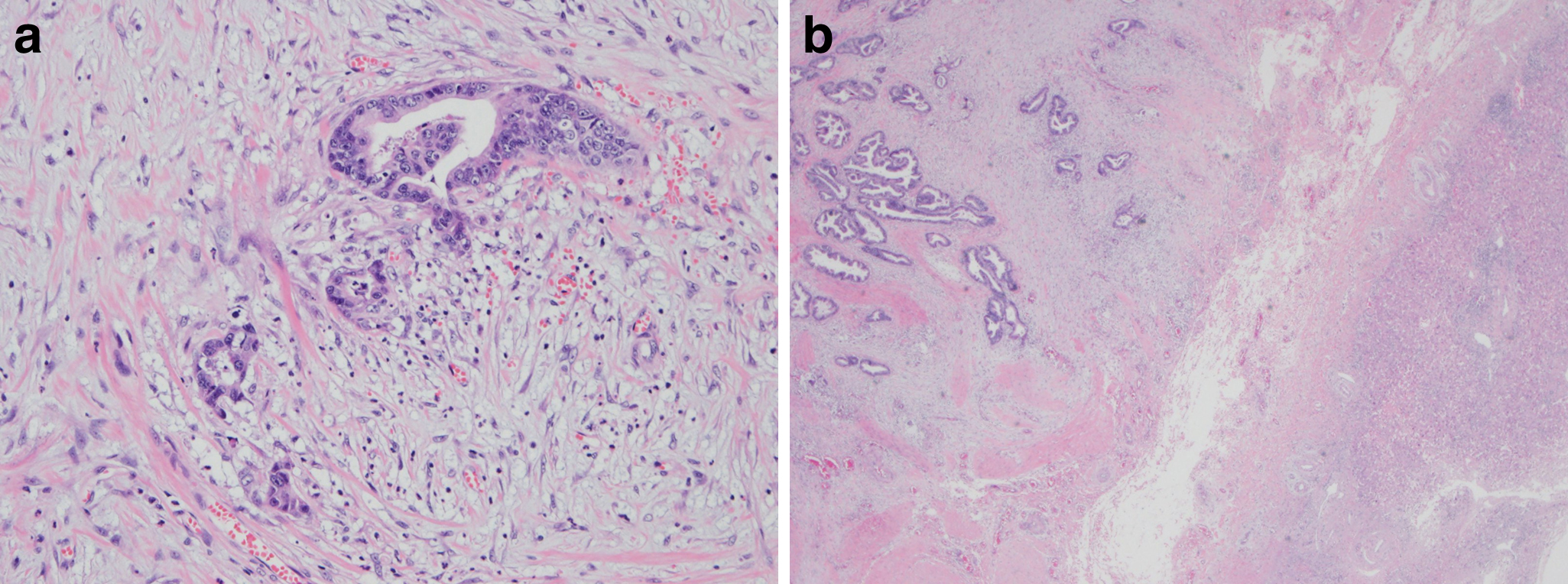
Pathological findings of the resected specimen revealed a well- to moderately-differentiated tubular adenocarcinoma with fibrosis in the abdominal wall (a). Cancer invasion did not reach the liver (b).
術後経過:10病日に退院した.術後2週からGEM+S-1併用療法(S-1 120 mg/body/day d1~d7,GEM 1,800 mg/body d8,q2w)を6コース施行後ゲムシタビン療法(1,600 mg/body d1,d8,d15,q4w)を10コース施行した.2年6か月後にCTで右季肋部腹壁転移再発の診断となった(Fig. 5)ため,2015年9月に腫瘍摘出術+第VIII・IX肋骨合併切除を施行した.腹壁欠損部は右大腿筋膜グラフトを用いて再建した.病理組織学的検査では,高~中分化腺癌で腹壁の筋肉および一部で肋骨の骨膜を超えた浸潤を認めた.筋肉内の微小転移部分で断端陽性であった(Fig. 6)ため体外照射50 Gyを施行した.その後GEM+S-1併用療法(S-1 100 mg/body/day d1~d7,GEM 1,600 mg/body d8,q2w)を30コース施行後S-1療法(120 mg/body/day,隔日内服)を10か月施行し現在経過観察中であるが,胆囊摘出術から8年5か月(腹壁再発腫瘍摘出術から5年7か月)後の現在,再発の徴候なく生存中である.

An irregular abdominal wall tumor (arrow) 4 cm in size was observed in the right hypochondrium on CT. The costal bone was involved in the tumor (arrowhead).

Histopathological findings. Pathological findings of the resected specimen revealed micro-metastasis in the muscle invading the surgical stump.
胆囊癌術後腹壁再発はまれで,予後不良とされている.ほとんどの報告がLC後のポートサイト部または手術創部に発生している.LCが施行された胆囊癌症例におけるポートサイト部再発の頻度は,本邦からの報告では1.67~9.8%5)~7),欧米からの報告では10.3~29%となっている3)8)~11).胃癌と大腸癌でのポートサイト部再発の頻度はいずれも1%前後12)とまれであり,胆囊癌に特徴的な再発形式といえる.腹壁再発の成因としてはほとんどの症例で発生部位に何らかの手術操作が加わっていることから,血行性転移よりも胆汁中の癌細胞のimplantationと考えられている13).動物実験では,二酸化炭素による気腹によりポートサイト部再発のリスクが高くなること14)15)と,癌細胞が腹膜損傷部に着床しやすいこと16)が示されている.一方,英語文献のシステマチックレビュー3)では,開腹胆囊摘出術術後に胆囊癌と診断された偶発胆囊癌における腹壁再発の頻度は7%で,LC後の偶発胆囊癌におけるポートサイト部再発の頻度の10.3%と大差がなく,胆囊癌でポートサイト部再発が多いのは胆囊癌の播種しやすい性質にも起因しているとも考えられている.
医学中央雑誌で1964年から2017年12月の期間で「胆囊癌」,「腹壁転移」,「腹壁再発」,「ポートサイト再発」をキーワードとして検索した結果,胆囊癌の腹壁再発の報告は26例であった(会議録を除く)(Table 1)1)2)17)~37).以下に自験例を加えた27例について検討を加えた.年齢は平均年齢64.6歳(45~88歳)で男女比は11:16であった.初回術式は,LCが21例(77.8%),開腹胆囊摘出術が2例(7.4%),右葉切除術+膵頭十二指腸切除術が1例(3.7%),右葉切除+肝外胆管切除術が1例(3.7%),胆囊床切除術+膵頭十二指腸切除術が1例(3.7%),胆囊床切除術+肝外胆管切除術が1例(3.7%),であった.胆囊癌の診断時期は初回手術前/初回手術後/腹壁再発後が4/14/5例(1例は記載なし)で,3例は腹壁再発後に胆囊癌が疑われ病理学的に再検索をしたが胆囊癌を認めなかった.これらの3例を除く24例の深達度はpT1a/pT1b/pT2p/pT3aが2/3/14/2例(3例は記載なし)であった.初回術式がLCまたは開腹胆囊摘出術で術後に胆囊癌と診断された14例中10例(pT2が9例でpT3aが1例)で二期的根治手術が施行された.二期的根治切除の術式は,胆囊床切除が5例21)23)~25)36),胆囊床切除+肝外胆管切除が2例34),肝S4a+S5切除+肝外胆管切除が1例32),肝外胆管切除が1例35),胆囊管切除が1例22)であった.胆囊癌を認めなかった3例を除いた24例の組織型はpap/tub1/tub2/腺癌/asc/MCN/癌肉腫その他が3/8/3/2/1/1/1例(記載なし5例)で,porは認めなかった.リンパ節転移は6例に認め17例で陰性であった(記載なし4例).術中の胆汁漏出(胆汁吸引,胆囊穿孔および胆囊亜全摘を含む)は,12例で認め,3例で認めなかった(記載なし12例).術中の胆汁漏出に対して自験例では,生理食塩水1,000 mlで腹腔内洗浄が施行されたが,その他の11例については洗浄の有無は記載がなかった.自験例は,後方視的には前医で施行されたCTで胆囊頸部に限局性壁肥厚を認め胆囊癌を疑う余地はあったが,穿孔とそれに伴う胆囊周囲膿瘍を認め術前から胆汁漏出が存在したので,一期的に胆囊癌に対する根治切除を施行していても腹壁再発は回避できなかった可能性がある.
| No. | Author | Year | Age | Sex | GBC | Abdominal wall recurrence | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Operative precedure | Bile spillage during surgery | Histologic type | Timing of diagnosis of the GBC | pT | Lymph node involvement | Site of the recurrence | Interval between initial surgery and recurrence (month) | Other recurrence | Maximal diameter (cm) | Treatment for abdominal wall recurrence | Prognosis (months) | |||||
| 1 | Kondo17) | 1988 | 55 | F | Open cholecystectomy | ? | ? | ? | ? | ? | Surgical scar | 48 | Hepatic hilum | ? | Extirpation | 16, dead |
| 2 | Kondo17) | 1988 | 77 | F | Extended right hemihepatectomy+PD | ? | ? | Before surgery | ? | Yes | ? | 8 | No | ? | Extirpation | 6, alive |
| 3 | Kondo17) | 1988 | 62 | F | Extended right hemihepatectomy+BDR | ? | ? | Before surgery | ? | Yes | ? | 5 | No | ? | Extirpation | 7, dead |
| 4 | Kiyasu1) | 1992 | 54 | F | GB bed resection+BDR | ? | pap | Before surgery | 2 | No | Surgical scar | 21 | No | ? | Extirpation+chemothterapy | 51, alive |
| 5 | Takahashi18) | 1994 | 57 | F | LC | Yes | ? | After recurrence | 1b | No | Port site | 10 | No | ? | Extirpation+chemothterapy | 12, alive |
| 6 | Oumi19) | 1994 | 61 | M | LC | ? | ? | After surgery | 2 | No | Drain insertion site | 4 | Peritoneum | ? | Extirpation | ? |
| 7 | Nishio20) | 1995 | 69 | M | LC | ? | tub1 | After recurrence | 1b | No | Port site | 12 | No | ? | Extirpation | ? |
| 8 | Nishizaki21) | 1998 | 59 | F | LC | ? | tub2 | After surgery | 3a | Yes | Port site | 10 | Hepatoduodenal ligament | ? | Extirpation | 14, dead |
| 9 | Nishimura22) | 1999 | 49 | F | LC | Yes | tub1 | After surgery | 2 | No | Port site | 9 | No | 5 | Extirpation | 13, dead |
| 10 | Tajima23) | 1999 | 45 | M | LC | Yes | adsq | After surgery | 2 | No | Drain insertion site | 3 | No | ? | Extirpation | ? |
| 11 | Ohmura24) | 1999 | 71 | F | LC | Yes | tub1 | After surgery | 2 | No | Port site | 31 | No | 4 | Extirpation | 23, alive |
| 12 | Nakagawa25) | 2000 | 73 | F | LC | Yes | ? | After surgery | 2 | Yes | Port site | 46 | No | ? | Extirpation | ? |
| 13 | Nakagawa26) | 2003 | 77 | F | LC | ? | No cancer | — | — | — | Port site | 6 | No | 5 | Extirpation | 16, alive |
| 14 | Igami27) | 2003 | 67 | M | LC | Yes | tub1 | After recurrence | 1a | No | Port site | 18 | No | ? | Extirpation | 46, dead |
| 15 | Igami27) | 2003 | 72 | F | LC | Yes | tub1 | After surgery | 2 | No | Port site | 12 | No | ? | Extirpation | 30, alive |
| 16 | Takamizawa28) | 2003 | 49 | F | LC | Yes | Mucinous cystic neoplasm | After recurrence | ? | No | Port site | 21 | Peritoneum | ? | Extirpation | 11, dead |
| 17 | Kamiya29) | 2004 | 83 | M | LC | No | tub2 | After surgery | 2 | No | Port site | 55 | No | ? | Extirpation | 28, alive |
| 18 | Hirata30) | 2007 | 67 | M | LC | Yes | tub1 | After recurrence | 1a | No | Port site | 28 | Peritoneum | 4 | Extirpation | 10, dead |
| 19 | Hirai31) | 2008 | 70 | F | LC | No | No cancer | — | — | No | Port site | 19 | Peritoneum | 8 | Extirpation | 4, dead |
| 20 | Shinohara32) | 2008 | 60 | M | LC | Yes | tub1 | After surgery | 2 | Yes | Port site | 11 | No | 4 | Extirpation | ? |
| 21 | Koshizuka33) | 2008 | 88 | M | LC | Yes | pap | After surgery | 1b | No | Port site | 54 | No | 6.3 | Extirpation | 23, alive |
| 22 | Taura34) | 2011 | 62 | F | LC | ? | tub2 | After surgery | 2 | Yes | Port site | 8 | Liver, para-aortic lymph node | ? | Extirpation+chemothterapy | 18, alive |
| 23 | Amikura2) | 2013 | 57 | M | LC | ? | No cancer | — | — | — | Port site | 43 | No | 8 | Extirpation+chemothterapy | 86, dead |
| 24 | Amasaki35) | 2013 | 60 | F | LC | No | tub1 | After surgery | 2 | No | Port site | 41 | No | 5 | Extirpation+chemothterapy | 21, dead AMI |
| 25 | Tsujita36) | 2014 | 55 | M | LC | ? | Adenocarcinoma | After surgery | 2 | Yes | Port site | 139 | No | ? | Extirpation | 20, dead |
| 26 | Nagatsu37) | 2016 | 69 | F | GB bed resection+PD | — | Carcinosarcoma | Before surgery | 3a | No | ? | 3 | Hepatic hilum | ? | Chemoradiation | 2, alive |
| 27 | Our case | 75 | M | Open cholecystectomy | Yes | pap | After surgery | 2 | No | Surgical scar | 33 | No | 4.5 | Extirpation+chemothterapy | 61, alive | |
GBC: gallbladder carcinoma, PD: pancreatoduodenectomy, BDR: bile duct resection, GB: gallbladder, LC: laparoscopic cholecystectomy, PTCD: percutaneous transhepatic cholangio-drainage, PTGBD: percutaneous transhepatic gallbladder drainage, AMI: acute myocardial infarction
腹壁再発の部位は,ポートサイト部が19例,手術創部が3例,ドレーン刺入部が2例であった(記載なし3例).LCが施行された21例の再発部位はポートサイト部かドレーン刺入部のいずれかであった(ドレーン刺入部に術中ポートを留置したかどうかは記載なし).LCで胆囊を体外に取り出す際に回収バッグを用いるとポート部再発を防げる可能性が示唆されている29)34)が,LCが施行された21例中回収バッグは7例で使用され3例で使用されなかった(記載なし11例).開腹例においても創縁保護により手術創部の再発を防げる可能性があるが,自験例では創縁保護はなされなかったし,開腹手術創部に再発したその他の2例については創縁保護についての記載はなかった.また,ポートサイト部再発の2例で2か所27)28),1例で3か所32)に再発を認めた.再発病変の最大径は平均4.1 cm(0.2~7 cm)(記載なし20例)であった.再発までの期間は,平均25.9か月(3~139か月)であった.8例で他部位の再発を認めた.他再発部位は腹膜が4例,肝門部が2例,傍大動脈リンパ節が1例,肝+傍大動脈リンパ節が1例であった.腹膜再発を伴っていた1例の深達度はpT1aであった.腹壁再発に対する治療は,腫瘍切除術が20例,腫瘍切除術+化学療法が6例,化学放射線療法が1例であった.切除不能・再発胆囊癌に対する標準的化学療法は,GEM+CDDP併用療法(以下,GC療法と略記)であるが,長い点滴時間とCDDPの蓄積性腎障害による投与上限の問題がある38).そのため,GC療法に対する非劣性が証明されたGEM+S-1併用療法(以下,GS療法と略記)や,年齢やperformance statusによってはS-1またはGEMの単独療法が選択されることも多い.自験例は高齢であったため腹壁転移とその再発の術後にGS療法をまず投与し,GEMとS-1の単独投与に移行した.投与期間とレジメン変更についてはエビデンスがないため,患者と相談のうえ決定した.自験例以外で化学療法または化学放射線療法が施行された6例でのレジメンは,GMが2例34)35),MMC+UFT1),MMC+ADM18)およびGEM+S-1の併用療法が1例2)ずつであった(記載なし1例).
自験例のように腹壁欠損が大きいと再建が必要となるが,4例26)29)31)33)でメッシュ,2例2)で大腿筋膜,1例1)で腹直筋皮弁を用いて再建が行われた.腹壁再発後切除後の局所再発を5例に認め全例で再切除が施行された19)22)27).予後については,腹壁再発切除後の平均生存期間は23.3か月で(記載なし5例),報告時点で10例が癌死していた.pT1a 2例のうち腹膜再発を伴っていた1例は10か月後に癌死していた.pT1bであった3例中2例は報告時点では生存中であった(記載なし1例).他部位再発を認めた8例の平均生存期間は10.7か月で6例が18か月以内に癌死(記載なし1例)していた.他部位再発を認めなかった19例の平均生存期間は29.2か月で癌死が4例,他病死が1例であった(記載なし4例).5年以上生存は自験例を含めて2例のみで,手術創部再発では自験例が最長であった.自験例では2度目の腹壁再発手術では断端が陽性であったことから放射線照射と化学療法が有効と思われる.胆囊癌術後経過観察中には腹壁再発に留意するべきで,他に再発を認めない場合は長期生存の可能性もあるので,積極的な治療が望まれる.
利益相反:なし