Abstract
症例は78歳の男性で,健康診断の腹部超音波検査にて肝右葉に腫瘤を指摘され,当院に紹介となった.腹部ダイナミックCTでは,肝右葉に動脈相で濃染する部分を有し,門脈相で低吸収域を呈する8.5 cm大の腫瘤性病変を認め,肝細胞癌と診断した.門脈右枝に対して経皮経肝門脈塞栓術を行った後に,肝右葉切除術を施行した.術中,標本摘出後に超音波検査を施行したところ,残肝の門脈血流が確認されなかった.続けて確認のため術中門脈造影を施行すると,尾状葉のみが造影され門脈左枝以降の血流を認めなかった.肝左葉が右葉のあったスペースへ傾くことによる門脈左枝の捻転による閉塞と診断し,術中に門脈ステント留置を選択,施行した.ステント留置後は門脈血流の速やかな改善を認めた.術後は抗凝固療法を導入し,第23病日に退院となった.術後13か月経過するが,ステント内血栓は認めず良好な門脈血流を維持している.
Translated Abstract
A 78-year-old man was referred to our hospital for further investigation of an 8.5-cm large mass in the right lobe of the liver. Abdominal dynamic CT revealed a tumor that was enhanced in the arterial phase and that showed low-density in the portal phase in the right liver. He was given a diagnosis of hepatocellular carcinoma and underwent right hepatectomy after percutaneous transhepatic portal vein embolization in the right branch of the portal vein. During surgery, the portal vein blood flow of the remnant liver was not confirmed by US after right hepatectomy. In intraoperative portal venography, only the portal vein of the caudate lobe could be observed. Therefore we diagnosed obstruction due to torsion of the left branch of the portal vein. Portal vein stent placement was performed during surgery. After stent placement, portal vein blood flow improved. Postoperatively, he received anticoagulation therapy and was discharged 23 days after surgery with good general condition. At present, 13 months after surgery, the portal vein blood flow is good and remains patent.
はじめに
肝右葉切除を行った際に,肝左葉が右に傾き,肝十二指腸靭帯の脈管,特に門脈左枝が捻転する可能性のあることが一般的に知られている.残肝の門脈閉塞は致死的な肝不全を来す可能性があり,肝右葉切除後には留意しなければならない合併症の一つである.一方,近年種々の門脈狭窄や閉塞に対して門脈ステント留置が有用であるという報告が散見される1)2).
今回,肝右葉切除直後の門脈左枝の捻転に対して術中に門脈ステントを留置し,門脈血流を維持することができた症例を経験した.同様の報告は過去になく,示唆に富む症例と思われたので報告する.
症例
患者:78歳,男性
主訴:なし.
既往歴:虫垂切除,大腸腺腫,逆流性食道炎,前立腺肥大症,高血圧,肺炎
嗜好歴:日本酒1合を毎日.
現病歴:高血圧のため通院中であった前医での健康診断で,腹部超音波検査にて肝右葉を大きく占居する8.5 cm大の腫瘤性病変を認めた.前医で行われた精査目的の腹部造影CTで肝細胞癌が疑われ,精査加療目的に当院に紹介受診となった.
来院時身体所見:PS 0,身長165.9 cm,体重65.2 kg.腹部は平坦・軟で,腫瘤は触知しなかった.
血液検査所見:血液生化学検査,腫瘍マーカーはいずれも正常範囲内であり,ICG15分停滞率18%であった(Table 1).
Table 1
Clinical laboratory data on admission
| Alb |
4.3 g/dl |
WBC |
6,990/μl |
| AST |
37 U/l |
RBC |
539×104/μl |
| ALT |
25 U/l |
Hb |
13.7 g/dl |
| T-Bil |
0.5 mg/dl |
Ht |
42.6% |
| LD |
162 U/l |
PLT |
21.4×104/μl |
| ALP |
624 U/l |
|
|
| γGTP |
400 U/l |
HBsAg |
(−) |
| PT-% |
>100% |
HCV-Ab |
(−) |
| ChE |
257 U/l |
|
|
| BUN |
24 mg/dl |
PIVKA-II |
31 mAU/ml |
| CRE |
0.92 mg/dl |
AFP |
1.7 ng/ml |
|
|
ICG R15 |
18% |
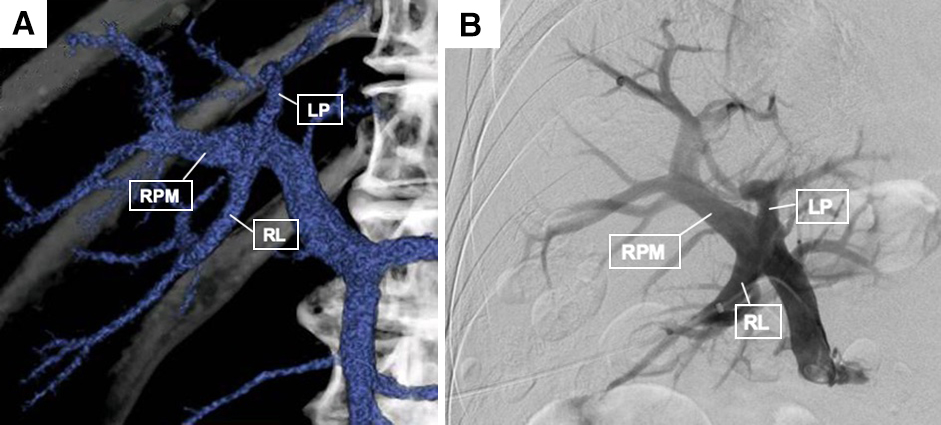
腹部ダイナミックCT所見:肝右葉,前後区域枝の分岐に近接して8.5 cm大の腫瘤性病変を認め,同病変は動脈相で濃染する部分を有し,門脈相で低吸収域を呈した.肝臓には他に腫瘤性病変を認めず,肺転移,腹膜播種,腹水を示唆する所見は認められなかった(Fig. 1).3D-CTによる門脈構築像では,門脈左枝・右前区域枝・右後区域枝はほぼ同時に分岐しており,Couinaud3)の分類で3分岐型と考えられた(Fig. 2A).
Gd-EOB-DTPA(プリモビスト)MRI所見:CT同様肝右葉に腫瘤性病変を認め,動脈相で高信号を呈する部分と低信号の混在する腫瘍として描出され,肝細胞相では取り込み欠損像として描出された.
以上より,肝細胞癌,T2N0M0 Stage II(原発性肝癌取扱い規約 第6版)と診断した.肝右葉切除を予定したが,術前のCT volumetryにて残肝予備能不足と判断し,切除に先立って門脈右枝に対して経皮経肝門脈塞栓術(percutaneous transhepatic portal embolization;以下,PTPEと略記)を行い,その3週間後に手術を施行した.PTPE時の門脈造影でも,上述のような同時分岐と考えられた(Fig. 2B).
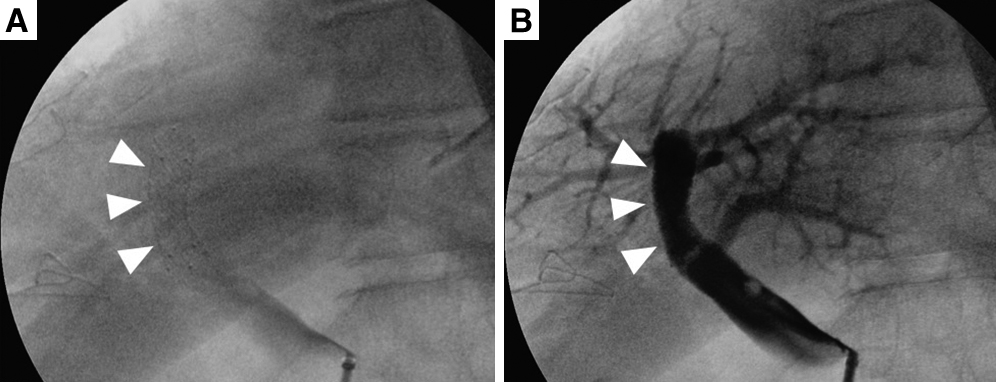
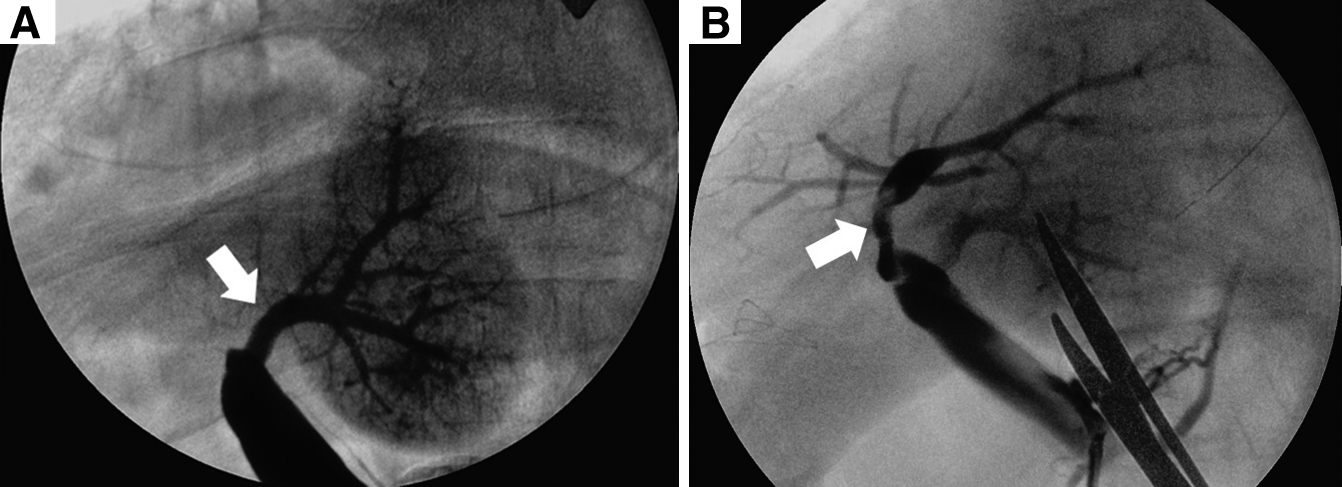
手術所見:右季肋下切開で開腹した.腹水および明らかな遠隔転移は認められなかった.肝円索および肝鎌状間膜を切離して術野を広げ,前方アプローチにより肝右葉切除を行った.肝門部グリソンは個別処理を行い,門脈右前区域枝・右後区域枝は,門脈本幹から十分に離れた位置で門脈左枝が狭窄しないように注意してそれぞれを切断した.具体的には,分岐部から約15 mmのそれぞれの門脈を切断し,断端を連続縫合閉鎖した.肝左葉の脱転は行わなかった.標本摘出後に術中超音波検査を施行したところ,肝左葉の門脈血流が確認されなかった.回結腸静脈から7 Frのシースを留置し門脈造影を行うと,尾状葉枝のみが造影され門脈左枝より末梢は造影されなかった(Fig. 3A).肝右葉のあったスペースに傾いている残肝を左側に戻すと門脈血流の再開が確認されたため,血栓による血流障害ではなく肝左葉がこのスペースへ傾くことに伴う門脈左枝の捻転が原因と考えられた.しかし,残肝を左側に戻したときの再開門脈血流はその位置により変化し非常に不安定であったため,このまま肝円索を腹壁に固定することで肝左葉を固定する方法では不十分と判断した(Fig. 3B).また,門脈の切除・再建による捻転の解消も検討したが,この段階で門脈本幹周囲の剥離は十分でなく,また門脈が余剰とはいえない所見であったため,切除・再建は容易でなく,また確実性は少ないと判断した.以上より,放射線科医師の協力のもと門脈ステント留置の方針とした.先に留置したシースより,門脈臍部から門脈本幹にかけてステントを留置した(Fig. 4).ステントはEpic Vascular self-expanding stent system;10 mm径×40 mm長(Boston Scientific Co.)を使用した.門脈圧格差は計測しなかった.ステント留置後の門脈造影では門脈左枝の血流は十分に再開し,超音波検査でも門脈血流を確認することができた.術後に門脈血栓予防としてヘパリンを注入するため上腸間膜静脈内にカテーテルを留置し,手術を終了した.
病理組織学的検査所見:moderately differentiated hepatocellular carcinoma,compact type,eg,fc(+),fc-inf(+),sf(−),s0,vp0,vv0,va0,b0,p0,sm(−)2 mm,f1,最終診断T2N0M0 stage IIであった.
術後経過:ステント留置による血栓形成予防のため,手術終了後から上腸間膜静脈内カテーテルよりヘパリン10,000単位/日の持続投与を開始した.腹部造影CTと腹部超音波検査でフォローアップしたが門脈血栓形成することなく経過し,術後第10病日から経口FXa阻害薬アピキサバン10 mg/日の内服へ切り替え,その他の合併症も認めず術後第23病日に退院となった.
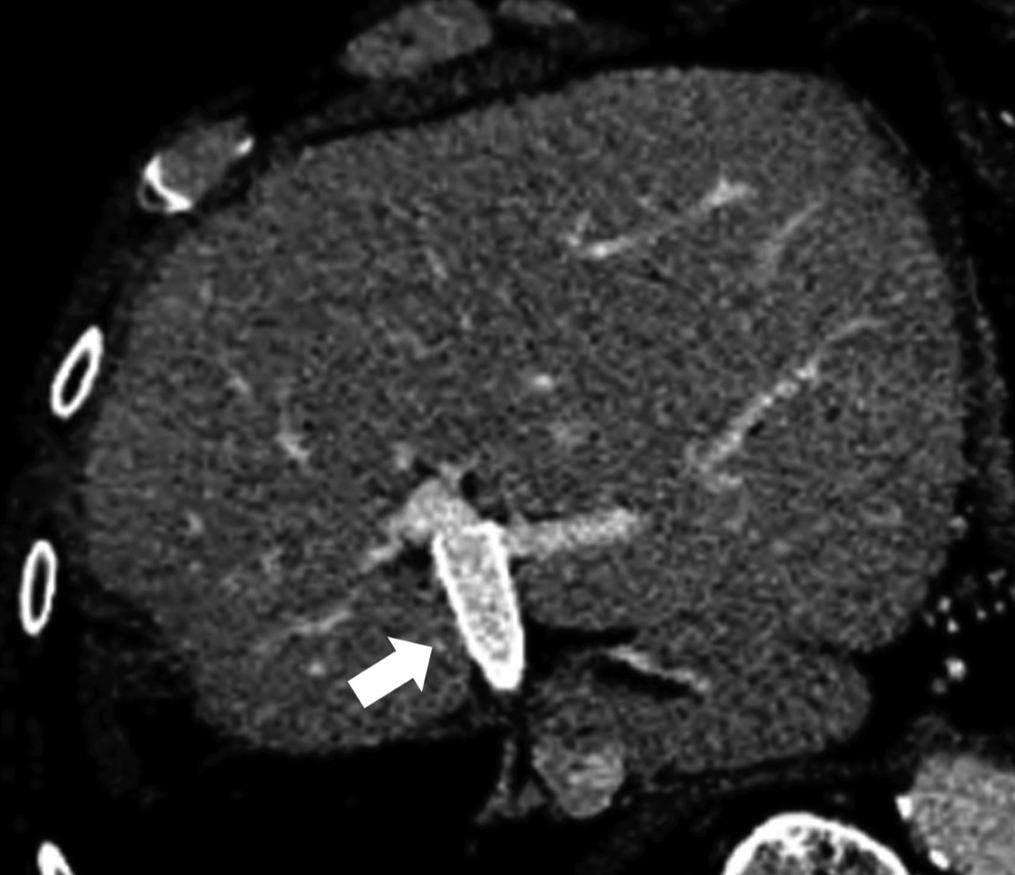
退院後は2か月ごとのD-dimerを含めた採血検査と,6か月ごとの腹部造影CTで経過観察している.現在術後13か月経過したが,血栓を形成することなく門脈血流は開存を認めている(Fig. 5).
考察
肝右葉切除術は広く行われている術式である.肝右葉切除を行うと,重力により肝左葉は右葉のあったスペースへ傾く.このために肝十二指腸靭帯の脈管,特に門脈左枝が捻転する可能性のあることが一般的に知られている.本症例でも,術中に肝左葉は一切脱転しなかったにもかかわらず,肝左葉は右側へ傾き,門脈左枝の捻転が起こった.清水ら4)は,肝門部胆管癌手術では尾状葉切除を併施するため,門脈一次分枝レベルにおける支持組織が消失し門脈は屈曲しやすい状態になると報告している.また,左側肝切除の場合は門脈の分岐形態から門脈本幹から門脈右枝はほぼ一直線となるため,門脈の屈曲が起こる可能性は低いとも報告している.本症例は尾状葉切除を併施していないが,同様の機序で門脈一次分枝レベルの支持組織が消失し,捻転から血流障害を来したものと考えられた.また,清水ら4)は,門脈本幹と左枝の分岐角度がより鋭角であれば,肝右葉切除手術後に門脈血栓が発症しやすいと述べている.本症例の門脈分岐はいわゆる3分岐型3)であり,門脈左枝の分岐角は通常よりも鋭角であったことも発症要因であると思われた.さらに,本症例では術前にPTPEを施行したが,このために肝左葉の容量が増大し重量が重くなったことも捻転の原因と考えられた.
この肝右葉切除後の門脈捻転に対する予防策としてKubokiら5)は門脈を下大静脈と固定する方法が有効であったと報告している.本症例も術中に同手技を検討したが,捻転の程度が強く効果に乏しいと判断した.また,肝円索を左側に牽引し腹壁に固定する方法が一般的に認知されている.本症例でも残肝を左側に戻すことにより門脈血流がやや再開したが,捻転の程度が強かったせいか再開門脈血流は非常に不安定で,このまま肝左葉を固定するだけでは十分ではないと判断した.実際,会議録ではあるが,竹田6)は肝右葉切除後3年後に残存左肝の腫大に伴い門脈が捻転し,門脈血栓から食道静脈瘤破裂を来した例を報告しており,不安定な状態での手術終了は避けるべきであると考えられる.さらに,門脈本幹から門脈左枝の分岐角を切除し再建する方法も選択肢の一つとして検討したが,門脈が余剰とはいえない所見であったため,有効とはいえないと判断した.以上より,強い捻転の状態であっても血流を維持できる方法として,門脈ステント留置を選択した.留置後,門脈血流は安定して再開し,その後も血栓形成することなく血流を維持することができている.
門脈ステントは,合併症も少なく安全な手技であるとされ1)2),近年,報告が散見されている7)~15).それらの報告によると,門脈ステント留置術の対象疾患としては,良性疾患では膵炎や膵頭十二指腸切除術後の門脈狭窄7)~9),門脈切除再建術後の吻合部狭窄・静脈瘤10)や肝移植後の門脈吻合部狭窄11)~13)などがある.悪性疾患では,膵癌・胆道癌による門脈浸潤14)~16),肝細胞癌の門脈腫瘍塞栓,転移性肝癌や転移リンパ節などによる門脈圧排などが挙げられる.生体肝移植の分野では,本症例と同様に,門脈の閉塞・狭窄に対して術中に門脈ステント留置を行ったという報告が存在する13).しかし,PubMedで1950年から2019年までの期間で「portal vein」および「stent」と,「torsion」,「volvulus」,「distortion」,「axis rotation」,「flexure」,「bending」,「twist」もしくは「tortuous」をキーワードとして検索したが,本症例と類似の肝切除後の門脈捻転に対する術中門脈ステント留置の報告はなかった.また,医学中央雑誌において1964年から2019年2月までで「肝切除」,「門脈」および「ステント」と,「捻転」,「ねじれ」もしくは「屈曲」をキーワードとして検索すると,胆管癌手術後の局所再発による門脈狭窄について述べたMizunoら16)の報告と,胆囊癌に対する拡大肝右葉切除術後に門脈屈曲を来し,門脈ステントを留置した落合ら17)の報告のみが認められた.落合ら17)の報告は本症例と同様に門脈は3分岐型で,拡大肝右葉切除の手術後に門脈左枝の血流障害・血栓を認め,経皮経肝的に門脈ステントを留置したものであった.しかし,本症例のように肝右葉切除に伴う門脈左枝捻転に対して術中に門脈ステントを留置したという報告はなく,国内外で初の報告であると思われる.
門脈ステント留置術の標準的な適応基準はいまだ定まっていないが,森田ら1)2)は門脈ステントの適応を,①門脈系の狭窄・閉塞に伴う明瞭な臨床症状を有する場合,②緊急避難的な措置である場合,③良好な予後あるいはQOLが期待できる場合,と報告しており,具体的には④狭窄〜閉塞部位が3 cm前後と短い場合,⑤求肝性側副血行路に乏しい場合,⑥可及的に門脈本幹に近い場合など,としている.一般的な門脈閉塞・狭窄の原因の多くは膵癌であり,これまでの予後は極めて不良であった.しかし,近年の新規化学療法の登場に伴い長期生存する例も増えてきたため,腫瘍の再発による門脈狭窄や手術後の中長期的な合併症としての術後良性狭窄も増加しており18)19),門脈ステント留置術の必要性も今後はより高まっていくのではないかと推測される.
門脈ステント留置術の成績について,Kimら20)は門脈ステント留置が18例(95%)で成功し,臨床症状は84%で改善し,良性門脈狭窄例の平均門脈ステント開存期間は30.1か月であったが,悪性腫瘍再発例の平均開存期間は7.3か月で有意に短かったと報告している.合併症については,塚本ら15)が19例に対して門脈ステントを留置し,門脈ステント留置に伴う合併症は全例で認めなかったとの報告がある.竹下ら21)は,良性狭窄で8年6か月開存したとの長期ステント開存例も報告している.また,血栓形成予防を目的として,門脈ステント留置後の抗凝固療法は行うべきとの意見が一般的には強い.しかし,抗凝固療法を行っても血栓形成を認めたという報告もあり1),発症を予測する因子は現時点では明らかではなく,個々の症例に応じて対処すべきとされる.竹下ら21)は,術後血栓形成を防止するうえでは抗凝固療法のほかに,ステントと血管内皮が密着しているほど内皮化が起こりやすいため,より血管に密着する柔軟なステントを選択することも重要であると報告している.本症例では,手術終了後から上腸間膜静脈内カテーテルからのヘパリン投与による抗凝固療法を行い,術後第10病日から経口FXa阻害薬に切り替えたが,ヘパリン中止後も門脈内血流は良好であり,門脈内血栓の形成は認めなかった.いずれの報告でも,原疾患による直接の影響と思われる再閉塞や合併症を除けば,ステント留置後の開存率は良好であり,また開腹手術中であれば回結腸静脈からのアプローチは容易であり,術中門脈ステント留置術は合併症も少なく安全に施行できる手技といえる.
門脈ステント留置術は汎用されている手技ではないが,比較的容易かつ安全に施行でき,肝右葉切除後の門脈捻転に対しても有効であると考えられた.門脈ステント留置術は,悪性腫瘍や肝移植後の狭窄・閉塞,さらに本症例のような肝切除後の門脈捻転に至るまで今後もその需要は増えていくものと考えられ,症例を蓄積し,標準的な適応基準や安全性についてさらなる検討をしていくことが必要と考えられる.
利益相反:なし
文献
- 1) 森田 穰, 小川 肇, 佐藤 幸彦, 清水 匡, 宮崎 恭介, 加藤 紘之.悪性門脈閉塞性病変に対する門脈〜上腸間膜静脈内ステント留置の臨床的検討.IVR: Interventional Radiology.1996;11(3):356–364.
- 2) 森田 穰.門脈内ステント留置術.医学のあゆみ.2000;195(7):511–517.
- 3) Couinaud C. Surgical anatomy of the liver revisited. 1st ed. Paris: Couinaud C; 1989. p. 109–110.
- 4) 清水 貞利, 塚本 忠司, 金沢 景繁, 村田 哲洋, 田内 潤, 栄 政之.肝門部胆管癌術後門脈血栓症をきたした2例の検討―特に門脈分岐角について―.胆道.2016;30(2):234–240.
- 5) Kuboki S, Shimizu H, Ohtsuka M, Kato A, Yoshitomi H, Furukawa K, et al. Incidence, risk factors, and management options for portal vein thrombosis after hepatectomy: a 14-year, single-center experience. Am J Surg. 2015;210:878–885.
- 6) 竹田 康男.胆囊がんにて肝切除後,肝腫大に伴う門脈のねじれにより,食道静脈瘤破裂,門脈血栓症をきたした1例.日本臨床内科医会会誌.2006;21(3):331.
- 7) 浅井 浩司, 渡邉 学, 松清 大, 齋藤 智明, 鯨岡 学, 森山 穂高,ほか.膵頭十二指腸切除後の門脈狭窄に伴う繰り返す挙上空腸静脈瘤出血に対して門脈ステント留置が奏功した1例.日本腹部救急医学会雑誌.2018;38(6):1059–1064.
- 8) 平井 一郎, 布施 明, 竹下 明子, 木村 理.術後の門脈狭窄に対するステント留置.胆と膵.2016;37(5):471–473.
- 9) 安田 祥浩, 加藤 文昭, 鈴木 芳明, 尾形 高士, 高木 眞人, 寿美 哲生,ほか.膵頭十二指腸切除後の門脈狭窄に対し門脈内ステント留置術を行った1例.日本消化器外科学会雑誌.2006;39(12):1834–1838.
- 10) 佐野 周生, 寺田 卓郎, 三井 毅, 呉林 秀崇, 斎藤 健一郎, 天谷 奨,ほか.門脈合併切除再建を伴う膵頭十二指腸切除術後に出現した吻合部門脈瘤に対しステント留置が有効であった1例.日本消化器外科学会雑誌.2016;49(8):812–818.
- 11) 大矢 雄希, 内田 皓士, 川端 誠一, 橋本 晋太朗, 三浦 宏平, 磯野 香織,ほか.乳児生体肝移植後早期の門脈血栓症に対する門脈ステント留置.日本小児外科学会雑誌.2018;54(1):59–63.
- 12) 栄 由香里, 諸冨 嘉樹, 里見 美和.生体肝移植後の遅発性門脈狭窄に対する門脈ステント留置術の1例.日本小児外科学会雑誌.2015;51(5):927–931.
- 13) Cheng YF, Ou HY, Tsang LL, Yu CY, Huang TL, Chen TY, et al. Vascular stents in the management of portal venous complications in living donor liver transplantation. Am J Transplant. 2010;10(5):1276–1283.
- 14) 上月 章史, 高松 学, 原田 直樹, 田中 智浩, 阿部 紘一郎, 西村 透,ほか.亜全胃温存膵頭十二指腸切除後に急速進行した門脈狭窄・門脈血栓症に対して門脈ステント留置が有効であった1例.膵臓.2018;33(5):815–825.
- 15) 塚本 忠司, 金沢 景繁, 久保 正二.悪性門脈狭窄に対するステント留置.胆と膵.2016;37(5):475–482.
- 16) Mizuno T, Ebata T, Yokoyama Y, Igami T, Sugawara G, Mori Y, et al. Percutaneous transhepatic portal vein stenting for malignant portal vein stenosis secondary to recurrent perihilar binary cancer. J Hepatobiliary Pancreat Sci. 2015;22(10):740–745.
- 17) 落合 登志哉, 満田 雅人, 石本 武史, 當麻 敦史, 大辻 英吾.胆囊癌に対する術後門脈屈曲に対しExpandable Metallic Stentが有効であった1例.癌と化学療法.2015;42(12):1737–1739.
- 18) 小薗 真吾, 千々岩 一男, 大内田 次郎, 今村 直哉, 旭吉 雅秀, 大谷 和広,ほか.膵頭十二指腸切除後の門脈狭窄に伴う消化管出血に対して門脈内ステントが有効であった1例.日本消化器外科学会雑誌.2009;42(11):1711–1716.
- 19) Fujii T, Nakao A, Yamada S, Suenaga M, Hattori M, Takami H, et al. Vein resections >3 cm during pancreatectomy are associated with poor 1-year patency rates. Surgery. 2015;157(4):708–715.
- 20) Kim KR, Ko GY, Sung KB, Yoon HK. Percutaneous transhepatic stent placement in the management of portal venous stenosis after curative for pancreatic and biliary neoplasms. AJR Am J Roentgenol. 2011;196:446–450.
- 21) 竹下 明子, 布施 明, 平井 一郎, 木村 理.門脈狭窄に対する門脈内ステント留置の検討.胆道.2005;19(4):433–439.
 https://orcid.org/0000-0002-5270-7003
https://orcid.org/0000-0002-5270-7003