2020 Volume 53 Issue 9 Pages 701-709
2020 Volume 53 Issue 9 Pages 701-709
腹腔動脈(celiac artery;以下,CAと略記)に狭窄を伴う症例に対して膵頭十二指腸切除術(pancreaticoduodenectomy;以下,PDと略記)を施行する場合,胃十二指腸動脈(gastroduodenal artery;以下,GDAと略記)切離による上腹部臓器の虚血とそれに伴う合併症を回避するために,上腹部の血流確保が必要である.その方法には,大きく分けて正中弓状靭帯切除と血管ステント留置術と血行再建術がある.今回経験した症例は,89歳男性の下部胆管癌(cT2,cN0,cM0,cStage II)である.術前の画像検査で,CA起始部の石灰化を認めていたが,GDA・下膵十二指腸動脈・膵内血管アーケードの拡張は認められなかった.しかし,術中のGDAテストクランプにて総肝動脈血流・胃血流の低下が疑われたため根治切除せずに手術を終了した.後日,血管造影検査を施行したところ,CA起始部に狭窄を認めた.確実な血流確保を目的に,血管ステント留置術と血行再建術(右胃大網動脈-第3空腸動脈)を併用したPDを施行した症例を経験したので報告する.
When pancreaticoduodenectomy (PD) is performed in a patient with stenosis of the celiac artery, the intrapancreatic arcade is resected at the same time, which may increase the risk of ischemia of the upper abdominal organs, and lead to serious complications. To maintain sufficient upper abdominal blood flow in these cases, there are three methods, preoperative intravascular stenting, intraoperative median arcuate ligament resection, and intraoperative revascularization. Ordinarily, stenting alone, or one or two of these intraoperative methods described above are selected. We experienced an 89-year-old man with lower bile duct carcinoma (cT2, cN0, cM0, cStage II). Preoperative imaging showed a calcification at the root of the celiac artery, but almost no development of intravascular pancreatic arcades. In the first surgery, intraoperative gastroduodenal artery (GDA) clamping-test caused a marked decrease in hepatic artery pulsation and gastric blood flow, and we determined it was prudent to not perform radical resection. For an elderly patient like our case with angina/diabetes as a comorbidity, it is more important to ensure sufficient upper abdominal blood flow. We performed the second surgery (PD) successfully, using two of the methods together, preoperative vascular stenting and intraoperative revascularization (right gastroepiploic artery–3rd jejunal artery).
肝臓の動脈血流は,主に腹腔動脈(celiac artery;以下,CAと略記)由来の総肝動脈より供血される.しかし,CA起始部に狭窄や閉塞を伴う症例では,上腹部臓器への血流は,膵臓内の血管アーケードを介して上腸間膜動脈(superior mesenteric artery;以下,SMAと略記)より供血される.CAの狭窄頻度は,アジア人で約2~7%と報告されている1).さらに,腹部血管造影検査上では12.5~49%に認めるとの報告もある2)3).そのような症例に対して膵頭十二指腸切除術(pancreaticoduodenectomy;以下,PDと略記)を施行する場合,膵臓内血管アーケードを同時切除するため,上腹部臓器の虚血と胆腸吻合,胃腸吻合,膵空腸吻合の縫合不全のリスクが増加する4)~6).そのためPDを施行する場合は,術前・術中の血流評価ならびに切除後の血流確保が必要不可欠である.
血流確保の方法として,正中弓状靭帯切除・血管内ステント留置術・血行再建術が報告されている.それぞれの治療法における報告は散見されるが,いずれも利点・欠点があり,一定の見解は得られておらず議論の余地がある.
今回,我々は動脈硬化によるCA起始部狭窄を伴う下部胆管癌に対するPDに際し,血管ステント留置術と血行再建術を併用して血流確保を行った症例を経験したので報告する.
症例:89歳,男性
主訴:白色便・食欲不振
現病歴:2017年6月,白色便・食欲不振を主訴に当院を受診された.来院時の血液検査にて閉塞性黄疸(T.Bil:4.62 mg/dl,D.Bil:3.43 mg/dl)を認め,画像検査にて下部胆管癌が疑われたため,外科紹介となった.
家族歴は特記すべきものなかった.既往歴は糖尿病,狭心症があり,バイアスピリン(100 mg)を内服していた.
ERCPでは下部胆管に狭窄(Fig. 1a)を認め,狭窄解除の目的に胆管ステントを挿入した(Fig. 1b).胆汁細胞診では悪性所見は認めなかった.
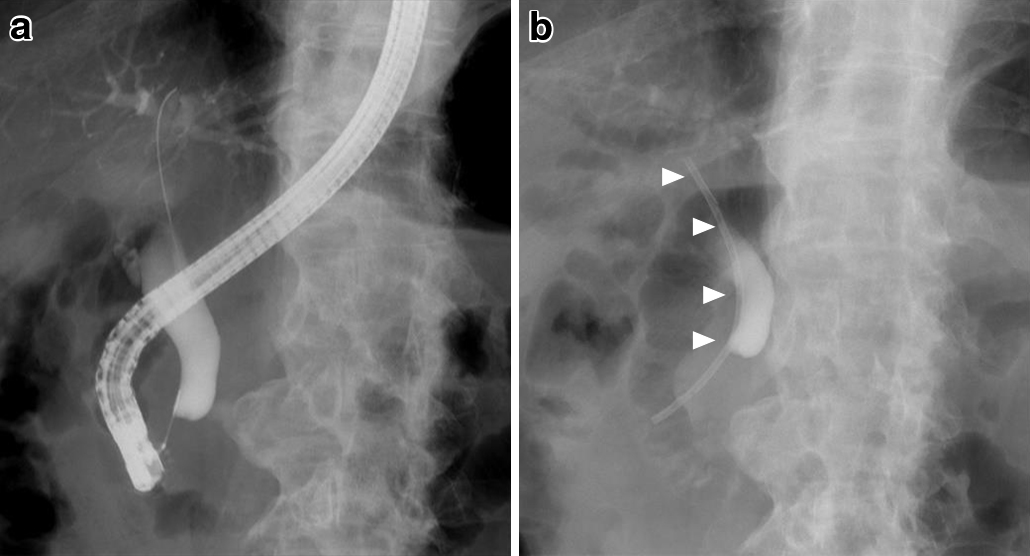
Endoscopic retrograde cholangiography (ERC). a: ERC examination showed lower bile duct stenosis. b: A biliary stent was placed into the lower bile duct (arrowheads).
腹部造影CTでは胆管拡張を認め,下部胆管に途絶像を呈していた.下部胆管には22×14 mm程度の遷延性に造影される結節を認めた(Fig. 2a).主膵管の拡張は軽度であった.肝臓や傍大動脈リンパ節への転移を疑う所見は認めなかった.CA起始部の石灰化は認めたが,胃十二指腸動脈(gastroduodenal artery;以下,GDAと略記)・下膵十二指腸動脈(inferior pancreaticoduodenal artery;IPDA)・膵内血管アーケードの著明な拡張は認めなかった(Fig. 2b, c).
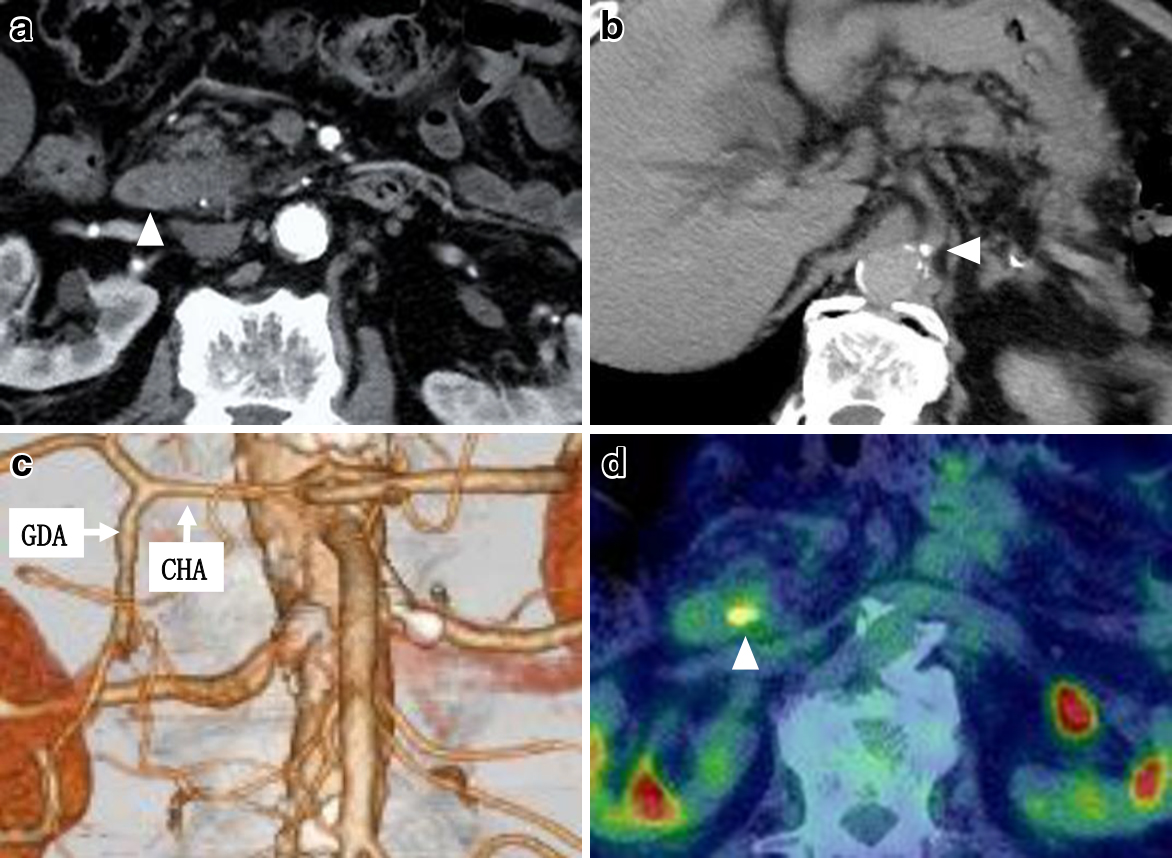
Preoperative CT, 3D vascular structure and PET. a: Enhanced abdominal CT showed a 22×14 mm mass near the lower bile duct (arrowhead). b: Abdominal CT demonstrated calcification at the celiac axis (arrowhead). c: CT scan with 3D arterial reconstruction. d: Enhanced abdominal PET showed a 22 mm mass in the lower bile duct (arrowhead).
PET-CTは下部胆管に14×14 mm大の結節とSUVmax:8.1の異常集積を認めた(Fig. 2d).その他に異常集積は認めなかった.
術前診断Bd circ cT2,cN0,cM0 cStage II,亜全胃温存膵頭十二指腸切除術,リンパ節郭清術による摘出術の方針とした.
2017年7月末,上腹部正中切開にて開腹した.(1度目の手術所見)Kocherの授動,門脈直上でのトンネリングの後,肝十二指腸間膜を剥離して,門脈,左右肝動脈,固有肝動脈,総胆管,GDA,総肝動脈をskeletonizationした.GDAをテストクランプしたところ触診にて総肝動脈の拍動が消失しており上腹部臓器の血流低下が疑われた.術中超音波検査にて肝血流低下が認められた.さらに,胃壁の色調の悪化も認められた.弓状靭帯圧迫を疑う所見はなく,動脈硬化に伴う狭窄の可能性が疑われた.GDA切離は肝臓・残胃への血流低下を来し,危険なため,膵頭部切除は困難と判断し,著明な腫大を伴う慢性胆囊炎に対する胆囊摘出術のみ施行し,閉腹した.
術後は合併症なく11日目退院した.ご本人・ご家族と治療方針に関し,再手術や血行再建などのリスクを含めて説明したところ,根治切除を強く希望された.今後の治療戦略として,①術前にCA起始部に血管ステントを留置して血流の確保,②術中にGDAまたは右胃大網動脈(right gastroepiploic artery;以下,RGEAと略記)と空腸動脈(jejunal artery;以下,JAと略記)を血管吻合し血流確保を併用し,膵頭十二指腸切除の方針とした.
2017年8月(初回手術退院後6日目)血管ステント留置術を施行した.
SMA造影で肝動脈や脾動脈が描出され,CAからの造影では呼吸変動を伴わないCA起始部の狭窄を認めた(Fig. 3a, b).
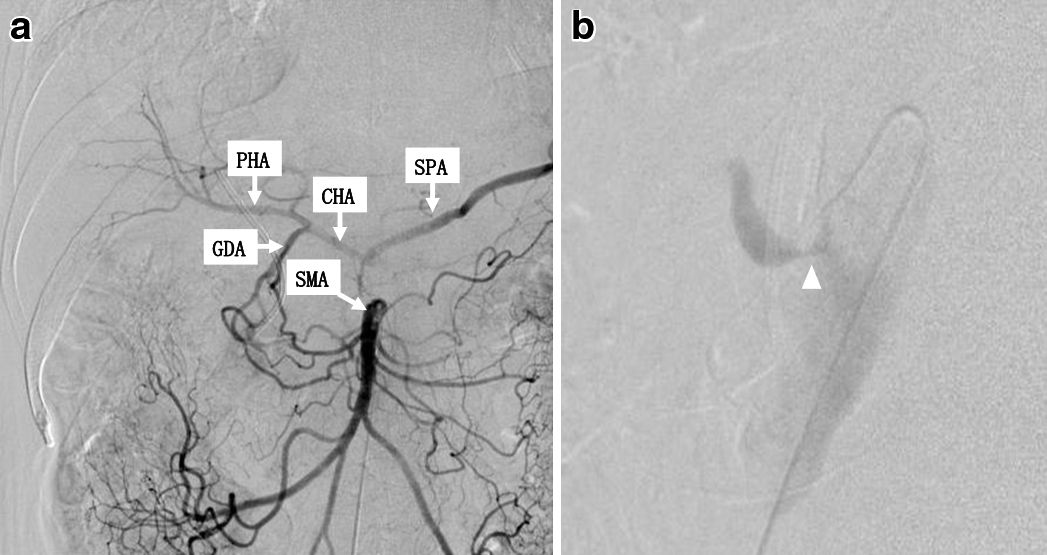
Preoperative angiography. a: The hepatic and splenic arteries were visualized via the SMA. b: There was severe stenosis into the celiac artery (arrowhead).
CA起始部の狭窄点を確認し,呼吸変動にて狭窄の増悪がないことを確認したうえで,径6 mm×長さ18 mmの血管ステントを腹腔動脈内に留置した(Fig. 4a, b).ステント留置後,バイアスピリン錠(100 mg)内服による抗凝固療法を再開した.
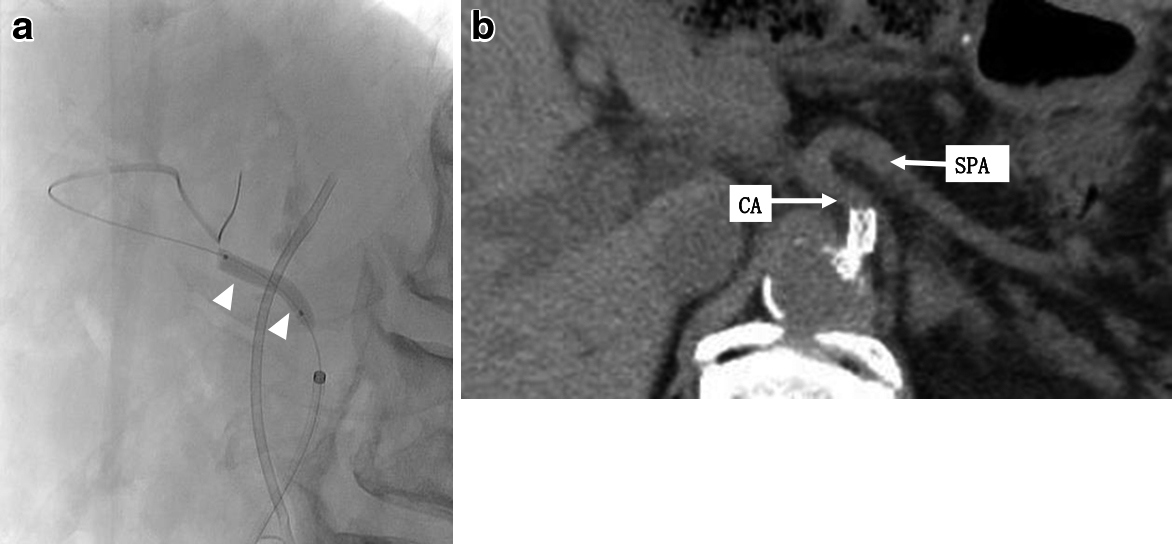
SMA angiography and preoperative CT after replacement of the stent. a: Vascular stent was replaced in the celiac artery (arrowheads). b: Stent was replaced into the celiac artery.
血管ステント留置後11日目にヘパリン置換目的で入院し,2017年8月末(血管ステント挿入後21日目)に下部胆管癌の根治を目的にPDを施行した.
術式は,亜全胃温存膵頭十二指腸切除術(SSPPD-2A-1)+血行再建術【RGEA-JA(3rd)】,手術時間は17時間12分,出血量は3,136 ml,輸血量は840 mlであった.
剣状突起から臍下に至る正中切開にて再開腹した.腹腔内は前回手術の影響で強固に癒着を認め,剥離に長時間を要した.癒着剥離の操作中に肝下面に癒着した小腸を一部損傷したため,小腸部分切除術および吻合術を併施した.肝十二指腸間膜を前回同様にskeletonizationしたうえで,GDAをクランプし,触診にて肝血流量の低下のないこと,残胃の血流低下がないことを確認したうえで,亜全胃温存膵頭十二指腸切除術を施行した.膵臓自体は,hard pancreasで柿田式にて膵腸吻合を施行した.
CA起始部のステントは,再狭窄する可能性があると判断し,予定通り動脈吻合を併用する方針とし,RGEAをGDAとの分岐部から約13 cm確保し,顕微鏡下にRGEA-JA(3rd)の血管吻合(形成外科医による9-0 Ethilonを用いた一層縫合)した(Fig. 5a, b).
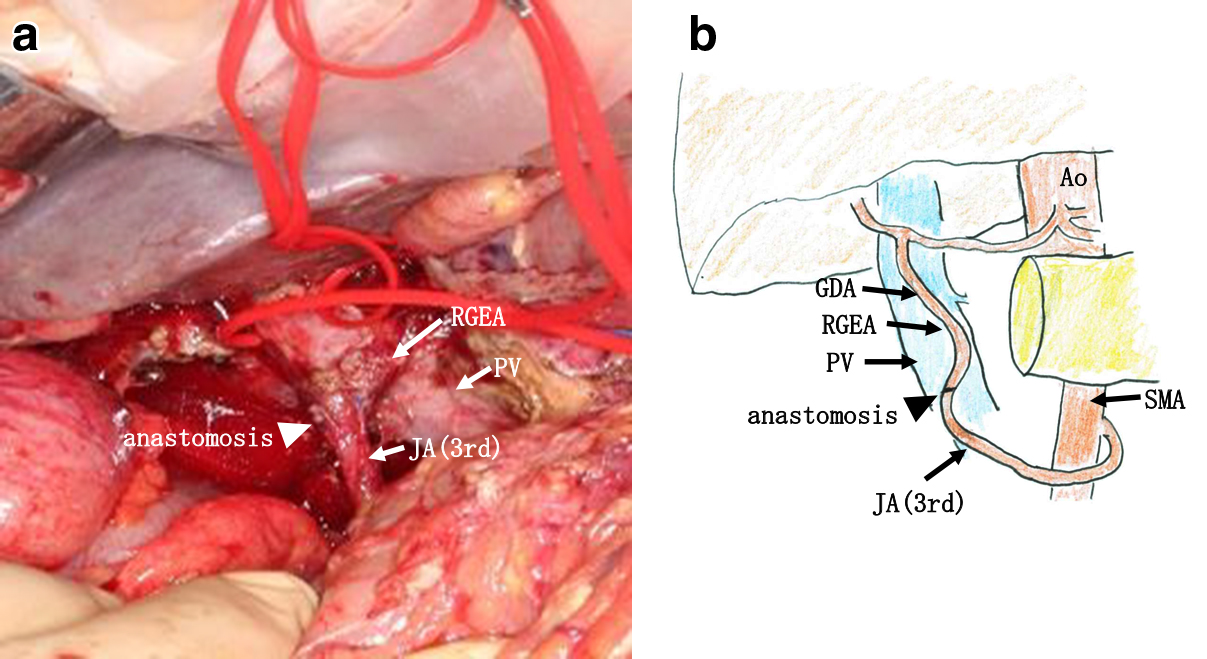
Intraoperative pictures. a: Anatomic representation of the pancreaticoduodenectomy with right gastroepiploic artery and 3rd jejunal artery bypass (arrowhead indicates the anastomosis site). b: Schema of anatomic representation. Pancreaticoduodenectomy with right gastroepiploic artery and 3rd jejunal artery bypass (arrowhead indicates the anastomosis site).
病理学的所見は,Tubular adenocarcinoma,moderate differentiated;Bd,int,INFb,ly1,v3,pn1,pT3a(膵臓・十二指腸),pHM0,pEM0,pPV0,pA0,pN1(LN13a,LN14p,LN17b),pM0,pStage IIBであった.
術後,上腹部臓器虚血などは認めなかった.胃内容物排泄遅延(Clavien-Dindo分類,Grade II),創感染(Clavien-Dindo分類,Grade I)を発症したが,術後44日目には軽快退院となった.
退院前の術後40日目の血管造影検査ではCA造影にて,血管ステントの開存,SMA造影にてSMA-JA-RGEAの開存を確認した(Fig. 6).
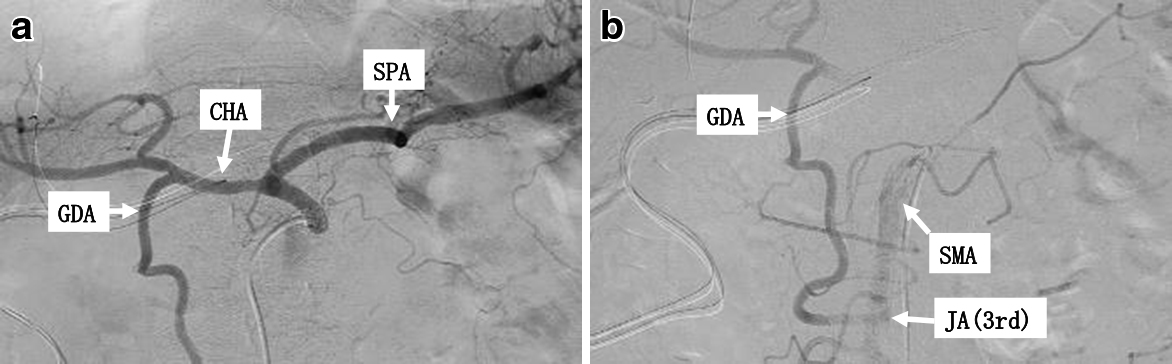
Postoperative angiography. a: The hepatic and splenic arteries were visualized via the CA. b: The hepatic artery was visualized via the SMA.
退院後,高齢であることより術後補助化学療法は施行しなかった.術後7か月でSMA周囲のリンパ節再発を認めた.S-1+gemcitabineによる抗癌剤治療を施行したが,病状進行により術後18か月目に永眠された.
CA起始部の狭窄はPDを施行する症例の5.0~10.5%にみられるとの報告があり,そのような症例では,術後の上腹部臓器(肝臓・残胃・脾臓・残膵)の血流確保に注意が必要である1)~4).術後の肝動脈血流途絶は胆管炎,肝膿瘍など重篤な虚血肝障害を来すため,致死的であると考えなければならない.また,虚血性肝障害にとどまらず,他の臓器虚血は胆腸,胃腸,膵腸吻合での縫合不全の原因にもなりうる5).
血流評価において,血管造影検査の必要性に対する議論の余地はあるが,造影CTの3D構築に比べて,GDA,CHA,吻合血管の血流方向を知るうえではより有用と考えており,当科では,必要に応じて施行している.実際に,自験例において通常の造影CT,3D構築像のみでは,膵内血管アーケードの発達を認めずCA狭窄を見抜けなかった.
ただ自験例では,術後の血流確認にも血管造影検査を施行した.CAとSMAそれぞれから造影し血流を確認,また血流の方向も含めて有用な情報を得ることができた.しかし,現在の造影CTは冠動脈の精査にも用いられるレベルで非常に詳細な情報を得られるため,安全性を考慮すると造影CTのみで十分な情報を得られた可能性はある.
術中の血流評価方法については,術中胃十二指腸動脈クランプ法の有効性が報告されている7).
CA狭窄・閉塞の原因には,血管性(動脈硬化・血管炎など)と外因性(弓状靱帯圧迫など)のものがある.多くは血管性であるが,中には外因性,特に弓状靱帯圧迫のことがある.弓状靱帯圧迫の場合,横隔膜の呼吸性変動により吸気時には圧迫が軽減されるのが特徴であり,血管造影検査で確認することができる.靱帯切開のみで狭窄が解除される場合が報告され,通常血管ステント留置術よりも靭帯切開術が推奨されている8).
一方,血管性あるいは弓状靭帯切開で血流改善が得られなかった場合,血流確保の方法として,血管ステントの狭窄部への留置,動脈吻合による血行再建術がある.血管ステントを留置する利点としては,血管吻合を行わずにすむため,血管吻合に伴うトラブルがないこと,欠点としては留置後にステントの狭窄・閉塞のリスクがあること,抗凝固薬の内服が必要なことが挙げられる.ただし,閉塞した場合でも側副血行路が形成されていることが多く,臨床上問題になることは少ないとの報告もある9).近年,開腹バイパス術の代替治療法としてCAやSMA狭窄に伴う慢性腸間膜虚血症に対して,ステント留置術が行われるようになってきている.これらの報告では,ステント留置術後,CAに留置したステントの開存率は,報告により差はあるもののおおよそ術後1年で60~75%とされている10).
アテローム性硬化,留置血管の血管径が6 mm以下が有意な血管ステントの再狭窄リスク因子と報告されている11).
これらを考慮すると,ステントの再狭窄が一定の確率で生じることを念頭におき,対処する必要がある.
血行再建術の利点としては,長期的な血流確保が行えること,欠点としては術中吻合トラブルのリスク,吻合血管の準備困難,CAの狭窄の程度にもよるが吻合操作中の一時的な上腹部臓器の血流が低下もしくは途絶が挙げられる.血管再建の方法として,グラフトを用いたバイパス術と用いないバイパス術が報告されている.グラフトによる血行再建術は,吻合血管間の距離に自由度ができるため,再建消化管の位置の影響を受けにくい一方,吻合箇所が2か所となるため,狭窄・閉塞のリスクが高くなる.人工血管グラフトに関しては,消化器手術の特性より感染のリスクが高いため用いないほうが良いとされている12⁾.本症例では,RGEAの血管をGDAから十分長く準備することにより,自由度を確保し,容易に再建血管として利用できた.
本症例と同じように,CA起始部で狭窄を有する症例に対してグラフトを用いずに血行再建術を併用したPDの報告を10例集計した(Table 1)6)13)~18).4例は供血路として中結腸動脈(middle colic artery;MCA)が使われていた.また,4例は給血路としてGDAが使われ,1例ずつではあるがRGEAやSMAも使われていた.
| No | Author | Year | Age | Gender | Disease | Cause of CA stenosis | Operation | Vessl of anastomosis | Progress |
|---|---|---|---|---|---|---|---|---|---|
| 1 | Thompson13) | 1981 | 66 | Male | Pancreatic head cancer | Arteriosclerosis | PD | SPA-SMA | Good |
| 2 | Maeba6) | 1996 | Unknown | Unknown | Unknown | Arteriosclerosis | PD | SMA-CHA | Good |
| 3 | Machado14) | 1998 | Unknown | Unknown | Chronic pancreatitis | Unknown | PD | MCA-GDA | Good |
| 4 | Machado15) | 2004 | 56 | Female | Pancreatic head cancer | Unknown | PD | MCA-GDA | Good |
| 5 | Machado15) | 2004 | 45 | Female | Chronic pancreatitis | Unknown | PD | MCA-GDA | Good |
| 6 | Nara16) | 2005 | 57 | Male | Duodenal cancer | Arteriosclerosis | PD | MCA-RGEA | Good |
| 7 | Doh17) | 2013 | 75 | Male | Pancreatic head cancer | MAL | PD | IPDA-GDA | Good |
| 8 | Piardi18) | 2019 | 78 | Unknown | Pancreatic head cancer | Unknown | PD | SPA-Aorta | Good |
| 9 | Piardi18) | 2019 | 63 | Unknown | IPMN high-grade dysplasia | Unknown | PD | SPA-Aorta | Spleen abscess |
| 10 | Piardi18) | 2019 | 77 | Unknown | Pancreatic head cancer | Unknown | PD | SPA-Aorta | Good |
celiac artery=CA, pancreatoduodenectomy=PD, median arcuate ligament=MAL, superior mesenteric artery=SMA, common hepatic artery=CHA, middle colic artery=MCA, gastro-duodenal artery=GDA, right gastro-epiploic artery=RGEA, inferior pancreatic duodenal artery=IPDA, splenic artery=SPA
本症例は,高齢症例であることや,他の部位にも動脈硬化が散見されることから,術中および術後の上腹部臓器の一次的な虚血を最小限に抑える必要があると考え,血管ステント留置術と血行再建術を併用することとした.ただし,両方の手技を行うことで,動脈ステントの挿入位置のずれや閉塞など,開腹手術前のリスクは確実に付加される.しかし,初回の動脈ステント処置の成功を確認したのちに次の手術を迎えることができることから,総じて非常に高度なリスクではあるものの,段階的な治療だからこそ乗り切れた,とも考えられる.
医学中央雑誌で1964年から2019年4月の期間で「腹腔動脈起始部狭窄」,「胆管癌」,「膵頭十二指腸切除術」,PubMedで1950年から2019年4月の期間で「celiac axis occlusion」,「bile duct cancer」,「pancreaticoduodenectomy」をキーワードとして検索した結果,計画的に血管ステント留置術と血行再建術を併用した報告は渉猟できなかった.血管ステント留置術と血行再建術を併用する治療は,どちらか一方に狭窄・閉塞が生じた場合でも,周術期のみならず,中長期的に上腹部臓器への血流が維持でき,安全性が向上すると考えられた.
利益相反:なし