2020 Volume 53 Issue 9 Pages 740-748
2020 Volume 53 Issue 9 Pages 740-748
症例は22歳の男性で,右下腹部痛を主訴に来院した.腹部造影CTで骨盤腔内に10 cm大の腫瘤性病変と右水腎症を認め,右尿管と右外腸骨動静脈への浸潤が疑われた.Volume rendering画像で内腸骨動脈と回結腸動脈から腫瘍への多数の流入血管を認めた.CT下生検でデスモイド腫瘍と診断され腫瘍摘出術,回盲部,右尿管および右内外腸骨動静脈の合併切除,左右大腿動脈血管バイパス,尿路再建術,小腸結腸瘻造設を行うことで,剥離断端を確保し腫瘍を摘出した.病理組織学的検査所見では,腫瘍細胞は均一な紡錘形細胞が束状で流れるように増殖していた.免疫染色検査では,vimentin(+),S-100(−),desmin(少数弱陽性),caldesmon(−),CD34(−),β-catenin(+),ALK1(−),CD68(−),STAT6(−)で,後腹膜原発デスモイド腫瘍と診断した.術後8月で人工肛門を閉鎖し,術後10月経過した現在まで再発なく健存中である.非常にまれな後腹膜原発の巨大な単発デスモイド腫瘍に対して機能温存に配慮した多数臓器合併切除を行い根治しえたので報告する.
A 22-year-old man was admitted to our hospital with pain in the right lower quadrant. Abdominal enhanced CT showed a tumor in the pelvic cavity measuring 10 cm in size, invasion to the right external iliac vessels and the right ureter causing hydronephrosis. Volume rendering image showed many feeding vessels to the tumor from the right internal iliac artery and the ileocolic artery. The tumor was histologically diagnosed as desmoid tumor by CT-guided biopsy. Radical tumor resection and right hemicolectomy with combined resection of right ureter, right internal and external iliac vessels were performed. Diverting ileostomy, ureteroneocystostomy and bilateral femoral arteries bypass were performed, and complete tumor resection with a wide margin was able to be performed. Histological examination of the resected tumor revealed that it was comprised of uniform spindle cells arranged in flowing fascicles. Immunohistochemically, the tumor cells were positive for vimentin, β-catenin and desmin, but not for S-100, caldesmon, CD34, ALK1, CD68 or STAT6. The tumor was histologically diagnosed as a retroperitoneal primary desmoid tumor. The ileostomy was closed 8 months after the surgery. The patient has been well more than 10 months after initial surgery, with no recurrence of disease. We report a rare case of retroperitoneal primary desmoid tumor that was treated by curative surgery with combined resection of multiple organs, while preserving postoperative anorectal and urinary functions.
デスモイド腫瘍は原因不明の繊維性腫瘍で,家族性大腸腺腫症の併存病変として腹腔内に発生することが多く,単独で後腹膜に発生することは極めて少ない.切除手術が施行されるが,周囲臓器の合併切除による術後機能低下と高い局所再発率が問題とされる1).今回,我々は巨大な後腹膜デスモイド腫瘍に対して多数臓器の合併切除により根治手術を施行しえた症例を経験したので文献的考察を含め報告する.
症例:22歳,男性
主訴:右下腹部痛
家族歴:特記すべきことなし.
既往歴:特記すべきことなし.
現病歴:右下腹部痛で近医を受診し,虫垂炎膿瘍形成の診断で当院へ救急搬送となった.
入院時現症:体温38.3°C,血圧116/88 mmHg,脈拍126回/分,整.呼吸音,心音に異常を認めなかった.右下腹部に手拳大の腫瘍を触知し,圧痛を認めたが反跳痛は認めなかった.腸蠕動音は弱く,金属音は聴取しなかった.
入院時血液検査所見:WBC 12,300/μl,CRP 10.98 mg/dlと炎症反応が高値で,BUN 22.2 mg/dl,Cr 1.41 mg/dl,eGFR 54.9 ml/min/1.73 m2と軽度の腎機能障害を認めた.腫瘍マーカー値はCEA 0.7 ng/ml,CA19-9 6.7 U/ml,SCC 1.2 ng/ml,NSE 12.1 ng/mlといずれも正常値範囲内であったが,IL-2R 724 U/ml(142~500 U/ml)は軽度の上昇を認めた.
入院時尿検査所見:糖,蛋白ともに陰性で,白血球も1–4/HPF以下と正常範囲内であった.
腹部骨盤部造影CT所見:骨盤部右側に腫瘍を認め,内外腸骨動脈や腸腰筋の表面に沿って広範囲に接していた(Fig. 1).腫瘍近傍から上行結腸周囲の脂肪織濃度上昇,腸間膜リンパ節の腫大を認めた.右尿管は腫瘍内を貫通するように見られ,右水腎症を認めた.

Abdominal CT showed that the right psoas was widely compressed by the tumor.
Volume rendering画像では内腸骨動脈領域・回結腸動脈から腫瘍への多数の流入血管を認めた(Fig. 2).
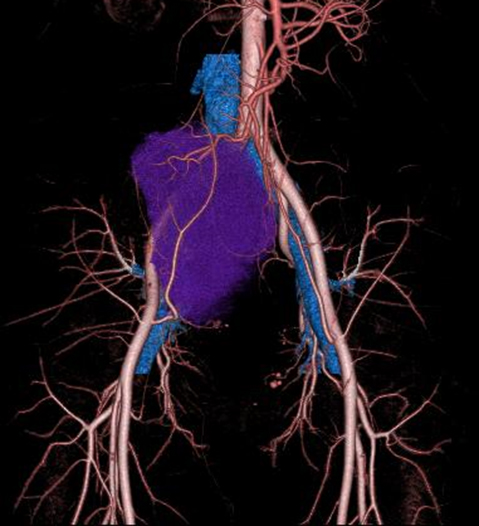
Contrast enhanced CT findings·volume rendering: The branches of the right internal iliac artery and the ileocolic artery were the main feeders.
骨盤部造影MRI所見:腫瘍は85×75×100 mm大,内部は不均一でT1強調像では低~等信号,T2強調像では低~高信号が混在していた.腫瘍の境界は明瞭で,右腸腰筋とは広範囲で接しつつも境界は保たれていた.また,外腸骨動静脈とは広範囲に密接し,血管壁に沿うように存在した.回盲部を含め周囲の腸間膜脂肪織は脂肪抑制T2強調像で不均一な高信号であり,右側精索も同様の所見であった(Fig. 3).
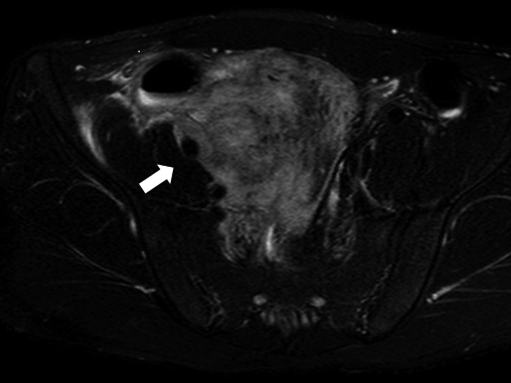
The right external iliac artery was involved in the tumor by contrast enhanced MRI (arrow).
PET-CT所見:骨盤内右側に腫瘤性病変を認め,同部に不均一なFDG集積亢進(SUVmax 8.49)を認めた(Fig. 4).
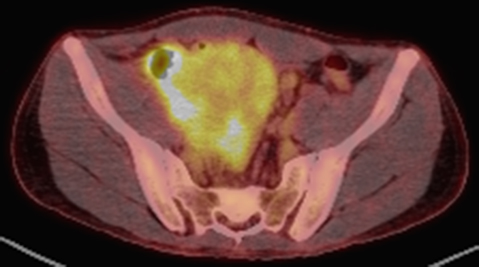
PET-CT showed high accumulation (SUVmax=8.49).
上部・下部消化管内視鏡検査所見:特記すべき異常所見なし.
入院後経過:術前画像検査で腫瘍は右尿管を取り囲むように存在し,回盲部を腹側に圧排するように発育しており後腹膜発生の腫瘍が疑われた.絶食,抗生剤治療を行い,炎症反応の低下を認めた後にCTガイド下生検を行った.診断結果はvimentin,desmin,β-cateninは陽性であり,S-100,caldesmon,CD34,ALK1,CD68,STAT6,ERは陰性で,デスモイド腫瘍を示唆する所見であった.MIB-1 labeling indexは5%であった.
腫瘍の尿管圧排による水腎症と腎機能障害に対して腎瘻を造設し,食事摂取により再度熱発を認めたため絶食とし,中心静脈栄養管理を行った.
手術所見:画像所見より腫瘍摘出に合わせ回盲部,右内外腸骨動静脈,右精索,右尿管の合併切除術を計画した.
正中切開で開腹した.腫瘍は11 cmで骨盤内右側の後腹膜に存在した.腹水や腹膜播種を疑う所見は認めなかった.術中所見において回腸部腸間膜,右尿管,右内外腸骨動静脈,右閉鎖神経は腫瘍に巻き込まれていた.腫瘍を摘出する際に右外腸骨動静脈を切除する必要があり,左右大腿動脈バイパス術を先行して行った.まず左大腿動脈と人工血管を吻合し,左下肢血流を再開させた後に,右大腿動脈と人工血管と吻合した.左および右下肢の阻血時間はそれぞれ13分と14分であった.右尿管は約15 cmを合併切除したため,吻合のための十分な距離を確保できず,また術後の尿管狭窄の可能性を考慮し膀胱と再吻合するpsoas hitchや右左尿管吻合術ではなく,右尿管腸管置換-尿管膀胱吻合術を施行した.Marginを確保して腫瘍を完全切除するために腫瘍摘出と右腸腰筋腱膜一部切除,右尿管,右内外腸骨動静脈の合併切除術および結腸右半切除術,右精巣摘出術,右尿管腸管置換-尿管膀胱吻合術,左右大腿動脈血管バイパス術を行った(Fig. 5a~c).
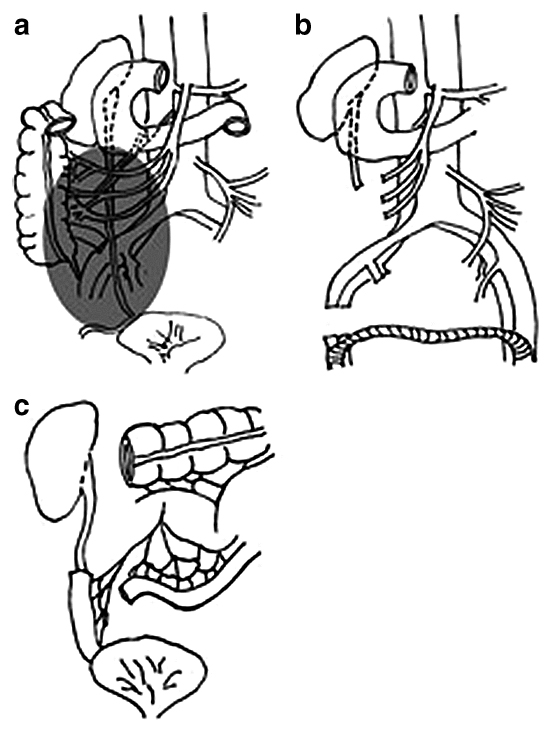
a: Tumor localization in the abdominal cavity. b: Postoperative schema. Resection right ureter, right internal and external iliac artery and vein, right hemicolectomy and orchiectomy, bypass surgery left and right femoral artery. c: Postoperative schema. Right uretero-ileo-vesicostomy.
手術侵襲を考慮して腸管吻合は施行せず双孔式の小腸結腸瘻を造設した.手術時間は1,094分,出血量6,489 mlであった.出血は巨大な腫瘍の背側となり剥離授動の際に十分に視認できなかった内腸骨静脈の分枝からの出血が主であった.
病理組織学的検査所見:肉眼的割面では境界明瞭な被膜を認め,出血を伴うが壊死は観察されなかった(Fig. 6a, b).組織学的所見では腫瘍細胞は均一な紡錘形細胞が束状に増殖し,細胞間には中小の血管や豊富な膠原繊維の介在が観察された(Fig. 7a).核分裂像は1個以下/50HPFであった.免疫組織化学所見は術前生検結果と同様にβ-cateninの核内染色像を呈しており,デスモイド腫瘍と診断された(Fig. 7b).合併切除した結腸の固有筋層,周囲脂肪織,血管周囲組織,尿管では強固な線維性の癒着が観察されたが血管壁や尿管壁への浸潤は認めなかった.
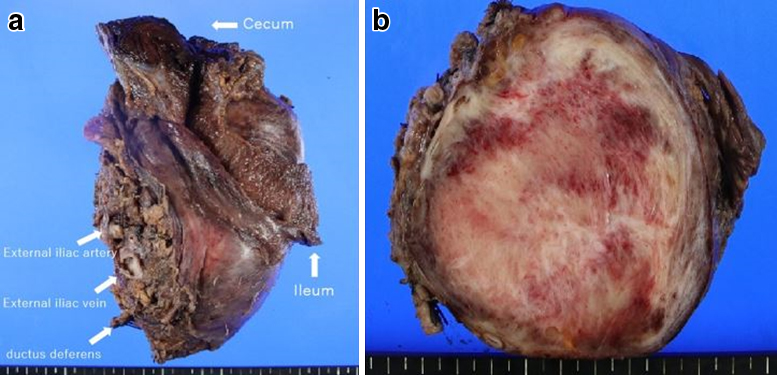
a: Macroscopic findings. b: The tumor showed a white to reddish-brown mosaic pattern.
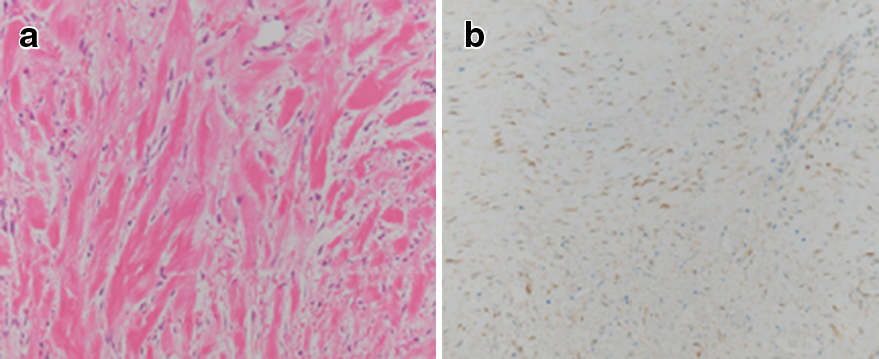
a: The histological findings showed plexiform of spindle cells (HE stain, ×100). b: Nuclei were positive for β-catenin (HE stain, ×100).
術後経過:術後,右下肢の軽度浮腫を認めたが,1週間で消退した.術後の血液検査では凝固系を含め異常所見は認めなかった.内ヘルニアによる腸閉塞で再手術を行ったが後の経過は良好で軽快退院となった.術後8か月で小腸瘻閉鎖術を施行した.術後10か月を経過した現在まで排尿機能障害や歩行障害を認めることなく,無再発健存中である.
デスモイド腫瘍はfibromatosis(線維腫症)ともよばれ,100万人あたり2.4~4.3例のまれな疾患で2)3),1)周囲軟部組織への浸潤性の発育があり境界が不明瞭となる,2)分化した線維芽細胞の増殖,3)増殖細胞間に多量の膠原線維の存在,4)高度異型細胞や異型核分裂像は認めない,5)局所再発を起こすが転移はない,などの病理学的特徴がある4).線維腫の一種の良性疾患で遠隔転移を来すことはないが,周囲に浸潤しやすく,根治術を行っても局所再発を繰り返す難治性疾患である.
発生部位により腹腔外(腹壁を含む)と腹腔内(腸間膜,後腹膜)に分類され5)6),発生頻度は腹壁49%,腹壁を除く腹腔外43%,腹腔内(腸間膜)8%とされ,後腹膜発生はまれとされる,医学中央雑誌(1964年~2018年)で「デスモイド」と「後腹膜発生」,さらに「腹腔内デスモイド腫瘍」をキーワードとして検索したところ,後腹膜発生と考えられるデスモイドの本邦での誌上報告は自験例を含めて11例であった7)~14).また,デスモイド腫瘍に対する多数臓器切除(2臓器以上切除・主要血管切除・部分切除も含む)の誌上報告は自験例を含めて10例で,後腹膜発生のデスモイド腫瘍では自験例のほかは1例のみであった(Table 1)15)~23).
| No. | Author/Year | Age/Sex | Past history | Op history | Tumor size (cm) | Origin | Treatment (combined resected organ) | Complication | Recurrence | Follow-up period |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | Isa15)/1994 | 44/F | non | + | 20×15×13 | mesentery of small intestine | small intestine*, superior mensenteric venous* | — | — | 30 months |
| 2 | Itano16)/1998 | 26/M | FAP | − | 10.5×9×5/7.5×6×5 | mesocolon | total colectomy, small intestine (100 cm resection) * | — | unknown | unknown |
| 3 | Saito17)/2005 | 51/F | FAP | + | 23×18×12 | mesentery of small intestine | small intestine (80 cm survival) *, total colon,right kidney, inferior vena cava* | short bowel syndrome | — | 4 months |
| 4 | An18)/2008 | 54/M | non | − | 4×3×3 | mesocolon/omentum | right hemicolon, duodenum* | — | — | 25 months |
| 5 | Tanaka19)/2010 | 38/M | FAP | − | 28 | mesocolon | duodenum*, ileum*, pancreas*, right hemi colon, superior mensenteric arterial* | anastomotic stenosis | — | 60 months |
| 6 | Yamakawa20)/2010 | 21/F | non | − | 12×11×6 | retroperitoneum (pancreatic capsule) | distal pancreas, spleen | delayed gastric emptying | — | 6 months |
| 7 | Tani21)/2015 | 54/M | non | + | 12×10×7.5 | gastrosplenic ligament | cardiac stomach*, spleen | — | — | 12 months |
| 8 | Hashimoto22)/2015 | 17/F | non | − | 22×22×7.5 | mesocolon | transverse colon*, diaphragm* | — | — | 56 months |
| 9 | Hoshi23)/2015 | 22/F | FAP | + | 10/15 | mesentery of small intestine | duodenum*, ileum*, right fallopian tube*, rectum* | — | — | 4 months |
| 10 | Our case | 22/M | non | − | 8.5×7.5×10 | retroperitoneum | right ureter, right internal and external iliac artery and vein, right hemicolon, right testis | internal hernia | — | 15 months |
FAP: familial adenomatous polyposis, Op history: operation history, *: partial resection
家族性大腸腺腫症の12%にデスモイド腫瘍が合併し,主に腹壁や腹腔内に発生することが知られている24).また,外傷や手術創に好発するとされ,手術操作自体がデスモイド腫瘍の発生に関わっているともされている24).さらに,デスモイド腫瘍の33%にエストロゲン受容体を認めるとする報告があり,ホルモンの関与も推測されている24).本症例では,手術や外傷の既往歴もなく,若年であったが消化管内視鏡検査でポリポーシスを認めなかったためAPC遺伝子変異について検査は行わなかった.
デスモイドの多くは腹部腫瘤として発見され鑑別疾患として,GIST,平滑筋腫,リンパ腫,神経原生腫瘍,肉腫,などが挙げられる18).デスモイドの画像診断はCTやMRIで行われるが,組織の紡錘細胞や膠原線維,粘液基質の割合によりさまざまな所見を呈し,典型的な所見はないとされる.先に挙げた鑑別疾患も疾患の状態によりさまざまな画像所見を呈し,画像による確定診断は困難である.デスモイドは一般的にCTでは筋肉よりやや高濃度な,境界不整な腫瘤として描出され,MRIでは紡錘細胞が密に存在する状態ではT2強調像でやや高信号を呈し,膠原線維が増生してくると低信号化が見られる25).また,PET-CTではSUVmaxが2.4~4.7程度の軽度上昇を示すのみで,後期相に集積が著明な上昇をすることはないとされる26).本症例ではCT,MRIの所見はデスモイド腫瘍として矛盾ないものであったが,PET-CTのSUVmaxは8.49と高値であったことから,治療方針を決定するに際して良性悪性を含めた確定診断が必要と考えられた.一般的に悪性を疑う腫瘍の生検は手術での生検ルートの合併切除を考慮し計画的に行う必要がある27).本症例では組織診断のために下腹部正中近傍でPET-CTでSUVmaxが高値の部位を経皮的CTガイド下針生検を行い,免疫染色検査でデスモイド腫瘍に特徴的なβ-cateninの核内発現陽性28)が証明されたことから確定診断された.
確定診断ののち放射線治療,化学療法,ホルモン治療についても考慮をしたがエストロゲン抗体陰性であったこと,腎機能障害,食事摂取により熱発を繰り返すこと,また根治切除が可能と判断したことから外科的手術を選択した.術中所見は術前画像検査に示されたように腫瘍が右尿管,右外腸骨動静脈,右閉鎖神経に直接浸潤してはいないものの,圧排性に発育することで最終的にこれらを取り囲むようになっており,合併切除とした.軟部腫瘍切除には少なくとも2 cmのmarginを確保することが必要であるとされてきたが,デスモイド腫瘍の特性と術前画像所見,術中所見より腸腰筋浸潤はないと判断し,腫瘍に接している腸腰筋腱膜を一部切除することでmarginを確保した29)30).術中右外腸骨静脈は再建しなかったため,下肢静脈の側副血行路の発達まで1週間は右下肢に浮腫予防のため弾性包帯を巻いた.右下肢に軽度の浮腫を認めたが,血液検査での凝固異常は認めなかった.閉鎖神経の切断により,歩行障害の出現を懸念したが認めなかった.歩行では筋肉が複合的に協調運動を行うため,一部の神経損傷では歩行障害を認めなかったと考えられた.
後腹膜腫瘍では周囲の重要臓器に近接することから,周辺臓器の合併切除が必要となることが多いが27)31)32),他臓器の合併切除はQOLの低下を招く可能性があること,不十分な切除で切除断端が陽性となると局所再発の原因となりうることから,十分な術前計画が必要と考えられる.Table 1に示す本邦報告例からは腫瘍の大きさではなく,発生部位が合併切除せざるをえない臓器数に影響することが示唆される.報告例の多くは手術時間や出血量の記載がないものの,複数臓器を合併切除していることから手術侵襲は大きいものと推察される.術後の合併症や機能障害は自験例を含む4例で報告されているが,いずれも日常生活に支障ない程度で,社会復帰が可能であった.さらに,これらの観察期間は十分とはいえないまでも再発の報告がないことから,デスモイド腫瘍に対する積極的な多数臓器合併切除は患者にとって有益である可能性が示唆される.しかし,完全切除例でも再発率は家族性大腸腺腫症を合併した症例で90%,合併しない症例でも約11%と報告されている.再発は術後2~3年に多いとされ,必要なフォローアップ期間は示されていないが,少なくとも術後2~3年間は半年に1回程度の腹部造影CTによるフォローアップが推奨されている18)22).本症例においても注意深く経過観察する必要があると考える.
本症例では詳細な術前画像検査やデスモイド腫瘍の臨床病理学的特徴をもとに合併切除を行うことで根治切除が可能と判断し,心臓血管外科,泌尿器科とともに術式を計画した27).画像診断とともに生検による組織学的な評価によって腫瘍の特性を理解することで,適切に治療方針を判断し,さらに合併切除臓器と切除後の再建について十分に検討することで術後の機能温存に配慮した根治切除が可能となったと考えられた.
利益相反:なし