2020 Volume 53 Issue 9 Pages 725-731
2020 Volume 53 Issue 9 Pages 725-731
症例は60歳の男性で,前医にて潰瘍性大腸炎(ulcerative colitis;以下,UCと略記)と診断され,内科的治療を開始したが効果に乏しく当院へ紹介となった.内科的治療不応と診断し,腹腔鏡下大腸全摘術を施行した.術後に播種性血管内凝固症候群(disseminated intravascular coagulation;以下,DICと略記)となり,その原因として当初肺炎を疑い,抗菌薬・DIC加療を施行するも発熱と意識障害の遷延を認めた.術後第63病日目に施行した頭部MRIで髄膜炎所見を認めた.さらに,髄液培養検査でEnterococcus faeciumが検出され,細菌性髄膜炎と診断した.約6週間の抗菌薬治療を継続後,発熱と意識障害は著明に改善し,再検した頭部MRI,髄液培養検査においても髄膜炎所見は消失した.今回,我々はUCに対する腹腔鏡下大腸全摘術後に極めてまれで診断に苦慮したEnterococcus faeciumによる術後細菌性髄膜炎の1例を経験したため,報告する.
Herein, we report a case of bacterial meningitis caused by Enterococcus faecium that was diagnosed following laparoscopic total proctocolectomy to treat ulcerative colitis. A 60-year-old man with refractory, active-phase ulcerative colitis was admitted and treated with laparoscopic total colectomy, ileal pouch-anal anastomosis, and ileostomy. The patient suffered from sepsis-associated disseminated intravascular coagulation during the perioperative period, and despite antibiotic treatment for differential diagnoses, including pneumonia and intra-abdominal infection, his remittent fever and disturbance of consciousness persisted. Sixty-three days after surgery, we performed head MRI and cerebrospinal fluid analysis, both of which indicated bacterial meningitis. Accordingly, after we treated the patient with targeted antibiotics for six weeks, his remittent fever and disturbance of consciousness dissipated. No evidence of bacterial meningitis was found in a subsequent head MRI or cerebrospinal fluid analysis. Perioperative bacterial meningitis following surgery for ulcerative colitis is, as in this case, extremely rare and difficult to diagnose.
潰瘍性大腸炎(ulcerative colitis;以下,UCと略記)は腸管粘膜バリア機構の脆弱性や慢性炎症による全身状態の低下,ステロイドや免疫抑制剤などの使用により易感染性であることはよく知られている1)~5).そのため,UCに対する大腸全摘術後には感染性合併症が多く認められるが,その多くは創部感染や縫合不全などの手術部位感染であり,遠隔部位感染である細菌性髄膜炎の報告は極めて少ない.今回,我々はUCに対する腹腔鏡下大腸全摘術後に極めてまれで診断に苦慮したEnterococcus faeciumによる術後細菌性髄膜炎の1例を経験したため,文献的考察を加えて報告する.
症例:60歳,男性
主訴:血便,発熱
既往歴:鬱病(選択的セロトニン取り込み阻害薬を内服).
アレルギー:特記事項なし.
家族歴:特記事項なし.
生活歴:喫煙なし,機会飲酒
現病歴:2015年12月より血便が出現し,増悪を認めたため2016年2月に前医を受診した.UCと診断され(全結腸炎型,活動期,中等症,Matts分類grade 4),内科的治療を開始した.ステロイド強力静注療法にインフリキシマブを併用するも治療効果に乏しく,2016年3月に当院へ紹介となり精査・加療目的に入院となった.
入院時現症:Japan Coma Scale 1,身長181.5 cm,体重68.9 kg,体温37.6°C,血圧102/54 mmHg,脈拍65回/分,SpO2 99%(room air),血性下痢15行/日,胸部異常なし,腹部は平坦で軟,腸蠕動音やや低下,間歇的に下腹部痛あり,筋性防御なし,鼓腸なし,痔瘻なし,四肢異常なし,リンパ節腫大なし,皮膚異常なし.
術前血液検査所見:WBC 2.4×103/μl,Hb 11.0 g/dl,PLT 34.7×104/μl,PT 66%,PT-INR 1.27,D-dimer 2.7 μg/ml,Alb 1.8 g/dl,T-Bil 0.6 g/dl,GOT 82 U/l,GPT 206 U/l,LDH 224 U/l,ALP 243 U/l,γ-GTP 55 U/l,BUN 21.5 mg/dl,Cre 0.93 mg/dl,Na 127.4 mEq/l,Cl 93 mEq/l,K 5.0 mEq/l,CRP 16.3 mg/dl.
大腸内視鏡検査所見(下行結腸まで):下行結腸から直腸にかけて広範な粘膜脱落を伴う深い潰瘍を認めた(Fig. 1).

Colonoscopy revealed ulcer in the descending colon (A), decreased vascular permeability and diffuse redness in the sigmoid colon (B), and a deep ulcer with diffuse mucosal sloughing in the rectum (C).
以上の所見より,内科的治療不応UCと診断し,手術を施行することとなった.
手術所見:術式は腹腔鏡下大腸全摘術,J型回腸囊肛門管吻合,回腸人工肛門造設術とした.以下に手術所見を記載する.腹腔鏡下に観察すると,癒着はなく小腸には異常所見を認めなかったが,炎症により大腸全体が浮腫状であった.粘膜脱落は直腸で著明であったが,肛門管は炎症所見に乏しかった.肛門管粘膜を全周性に切開し,肛門側切離ラインとして大腸全摘術を行った.回腸切離断端を15 cm折り返し,J型回腸囊を作成し,回腸囊肛門管吻合を施行した.回腸囊肛門管吻合部から20 cm口側回腸で,双孔式人工肛門を造設した.手術時間は306分,出血量は10 gであった.
術後経過:入院後の経過をFig. 2に示す.
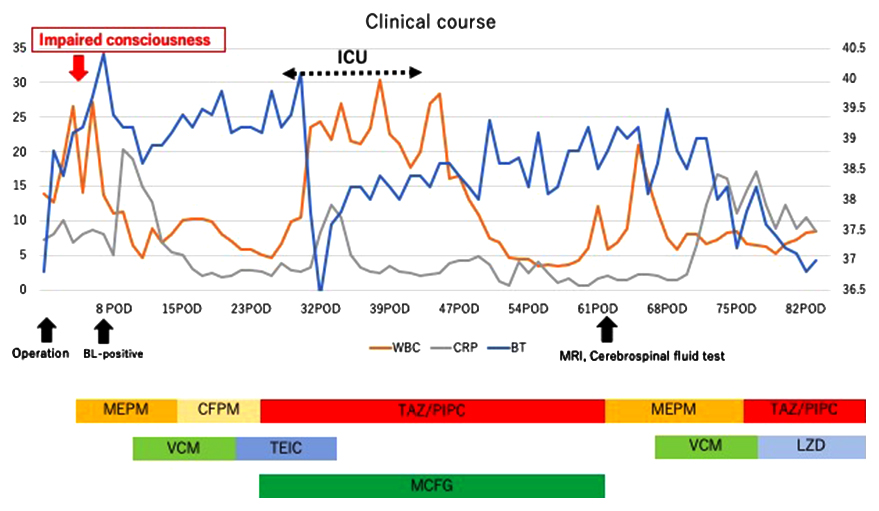
Clinical course of the patient. Continuous high fever and altered mental status was protracted. BL: blood culture, BT: body temperature, CFPM: cefepime, ICU: intensive care unit, LZD: linezolid, MCFG: micafungin, MEPM: meropenem, MRI: magnetic resonance imaging, TAZ/PIPC: tazobactam/piperacillin, TEIC: teicoplanin, VCM: vancomycin.
術後38°C以上の発熱が遷延し,炎症反応も高値であった.第3病日からは意識障害を認めた.第7病日には血液培養陽性(Enterococcus faecium),SOFA scoreは8点となり敗血症性播種性血管内凝固症候群(disseminated intravascular coagulation;以下,DICと略記)と診断した.CTでは肺炎像を認めるのみであり(Fig. 3),その他に縫合不全や腹腔内膿瘍といった腹腔内感染を示唆する所見を認めなかった.また,心臓超音波検査で感染性心内膜炎は否定的であった.これらの結果から術後肺炎による敗血症性DICと診断した.喀痰培養検査ではKlebsiella pneumoniae,Enterobacter aerogenes,Pseudomonas aeruginosaなどが検出され,薬剤感受性試験の結果に基づき予防的抗菌薬として投与していたセフメタゾール(CMZ)からメロペネム(meropenem;以下,MEPMと略記)+バンコマイシン(vancomycin;以下,VCMと略記)に変更した.その結果,炎症反応は改善傾向を示したが,発熱と意識障害は依然として遷延していたため薬剤熱の可能性を鑑みてICT(Infectious Control Team)とも協議の結果,VCMをテイコプラニン(teicoplanin;以下,TEICと略記)に変更した.血液検査では電解質やホルモン値などは正常範囲内であり,低Na血症や甲状腺機能低下症といった意識障害の原因となりうる疾患の存在は否定的であった.薬剤熱や悪性症候群などが疑われ,被疑薬の中止・変更,ダントロレン投与を行ったが,発熱と意識障害は改善しなかった.さまざまな検査にもかかわらず熱源の診断に至ることができず,一般的な術後管理の範疇を超える病態と考えられたため神経内科コンサルトを行い,UCに合併するIgG4関連肥厚性硬膜炎や易感染性に伴う細菌性・真菌性髄膜炎が鑑別診断として挙げられた.しかしながら,Kernig徴候や項部硬直などの神経学的所見に乏しく,第50病日に施行した頭部CT所見でもこれらの疾患を示唆する髄膜・辺縁系・基底膜の造影効果増強といった有意な所見は得られず,診断に至ることはできなかった(Fig. 4).第63病日からKernig徴候と項部硬直が顕在化し,頭部MRI拡散強調像で脳室内高信号を認め,髄膜炎が熱源であることが示唆された(Fig. 5).髄液検査においても蛋白の上昇と糖の低下を認め,さらに,髄液培養検査でEnterococcus faeciumを検出し,最終的に細菌性髄膜炎の診断に至った.髄液培養検査と感受性試験の結果を考慮し,抗菌薬をタゾバクタム/ピペラシリン(TAZ/PIPC)からMEPMとVCMに変更し,約6週間継続したところ,発熱と意識障害は改善した.その後施行した髄液培養検査にて細菌培養は陰性化し,頭部MRIで髄膜炎を示唆する脳室内高信号所見の消失を確認し,細菌性髄膜炎は治癒したと診断した.
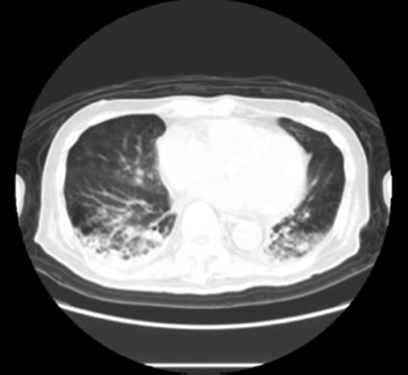
Chest CT performed 5 days after the surgery revealed consolidation and infiltration on the dorsal side of the lower lobe of both lungs indicated pneumonia.
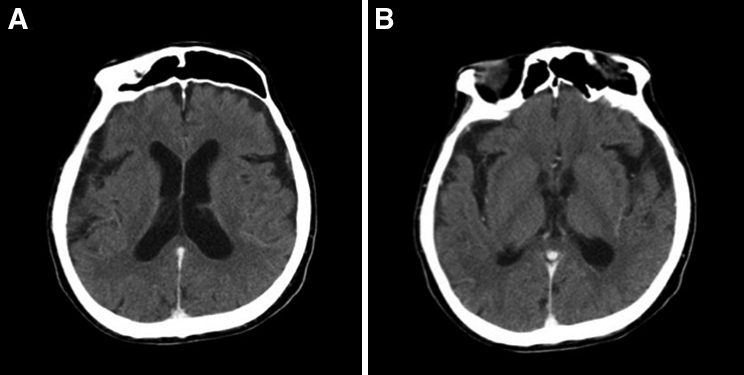
Head CT performed 50 days after the surgery revealed no evidence of meningitis in the intraventricular (A) and leptomeningeal (B) regions.
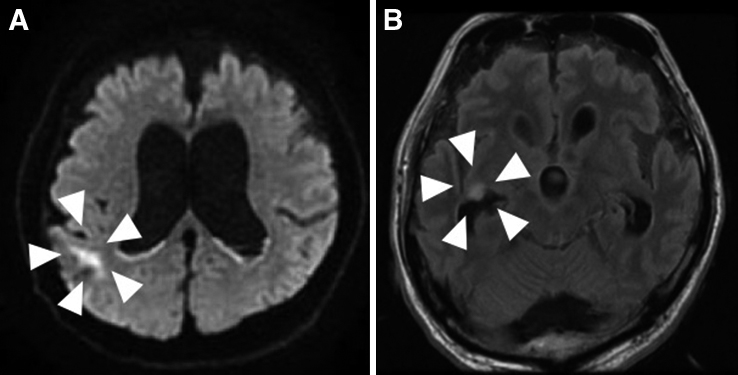
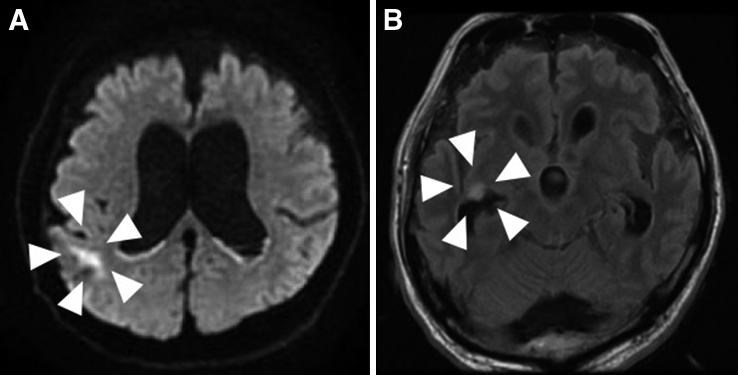
Head MRI performed 63 days after the surgery using diffusion weighted imaging revealed high signals in the ependyma and intraventricular region (A). Leptomeningeal high signal confirmed in FLAIR imaging indicated meningitis (B).
UCに対する腹腔鏡下大腸全摘術後に極めてまれで診断に苦慮したEnterococcus faeciumによる術後細菌性髄膜炎の1例を経験したので報告した.一般に,下部消化管手術後に認められる感染症の多くは,創部感染や腹腔内膿瘍などのいわゆる手術部位感染(surgical site infection;以下,SSIと略記)であり,UCにおいてはそのリスクはさらに増加すると報告されている1)~5).また,呼吸器感染,尿路感染,カテーテル関連感染などの術後遠隔部位感染も多い6).しかしながら,医学中央雑誌で「潰瘍性大腸炎」,「髄膜炎」をキーワードに1960年から2019年を検索したかぎりでは,UCに対する腹腔鏡下大腸全摘術後に細菌性髄膜炎が生じた症例を認めず,遠隔部位感染として細菌性髄膜炎を合併するのは極めてまれと考えられた.
通常,細菌性髄膜炎は緊急対応を要するneurological emergencyといわれるように,急性の経過を示す7).そして抗菌薬の初期選択と初期治療までの時間が患者の転機に大きく影響するため7),髄膜炎の起炎菌や病態に対する深い理解が求められる.細菌性髄膜炎の発症は,脳神経手術後あるいは頭部外傷後のような脳脊髄腔が外界と交通し細菌が直接侵入する経路と先行する敗血症に由来する血行性経路の二つに分けられる.術後に生じる髄膜炎は,そのほとんどが前者の経路によるものとされているが8)9),自験例の起炎菌を鑑みると,その侵入経路は血行性経路と考えられ,術後の細菌性髄膜炎という観点でもまれであった.
自験例で髄膜炎の起炎菌として検出されたEnterococcus faeciumは,感染力の低い弱毒菌の常在腸内細菌である.通常,同菌種による髄膜炎は前述のように脳神経手術や頭部外傷に続発する形で発症するか8)9),または他の髄膜炎に混合する形で検出されることが多く,その発生頻度は全細菌性髄膜炎の0.3~4.0%と,まれである10).細菌性髄膜炎のきっかけとなりうるEnterococcus faeciumの菌血症をじゃっ起する因子として,感受性のない抗菌薬の投与,免疫能低下,消化管手術,中心静脈栄養がこれまでに報告されている11).自験例では活動性の炎症性腸疾患の治療として術前から高用量のステロイドと生物学的製剤が投与され,大腸全摘術に伴い高度な侵襲を受けていたことから易感染状態となり,結果的にEnterococcus faecium菌血症の罹患リスクが非常に高い状況にあったと考えられた.そのような背景から推測される自験例における細菌性髄膜炎の感染経路は,易感染状態にある中で炎症性腸疾患に伴う腸管粘膜バリアの破綻を来し,bacterial translocationによる菌血症からEnterococcus faeciumが血液脳関門を突破し,細菌性髄膜炎になったと推測された.
自験例では,喀痰培養検査でKlebsiella pneumoniaeやEnterobacter aerogenesなどの常在腸内細菌を検出し,CTで肺野の浸潤影を認めたため,敗血症性DICの感染巣として当初,誤嚥性肺炎を疑い抗菌薬加療を行った.しかし,その効果に乏しかったため,術後の特殊な病態を鑑別疾患として考えざるをえず,薬剤熱や悪性症候群に対する被疑薬の中断やダントロレンの投与といった診断的治療を行うことになり,最終的に細菌性髄膜炎の診断に至るまでに多くの時間を要した.一般的に細菌性髄膜炎では中枢性移行が完成した場合,項部硬直を始めとした理学所見と比較的急性から亜急性の経過,頭部CTなど画像検査でも髄膜炎の病態に沿うような病的所見が診断するうえで重要な情報であるが,自験例では当初いずれも認めず比較的慢性的な臨床経過であった.これには,感染巣の認識は異なるものの,起炎菌であるEnterococcus faeciumに治療スペクトラムを有する抗菌薬を継続していたことで本来顕在化するべき理学所見がマスクされた可能性が考えられた.しかし,結果として感染巣の診断に時間を要したことを顧みて早期診断への糸口を見出すのであれば,治療中の血液培養検査と喀痰培養検査の結果の不一致は感染巣の診断が誤っていることを示唆し,正しい診断に至るための足がかりとなったのかもしれない.
腸球菌による髄膜炎では項部硬直やKernig兆候といった髄膜炎を示唆する理学所見は全体の37%にしか認めないという報告もあり,これらが髄膜炎を否定する根拠として十分でないことを示唆しているが,一方で発熱や意識障害はほとんどの症例で認めており髄膜炎を鑑別に挙げるうえで有用な臨床情報である10).これらを鑑みて自験例を振り返ると,髄膜炎としては非典型的な経過を示しながら,当初より一貫して発熱と意識障害は遷延していた点は,細菌性髄膜炎に合致する所見であったと考えられる.消化器手術後に発熱と意識障害の遷延を認めた場合には,自験例のように術後髄膜炎の可能性を想起し,頭部MRIと髄液検査の施行を躊躇しないことが重要であると考えられた.
利益相反:なし