2020 Volume 53 Issue 9 Pages 710-717
2020 Volume 53 Issue 9 Pages 710-717
症例は50歳の女性で,1歳11か月のときに先天性胆道拡張症に対して肝外胆管切除術,胆管空腸吻合術を施行された.22歳のときに膵頭部の膵石症に対して膵頭十二指腸切除術を施行された.49歳ごろから逆行性胆管炎を繰り返すようになり,当科紹介となった.CTで挙上空腸に狭窄および胆管空腸吻合部近傍に囊状拡張を認め,ERCPにて肝門部胆管に顆粒状粘膜がみられ,生検により腺癌と診断した.病変は左右肝管二次分枝を越えて進展しており,挙上空腸に直接浸潤し狭窄を来していたため,切除不能肝門部胆管癌と診断した.挙上空腸拡張部と小腸のバイパス術を行い,全身化学療法を施行したが術後12か月に癌死した.先天性胆道拡張症に対する胆囊摘出,胆管切除,および胆管空腸吻合術施行後の胆管癌発症についての報告はあるが,本症例のように膵頭十二指腸切除術が付加され胆管内への膵液逆流症状が再燃し胆管癌を発生した症例はまれであり報告する.
A 50-year old woman had been diagnosed with congenital biliary dilatation and underwent choledochojejunostomy with extrahepatic bile duct resection at the age of 1 year 11 months. When she was 22 years old, pylorus-preserving pancreaticoduodenectomy was performed for pancreatic duct stones. At the age of 49 years, she visited our hospital because of repeated acute cholangitis. CT demonstrated dilatation of the jejunal limb and subsequent stenosis near the choledochojejunostomy site. Endoscopy revealed a granular mucosal pattern in the perihilar bile duct, which spread widely beyond the secondary branch of both the right and left hepatic ducts and invaded the jejunal limb. The histological diagnosis was adenocarcinoma based upon biopsy of the granular mucosa of the right and left hepatic bile ducts and perihilar bile ducts, and we clinically diagnosed the case as unresectable perihilar cholangiocarcinoma, T4aN1M0, stage IVA. The patient underwent jejunal bypass between the dilated jejunal limb and the intact jejunum for recurrent cholangitis. She was treated with systemic chemotherapy, and died 12 months after the surgery. In congenital biliary duct dilatation, many reports discuss bile duct cancer even after extrahepatic bile duct resection with choledochojejunostomy. Ours was a rare case in which bile duct cancer occurred after pancreatic juice flowed into the perihilar and hepatic bile ducts again following pancreaticoduodenectomy, even though pancreatic juice flowing into the ducts was avoided from 1 year to 22 years of age.
先天性胆道拡張症は,膵・胆管合流異常症を高率に合併するため胆道癌を発生しやすいことが報告されている1)~3).先天性胆道拡張症における胆道癌のほとんどは拡張胆管,および胆囊に発生するため,胆囊摘出術を含めた肝外胆管切除術,および胆道再建が標準術式として行われる4).しかし,近年では拡張胆管切除後の遺残胆管に生じた胆管癌(遺残胆管癌)の報告が徐々に増加しており,先天性胆道拡張症に対する術後の新たな課題として認識されている5).今回,我々は先天性胆道拡張症に対して幼児期に胆囊摘出,肝外胆管切除,および胆管空腸吻合術が行われたにもかかわらず,その後,膵頭部に発生した膵石症のため膵頭十二指腸切除術が行われ,長期にわたり膵液が胆管内に逆流したことにより胆管癌発症の危険因子となった可能性のあるまれな症例を経験したので,文献的考察を交えて報告する.
患者:50歳,女性
主訴:発熱
既往歴:1歳11か月時先天性胆道拡張症に対して肝外胆管切除,胆管空腸吻合術,および22歳時膵頭部膵石症に対して膵頭十二指腸切除術,Child法再建術を施行された.このときの膵頭十二指腸切除では挙上空腸から胆管空腸吻合部までを切除し,新たに挙上空腸をretrocolicに挙上して胆管空腸吻合,および挙上空腸断端への膵空腸吻合術が行われていた.
家族歴:特記事項なし.
現病歴:2017年5月頃から急性胆管炎を繰り返すようになり保存的加療を受けていた.2018年10月発熱を主訴に前医を受診した際に,急性胆管炎の再燃と診断され,発症が頻回になってきていたため,今回精査加療目的に当科紹介となった.
初診時現症:151 cm,63.6 kg.体温38.0°C,血圧:120/75 mmHg,脈拍数:100回/分,呼吸数:18回/分.意識は清明で,眼瞼結膜に黄疸を認めた.腹部は平坦・軟で,圧痛,および腹膜刺激症状は認めなかった.
血液生化学的検査所見:WBC 12,600/μl,CRP 8.6 mg/dl,T-Bil 5.3 mg/dl,AST 40 U/l,ALT 26 U/l,γ-GTP 702 U/l,ALP 1,500 U/l.
腫瘍マーカー:CEA 5.8 ng/ml,CA19-9 88 U/ml.
腹部造影CT所見:肝門部尾側に挙上空腸を認め,囊状に拡張していた.一方で肝内胆管は軽度拡張していたものの,胆管結石を疑う高吸収域や明らかな腫瘤性病変は認識していなかった(Fig. 1).
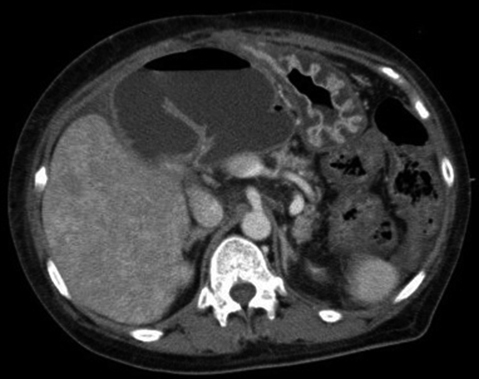
Contrast enhanced CT demonstrated the dilated jejunal limb.
経過:繰り返す胆管炎の臨床的経過,および腹部造影CTでの挙上空腸の囊状拡張の所見から,挙上空腸に何らかの通過障害が疑われたため,ERCPを施行した.胆管空腸吻合部近傍の挙上空腸に狭窄を認めたものの,胆管空腸吻合部まで内視鏡は到達可能であった.胆管空腸吻合部には明らかな狭窄は認めなかったが,胆管空腸吻合部より盲端側の挙上空腸は著明に拡張し,腸管内に腸石,および胆石を認めた(Fig. 2a).以上より,挙上空腸の狭窄に伴う急性胆管炎の可能性を考え,挙上空腸内に内視鏡的胆道ドレナージ(endoscopic nasobiliary drainage;ENBD)用の6Frチューブを留置し,その後速やかに胆管炎は軽快した(Fig. 2b).しかし,ステント挿入1週間後にステント閉塞による急性胆管炎が再燃したため囊状拡張した挙上空腸を経皮的に穿刺ドレナージを行った.この時のドレーン造影では,拡張した挙上空腸内から肛門側腸管内への造影剤の排出は認められなかった(Fig. 3).ERCP施行時,胆管空腸吻合部から左右肝管二次分枝まで広範囲にわたって胆管上皮にびまん性の大小不同の顆粒状粘膜を認めており(Fig. 2c),さらに入院時の腹部造影CTを見直すと,挙上空腸の狭窄部は肝門部に集束するようにひきつれ,狭窄しており,癌による浸潤と考えた.また,肝十二指腸間膜内には腫大したリンパ節を認めた(Fig. 4a~f).左右肝管,および肝門部胆管上皮から生検を施行したところ,病理学的検査にて腺癌と診断された(Fig. 5a~c).以上より,切除不能肝門部胆管癌,T4aN1M0 stage IVAと診断した.
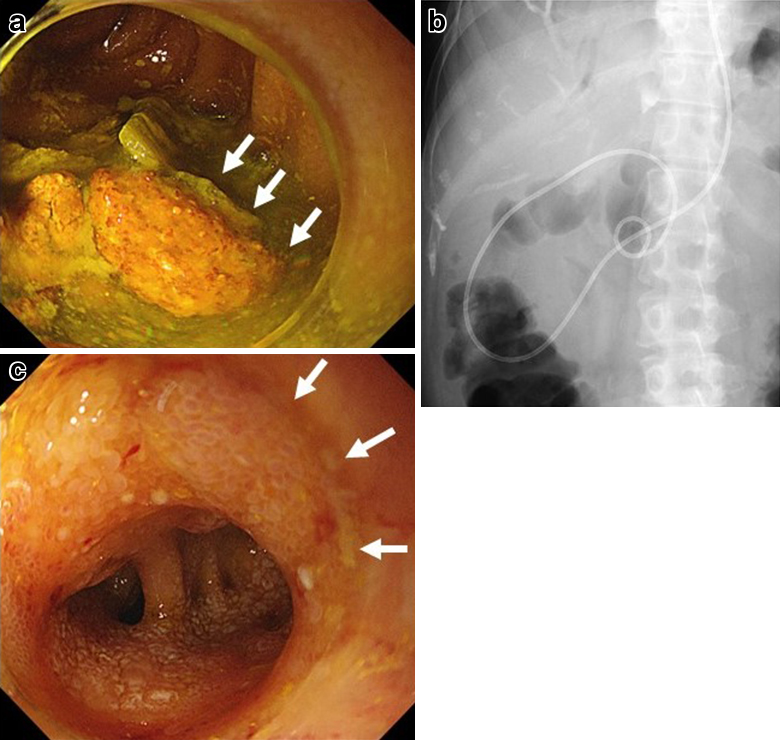
a) Endoscopic findings revealed bile duct stone and enterolith in the jejunal limb. b) An endoscopic naso-biliary drainage tube was placed in the dilated jejunal limb. c) Granular mucosa of the bile duct was observed diffusely from the choledocho-jejunal anastomosis to the distal side of the bilateral secondary branches of the hepatic duct.
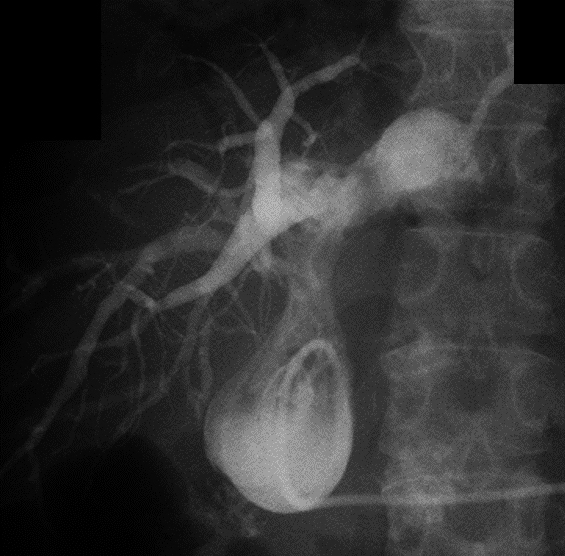
Infusion of contrast medium to the proximal jejunal limb identified dilatation, but the medium was not discharged to the distal side of the jejunal limb.
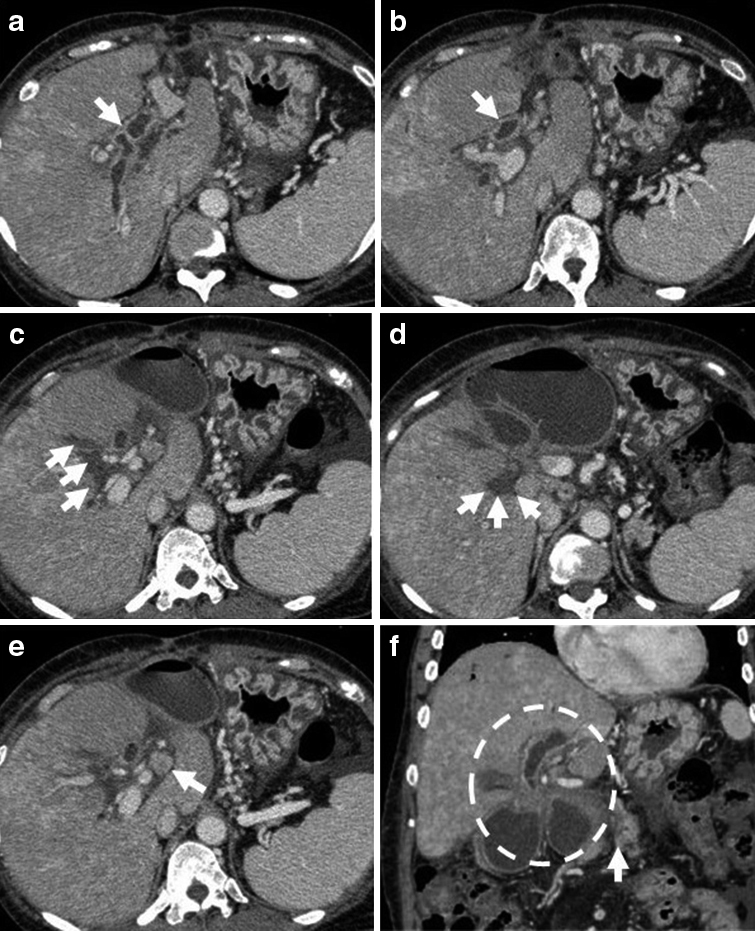
a) Choledocho-jejunostomy was indicated by the white arrow in contrast enhanced CT, and the wall thickness of the hepatic duct was shown with contrast enhancement. b) The undilated jejunal limb was demonstrated by the white arrow. c-d) Soft tissue infiltration was widespread. e) A lymph node of the hilus hepatis was enlarged. f) The jejunal limb was involved in the soft tissue mass and was dilated. White arrow indicating the pancreatico-jejunostomy.
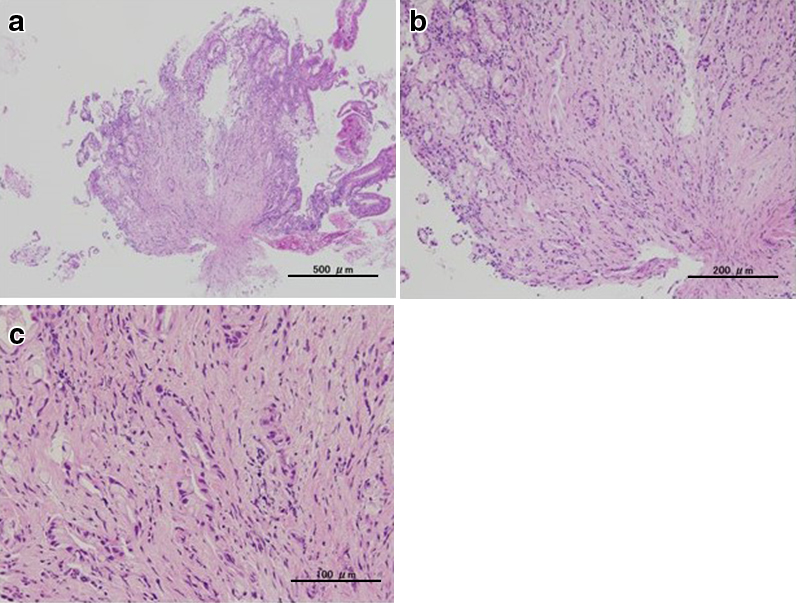
a–c) Sections shows the proliferation of atypical epithelial cells with abundant intracytoplasmic mucin and hyperchromatic nuclei, forming irregular tubules with stromal invasion.
治療経過:挙上空腸の狭窄により急性胆管炎を繰り返していたため,挙上空腸と輸入脚を側々吻合し空腸バイパス術を行った.術後経過は良好で術後30日目に退院となった.退院後,外来にてgemcitabine+CDDP療法を継続していたが,腹水貯留によってPSが低下し,病勢のコントロールが困難となり,術後12か月に死亡した.
先天性胆道拡張症は腹痛,発熱および腹部腫瘤などの症状を契機に発症し診断される比較的まれな疾患であり,拡張型が11.1%,非拡張型が37.5%と高率に胆道癌を発生することが報告されている1)6).その原因として先天性胆道拡張症に高率に合併する膵・胆管合流異常の存在が挙げられる7).膵・胆管合流異常では膵管と胆管が十二指腸壁外で合流するため,十二指腸乳頭括約筋の作用が及ばず,膵液が胆管内に持続的に逆流し,胆道壁の化学的障害から発癌にいたると考えられている8).そのため,先天性胆道拡張症における胆道癌のほとんどは拡張胆管,および胆囊に発生するため,胆囊摘出術を含めた肝外胆管切除術,および胆道再建を行う,いわゆる分流手術が標準術式として行われる4).しかしながら,近年,拡張胆管切除,胆管空腸吻合術後に残存胆管からの発癌が起こることが報告されており,手術後のフォローアップをどのようにすべきか問題とされている.拡張胆管切除,胆管空腸吻合後の胆管癌の発生については,腸内細菌の胆管内への逆流,胆汁のうっ滞,および肝内結石の形成などによる慢性的な炎症が影響を及ぼすと考えられている9)~11).また,胆管切除術を施行した時点で残存した胆管上皮にも既に遺伝子変異が生じ,前癌状態となっており,遺伝子学的変化が手術後も持続することで発癌に至る可能性も指摘されている12).特に,冨重ら13)の小児先天性胆道拡張症例におけるK-rasがん遺伝子の報告によると,生後1か月から14歳までの45例について解析を行い,0~3歳のグループにおいてすでに57.7%(26例中15例)の症例にK-rasの点突然変異を認めており,幼小児期に肝外胆管切除術,胆管空腸吻合術が行われたとしても遺伝子レベルの異常をすでに有している可能性があることが明らかにされた.本症例においても1歳のときに先天性胆道拡張症に対して肝外胆管切除術,胆管空腸吻合術が施行されているが,手術した時点ですでに前癌病変であった可能性も否定はできない.しかしながら,一方で,膵石症に対して行われた膵頭十二指腸切除の手術時に,胆管空腸吻合部を含めた挙上空腸が同時に切除されており,少なくともこの時点での標本では吻合部の胆管上皮には異型細胞を認めなかった.
さらに,本症例は肝外胆管切除,胆道再建術22年後に膵頭部膵石症に対して,膵頭十二指腸切除術を施行されている.先天性胆道拡張症では,共通管や膵管内に蛋白栓がしばしばみられるが,これは,合併する膵・胆管合流異常により胆汁と混和した膵液が拡張した共通管や主膵管にうっ滞することで非陽性結石である蛋白栓が形成されると推察されている14).具体的には,膵・胆管合流異常における蛋白栓の多くがリトスタチンを主成分としており,トリプシノーゲンとリトスタチンが胆道内に逆流し,トリプシンが活性化することで不溶性リトスタチンが生じ,蛋白栓を形成するのではないかと報告されている15).1960~1980年代の拡張胆管切除術は15~40%の術後合併症や高い死亡率がみられていたため,膵管損傷を回避する目的で膵臓から少し入った部分で膵内胆管を一部残す術式もいわゆる先天性胆道拡張症に対する肝外胆管切除術として行われていた16).2016年のアンサーパッドによる調査では,膵内胆管を合流部直上で切離しているのは19.2%で,合流部の少し上,もしくは膵上縁から少し膵内に入ったところでの胆管切除が61.7%と多くの外科医が膵内胆管を残存させる手術を行っていることが明らかとなり,遺残膵内胆管のprotein plug形成による腹痛症状などの晩期合併症を多くの外科医(77.9%)が経験していることがわかった17).また,膵頭部膵管の形態異常による膵液の排出障害とこれに伴う膵石および膵炎の発症についても報告がみられている18)19).これまでに先天性胆道拡張症術後の膵内遺残胆管内に膵石がみられる症例も報告されており,本症例のように胆管切除,胆道再建術後に膵頭十二指腸切除術を余儀なくされる症例が存在している20).本症例では,胆管空腸吻合術後に膵頭十二指腸切除術を施行したことで,再度,膵液が胆道内へ逆流する環境となった.膵頭十二指腸切除術後,年に数回程度,逆行性胆管炎を繰り返しており,消化液が胆管空腸吻合部を経由して胆管内に逆流していた可能性が高いと考えられる.特に,逆流した消化液の中には膵空腸吻合部から排出された膵液が高濃度に存在していた可能性がある.さらに,慢性胆管炎そのものも胆道癌発生の危険因子の一つとして考えられている.胆管の慢性炎症は胆管上皮における化学的・物理的障害をじゃっ起し,炎症・胆汁うっ滞が長期にわたることで胆管上皮の変性・脱落・再生が繰り返され,上皮細胞の過形成・異形成を経て癌化に至るものと考えられる21).Tocchiら9)は,1,003例に対して行われた胆管消化管吻合後132~218か月の経過観察中に55例の胆管癌発症を認めたと報告している.胆管癌を発症した55例中40例は胆管炎を繰り返しており,一方で胆管炎を発症しなかった群では胆道癌の発生はなく,胆管炎と胆道癌の因果関係について言及している.本症例の胆管癌発生は,先天性胆道拡張症に対して,手術した時点ですでに前癌病変であった可能性も考えられるが,膵頭十二指腸切除時に切除された胆管空腸吻合部の胆管上皮に異型細胞を認めなかったこと,また,膵頭十二指腸切除後28年後の発症であり術後逆行性胆管炎を繰り返していたことを考えると,一旦は肝外胆管切除,胆管空腸吻合術を行ったものの,その後膵石症に対して膵頭十二指腸切除術が行われ,再建の結果,胆管上皮に膵液を含む消化液が長期間暴露されており慢性胆管炎を経由して胆管癌発症の危険因子となった可能性がより強く考えられる.
胆管空腸吻合術後の膵頭部病変に対する膵頭十二指腸切除を行う際には,先天性胆道拡張症手術時にすでに胆管上皮に遺伝子異常を来している可能性もあることから,膵液の胆道内逆流に対してより強い注意を払う必要がある.膵管空腸吻合と胆管空腸吻合部の位置関係について,それぞれに挙上空腸を持ち上げるなど工夫し,慎重かつ長期的な胆道癌スクリーニングを行う必要があると考える.
利益相反:なし