2016 Volume 58 Issue 2 Pages 65-71
2016 Volume 58 Issue 2 Pages 65-71
歯周病は日本において国民病とも言われるほど高い罹患率を示し,その治療法のアップデートは急務である。従来から知られるプラークコントロール,スケーリング・ルートプレーニングを主体とした歯周基本治療の重要性は広く認識されているところだが,近年ではそれに加えてより効率的に除菌静菌を進めるためにマクロライド系抗菌薬の使用や光線力学療法,新規抗菌性バイオマテリアルを使用した治療法が次々に提案されている。また日常臨床において骨移植術,GTR法,エナメルマトリックスデリバティブ(EMD)等の歯周組織再生療法が盛んに行われているが,重症な歯周病罹患歯には未だ十分な効果を発揮できないのが現状であり,新しい骨補填材やティッシュエンジニアリング法が開発され,歯周病治療にも多面的に新技術が応用されつつある。
次世代的材料であるナノカーボンは,炭素原子からなる六員環構造の違いによって様々な形態を創製でき,さらに近年ナノ材料の単分散技術が確立されたことから,その優れた特性が次々に明らかになっている。ナノカーボン素材には,カーボンナノチューブ,カーボンナノホーン,カーボンナノファイバー,フラーレン,グラフェン等が知られ,それぞれに異なったユニークな特性がある。ナノカーボンを医薬品,医療機器として生体へ応用できないか世界的に試みが行われているが,なかでもグラファイトから生成されるカーボンナノシート「酸化グラフェン」は,安全性が高く優れた理工学的特性を有するとともに,抗菌性やドラッグデリバリー効果,培養細胞へのポジティブな効果が報告されている。著者らは近年,酸化グラフェンの生物学的特性を評価するとともに,酸化グラフェンを含有する三次元スキャフォールドを創製し,動物実験レベルで骨などの生体組織の再生を促進することに成功した。また酸化グラフェンの抗菌性を確認し,次世代の歯周治療への発展性を示した。そこで本レビューではこれまでの研究報告を整理し,酸化グラフェンを用いた歯周病治療への新しい医療技術展開の可能性を紹介する。
酸化グラフェンは名のとおりグラフェンが酸化されたものであり,グラフェンの構造によく似ているがまったく異なる特性を示す。グラフェンとはsp2炭素による六員環の二次元シート構造で,厚みが炭素原子1個分であり,世界で1番薄い材料(厚み1nm以下)である。GeimとNovoselovらはグラファイトを粘着テープで何度も剥離する方法でグラフェンを作製し(スコッチテープ法1)),2010年にノーベル物理学賞を受賞した。このグラフェンにはあらゆる材料を凌駕する通電性があることが判明したものの,疎水性で水分散せず凝集しやすいため,安定して製品化することが非常に難しかった。一方で酸化グラフェンは,グラファイトを酸化しながら化学的に単層剥離して生成される。例えばHummers-Offeman法2)ではグラファイトを硝酸ナトリウム,硫酸,過マンガン酸カリウムにより強く酸化することで酸化グラフェンを作製する(図1)。その結果,酸化グラフェンのシートにはsp3炭素が混在し,エポキシ基,水酸基,カルボン酸基等の極性官能基が数多く存在することになる。これにより酸化グラフェンは水に大変良く分散し,一般のナノ物質で頻繁にみられる凝集が防がれるのである。
そこでグラフェンを安価に大量に得る方法の一つとして,酸化グラフェンを作成後に還元して酸素官能基を除去してグラフェンにする方法が考案され進化していったのだが,近年酸化グラフェンそのものがグラフェンと異なる優れたナノ材料特性を示すことが次々と明らかになった。電池,電極,潤滑剤,触媒,複合材等の理工学的使用例に加えて,豊富な酸素官能基には発光物質,薬剤,生理活性物質を結合できることから,バイオイメージング3,4)やドラッグデリバリー5-8)の効果が期待されている。
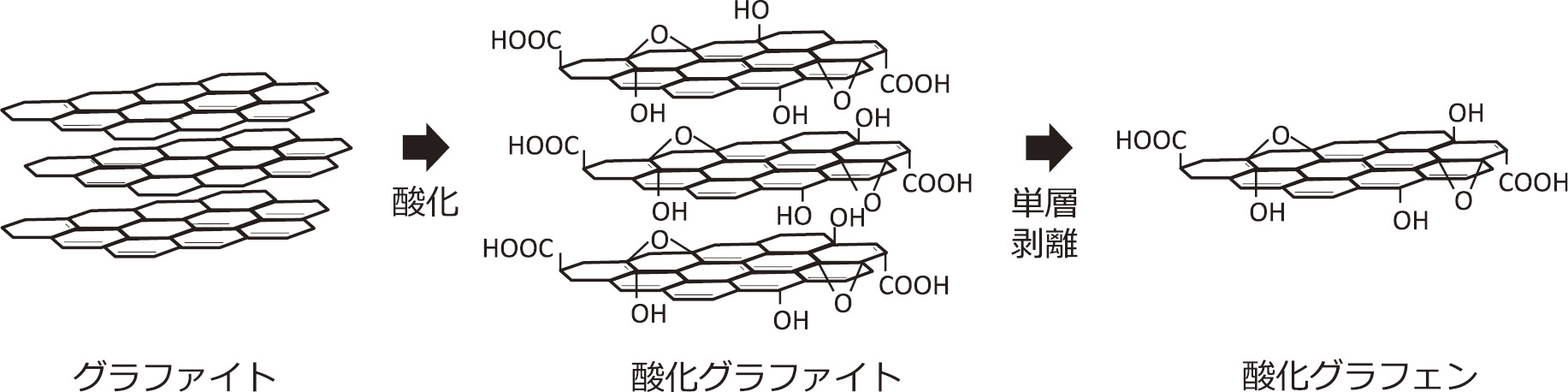
グラファイトを酸化すると酸素官能基が付加され,グラファイトの層間距離が拡大して親水性の酸化グラファイトが生成される。これをさらに水中にて超音波処理等を行うと層間に水分子が浸透するために単層剥離して酸化グラフェンとなる。
酸化グラフェンが容易に得られるようになったことで,酸化グラフェンの生体応用への足掛かりが次々と報告されている。Leeらは酸化グラフェンフィルムを作製してその上にヒト骨髄由来細胞を播種培養したところ,細胞の増殖分化を促進することを明らかにした。彼らは,酸化グラフェンが培地中に含まれる生理活性化物質のデキサメタゾンを吸着,濃縮したことによって細胞活性が向上したと考察している9)。Kimらはヒト脂肪由来幹細胞(hASCs)を用いて酸化グラフェンフィルム上で培養試験をおこなったところ,良好な接着と高い細胞親和性を示し,また酸化グラフェンがhASCsの骨,脂肪,上皮形成に関連する遺伝子発現を増強したことを報告した10)。またマウス骨格筋芽細胞を酸化グラフェン上へ播種培養した研究では,良好な細胞接着と増殖,ならびに細胞の分化促進が報告された11)。酸化グラフェンによる細胞活性上昇の作用機序は十分には明らかにはなっていないが,前述のとおり多くの酸素官能基が存在することから,血清タンパク質を多く吸着し,それが細胞の付着や成長に必要な接着分子を多く引き寄せることで,酸化グラフェン表面が選択的に細胞活性を上げる生物学的な環境になり得るようである9,12,13)。
一方で酸化グラフェン表面の酸化度や還元度の違い,つまり酸素官能基の量によって細胞挙動が変わるとの報告がある。Kuらは酸化グラフェンと還元型酸化グラフェン上でのマウス筋芽細胞の接着,増殖,分化について検討したところ,特に酸化グラフェンにおいて細胞分化が促進したことを報告した14)。我々も還元型酸化グラフェンの細胞挙動に関して調査した結果,還元型酸化グラフェンフィルム上で骨芽細胞様細胞を培養すると酸化グラフェンフィルムに比較してALP活性の向上が見られ,またラット生体内でのこれら両者に対する細胞組織挙動が異なった15)。近年酸化グラフェン上の酸素官能基量を制御出来るようになってきたことから,生体応用に適した酸化度の酸化グラフェンを見つけ出すことが必要と思われる。Gurunathanらは,緑膿菌バイオマスによる還元型酸化グラフェン(M-rGO)とヒドラジンによる酸化グラフェン(H-rGO)を添加して初代マウス胚線維芽細胞を用いて培養実験を行ったところ,M-rGOでは酸化グラフェンと同様の良好な細胞増殖を示したがH-rGOでは死細胞が増加したことを報告した16)。このように酸化グラフェンの還元方法によっても細胞挙動が変化すると考えられ,さらなる解明が待たれている。
ティッシュエンジニアリングの3要素,細胞,シグナル因子,足場材(スキャフォールド)の利用が1993年17)に提唱されてから,新しいコンセプトに基づく組織再生法が次々と生み出され,同時にスキャフォールドへの酸化グラフェンの配合使用例が報告されている。Depanらはキトサンと酸化グラフェンによって創製されたスキャフォールドが高弾性率,高強度を示すこと,また酸化グラフェンの添加によってスキャフォールドへのマウス骨芽細胞様細胞の付着増殖を促進させたと報告している18)。Qiらもポリビニルアルコールと酸化グラフェンの複合スキャフォールドを作製し,酸化グラフェンの添加によって引っ張り強さが約20%増加したこと,培養骨芽細胞の付着増殖が促進したことを報告している19)。Zhangらが作製したコラーゲン-酸化グラフェン複合体の研究では,酸化グラフェンによって間葉系幹細胞の骨芽細胞分化が加速されたことを報告している20)。我々も近年,コラーゲン-酸化グラフェン複合スキャフォールドを創製し(図2),コントロールのコラーゲンスポンジに比べて1.7倍の強度向上,1.6倍の細胞増殖効果を確認した。酸化グラフェン混和材は高い強度が発揮されるが,興味深いのは酸化グラフェンの添加によってスキャフォールドの細胞活性も同時に上昇することであり,これは前述の細胞への効果によると考えられ,酸化グラフェンはティッシュエンジニアリングにおけるシグナル因子のような働きをすると想像できる。
酸化グラフェンを用いた組織再生例は,心筋,神経,骨格筋,骨,軟骨,皮膚と多岐にわたって報告されているが,ここでは歯周病に関連の深い骨の再生例を一部紹介する。Wuらは骨補填材として広く用いられているβ-三リン酸カルシウム(β-TCP)に酸化グラフェンを添加して骨増生試験を行っており,ウサギ頭蓋骨にトレフィンバーで骨欠損を作製して試料を埋植し4,8週間観察した。その結果,β-TCP-酸化グラフェン複合体はβ-TCP単独に比較して新生骨量が8週で約1.5倍増加したことを報告している21)。またインプラントを想定してチタン表面を酸化グラフェンでコーティングし,骨誘導タンパク(bone morphogenetic protein-2,BMP-2)を吸着させてマウス頭蓋骨に移植することで,新生骨形成の増強とともに強固な骨結合が得られている22,23)。キトサンと酸化グラフェン,BMP-2,銀ナノ粒子の複合化スキャフォールドも開発されており,良好な生体適合性と骨髄間質細胞の増殖および分化増強,ならびに骨誘導効果が発揮されている24)。
我々もコラーゲン-酸化グラフェンスキャフォールドの足場としての有効性と組織構築効果を見るために,ラット生体内への埋植実験を行った15,25)。その結果,酸化グラフェンの添加はスキャフォールド内部への細胞増殖(イングロース)を著しく上昇した(DNA量にて1.4倍)。そこで細胞挙動を詳細に検討するために免疫組織学的に調査したところ,酸化グラフェンの配合は線維芽細胞や血管関連細胞の著しいイングロースを促した。さらに特徴的なことにコントロールのコラーゲンスポンジではED-1陽性の炎症性マクロファージ(M1マクロファージ)が発現したが,酸化グラフェンスキャフォールドではM1マクロファージに加えてED-2陽性の組織修復型マクロファージ(M2マクロファージ)の発現を認めた(図3)26)。このことから酸化グラフェンの効果には次のような仮説が考えられる。まず酸化グラフェンは生体内で血漿等から選択的にグロースファクターを含む生理活性物質やコラーゲン等の生体線維を吸着凝集する。また酸化グラフェンそのものが異物として認識されマクロファージを誘導してリモデリングが開始される。その結果,多くのシグナル因子によって細胞のスキャフォールド内部への遊走増殖が促進され,スキャフォールドを足場にして細胞外マトリクスを分泌,また同時に血管網の構築が起こり自己組織化するというものである。その際に,組織修復型マクロファージ発現による免疫反応の抑制が,組織再構築に重要な役割を果たしているものと思われる。我々はさらに酸化グラフェンスキャフォールドの埋植が,抜歯窩治癒26),歯周組織再生27)を促進することを明らかにした(図4)。これは将来,歯周組織再生療法において酸化グラフェンを応用できる可能性を示唆するものである。
ナノカーボンの中には発がん性が懸念される材料もあるが,酸化グラフェンは以前より安全性が報告され生体親和性の良い材料として広く認識されている。低濃度の酸化グラフェンをラットへ投与した場合に,細胞死などの傷害を引き起こさないこと28),酸化グラフェンをラットに静脈注射で投与して,血液生化学データの異常や臓器の明らかな損傷は認められず,肝臓・脾臓に蓄積後排泄されたことが報告されている29)。しかしヒト生体内へ長期的に留置されることを前提とした場合には,安全性の評価,生体内動態の検討は引き続き行われるべきである。

(A)肉眼所見,(B)断面のSEM像,(C)表面のSEM像。酸化グラフェンの皺構造(矢印)が観察された。文献26から引用改変。
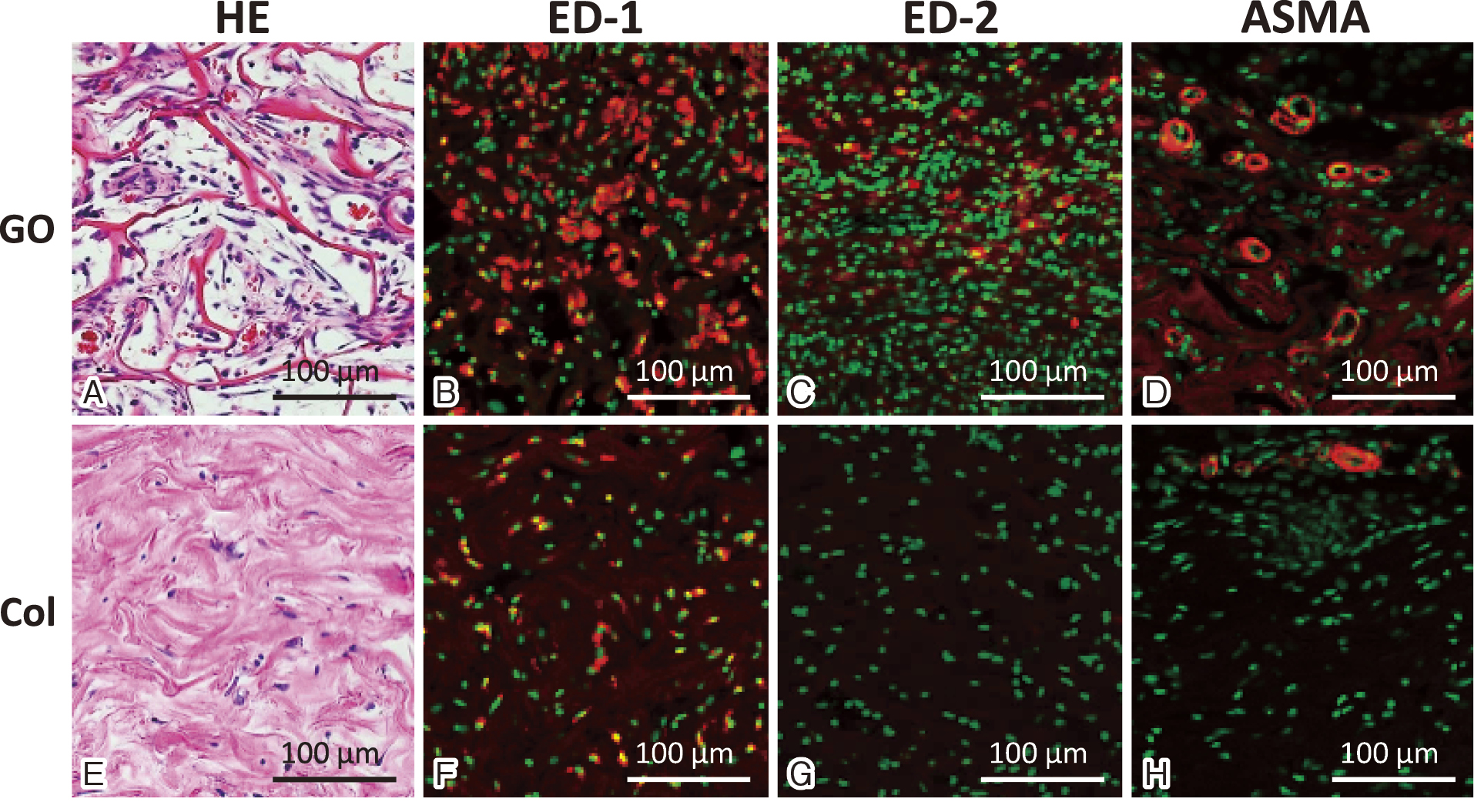
(A-D)酸化グラフェンスキャフォールド,(E-H)コラーゲンスポンジ,(A, E)HE(ヘマトキシリンエオシン)染色,(B, F)ED-1(mouse anti-CD68)染色,(C, G)ED-2(mouse anti-CD163)染色,(D, H)ASMA(mouse anti-α-smooth muscle actin)染色。酸化グラフェンスキャフォールド内部に赤色の蛍光を発するM1,M2マクロファージ,血管平滑筋細胞が多く観察された。文献26から引用改変。
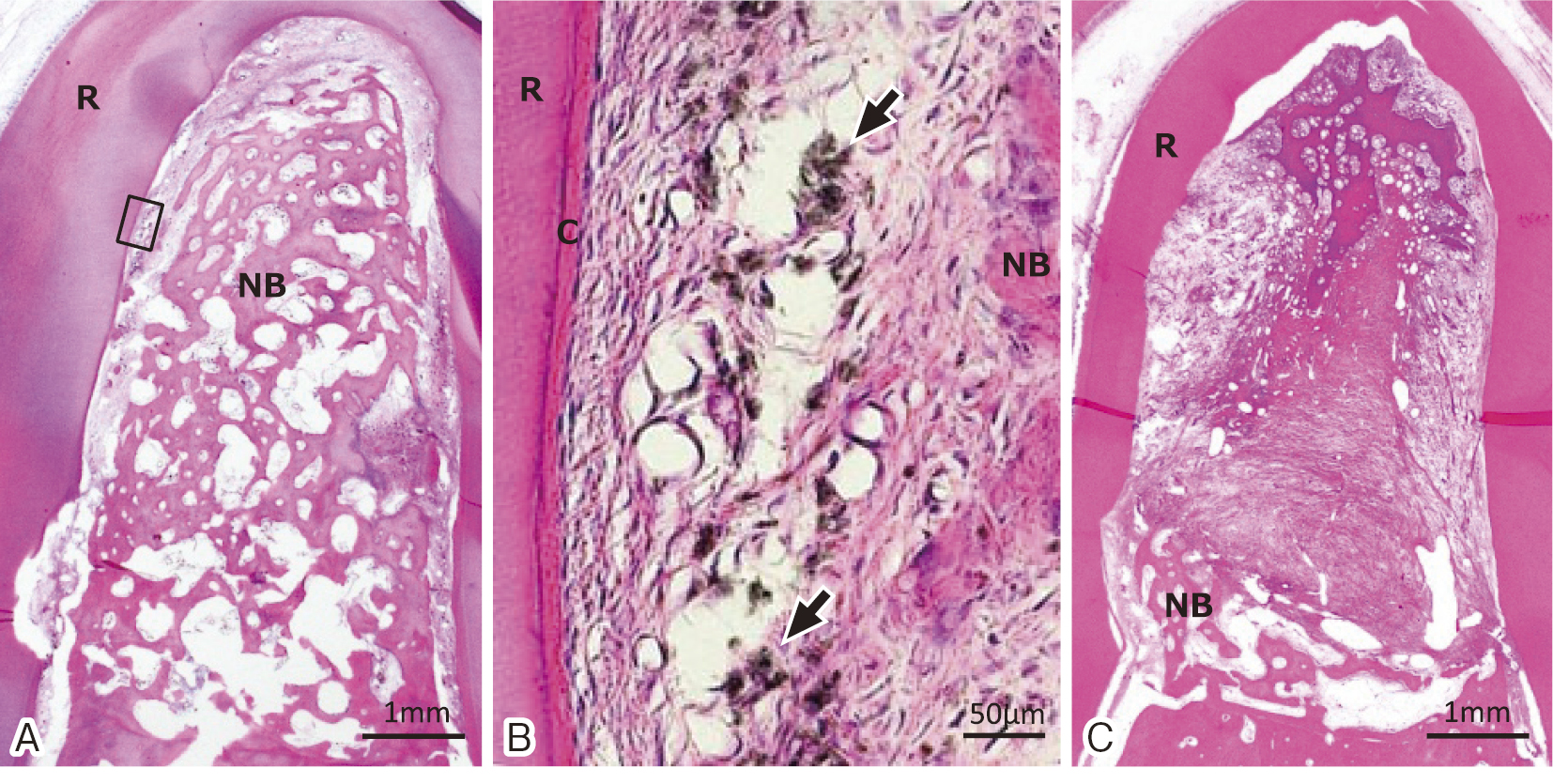
(A)酸化グラフェンスキャフォールド埋入後の組織像。良好な歯槽骨新生を認めた。(B)Aの歯根表面の強拡大像。歯根膜様組織と凝集した酸化グラフェン(矢印)が観察された。(C)コラーゲンスポンジ埋入後の組織像。上皮や結合組織が多く,新生骨はわずかだった。R:歯根,NB;新生骨,C;セメント質。文献27から引用改変。
酸化グラフェンという素材の魅力の一つに,細胞活性向上効果と同時に抗菌性を保有していることが挙げられる。抗菌性は酸化グラフェンの量,濃度に依存すると考えられ,特に高濃度の使用によって効果が強く発揮されるようである。酸化グラフェンの抗菌性は表面酸素官能基からの活性酸素の発生30)と考えられているが,他にもユニークな抗菌効果の報告がある。例えば酸化グラフェンのシートのエッジによる直接接触で細菌の細胞膜損傷がおきるとの報告や31),酸化グラフェンシートが細菌を直接ラップすることで増殖できなくなり,細菌が不活化するといったものである32,33)。Huらは酸化グラフェンナノシートが抗菌性を発揮するものの,細胞毒性は最小限であったと報告しており34),2015年に酸化グラフェンナノシートが齲蝕,歯周病原菌のS. mutans,F. nucleatum,P. gingivalisの細胞膜を損傷させ,抗菌性を発揮することが示されている35)。したがって新しい歯周病治療法として酸化グラフェンを応用できる可能性がある。我々も,ヒト象牙質ブロック表面に酸化グラフェンを局在させ,抗菌性歯面を獲得することに成功した36)。S.mutansは酸化グラフェン処理歯面上で付着増殖が抑制され(図5),これはA. actinomycetemcomitansを用いた試験においても同様であった。また,ラット臼歯に窩洞を形成し,酸化グラフェン分散液の塗布を行った歯面において,プラークの付着が長期的に抑制された。したがって歯周病治療のほか,う蝕予防等を含めオーラルケア製品として開発できる可能性もある。
また酸化グラフェンは長波長光を吸収して発熱すること,単波長光によってフリーラジカルを産生することができるので,光線力学療法への使用が検討されている。図6は酸化グラフェンフィルム上にS.mutansを播種後,赤外線を1秒間照射した実験であり,細菌を短時間で死滅することに成功した。歯周病や歯内療法における光殺菌療法の一つに成り得るであろう。また,酸化グラフェンに抗がん剤を結合させるドラッグデリバリーシステムの開発も行われている37,38)。これはがん病巣へ酸化グラフェンを輸送後に赤外線やマイクロウェーブを照射して抗がん剤を切り離し,がん病巣を攻撃するという新しいコンセプトの治療法である。

(A)酸化グラフェン処理象牙質のSEM像。S.mutansがわずかに観察された。(B)コントロール(処理無し)。S.mutansの増殖を認めた。文献36から引用改変。
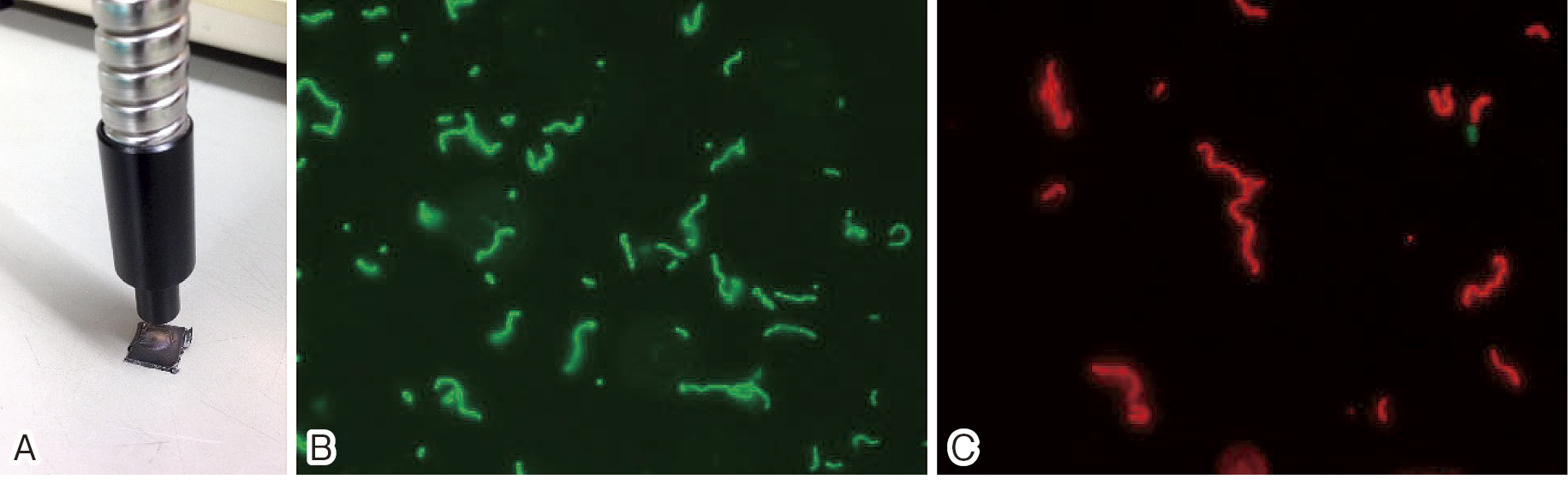
(A)赤外線照射によって酸化グラフェンは発熱し還元される。(B, C)LIVE/DEAD染色。酸化グラフェン被膜上に播種されたS.mutansは生菌(緑色蛍光)であるが(B),1秒間の赤外線照射後はほぼ死滅(赤色蛍光)した(C)。
酸化グラフェンは,安全性も高く大量生産が可能なカーボンナノシート材料であり,酸素官能基の存在による細胞増殖効果,ドラッグデリバリーシステム,抗菌効果など様々な機能を有し,医用材料として無限の可能性がある新素材である。研究報告は近年になって爆発的に増加し,これまでに見られなかった新たな特性や利用方法が提唱され,酸化グラフェン療法の効果や体内動態のエビデンスも構築されつつある。歯周病のみならず歯内療法,う蝕抑制等に応用できる可能性があり,近い将来,歯科において酸化グラフェンによるイノベーションが起こることを強く期待している。
今回の論文に関連して,開示すべき利益相反状態はありません。