1. 歯周炎と心臓血管疾患との関わり
歯周炎と心臓血管疾患との関わりについては既に数多くの報告がなされており,その多くは歯周炎が心臓血管疾患のリスク因子であることを示唆している。しかしながら歯周炎が心臓血管疾患に与える分子機構は十分に明らかとなっていない1,2)。
歯周炎が心臓血管疾患に与える影響としては,大動脈瘤などの血管病変から歯周病原細菌が検出されたことから,歯周病原細菌が菌血症によって全身に運ばれて血管への感染などを引き起こす直接作用が考えられる。しかし動脈硬化を有する歯周炎患者では血清中の炎症性サイトカイン濃度が高かったことや,P. gingivalisの熱ショック蛋白が宿主の熱ショック蛋白と相同性を持つために,宿主と細菌の両方に反応する自己反応性のT細胞が動脈硬化病変部に浸潤していたこと3)などから,歯周病原細菌に対する免疫反応が心臓血管疾患を引き起こす間接作用にも注目が集まっている。
口腔から始まる消化管では咀嚼・嚥下された食物がさらに消化液や常在細菌によって処理されたのちに体内に吸収される。消化管は内腔におびただしい数の常在菌と共存する中で,本来は異物である食物を体内に取り入れる必要があるため,特殊な免疫系が存在する。血液中の抗体はIgGが主であるのに対し粘膜表面はIgA抗体で覆われ,さらに粘膜面を守る免疫細胞は常在細菌と共存していることが以前より知られていたが4),最近になって脂質や糖代謝にも消化管免疫が重要であることが明らかとなってきた5)。
肉や卵など欧米型の食事を過剰に摂取することで心臓血管疾患のリスクが上昇することは良く知られているが,脂質・糖代謝異常は食事,常在細菌および免疫機構のバランスが崩れることで引き起こされる可能性が示唆されている6)。本稿ではリン脂質に関係する歯周病の細菌・免疫応答に着目し,リン脂質に対する免疫応答を介した歯周炎と心臓血管疾患の関係について考察を加える。
2. B細胞が心臓血管疾患と歯周病に与える影響
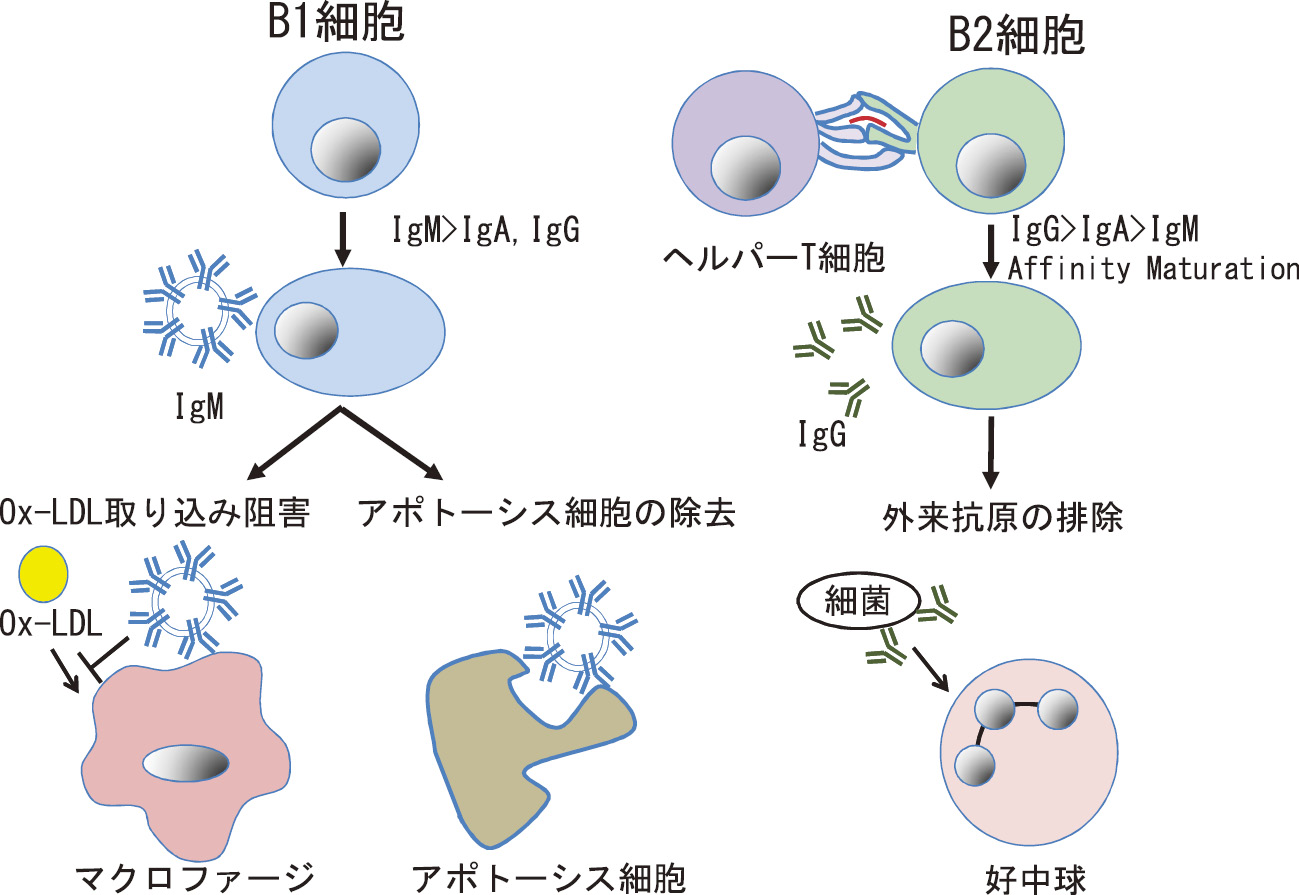
B細胞は抗体産生細胞(形質細胞)へと分化し,様々な抗体を産生する。B細胞は反応する抗原や分化経路が異なるB1細胞とB2細胞に大別される。B1細胞は胎生期の肝臓で造血幹細胞から分化して抹消に分布し,自己複製して維持される。B1細胞のうち細胞表面にCD5分子を発現するものはCD5+B細胞(B1a細胞)細胞,CD5の発現の無いものはB1b細胞として区別されている。B1細胞はヘルパーT細胞の助けを借りることなく主としてIgM形質細胞に分化する。消化管ではIgA抗体へのクラススイッチも行われ,分泌型IgA抗体産生の一部を担っている。関節リウマチや7)シェーグレン症候群8)などの自己免疫疾患でCD5+B細胞が増加することが報告されたため,CD5+B細胞(B1a細胞)は自己抗体を産生する特殊なB細胞と考えられていた。しかし現在ではB1細胞は自然抗体を産生するB細胞であり,自己免疫疾患に特有なB細胞ではないことが明らかとなっている。B1細胞はPhosphoryl choline(ChoP)や酸化LDLコレステロール(oxidized low density lipoprotein:Ox-LDL)など酸化に特異的なエピトープを抗原としてIgM抗体を産生する。B1細胞によって産生されたIgM抗体は,Ox-LDLに結合してマクロファージによるOx-LDLの取り込みを阻害する。またIgM抗体はアポトーシス細胞にも結合して細胞除去を促進する(図1)9)。
B2細胞は血中やリンパ節にみられる通常のB細胞(conventional B cell)で,常に骨髄幹細胞から供給されている。B2細胞は血液を介して運ばれた細菌などの外来抗原に対して迅速に反応し,ヘルパーT細胞の補助の下でIgG,IgA,IgE抗体などにクラススイッチを行うとともに抗原との親和性を増強する(Affinity maturation)。産生された抗体は毒素の中和や細菌のオプソニン化などによって外来抗原に対する感染防御を行う(図1)9)。
B細胞が心臓血管疾患に与える影響はB1細胞とB2細胞で異なることが報告されている9,10)。B1細胞が産生するIgM抗体はマクロファージによるOx-LDL取り込みを阻害し,アポトーシス細胞の処理を促進するなど,動脈硬化を抑制する。またヒトのB1細胞の分化に関係するInhibitor of differentiation 3(Id3)の1塩基多型でRS11574がAAの人はB1細胞の数が多く,かつ動脈硬化のリスクが低いことが報告されている11)。これらのことからB1細胞は動脈硬化を抑制し,心臓血管疾患から守る働きがあることが明らかとなっている。これに対してB2細胞はOx-LDLに対するIgG抗体を産生し,動脈硬化を促進する可能性が示唆されているが,異なる報告もあり,見解は一致していない10)。ゲノムワイド関連解析のデータを応用してシステム生物学的に冠動脈疾患と脂質代謝異常に関わる遺伝子を検討した報告では,B細胞に関係する遺伝子の異常が心臓血管疾患に関わることを報告している12)。B細胞が心臓血管疾患に与える影響について,今後は分子レベルの詳細な解析が期待される。
歯周病においても歯周炎患者と歯周組織が健康な人との間でB1細胞に違いがあるか検討されてきた13-20)(表1)。歯周炎患者では炎症歯肉や末梢血でB1a細胞が増加しており13-17),さらにB1a細胞が多い歯周組織では歯周炎が重度であることも報告されている16,21)。これらの報告から,歯周炎ではB1細胞が活性化することで自己抗体が産生され,歯周組織の破壊に関与していることが示唆されているが21),B1細胞が自己免疫による組織破壊を起こすと考えることには否定的な見解も存在する22)。
歯周炎局所で産生される抗体の主要なアイソタイプはIgGであり,その中のB1細胞とB2細胞の割合は不明である。歯周炎におけるB1細胞の働きを明らかにするためには,B1細胞が自己抗原と外来抗原(細菌など)のどちらに反応して歯周炎局所に集積しているのか,クラススイッチやaffinity maturationを経てIgG抗体を産生するのか,などについて更に検討する必要があると思われる。
3. リン脂質代謝が心臓血管疾患と歯周病に与える影響
3年以内に心臓血管イベント(死亡,心筋梗塞,脳梗塞)の既往があった50人とコントロール50人の血液を用いてメタボロミクス解析を行った研究では,phosphatidylcholine(PC)とその代謝物であるtrimethylamine(TMA),trimethylamine-N-oxide(TMAO)が,イベントがみられた患者に多い分子として同定された23)。マウスにPCを投与して動脈硬化を調べた結果,腸内細菌によるPCの分解で生じたTMAOがマクロファージに働いて動脈硬化を促進することが明らかとなった23)。
さらに同じグループは,ゆで卵を健常者40人に経口摂取させてPCの代謝産物の血中濃度を測定し,PCの摂取によってTMAOの血中濃度が増加すること,抗生物質で腸内細菌を抑制した場合にはこの上昇がみられないことを見出した24)。さらに彼らは冠動脈造影を行っている4000人の患者の3年間の経過を調査し,血液中にTMAOの上昇が見られた患者では心血管イベントを起こすリスクが有意に高いことを明らかにした24)。これらのことから,食物中のPCから腸内細菌によって代謝されてTMAが生じ,TMAは腸で吸収された後に肝臓でTMAOへと代謝されて動脈硬化をひきおこして心臓血管イベントのリスクを高めることが明らかとなっている(図2)。
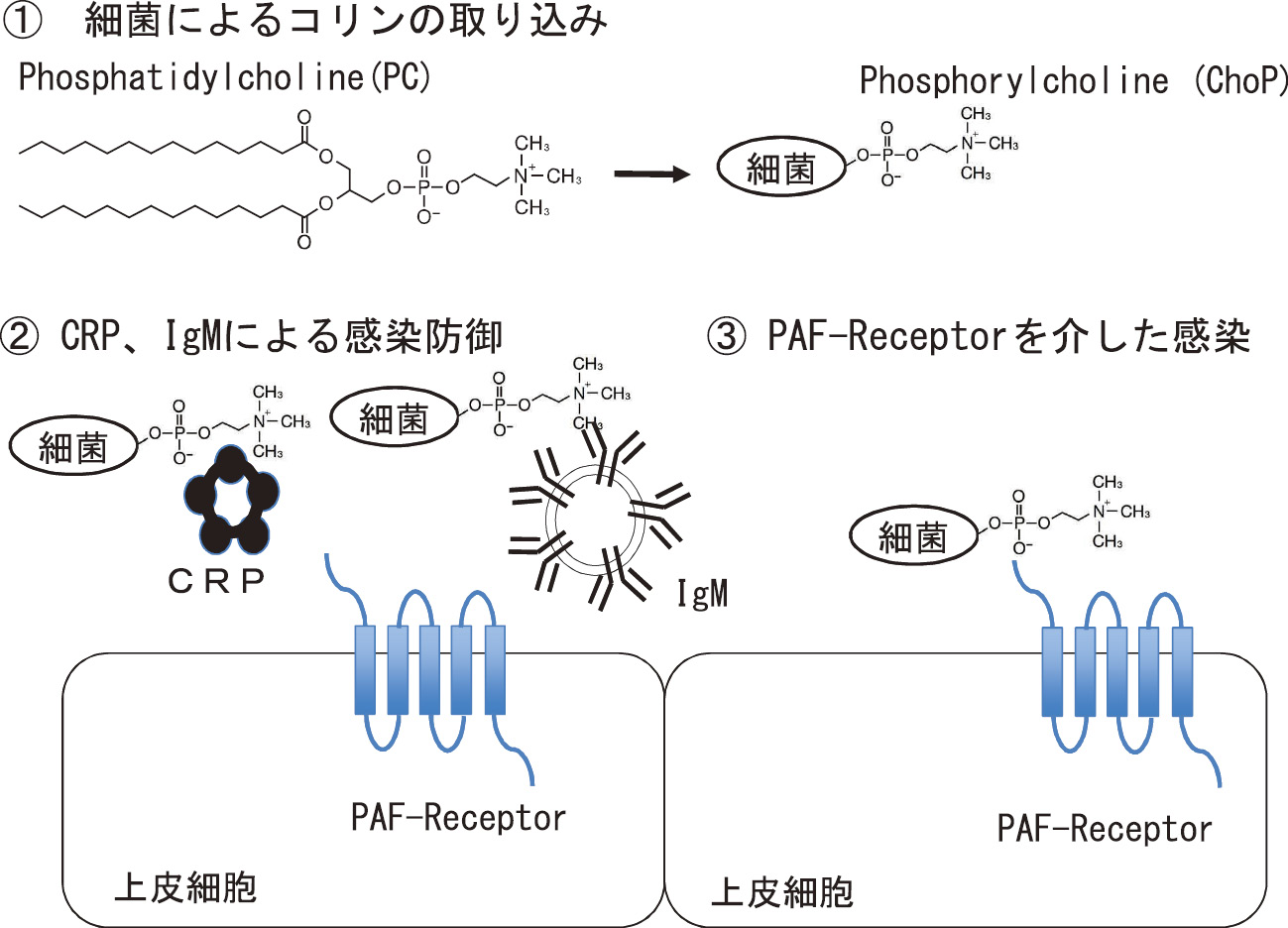
PC代謝を細菌の側から考察すると,細菌はコリンを自ら合成できないため宿主から取り入れている。細菌はコリンを取り入れた後にphosphorylcholine(ChoP)としてリポ多糖や莢膜多糖の一部とするため25),ChoPを細胞表面に持つ細菌は多い。ヒトのCRPは細菌のChoPに結合して補体を活性化して殺菌を行う。ChoPに対するIgM抗体も細菌の排除に働く。ChoPはヒトのPlatelet-activating factor receptor(PAF-R)にも結合するため,排除を免れた細菌はPAF-Rを介して上皮や血管内皮細胞に感染する(図3)。典型例としてH. influenzaeのChoPにCRPが結合すると補体が活性化して貪食・殺菌されるが25),攻撃をのがれたH. influenzaeはChoPとPAF-Rとの結合を介して鼻腔・咽頭に定着する26)。歯周病原細菌でもA. actinomycetemcomitans(Aa)はPAF-Rを介して血管内皮細胞に感染することが報告されている27)。
ChoPを有する細菌は口腔内のプラーク細菌の中にも数多く存在する28,29)。歯周炎患者の歯肉縁下プラークあるいはAa,F. nucleatum,A. israelii,S mitis,S. oralisといった細菌をマウスに免疫して作られる抗体を調べた研究では,多くの菌と交差反応性を有するIgMクラスのモノクローナル抗体が得られたことを報告している28)。これらのモノクローナル抗体が認識していたのは細菌上のChoPであったことから,ChoPはプラーク細菌の持つ主要な抗原の一つであり,ChoPに対する抗体は多くのプラーク細菌に結合することが明らかとなった28)。
歯周炎患者と歯周組織が健康な被験者の血清中の抗ChoP抗体を調べた研究では,歯周炎患者でChoPに対する血清抗体が上昇することが報告されている15,29)。米国歯周病学会のposition paperではAaに対する血清抗体が高いほど歯周炎が軽度であり,抗体が歯周組織を防御する役割を担うと考えている30)。Aaに対する血清抗体にはChoPに対する抗体も含まれており,このChoPに対する抗体も防御的に働くことが報告されている31)。また歯周炎患者におけるChoPや常在細菌に対する血清抗体を調べた研究では,歯周炎患者でChoPに対する抗体価が上昇するのと同時に腸内細菌に対する抗体価も上昇していたことから,ChoPに対する抗体は様々な常在細菌の共通抗原に対する抗体として防御的な役割を果たしている可能性が示唆されている15)。
ChoP,PCおよび酸化LDLなどは酸化に特異的な共通のエピトープを有しており,自然抗体はこのエピトープに結合する32)。この自然抗体は主としてIgMクラスであり,酸化LDLに結合してマクロファージによる酸化LDLの取り込みを抑制,アポトーシス細胞のPCに結合してマクロファージによる処理を促進するなど動脈硬化を抑制する働きがある(図1)。酸化に特異的なエピトープに対するIgM抗体が高い人では動脈硬化が軽度であることが明らかとなっているが,IgG抗体が動脈硬化を抑制するか促進するかについては報告が一致していない10)。
4. 歯周炎による抗リン脂質抗体の上昇が心臓血管疾患に与える影響
抗リン脂質抗体症候群(Antiphosphilipid syndrome:APS)はリン脂質に対する自己抗体が産生されて脳梗塞など全身の血管の血栓や習慣性流産がみられる疾患であり,基礎疾患を持たない原発性と全身エリテマトーデスなどの自己免疫疾患を伴う続発性に分けられる33)。APSの患者の血液からは抗カルジオリピン抗体や抗β2glycoprotein I抗体,ループスアンチコアグラントなどが検出されるが,全身的に健康な人の1~5%の人からも抗カルジオリピン抗体が検出されることが知られている33)。臨床基準の1項目以上が存在し,血液検査項目の1項目以上が陽性であった場合,APSと診断されるが,APSの発症頻度はおおむね10万人に40~50人とされている34)。また脳卒中の13%,心筋梗塞の11%,深部静脈血栓の9.5%,習慣流産の6%から抗リン脂質抗体が検出される34)。歯周炎が全身に与える影響として,心臓血管疾患や早期低体重児出産との関係が報告されていることから,歯周炎と抗リン脂質抗体の関係が注目されるようになった。
歯周炎と抗リン脂質抗体との関係を検討した研究では,歯周組織が健康な人と比較して歯周炎患者で抗カルジオリピン抗体が上昇していることが報告されている35,36)。また抗カルジオリピン抗体が上昇している広範型侵襲性歯周炎患者では血液中のsICAM-1,sVCAM-1などの可溶型接着分子も高値であった37)。バージャー病患者38),SLE患者39)では抗カルジオリピン抗体の上昇がみられるとともに,カルジオリピン抗体と歯周炎の臨床症状の間に相関が認められた。また歯周基本治療によって抗カルジオリピン抗体価が有意に低下したことから40,41),歯周治療によって抗リン脂質抗体が低下する可能性が示唆される(表2)。
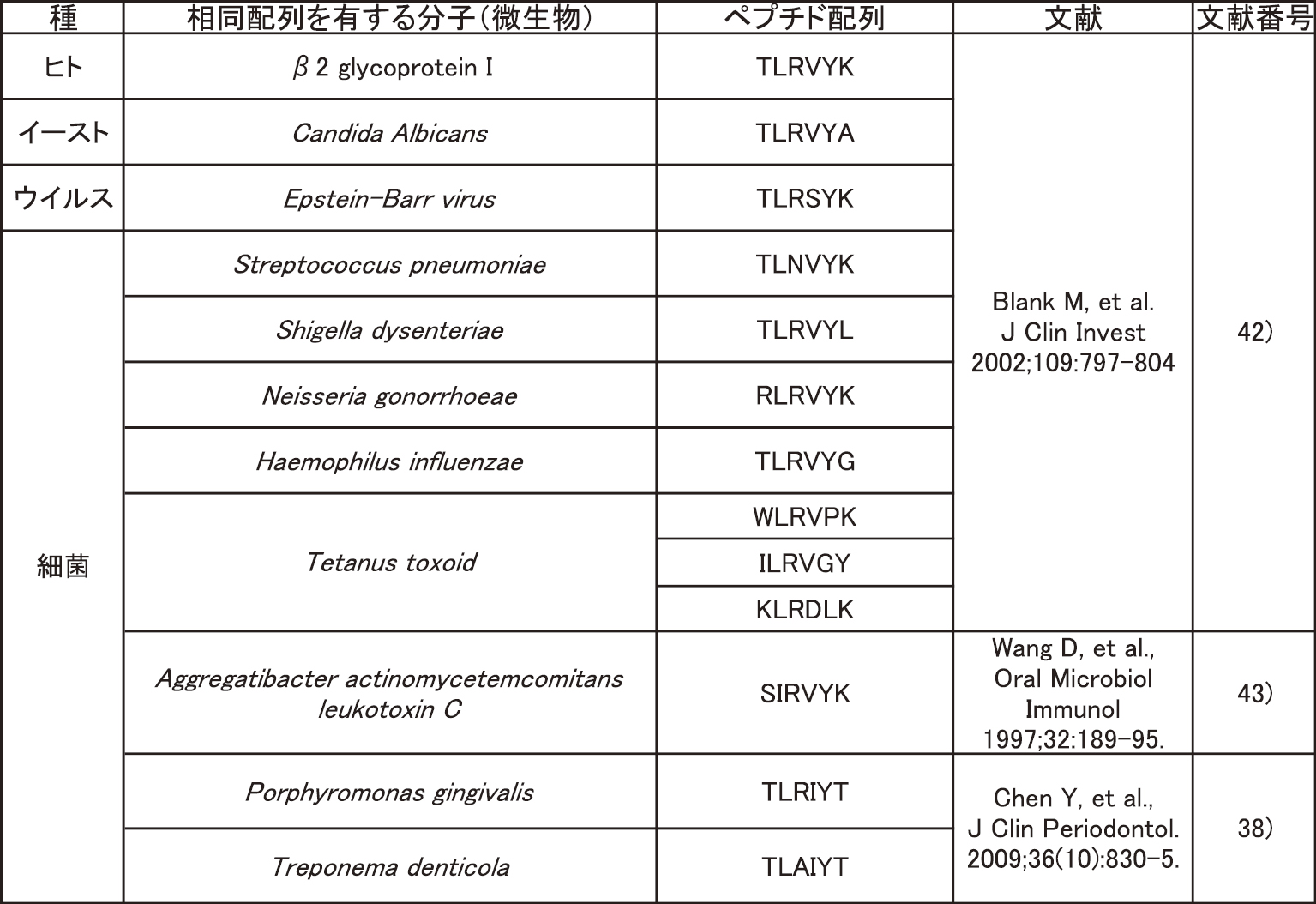
抗リン脂質抗体症候群の原因は未だ明らかになっていないが,原因のひとつとして微生物の感染が分子相動性によって自己抗体を誘導することが示唆されている。抗リン脂質抗体症候群を引き起こすモノクローナル抗体を調べた研究では,そのモノクローナル抗体が結合する部位がβ2glycoprotein I分子の配列の一部であるTLRVYKペプチドであった。様々な細菌の蛋白がこのペプチドと相同配列を有しており,それらの細菌をマウスに免疫して血清抗体を精製し,別のマウスに投与すると抗リン脂質抗体症候群が発症した42)。このことから宿主のβ2glycoprotein I分子と分子相動性を有する微生物が感染すると,その相同部位に対して作られた抗体が抗β2glycoprotein I抗体として抗リン脂質抗体症候群を引き起こす可能性が示唆された。
歯周病においてもβ2glycoprotein I上のペプチドであるTLRVYKと相同ペプチドを有する細菌の感染はβ2glycoprotein Iに反応する抗体を誘導する可能性がある(表3)。実際にAaに感染した歯周炎患者ではSIRVYKペプチドに対するIgG抗体価が上昇しており,またSIRVYKに対するIgG抗体価はTLRVYKに対する抗体価と有意な正の相関を示したことが報告され,歯周炎によってTLRVYKと分子相動性を有する細菌によってTLRVYKと交差反応性を有する抗体が誘導されることが明らかとなった43)。バージャー病38)や切迫早産44)においても歯周炎患者におけるTLRVYKの相同ペプチドに対するIgG抗体の上昇が報告されている。このシステムを応用してP. ginigivalis,TLR-4,およびβ2glycoprotein Iの相同ペプチドとしてPDDLPFST配列が報告され,P. gingivalisの感染によって産生された抗体がβ2glycoprotein Iに結合するだけでなく,TLR4を刺激して炎症を拡大するという報告もなされている45)。相同ペプチドに対するIgG抗体の測定は細菌感染による自己抗体の検出方法としてこれからも応用が期待される43)。しかし抗リン脂質抗体症候群でみられる自己抗体の主体はペプチド配列を認識する抗体ではなく,たんぱく質の3次構造を認識している抗体が主体であると考えられており,さらに詳細な検討が必要である。
5. リン脂質に対する免疫応答の制御
これまでの結果から以下の3点が明らかとなっている。(1)血栓や早産の原因となる抗リン脂質抗体は歯周炎患者で上昇していた。(2)抗リン脂質抗体の標的分子であるβ2glycoprotein Iは歯周病原細菌と分子相動性を有するため,歯周病現細菌の感染によってβ2glycoprotein Iに対する抗体産生がみられた。(3)歯周炎患者で上昇した抗リン脂質抗体は歯周治療によって低下した。これらのことからリン脂質に対する免疫応答は,歯周炎が心臓血管疾患のリスクを増加させる一因であると思われる。
Taiwaneese National Health Insuranceの51万人の歯周炎患者と20万人の歯周炎でない患者のデータに基づき,2000年から2010年までの脳梗塞発症を調べた後ろ向き研究では,歯周炎患者で歯周治療を受けなかった人の脳梗塞発症率は年間0.48%,歯周治療を受けた人で年間0.39%,定期的な口腔清掃を受けた人で年間0.14%,歯周炎の無かった人で年間0.32%であった。また歯周治療による脳梗塞発症率の低下は若年者ほど顕著であった46)。歯周治療は将来の脳梗塞発症を減少させる効果があり,特に若年者でその効果が高いことが期待される。脳梗塞は発症によって歯科治療そのものが非常に困難になる事から,リスクが高い患者に対しては発症前に十分な歯科治療を行うことが求められる。SLEや抗リン脂質抗体症候群は若年期に脳梗塞リスクが高く,最も厳密な歯周治療が必要である。
リン脂質に対する免疫応答は健常者でも認められる。腸内細菌は食事によって摂取されたリン脂質からTMAを産生し,腸から吸収されて宿主の動脈硬化を促進する。健康な腸内細菌は食事の多様性に依存することが明らかとなっている47)。腸内細菌の診断に基づいて個人に合わせて適切な食事を処方することも可能となってきた48)。歯科治療は咀嚼機能を改善することが可能であり,食生活の改善を通じてリン脂質に対する免疫応答をコントロールできる可能性がある。今後さらに知見が集積することによって新しい診断・治療へと発展することが期待される。
利益相反
今回の論文に関連して,開示すべき利益相反状態はありません。
References
- 1) Leira Y, Seoane J, Blanco M, Rodriguez-Yanez M, Takkouche B, Blanco J, Castillo J: Association between periodontitis and ischemic stroke: a systematic review and meta-analysis. Eur J Epidemiol, 2016 [Epub ahead of print].
- 2) Lockhart PB, Bolger AF, Papapanou PN, Osinbowale O, Trevisan M, Levison ME, Taubert KA, Newburger JW, Gornik HL, Gewitz MH, Wilson WR, Smith SC Jr, Baddour LM: Periodontal disease and atherosclerotic vascular disease: does the evidence support an independent association?: a scientific statement from the American Heart Association. Circulation, 125: 2520-2544, 2012.
- 3) Yamazaki K, Ohsawa Y, Itoh H, Ueki K, Tabeta K, Oda T, Nakajima T, Yoshie H, Saito S, Oguma F, Kodama M, Aizawa Y, Seymour GJ: T-cell clonality to Porphyromonas gingivalis and human heat shock protein 60s in patients with atherosclerosis and periodontitis. Oral Microbiol Immunol, 19: 160-167, 2004.
- 4) 長澤 敏行, 佐野 公仁夫, 多田 富雄: 免疫細胞分化の場としての消化管. 細胞工学, 9: 795-801, 1990.
- 5) Everard A, Cani PD: Diabetes, obesity and gut microbiota. Best practice & research Clinical gastroenterology, 27: 73-83, 2013.
- 6) Yamashita T, Kasahara K, Emoto T, Matsumoto T, Mizoguchi T, Kitano N, Sasaki N, Hirata K: Intestinal Immunity and Gut Microbiota as Therapeutic Targets for Preventing Atherosclerotic Cardiovascular Diseases. Circulation journal: official journal of the Japanese Circulation Society, 79: 1882-1890, 2015.
- 7) Burastero SE, Casali P, Wilder RL, Notkins AL: Monoreactive high affinity and polyreactive low affinity rheumatoid factors are produced by CD5+ B cells from patients with rheumatoid arthritis. The Journal of experimental medicine, 168: 1979-1992, 1988.
- 8) Dauphinee M, Tovar Z, Talal N: B cells expressing CD5 are increased in Sjogren's syndrome. Arthritis and rheumatism, 31: 642-647, 1988.
- 9) Tsiantoulas D, Sage AP, Mallat Z, Binder CJ: Targeting B cells in atherosclerosis: closing the gap from bench to bedside. Arteriosclerosis, thrombosis, and vascular biology, 35: 296-302, 2015.
- 10) Ait-Oufella H, Sage AP, Mallat Z, Tedgui A: Adaptive (T and B cells) immunity and control by dendritic cells in atherosclerosis. Circulation research, 114: 1640-1660, 2014.
- 11) Rosenfeld SM, Perry HM, Gonen A, Prohaska TA, Srikakulapu P, Grewal S, Das D, McSkimming C, Taylor AM, Tsimikas S, Bender TP, Witztum JL, McNamara CA: B-1b Cells Secrete Atheroprotective IgM and Attenuate Atherosclerosis. Circulation research, 117: e28-39, 2015.
- 12) Huan T, Zhang B, Wang Z, Joehanes R, Zhu J, Johnson AD, Ying S, Munson PJ, Raghavachari N, Wang R, Liu P, Courchesne P, Hwang SJ, Assimes TL, McPherson R, Samani NJ, Schunkert H, Coronary AGwR, Meta-analysis Consortium ICfBPG, Meng Q, Suver C, O'Donnell CJ, Derry J, Yang X, Levy D: A systems biology framework identifies molecular underpinnings of coronary heart disease. Arteriosclerosis, thrombosis, and vascular biology, 33: 1427-1434, 2013.
- 13) Afar B, Engel D, Clark EA: Activated lymphocyte subsets in adult periodontitis. J Periodontal Res, 27: 126-133, 1992.
- 14) Sugawara M, Yamashita K, Yoshie H, Hara K: Detection of, and anti-collagen antibody produced by, CD5-positive B cells in inflamed gingival tissues. J Periodontal Res, 27: 489-498, 1992.
- 15) Aramaki M, Nagasawa T, Koseki T, Ishikawa I: Presence of activated B-1 cells in chronic inflamed gingival tissue. J Clin Immunol, 18: 421-429, 1998.
- 16) Berglundh T, Liljenberg B, Tarkowski A, Lindhe J: Local and systemic TCR V gene expression in advanced periodontal disease. J Clin Periodontol, 25: 125-133, 1998.
- 17) Berglundh T, Liljenberg B, Tarkowski A, Lindhe J: The presence of local and circulating autoreactive B cells in patients with advanced periodontitis. J Clin Periodontol, 29: 281-286, 2002.
- 18) Donati M, Liljenberg B, Zitzmann NU, Berglundh T: B-1a cells in experimental gingivitis in humans. J Periodontol, 80: 1141-1145, 2009.
- 19) Donati M, Liljenberg B, Zitzmann NU, Berglundh T: B-1a cells and plasma cells in periodontitis lesions. J Periodontal Res, 44: 683-688, 2009.
- 20) Thorbert-Mros S, Larsson L, Berglundh T: Cellular composition of long-standing gingivitis and periodontitis lesions. J Periodontal Res, 50: 535-543, 2015.
- 21) Berglundh T, Donati M, Zitzmann N: B cells in periodontitis: friends or enemies? Periodontology 2000, 45: 51-66, 2007.
- 22) Ishikawa I, Nakashima K, Koseki T, Nagasawa T, Watanabe H, Arakawa S, Nitta H, Nishihara T: Induction of the immune response to periodontopathic bacteria and its role in the pathogenesis of periodontitis. Periodontology 2000, 14: 79-111, 1997.
- 23) Wang Z, Klipfell E, Bennett BJ, Koeth R, Levison BS, Dugar B, Feldstein AE, Britt EB, Fu X, Chung YM, Wu Y, Schauer P, Smith JD, Allayee H, Tang WH, DiDonato JA, Lusis AJ, Hazen SL: Gut flora metabolism of phosphatidylcholine promotes cardiovascular disease. Nature, 472: 57-63, 2011.
- 24) Tang WH, Wang Z, Levison BS, Koeth RA, Britt EB, Fu X, Wu Y, Hazen SL: Intestinal microbial metabolism of phosphatidylcholine and cardiovascular risk. The New England journal of medicine, 368: 1575-1584, 2013.
- 25) Young NM, Foote SJ, Wakarchuk WW: Review of phosphocholine substituents on bacterial pathogen glycans: synthesis, structures and interactions with host proteins. Molecular immunology, 56: 563-573, 2013.
- 26) Cundell DR, Gerard NP, Gerard C, Idanpaan-Heikkila I, Tuomanen EI: Streptococcus pneumoniae anchor to activated human cells by the receptor for platelet-activating factor. Nature, 377: 435-438, 1995.
- 27) Schenkein HA, Barbour SE, Berry CR, Kipps B, Tew JG: Invasion of human vascular endothelial cells by Actinobacillus actinomycetemcomitans via the receptor for platelet-activating factor. Infection and immunity, 68: 5416-5419, 2000.
- 28) Gmur R, Thurnheer T, Guggenheim B: Dominant cross-reactive antibodies generated during the response to a variety of oral bacterial species detect phosphorylcholine. Journal of dental research, 78: 77-85, 1999.
- 29) Schenkein HA, Gunsolley JC, Best AM, Harrison MT, Hahn CL, Wu J, Tew JG: Antiphosphorylcholine antibody levels are elevated in humans with periodontal diseases. Infection and immunity, 67: 4814-4818, 1999.
- 30) Califano JV; Research, Science and Therapy Committee American Academy of Periodontology: Position paper: periodontal diseases of children and adolescents. J Periodontol, 74: 1696-1704, 2003.
- 31) Purkall D, Tew JG, Schenkein HA: Opsonization of Actinobacillus actinomycetemcomitans by immunoglobulin G antibody reactive with phosphorylcholine. Infection and immunity, 70: 6485-6488, 2002.
- 32) Chou MY, Fogelstrand L, Hartvigsen K, Hansen LF, Woelkers D, Shaw PX, Choi J, Perkmann T, Backhed F, Miller YI, Horkko S, Corr M, Witztum JL, Binder CJ: Oxidation-specific epitopes are dominant targets of innate natural antibodies in mice and humans. The Journal of clinical investigation, 119: 1335-1349, 2009.
- 33) Levine JS, Branch DW, Rauch J: The antiphospholipid syndrome. The New England journal of medicine, 346: 752-763, 2002.
- 34) Gomez-Puerta JA, Cervera R: Diagnosis and classification of the antiphospholipid syndrome. Journal of autoimmunity, 48-49: 20-25, 2014.
- 35) Schenkein HA, Berry CR, Burmeister JA, Brooks CN, Barbour SE, Best AM, Tew JG: Anti-cardiolipin antibodies in sera from patients with periodontitis. Journal of dental research, 82: 919-922, 2003.
- 36) Turkoglu O, Baris N, Kutukculer N, Senarslan O, Guneri S, Atilla G: Evaluation of serum anti-cardiolipin and oxidized low-density lipoprotein levels in chronic periodontitis patients with essential hypertension. J Periodontol, 79: 332-340, 2008.
- 37) Schenkein HA, Best AM, Brooks CN, Burmeister JA, Arrowood JA, Kontos MC, Tew JG: Anti-cardiolipin and increased serum adhesion molecule levels in patients with aggressive periodontitis. J Periodontol, 78: 459-466, 2007.
- 38) Chen YW, Nagasawa T, Wara-Aswapati N, Ushida Y, Wang D, Takeuchi Y, Kobayashi H, Umeda M, Inoue Y, Iwai T, Ishikawa I, Izumi Y: Association between periodontitis and anti-cardiolipin antibodies in Buerger disease. J Clin Periodontol, 36: 830-835, 2009.
- 39) Wang CY, Chyuan IT, Wang YL, Kuo MY, Chang CW, Wu KJ, Hsu PN, Nagasawa T, Wara-aswapati N, Chen YW: beta2-Glycoprotein I-Dependent Anti-Cardiolipin Antibodies Associated With Periodontitis in Patients With Systemic Lupus Erythematosus. J Periodontol, 86: 995-1004, 2015.
- 40) Gunupati S, Chava VK, Krishna BP: Effect of phase I periodontal therapy on anti-cardiolipin antibodies in patients with acute myocardial infarction associated with chronic periodontitis. J Periodontol, 82: 1657-1664, 2011.
- 41) Kiany F, Hedayati A: Evaluation of serum anti-cardiolipin antibodies after non-surgical periodontal treatment in chronic periodontitis patients. Odontology / the Society of the Nippon Dental University, 103: 203-209, 2015.
- 42) Blank M, Krause I, Fridkin M, Keller N, Kopolovic J, Goldberg I, Tobar A, Shoenfeld Y: Bacterial induction of autoantibodies to beta2-glycoprotein-I accounts for the infectious etiology of antiphospholipid syndrome. The Journal of clinical investigation, 109: 797-804, 2002.
- 43) Wang D, Nagasawa T, Chen Y, Ushida Y, Kobayashi H, Takeuchi Y, Umeda M, Izumi Y: Molecular mimicry of Aggregatibacter actinomycetemcomitans with beta2 glycoprotein I. Oral Microbiol Immunol, 23: 401-405, 2008.
- 44) Ye C, Katagiri S, Miyasaka N, Bharti P, Kobayashi H, Takeuchi Y, Momohara Y, Sekiguchi M, Takamine S, Nagasawa T, Izumi Y: The anti-phospholipid antibody-dependent and independent effects of periodontopathic bacteria on threatened preterm labor and preterm birth. Archives of gynecology and obstetrics, 288: 65-72, 2013.
- 45) Colasanti T, Alessandri C, Capozzi A, Sorice M, Delunardo F, Longo A, Pierdominici M, Conti F, Truglia S, Siracusano A, Valesini G, Ortona E, Margutti P: Autoantibodies specific to a peptide of beta2-glycoprotein I cross-react with TLR4, inducing a proinflammatory phenotype in endothelial cells and monocytes. Blood, 120: 3360-3370, 2012.
- 46) Lee YL, Hu HY, Huang N, Hwang DK, Chou P, Chu D: Dental prophylaxis and periodontal treatment are protective factors to ischemic stroke. Stroke; a journal of cerebral circulation, 44: 1026-1030, 2013.
- 47) Heiman ML, Greenway FL: A healthy gastrointestinal microbiome is dependent on dietary diversity. Molecular metabolism, 5: 317-320, 2016.
- 48) Zeevi D, Korem T, Zmora N, Israeli D, Rothschild D, Weinberger A, Ben-Yacov O, Lador D, Avnit-Sagi T, Lotan-Pompan M, Suez J, Mahdi JA, Matot E, Malka G, Kosower N, Rein M, Zilberman-Schapira G, Dohnalova L, Pevsner-Fischer M, Bikovsky R, Halpern Z, Elinav E, Segal E: Personalized Nutrition by Prediction of Glycemic Responses. Cell, 163: 1079-1094, 2015.