2025 Volume 37 Issue 1 Pages 33-36
2025 Volume 37 Issue 1 Pages 33-36
植物と病原微生物の相互作用は、感染部位での両者の認識によって開始され、植物の免疫システムや病原微生物の病原力発揮システムが相互に影響を与えながら動的に変化していく複雑な現象である。このような時空間的ダイナミクスを内包する動的な現象を正しく捉え、その分子機構を理解するにはライブイメージングが重要な手段となる。本稿では、防御応答マーカー遺伝子発現の時空間的動態解析を行っている我々の研究を一例として紹介する。
Plant-pathogenic microbe interaction is a complex phenomenon that is initiated by the recognition of both organisms at the site of infection and dynamically changes as the plant immune system and the pathogenic microbial virulence system interact with each other. Live imaging is an important tool to correctly capture such a dynamic phenomenon that includes spatio-temporal dynamics and to understand its molecular mechanisms. Here, we present an example of our work analyzing the spatio-temporal dynamics of defense response marker gene expression.
Key words: Arabidopsis, immunity, jasmonate, live-imaging, promoter-reporter, salicylate
植物と病原微生物の相互作用は互いの「認識」によって開始される。植物細胞膜には、細菌の鞭毛や糸状菌の細胞壁成分のように特定の微生物種に広く保存された病原体/微生物関連分子パターン(Pathogen/Microbe-Associated Molecular Patterns; PAMPs/MAMPs)を認識するパターン認識受容体(Pattern Recognition Receptors; PRRs)が存在し、両者の認識が起きることでpattern-triggered immunity (PTI) が誘導される(Dodds and Rathjen 2010)。一方、微生物側では、それらPTIを抑制・撹乱し、感染を成立させるためのエフェクタータンパク質群を持つものが存在し、例えば、病原細菌であればIII型分泌機構などを介してエフェクターを植物細胞内に作用させ、感染を成立させていることが知られている(Dodds and Rathjen 2010)。こういった病原微生物への植物側のさらなる対抗手段として、植物細胞は抵抗性タンパク質とも呼ばれる、nucleotide-binding leucine-rich repeat immune receptors(NLRs)型のセンサータンパク質を持ち、植物細胞内での特定のエフェクター作用を特異的に認識することで、プログラム細胞死などを伴う強い防御応答effector-triggered immunity (ETI)を誘導することが知られている(Dodds and Rathjen 2010)。さらには、局所的な病原体感染が、植物体に全身獲得抵抗性 (systemic acquired resistance; SAR)などの全身的な抵抗性誘導現象を引き起こすことも知られており、このように植物―病原微生物相互作用に関するさまざまな事象が、分子レベルで理解されつつある(Vlot et al. 2021)。その一方で、これらPTI、ETI、SARなどは、病原体を認識した植物細胞から始まって、その周辺細胞、組織、個体レベルへと様々な形で発展・展開していく植物の持つ免疫システムの特徴的な一部を定義したものに過ぎないとも考えられ、植物免疫を正しく理解するためには、これらを包括的に捉えることが必要である。また、この相互作用の過程においては、病原微生物の方も病原力発揮システムを起動させて免疫を抑制し、増殖を試みており、植物と病原微生物の相互作用は一つの動的なシステムとして捉えることが必要である。このような時空間的ダイナミクスを内包するシステムを正しく捉え、その分子機構を理解するにはライブイメージングがひとつの重要な手段となる(Megason and Fraser 2007, Toyota and Betsuyaku 2022)。本稿では、その一例として、シロイヌナズナと病原細菌Pseudomonas syringae pv. tomato DC3000(Pst)との相互作用系において、植物免疫の指標となるマーカー遺伝子のプロモーターレポーター株を用いることで両者の時空間的ダイナミクスを捉え、それらを司る分子機構を解析しようとしている筆者らの取り組みを紹介する。
植物免疫が時空間的に制御されている例として、過敏感反応(Hypersensitive response; HR)が挙げられる。HRとは、上述のETIに伴ってみられることが多い現象で、感染部位の植物細胞がプログラム細胞死を起こすことが特徴である(Balint‐Kurti 2019, Mur et al. 2008)。この細胞死は特に過敏感細胞死(Hypersensitive cell death; HCD)と呼ばれており、病原微生物が感染を試みた細胞やそのごく近傍の細胞のみで見られることや、付随する防御応答遺伝子の発現もHCDのごく近傍の細胞でのみ見られることから、感染を受けた細胞から何らかのシグナル分子が分泌されることで、同心円的な防御応答遺伝子発現領域が形作られると考えられている(Kombrink and Somssich 1995)。このようなシグナル分子としては、HR誘導に必須な植物ホルモンであるサリチル酸 (SA) が候補として考えられており,感染部位で合成されたSAがその周辺の非感染細胞に濃度勾配を形成することで,SA濃度依存的に,高濃度側ではHCD,続いて防御遺伝子の発現,などが誘導されるというモデルが提唱されていた(Dorey et al. 1997, Enyedi et al. 1992, Yan and Dong 2014)。その一方で、HR誘導時にはSAと強い相互拮抗関係にあることが知られているジャスモン酸(JA)が蓄積することや、ETI誘導にJAが寄与しているなどの報告も出ており、HRを起こした葉組織において、互いに強く拮抗しあうSAおよびJAのシグナル経路がどのように同時に活性化し、機能するのかが未解明であった(Kenton et al. 1999, Liu et al. 2016, Spoel et al. 2003, Tsuda et al. 2009)。
そこで、筆者らのグループでは、イメージング技術を用いてこの課題に取り組むこととした。変異体を用いた遺伝学研究では、ある生物現象における特定の遺伝子(≒機能)の必要性の有無を解き明かすことができるが、どこでどのように機能するのかに関しては異なる手法が必要である。広く使われる手法として、注目した遺伝子のプロモーター活性を、何らかのレポーター遺伝子を用いて可視化するプロモーターレポーター生物を作出して解析する手法がある。ß-glucuronidase (GUS) 遺伝子などのレポーターの利用によって、特定の遺伝子機能に関して細胞レベルの解像度が得られるようになり、生命現象を組織レベルで理解することに多いに役立ったが、組織の固定・染色が必要であるため、時間的なプロモーター活性の変化を捉えるには多数の個体を用いて異なる個体で解析する必要があった(Jefferson et al. 1987)。一方で、蛍光タンパク質や発光タンパク質がレポーターとして整備・利用されるようになったことで同一サンプルでの経時的な変動をトレースすることが可能となり、生命現象の時空間的なダイナミクスの詳細な解析が進みつつある(Megason and Fraser 2007)。
筆者らは、核局在型enhanced Yellow Fluorescent Protein (eYFP-NLS) をレポーターとした系を用いることとした(Kubo et al. 2005)。レポータータンパク質を核に局在させることで、細胞レベルで活性の有無を解析することも可能となる利点に加え、防御応答が活性化した植物でよく見られるような二次代謝化合物由来の自家蛍光と、レポーター由来の蛍光を区別できると考えたからである。上述のSAシグナル経路の指標としては、その活性を示すマーカー遺伝子としてPathogenesis-Related Gene 1(PR1)がよく知られており、JAシグナル経路の指標に関しても、同様にVegetative Storage Protein 1(VSP1)というマーカー遺伝子が知られていた(Berger et al. 1995, Guerineau et al. 2003, Utsugi et al. 1998, Vlot et al. 2009)。両者のプロモーター(それぞれ、pPR1およびpVSP1と表記)制御下にeYFP-NLSを配置したpPR1-eYFP-NLSおよびpVSP1-eYFP-NLSを持つシロイヌナズナレポーター形質転換体を作出した(Betsuyaku et al. 2018)。
病原細菌感染に対しての植物免疫応答という動的な過程において、これらプロモーター活性の時空間的な動態を捉えるには同一接種葉を用いての定点撮影、すなわちタイムラプス撮影が適している。そのためには切断葉をプレパラート等の状態で観察するのではなく、実体顕微鏡で、非切断状態の葉を丸ごと撮影する形式が望ましい。近年の電動制御可能な蛍光実体顕微鏡であれば、ほとんどの機種で撮影プログラムを組んで自動でタイムラプス蛍光撮影を行うことは容易である。しかし、筆者らはここで二つの課題に直面した。一つは、植物葉が日周の中で大きく”動く”ことであった。プロモーター活性を示す領域の変遷や、葉の特定部位での蛍光値の増減を経時的に計測するには、撮影領域の中でサンプルの位置が動かないことが望ましい。この点に関しては、筆者らはサージカルテープなどを用いて植物葉を可能な限り弱い力で固定することで解決した(図1a, Betsuyaku et al. 2019)。もう一つの課題は、光の問題である。これまでの研究によって、ETI誘導時のSA蓄積やPR1発現誘導が暗黒下では強く抑制されること、すなわち、これらが光に強く依存していることが報告されている(Zeier et al. 2004)。一方で、蛍光タイムラプス撮影時には、通常、暗室などの環境が必要となり、各撮影タイムポイントの間の時間は暗黒条件になってしまう。筆者らの実験においても、接種後に通常の人工気象器環境においた植物と、タイムラプス撮影に供した植物とで、一定時間経過後に比較したところ、pPR1活性化領域の広がりや強度に大きな違いがみられた(data not shown)。撮影ポイント間での照明の照射方法にはさまざま手法が考えられたが、最もシンプルな解決法として、筆者らは撮影プログラムを調整して目的の明視野像とYFP像、Texas Red像(葉緑体自家蛍光を撮影)を撮る各サイクルの間の時間を、明視野像を撮像する時間として設定することで、各撮影サイクルの間に照明を入れる手法をとった(図1b, Betsuyaku et al. 2019)。無駄な撮影をすることでデータ量は大きくなるが、機器間の同期等の設定に忙殺されることなく目的を達することができた、という点で有効な手法であったと考えている。また、光毒性の問題など、適時、上述のように通常の人工気象器環境においた植物との比較を行うことで、ライブイメージングに関わるさまざまな処理の影響を検討することも基本的なことではあるが重要であったと考えている。
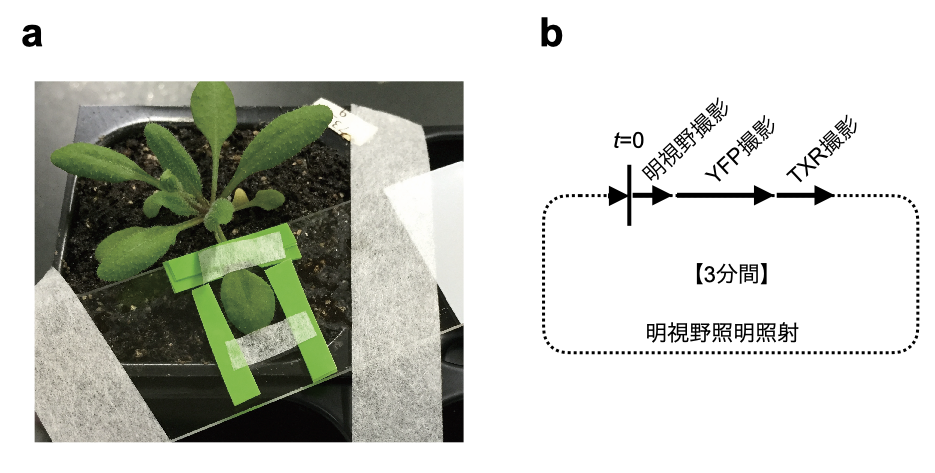
図1 プロモーターレポーター植物を用いたタイムラプス蛍光イメージングの例
(a)植物の動きを最小限にするための固定例。プラスチックテープをスペーサーとして、植物組織を保護しつつ、サージカルテープで固定している。 (b)タイムラプス撮影プログラムの例。一連の撮影プログラム(明視野、YFP、TXR)のあと、次のサイクルまでを明視野像を撮影する設定として簡易的に撮影プログラム間での明視野照明を簡易的に実現した。照明強度は、照度計等を用いて植物育成に適したものようになるよう調整した。 いずれも引用文献参照(Betsuyaku et al. 2019)。
上述のように構築したイメージング系を用いて、HR誘導時のSAシグナル経路およびJAシグナル経路の動態を解析した。エフェクターAvrRpt2を持つPstは、対応するNLR遺伝子RPS2を持つシロイヌナズナにHCDを伴うETI、すなわちHRを誘導する(Kunkel et al. 1993, Yu et al. 1993)。この系を用いて、pPR1-eYFP-NLSおよびpVSP1-eYFP-NLS植物に高濃度菌液を注入接種して局所的なHRを誘導し、それぞれの動態を解析したところ、感染領域周辺でSAシグナル経路活性を示すpPR1活性が接種後13時間付近をピークとして一過的に上昇することを見出した(図2)。また、そのpPR1活性化領域を取り囲むようにJAシグナル経路活性を示すpVSP1活性化領域が一過的に生じることも見出した(図2)。感染部で見られるHCDはSA依存的に誘導されることが報告されている(Delaney et al. 1994)。つまり、HR誘導時には感染部位周辺に、中心部にSAシグナル経路活性化ドメイン、そしてその外周部にはJAシグナル経路活性化ドメインという同心円的な二層構造が形成されていることが明らかとなった。このことは、HR(ETI)においては、SAおよびJAという強い相互拮抗関係にある二つのホルモンシグナル経路が同一葉内の異なる部位で同時に活性化されていることを示しており、この発見によって、これまでの知見を矛盾なく説明できることが示された。別の研究グループにおいても、さらに別のエフェクターAvrRpm1を持つPst接種シロイヌナズナを用いて、部位特異的なサンプリングによって感染部位とその周辺の網羅的な遺伝子発現解析が行われ、やはり、中央部ではSAシグナル経路の活性化が、そしてその外側ではJAシグナル経路の活性化を示す遺伝子発現が報告されており、感染部位での同心円的なSA/JAシグナル経路の活性化という現象は、Pst接種によって誘導されたHR(ETI)においての共通の現象である可能性が示された(Salguero-Linares et al. 2022)。イメージングを用いた研究が契機となり、植物免疫は感染部位近傍の細胞で一様に誘導されるようなものではなく、感染部位からの距離に応じて異なるシグナル経路の活性化が厳密に制御されるのであるという、いわば当たり前のことを我々に再認識させることとなった(Tsuda 2017)。
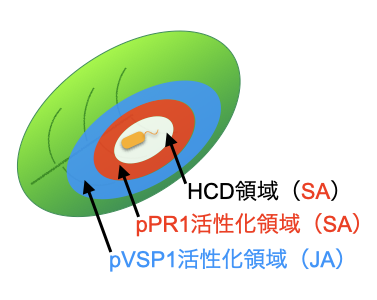
図2 HRで見られるSAおよびJAシグナル経路活性化ドメインからなる防御応答の二層構造の概略。
本稿では、植物免疫応答のライブイメージング例として、プロモーターレポーター植物を用いたHR誘導時の植物ホルモンシグナル経路活性化動態の研究例を紹介した。他の病原微生物を用いて、さらに植物ホルモンシグナル経路のマーカー遺伝子プロモーターに加え、さらに内部標準レポーターや細胞膜マーカーなどと組み合わせて、より細胞ごとの定量解析を可能にした系なども報告されており、ライブイメージングを基盤としての植物免疫動態の解析が進みつつある(Ghareeb et al. 2020) 。また、植物免疫の時空間的制御機構を理解する新たな技術として,single cell RNA-seqによるトランスクリプトーム解析が、近年、急速に進展しつつある。Pst感染に伴う植物免疫と植物の感受性に関わる遺伝子群を見出し、それらのプロモーターレポーター植物を作出し、解析することで、植物の抵抗性や感受性に関わる遺伝子発現の時空間的動態を明らかにするなど,今後ますますその発展が期待される分野である。これら次世代シークエンサー(NGS)の利点は、ハイスループットかつ定量的であることであり、さらに、核酸さえ抽出できれば植物種を問わずに適用可能なことである。一方、ライブイメージングでは、プロモーターレポーター形質転換植物の作出が必要であることから、時間やコストの問題、さらには、扱うことができる遺伝子の数に限りがあり、どうしても代表例となる「マーカー遺伝子」の解析になりがちなところや、そもそも形質転換の可否などが大きな課題である。これらの点を克服する新たな技術として、同一サンプルで、比較的安価に数多くの遺伝子発現パターンを解析することを可能としたPHYTOMap (plant hybridization-based targeted observation of gene expression map)なども報告されており、植物免疫の時空間的制御機構解析は非モデル植物にも広がりつつある(Nobori et al. 2023a, 2023b)。ただ、冒頭でも述べたように、動的な現象である植物―微生物相互作用の解析においては、同一サンプルにおけるさまざまな事象の時間的な変遷など、ライブイメージングだからこそ捉えられる課題も数多くある。NGS技術に劣らず、イメージング分野も日進月歩で発展しており、相互補完的な利点を持つ両技術の活用が、植物免疫に限らず、さまざま生命現象の時空間的制御機構への理解を深めてくれるに違いない。ただ、そんな最新技術を利用するとしても、特にライブイメージングにおいては、本稿で紹介した光条件の調整など、扱っている生物現象を正しく捉える上での古典的かつ基本的な条件設定には、十分留意して創意工夫する必要があることを付け加えておきたい。