2015 Volume 101 Issue 10 Pages 524-529
2015 Volume 101 Issue 10 Pages 524-529
Several studies have examined the reduction behavior of manganese ore at high temperature with the aim of reducing the manganese cost in the steelmaking process. However, the transformation behavior of manganese compounds at high temperatures had not yet been clarified. Therefore, in this paper, the effects of temperature and oxygen partial pressure, as well as chemical composition, on the transformation and melting behavior of manganese ore were investigated using high-temperature X-ray diffraction (XRD) and thermogravimetry-differential thermal analysis (TG-DTA) in order to obtain fundamental information on the pre-reduction process of manganese ore. The main manganese compound in the raw manganese ore used in this study was characterized as CaMn6SiO12 by XRD at room temperature, while the main manganese compounds in the sintered manganese ore were Mn3O4 and MnO. Under a vacuum condition, raw manganese ore and sintered manganese ore were reduced to MnO above 1473 K. However, under atmospheric conditions (pressure: 760 Torr), manganese ore was reduced to Mn3O4 rather than MnO at temperatures above 1073 K. The results of high-temperature XRD agreed with thermodynamic calculations. The melting point of the raw manganese ore evaluated by TG-DTA was lower than that of the sintered manganese ore due to the difference in the manganese oxide in each ore rather than the difference in the content of gangue components such as Al2O3, CaO, MgO and Fe2O3. The higher melting temperature of the sintered manganese ore is interpreted in terms of a higher content of MnO due to heat treatment.
近年,構造用鋼板の高強度化の要求が高まっており,構造用鋼板の高強度化を目的に,MnやPなどの固溶強化元素の添加が行われている1)。製鋼工程でのマンガン源の添加に関しては,転炉出鋼時や2次精錬工程での成分調整時にマンガン合金や電解マンガンを添加する方法がある2)。しかし,マンガン合金や電解マンガンは高価であるため,合金コスト削減の観点から,安価なマンガン源であるマンガン鉱石の製鋼工程での添加が行われている3,4,5,6,7,8)。
マンガン鉱石は,採掘後選鉱工程を経て出荷される未焼結鉱と選鉱工程後のマンガン鉱石の粉末に石灰等を添加し焼結した焼結鉱があり,未焼結鉱と焼結鉱ではマンガン純分や鉱石中の酸素量が異なる。マンガン鉱石中の酸素含有量が多いほどマンガン鉱石の還元には不利であり,溶鋼中マンガン歩留が低下してしまう8)ことから,マンガン鉱石中の酸素量は製鋼工程でのマンガン鉱石の使用を考える上で重要な要素である。また,マンガン鉱石の使用量拡大を志向する上で,高温でのマンガン鉱石中の化合物の分解反応や溶解挙動を理解することは非常に重要である。
過去にもマンガン鉱石の高温還元反応,ガス還元反応に関する検討が行われている8,9,10,11)。Terayamaらは,TG-DTAを用いてマンガン酸化物の炭素熱還元挙動を調査しており,マンガン鉱石を炭素と共に加熱した場合,マンガン鉱石の熱分解反応とCOおよびCO2を媒介した反応によりマンガン鉱石は還元され,1200 K近くでMnO相まで還元されることを報告している9,10)。さらに,FeがMnとMnFe2O4として共存する場合は1163 K辺りからFeO-MnO型の非化学量論的化合物が生成し,1273 K付近からCOを発生して金属鉄とMnOに還元された後,MnOの還元反応が進行することを報告している11)。Kanekoら8)は,昇温による鉱石中の酸素量の変化を調査することを目的に,60 kg鍋型焼結シミュレータを用いたマンガン鉱石の加熱試験を行い,未焼結鉱を1573~1673 K程度で焼結することにより,鉱石中の酸素量が減少し,鉱石中のMn酸化物はMnO2からMn3O4,MnOに還元されることを明らかにしている。さらに,Kanekoら8)は横型管状炉を用いてマンガン鉱石の溶融挙動を調査し,CaOを20%程度添加することで融点が約100 K低下することを報告している。しかし,雰囲気中の酸素分圧がマンガン鉱石の鉱物相の変化に及ぼす影響やマンガン鉱石中の化合物形態がマンガン鉱石の溶融に及ぼす影響については明らかでない。
本報では,マンガン鉱石の種類や熱処理がマンガン鉱石の還元や溶融等の高温挙動に及ぼす影響を明らかにすることを目的に,大気条件と真空条件でのマンガン鉱石の高温XRD測定を実施し,マンガン鉱石の還元挙動に及ぼす温度と酸素分圧の影響について検討した。また,マンガン鉱石中のマンガン化合物の形態がマンガン鉱石の溶融挙動に及ぼす影響についても報告する。
マンガン鉱石はA:未焼結鉱,B:焼結鉱,C:熱処理した焼結鉱の3種類を用いた。C:熱処理した焼結鉱は,マンガン鉱石中の酸素含有量がマンガン鉱石の溶融挙動に及ぼす影響を調査するために,B:焼結鉱を熱処理することにより得た。熱処理は高温真空炉を用い,Ar雰囲気下で1923 Kまで昇温後炉冷した。昇温速度は,室温~1473 Kまで5 K/min,1273 K~1923 Kまで6.5 K/minとした。また炉冷時の冷却速度の実績は約3 K/minであった。用いたマンガン鉱石の組成をTable 1に示す。A:未焼結鉱はマンガン純分が低く,鉱石中酸素量が高いのに対し,焼結鉱は焼結工程を経ているためマンガン純分が高く,鉱石中酸素量が低い。鉱石中の酸素量は,A:未焼結鉱では34.8%,B:焼結鉱 では27.8%,C:熱処理した焼結鉱では25.4%であった。A:未焼結鉱に比べて,B:焼結鉱,C:熱処理した焼結鉱の鉱石中の酸素量が低いのは,鉱石が加熱された際にマンガン鉱石中の酸素が除去されたためであると考えられる。また,B:焼結鉱とC:熱処理した焼結鉱でMgOやT.Feの濃度が異なるのは鉱石由来の成分のばらつきであると考えられる。
| (mass%) | |||||||||||
| Sample | Chemical Compound | T.Mn | T.Fe | SiO2 | Al2O3 | CaO | MgO | P | S | T.O | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| A | Raw Mn ore | CaMn6SiO12 | 42.8 | 5.9 | 5.9 | 0.8 | 7.9 | 1.5 | 0.033 | 0.265 | 34.8 |
| B | Sintered Mn ore | 2MnO·SiO2, Mn3O4, MnO | 61.8 | 3.2 | 6.2 | 7.7 | 0.5 | 0.3 | < 0.005 | 0.017 | 27.8 |
| C | Heat-treated Mn ore | MnO | 62.8 | 0.9 | 7.6 | 6.3 | 0.7 | 2.8 | < 0.005 | 0.015 | 25.4 |
マンガン鉱石加熱時のマンガン化合物の形態変化を調査するため,高温XRD測定を行った。試料はA:未焼結鉱,B焼結鉱の2種類を用いた。高温XRDの測定条件をTable 2に示す。測定は大気条件と真空条件(1 Torr)で行った。温度は303 K,1073 K,1473 K,1773 Kの4条件で,50 K/minで昇温し,所定の温度に到達後5分間保持した後測定を行った。試料は粉砕後白金基板に載せ測定を行った。また,熱力学平衡計算を行い,温度と酸素分圧を変化させた場合のマンガン酸化物の形態を確認した。計算には熱力学データベースFactSage12)を用いた。
| Radiation source | Cu |
|---|---|
| Voltage | 45 kV |
| Electric current | 40 mA |
| Degree (2θ) | 10 ~ 60° |
| Presure | Atmosphere (760 Torr) Vacuum (1 Torr) |
| Temperature | 303 K 1073 K 1473 K 1773 K |
| Holding time | 5 min. |
マンガン鉱石中のマンガン化合物の形態による溶融挙動の差異を調査するため,TG-DTA測定を行った。試料はA:未焼結鉱,B:焼結鉱,C:熱処理した焼結鉱の3種類を用いた。TG-DTA測定は,粉砕した試料0.1 gを白金坩堝に入れ,1923 Kまで10 K/minで昇温し,測定を行った。
Fig.1に大気中,303 Kでの各種マンガン鉱石のXRD測定の結果を示す。確認された化合物は,A:未焼結鉱ではCaMn6SiO12,B:焼結鉱では2MnO・SiO2,Mn3O4,MnO,C:熱処理した焼結鉱ではMnOのみであった。

X-ray diffraction patterns of manganese ores at room temperature. A: raw manganese ore, B: sintered manganese ore, C: heat-treated manganese ore. (Online version in color.)
Fig.2にA:未焼結鉱の大気中,真空中での高温XRD測定の結果をそれぞれ示す。Fig.2 a)の大気中の場合,1073 Kでは鉱石中の化合物は変化しないが,1473 KではMn3O4のみが確認された。また1773 Kでは基板として使用している白金のピークのみが確認されており,マンガン鉱石が溶融したと考えられる。一方,Fig.2b)の真空中で昇温を行った場合,鉱石中のマンガン化合物は大気条件と同じく1073 Kでは変化しないが,1473 KではMnOのみが確認された。

X-ray diffraction patterns of raw manganese ore at elevated temperature. a) in atmospheric condition, b) in vacuum condition (Online version in color.)
Fig.3に,B:焼結鉱の大気中,真空中での高温XRD測定の結果を示す。大気中1073 Kでは303 Kから存在していた2MnO・SiO2,Mn3O4に加え,Mn2O3が生成していた。また,1473 K,1773 KではMn3O4のみが同定された。一方,真空中では1073 Kまでは鉱石中の化合物の形態に変化はないが,1773 KではMnOのみであった。
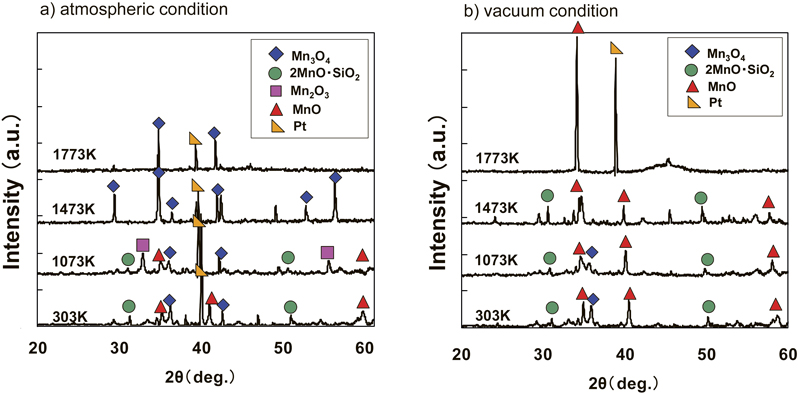
X-ray diffraction patterns of sintered manganese ore at elevated temperature. a) in atmospheric condition, b) in vacuum condition (Online version in color.)
Table 3に高温XRD測定結果のまとめを示す。A:未焼結鉱,B:焼結鉱共に大気中では,鉱石中のマンガン化合物は1473 K以上でMn3O4までしか還元されないが,真空中では1773 K以上ではMnOまで還元されていた。高温XRD測定の結果を,Mn-O系の相安定図と対比して考察した。熱力学データベースFactSageを用いて作成したMn-O系の相安定図をFig.4に示す。また,Fig.4中に高温XRD測定により同定されたマンガン化合物を併せて示す。マンガン化合物は温度の上昇に伴いMnO2,Mn2O3,Mn3O4,MnO,液相と変化し,この変化はB:焼結鉱の高温XRD測定の結果と概ね一致していた。また,マンガン酸化物は大気中では1073 K以上でMn3O4までしか還元されないが,真空条件(1 Torr)では1473 K以上でMnOまで還元されることが熱力学計算結果からわかった。この結果は高温XRD測定の結果と一致していることから,高温XRD測定の保持時間5分の間に平衡状態に到達していたと考えられる。
| a) Sample A: raw manganese ore | ||
| Temperature | Chemical compound | |
| Atmosphere | Vacuum | |
| 1473 K | Mn3O4 | MnO |
| 1073 K | CaMn6SiO12 Fe2O3 | CaMn6SiO12 Fe2O3 |
| 303 K | CaMn6SiO12 Fe2O3 | CaMn6SiO12 Fe2O3 |
| b) Sample B: sintered manganese ore | ||
| Temperature | Chemical compound | |
| Atmosphere | Vacuum | |
| 1773 K | Mn3O4 | MnO |
| 1473 K | Mn3O4 | 2MnO·SiO2 MnO |
| 1073 K | 2MnO·SiO2 Mn3O4 Mn2O3 MnO | 2MnO·SiO2 Mn3O4 MnO |
| 303 K | 2MnO·SiO2 Mn3O4 MnO | 2MnO·SiO2 Mn3O4 MnO |

Phase stability diagram of Mn-O system. (Online version in color.)
以上より,焼結鉱,未焼結鉱のいずれのマンガン化合物も,大気条件ではMn3O4までしか還元されないが,真空条件(1 Torr)ではMnOまで還元されることが明らかになった。
3・2 マンガン鉱石中のマンガン化合物の形態と溶融挙動前節の高温XRD測定の結果を受け,マンガン化合物の形態が高温でのマンガン鉱石の溶融挙動に及ぼす影響について検討した。Fig.5にマンガン鉱石のTG-DTA測定結果を示す。TGの測定結果から,A:焼結鉱,B:未焼結鉱,C:熱処理した焼結鉱ともに温度の上昇に伴って質量が減少した。303 Kから1973 Kまで温度が上昇する間に,A:未焼結鉱は約12 mg,B:焼結鉱は約5 mg,C:熱処理した焼結鉱は約0.5 mg質量が減少した。これは,マンガン酸化物が熱分解して酸素を放出したためと考えられ,鉱石中の酸素量が多いほど質量減少量が大きくなった。A:未焼結鉱は1000 K程度で質量の減少がはじまった。これは先の高温XRD測定の結果からCaMn6SiO12の熱分解によりMn3O4が生成する反応に対応するものと考えられる。またA:未焼結鉱,B:焼結鉱,C:熱処理した焼結鉱のいずれも1500~1650 K程度で質量が減少したが,これはマンガン鉱石中のマンガン化合物がMn3O4からMnOに変化したためであると考えられる。DTA測定の結果においても1500~1650 K程度でピークが見られるが,これらのピークもマンガン鉱石中のマンガン化合物がMn3O4からMnOに変化したことに対応していると考えられる。

TG-DTA curves of manganese ore in Ar atmosphere, a) raw manganese ore, b) sintered manganese ore, c) heat-treated manganese ore. (Online version in color.)
ここで,DTA測定での融点と,熱力学計算から求められる融点を比較して検討する。
まず,熱力学計算による融点の見積もりはFactSageを用いて以下のように行った。XRD測定の結果から,A:未焼結鉱,B:焼結鉱,C:熱処理した焼結鉱中のマンガン酸化物の形態をそれぞれ,Mn2O3,Mn3O4,MnOと仮定し,マンガン酸化物以外の化合物として,SiO2,Al2O3,CaO,Fe2O3,MgOを考慮した。計算に用いた組成比率をTable 4に示す。各組成において温度を変えて固相の割合を求め,固相が消失した温度を融点とした。以後熱力学計算により見積もられた融点を計算融点と記す。
| Sample | Mn2O3 | Mn3O4 | MnO | SiO2 | Al2O3 | CaO | MgO | Fe2O3 | |
|---|---|---|---|---|---|---|---|---|---|
| A | Raw Mn ore | 71.5 | 0.0 | 0.0 | 6.9 | 0.9 | 9.2 | 1.7 | 9.8 |
| B | Sintered Mn ore | 0.0 | 18.0 | 62.8 | 6.2 | 7.7 | 0.5 | 0.3 | 4.6 |
| C | Heat-treated Mn ore | 0.0 | 0.0 | 81.3 | 7.6 | 6.3 | 0.7 | 2.8 | 1.3 |
次に,DTA測定での融点の決定方法について述べる。マンガン鉱石は混合物のため,FactSageで見積もられた計算融点以下の温度で,鉱石中の化合物の溶融に対応すると考えられるピークがいくつか認められる。鉱石中にはマンガン化合物が最も多く含まれることを勘案すると,この計算融点に近い温度で最も大きなピークが,マンガン化合物の溶融に対応していると考えられる。そこで,FactSageで見積もられる計算融点の近傍で,DTAの時間変化が最も大きい温度をマンガン鉱石の融点と判断した。以後TG-DTA測定から求めた融点を実測融点と記す。
各マンガン鉱石の実測融点をFig.6に示す。A:未焼結鉱の実測融点は1688 Kであったのに対し,B:焼結鉱の実測融点は1732 Kであり,B:焼結鉱の方が高い融点を示した。また,C:熱処理した焼結鉱の実測融点は1884 Kであり,B:焼結鉱よりも高い融点を示した。Table 5に各マンガン鉱石の計算融点と実測融点を示す。Cの実測融点が最も高く,Aの実測融点が最も低い傾向は,FactSageにより見積もられた計算融点の傾向と定性的に一致した。

Melting point of manganese ore determined from DTA measurement. (Online version in color.)
| sample | Thermodynamic calculation | DTA |
|---|---|---|
| A | 1768 K | 1688 K |
| B | 1845 K | 1732 K |
| C | 2012 K | 1884 K |
そこで,A:未焼結鉱,B:焼結鉱,C:熱処理した焼結鉱で実測融点に差が生じた理由について検討した。
A:未焼結鉱,B:焼結鉱,C:熱処理した焼結鉱では,鉱石中のマンガン化合物以外の化合物の含有量とマンガン化合物の形態が異なることから,これらがマンガン鉱石の実測融点に及ぼす影響について調査した。A:未焼結鉱,B:焼結鉱,C:熱処理した焼結鉱の各成分をベースとし,Al2O3,CaO,Fe2O3,MgOの割合をそれぞれ変化させた場合の融点をFactSageを用いて計算した。Al2O3,CaO,Fe2O3,MgO以外の成分の重量比を一定にし,Al2O3,CaO,Fe2O3,MgOの量をそれぞれ変化させた。SiO2の含有量は,A:未焼結鉱,B:焼結鉱,C:熱処理した焼結鉱において大きな差がなかったことから,SiO2の融点への影響はほぼ同等と考え,本検討から除外した。計算結果をFig.7に示す。鉱石中のCaO,MgOの増加は,融点を上昇させ,Al2O3,Fe2O3の増加は,融点を低下させることがわかった。なお,A:未焼結鉱においてCaO 9mass%,Al2O3 1mass%付近に存在する変曲点は,Ca2SiO4の生成に対応するものであった。

Effect of a) CaO, b) Al2O3, c) Fe2O3 or d) MgO concentration on the melting point of manganese ore. (Online version in color.)
まず,A:未焼結鉱の方がB:焼結鉱に比べ融点が低い理由について検討した。Table 5に示すとおり,A:未焼結鉱とB:焼結鉱ではAl2O3,CaO,Fe2O3の含有量とマンガン化合物の形態が異なっていた。そこでFig.8に示すように,A:未焼結鉱,B:焼結鉱のマンガン化合物以外の成分量をベースとし,マンガン化合物(Mn2O3+Mn3O4+MnO)の存在割合を変化させた場合の融点を計算した。計算時はMn3O4とMnOの比をB:焼結鉱の値に統一し,Mn3O4/MnO=0.29(一定)とした。Mn2O3/(Mn2O3+Mn3O4+MnO)と計算融点の関係をFig.8に示す。Mn2O3比率0.5までは,Mn2O3比率の増加に伴い計算融点は減少したが,0.5以上では計算融点の大きな変化は見られなかった。MnO,Mn3O4,Mn2O3の融点はそれぞれ2123 K13),1973 K7),1853 K13)と報告されており,融点の低いMn2O3の比率の増加により系の計算融点が低下するという計算結果は,これらの報告と矛盾しない。すなわち,B:焼結鉱のマンガン化合物以外の成分量をベースとし,Mn2O3の比率を増加させると図中の実線に沿って計算融点が低下した。一方,Fig.8において,Mn2O3比率が同じ場合の計算融点の差,つまり2本の計算線の差分を,マンガン化合物以外の成分の含有量による差とみることができる。この場合,マンガン化合物以外の化合物の影響はB:焼結鉱の融点を上げる方向に作用していると見なせる。したがって,A:未焼結鉱の方がB:焼結鉱に比べ実測融点が低かったのは,Al2O3,CaO,Fe2O3といったマンガン化合物以外の成分の影響による融点上昇の作用よりも,マンガン化合物の形態の違いによる融点低下の作用の方が大きいためと考えられる。

Effect of Mn2O3 to (Mn2O3+Mn3O4+MnO) ratio on the melting point of manganese ore. (Online version in color.)
さらに,C:熱処理した焼結鉱の方がB:焼結鉱に比べ実測融点が高い理由について検討した。B:焼結鉱とC:熱処理した焼結鉱で大きく異なるのは,マンガン化合物の形態とMgO,Fe2O3の含有量である。先述の比較と同様に,B:焼結鉱,C:熱処理した焼結鉱のマンガン化合物以外の成分量をベースとし,マンガン化合物(Mn3O4,MnO)の存在割合を変化させた場合の融点を計算した。Fig.9にMn3O4/MnOと計算融点の関係を示す。Table 5に示したとおり,B:焼結鉱に対してC:熱処理した焼結鉱のMgO 含有量は高く,Fe2O3含有量は低かった。Fig.7から,MgOの増加とFe2O3の減少は,いずれも融点を増加させる要因となるため,同じMn3O4/MnO 比率で比較した場合,Fig.9に示すようにC:熱処理した焼結鉱の組成をベースとした計算線の方が高融点側に位置しているものと考えられる。また,Mn3O4/MnO比率の低下によっても計算融点は上昇しており,前掲のMn3O4およびMnOの計算融点の差を反映していると考えられる。Mn3O4/MnO比率の差から推定される計算融点の差をFig.9に併せて示す。MgO,Fe2O3といったマンガン化合物以外の化合物の影響による計算融点の差と,マンガン化合物の形態の違いによる計算融点の差を比較すると,後者の方が大きいと見なせる。すなわち,上記と同様に,マンガン化合物の形態の方が融点に及ぼす影響は大きいと考えられる。

Effect of Mn3O4 to MnO ratio on the melting point of manganese ore. (Online version in color.)
以上より,鉱石中のCaOやMgOの増加に伴って融点は上昇するが,Al2O3やFe2O3の増加に伴って融点は低下した。しかし,マンガン鉱石の融点はマンガン化合物の形態によっても変化し,マンガン化合物以外の化合物よりもマンガン化合物の形態が融点に及ぼす影響の方が大きいことが明らかになった。
大気条件と真空条件でのマンガン鉱石の加熱実験を実施し,マンガン鉱石の還元挙動に及ぼす温度と酸素分圧の影響,およびマンガン鉱石中の化合物が鉱石の溶融に及ぼす影響を調査し,以下の知見を得た。
1)大気中303 Kにおいて,マンガン鉱石中のマンガンは,未焼結鉱ではCa,Siとの化合物を形成しているのに対し,焼結鉱ではマンガン酸化物もしくは,MnO・SiO2の形態でSiO2との化合物を形成していた。焼結鉱,未焼結鉱のいずれも,マンガン鉱石中のマンガン化合物は,大気条件ではMn3O4までしか還元されないが,真空条件(1 Torr)ではMnOまで還元された。
2)DTAを用いてマンガン鉱石の融点を測定した結果,未焼結鉱の実測融点は1688 K,焼結鉱は1732 Kであった。また焼結鉱を1923 Kまで昇温後炉冷した試料の実測融点は1884 Kであった。これらの融点に及ぼす含有化合物の影響を調査した結果,マンガン鉱石の融点は,マンガン化合物以外の化合物の存在割合にも依存するが,マンガン化合物の形態の影響が大きく,Mn3O4やMnOが増加するほど,融点が上昇することがわかった。