2023 Volume 109 Issue 4 Pages 277-288
2023 Volume 109 Issue 4 Pages 277-288
The effect of brighteners on the deposition behavior of Zn–Ni alloys ant its microstructure was investigated. Zn–Ni alloys were electrodeposited on Cu electrode at 10–5000 A·m−2, 105 C·m−2, 308 K in unagitated zincate solutions containing various brighteners. Although the degree of suppression of hydrogen evolution was different depending on the kind of brightener, the transition current density at which the deposition behavior shifted from normal to anomalous was almost same in solutions containing brighteners. The current efficiency for alloy deposition significantly decreased with an addition of brighteners which had suppression effect on the Zn deposition. Since the brighteners more suppressed the Ni deposition than Zn deposition, the Ni content in deposited films decreased with an addition of brighteners. When the brightener of a straight-chain polymer composed of a quaternary ammonium cation (PQ) which can suppress the diffusion of ZnO22− and Ni ions in solution was added, the Ni content in deposited films increased with increasing current density at high current density region. This is attributed to that Zn which is preferentially deposited over Ni earlier reached the diffusion limitation of ZnO22− ions and Ni deposition didn’t reach the diffusion-limited current density. When both PQ and a quaternary ammonium salt with a benzene ring were added in solution, the films obtained at the diffusion-limited current density of ZnO22− ions exhibited the smooth surfaces composed of fine crystals. With an addition of brighteners to increase the overpotential for deposition, the γ-phase (intermetallic compound of Ni2Zn11) of the deposited films was formed easily.
電気Zn-Ni合金めっき鋼板は,耐食性に優れているため,自動車エンジン回りの部品,家庭電化製品,建材用部品などにおいて幅広く使用されている1–7)。Zn-Ni合金電析は,通常,硫酸塩浴や塩化物浴から行われるが,皮膜の均一電着性については,ジンケート浴からの電析の方が優れることが知られている8,9)。硫酸塩浴,塩化物浴からのZn-Ni合金電析については,従来より多数の研究が行われており,実用的な電流密度の領域では,電気化学的に卑なZnが貴なNiより優先析出する変則型共析挙動を示すことが知られている10–14)。
一方,ジンケート浴からのZn-Ni合金の電析挙動は,電析条件に応じて正常型を示す場合と変則型を示す場合が報告15–20)されているが,硫酸塩浴,塩化物浴からの場合に比べて研究例が少ない。更にジンケート浴からの電析においては,通常,浴中に光沢剤が添加されているが,その電析挙動への影響については不明な点が多い。そこで著者らは,前報にて光沢剤としてエピクロルヒドリンとイミダゾールの反応物(IME)を添加した浴からのZn-Ni合金電析挙動について調査し,IMEは,電析挙動が正常型から変則型へ移行する転移電流密度,電析膜のNi含有率および合金電析の電流効率を低下させることを報告した21–26)。しかし,Zn-Ni合金電析において溶液中のイオンの拡散律速となる高電流密度域における光沢剤の影響については明らかにされていない。また,IMEは電析における電荷移動過程を抑制する光沢剤であるが,光沢剤の中には溶液中のイオンの拡散を抑制する作用があるものも報告されている27–30)。
例えば,第四級アンモニウムカチオンが直鎖状に結合した高分子(PQ)は,ジンケート浴からの純Znめっきにおいて,ZnO22-イオンの拡散を抑制することが報告されており,ベンゼン環を含む第四級アンモニウム塩(QA)が共存すると,拡散の抑制効果が更に大きくなると報告されている27–30)。そこで,本研究では,IMEに加えて,ジンケート浴からの純Znめっきの光沢剤として,ZnO22-イオンの拡散を抑制することが報告されている第四級アンモニウムカチオンが直鎖状に結合した高分子(PQ)およびベンゼン環を含む第四級アンモニウム塩(QA)を選定し,10~5000 A·m-2の広電流密度域でのZn-Ni合金電析挙動に及ぼす光沢剤の影響をZn,Ni析出および水素発生の部分分極曲線に基づき考察した。
Table 1にジンケート浴の電解液組成および電解条件を示す。電解液は市販の特級試薬を用い,常温にてZnO 0.15 mol·dm-3, NiSO4·6H2O 0.016 mol·dm-3, N(CH2CH2OH)3 0.34 mol·dm-3, NaOH 2.5 mol·dm-3を純水に溶解させて作製した。この溶液にTable 2に示す光沢剤を添加した。ベンゼン環を含む第四級アンモニウム塩(以下,QAと称す)を0.07 g·dm-3,第四級アンモニウムカチオンが直鎖状に結合した高分子(分子長20 nm,以下,PQと称す)を1.45 g·dm-3,エピクロルヒドリンとイミダゾールの反応物(以下,IMEと称す)を3 ml·dm-3となるように添加した。PQは,ZnO22-イオンの拡散抑制剤として,QAはPQの補助剤として,またIMEは電析における電荷移動抑制剤として添加した。なお,IMEは,既報31,32)に従い作製した。
| ZnO | (mol∙dm−3) | 0.15 | Current density (A∙m−2)10 ~ 5000 |
| NiSO4∙6H2O | (mol∙dm−3) | 0.016 | Temperature (K)308 |
| N(CH2CH2OH)3 | (mol∙dm−3) | 0.34 | Amount of charge (C∙m−2)105 |
| NaOH | (mol∙dm−3) | 2.5 | CathodeCu or Fe (1×2 cm2) |
| Brightener | (ml∙dm−3) | 0 ~ 4.5 | AnodePt (1×2 cm2) |
| Quiescent bath |
| Symbol | Chemical agents | Suppression effect | Amount of addition |
|---|---|---|---|
| QA | Quaternary ammonium salt with a benzene ring | Adjuvant for PQ | 0.07 (g∙dm−3) |
| PQ | Straight-chain polymers composed of quaternary ammonium cation | Diffusion of ions in solution | 1.45 (g∙dm−3) |
| PQ + QA | — | Diffusion of ions in solution | 1.45 + 0.07 (g∙dm−3) |
| IME | Reaction product of epichlorohydrin and imidazole | Charge transfer of deposition | 3.0 (ml∙dm−3) |
電析は,定電流電解法により電流密度10~5000 A·m-2,通電量105 C·m-2,浴温303 Kにおいて無撹拌下で行なった。通電量105 C·m-2は,電流効率100%で純Znの電析を仮定すると膜厚4.7 μmに相当する。陰極にはCu板(1 cm×2 cm),陽極にはPt板(1 cm×2 cm)を用いた。ただし,SEM観察,XRD解析用のサンプルを作製する際は,陰極にはFe板(1 cm×2 cm)を用いた。電析合金組成,Zn,Ni電析の電流効率は,得られた電析膜を硝酸で溶解し,ICP発光分光分析法によりZn, Niを定量することで求めた。水素発生の電流効率は,100からZn, Ni析出の電流効率(%)を差し引いて求めた。Zn, Ni析出および水素発生の部分電流密度は,全電流密度にそれぞれの電流効率(%)/100を乗じて算出した。分極曲線を測定する際,参照電極としてAg/AgCl電極(飽和KCl, 0.199 V vs. NHE, 298 K)を使用したが,電位は標準水素電極基準に換算して表示した。
電析膜の表面形態観察は走査型電子顕微鏡(SEM)を,また相同定はX線回折装置(Cu-Kα,管電圧 40 kV, 管電流15 mA)を用いて行った。
Fig.1にZn-Ni合金電析の全分極曲線を示す。浴温298 Kにて純Znが析出すると仮定した場合のZn電析(ZnO22-+2H2O+2e-→Zn+4OH-)の平衡電位EZneqは-1.27 Vである33)。また,Ni2+イオンにはトリエタノールアミン(TEA)が2配位しており,その錯安定化定数K=104.74を基に浴温298 Kにて純Niが析出すると仮定した場合に算出されるNi電析(Ni(TEA)22++2e-→Ni+2TEA)の平衡電位ENieqは-0.41Vである34)。全分極曲線は,光沢剤の有無に関わらずZnの平衡電位(-1.27 V)より貴な電位域で立ち上がり,電流密度が20-50 A·m-2を超えると大きく卑な電位域に移行し,Znの平衡電位に到達すると再度立ち上がった。電流密度が約20-50 A·m-2において,陰極電位が大きく卑な方に移行する電流密度を見ると,光沢剤がない場合は,約50 A·m-2であるのに対して,光沢剤を添加した場合は,その種類に関わらず,約20 A·m-2と低くなった。
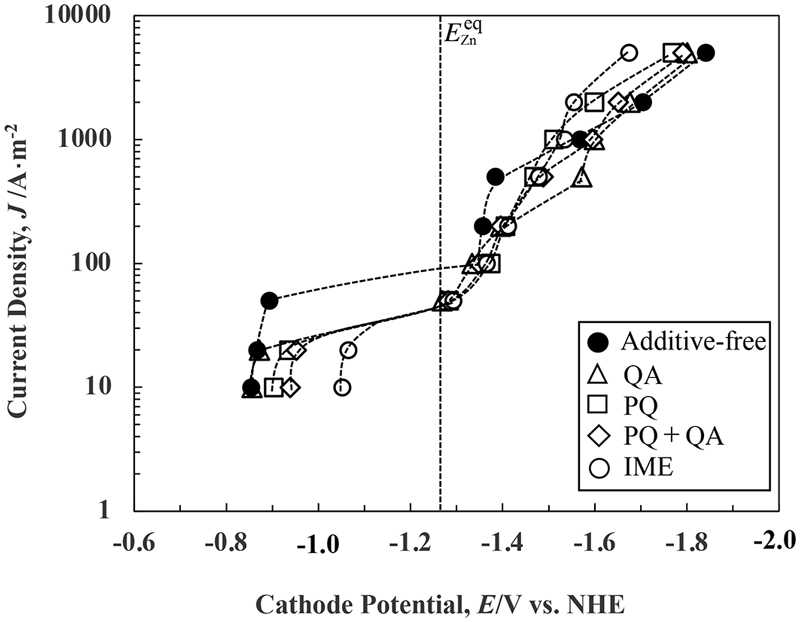
Total polarization curves in Zn-Ni alloy solutions containing various additives.
光沢剤の相違に着目すると,Znの平衡電位より貴な電位域では,IMEを添加すると最も大きく分極しており,その次にPQ+QA, PQの順で分極が大きくなった。QAによる分極はほとんど見られなかった。一方,Znの平衡電位より卑な電位域では電流密度により,光沢剤の影響が異なった。200-500 A·m-2の電流密度域では光沢剤を添加すると分極しているのに対して,2000 A·m-2以上の高電流密度域では,何れの光沢剤においても復極効果が見られた。
Fig.2にZn-Ni合金電析におけるZn析出の部分分極曲線を示す。Znの平衡電位(-1.27 V)より貴な電位域においてもZnの部分電流密度が検出され,その電流密度は光沢剤無しおよびQAを添加した溶液において比較的大きかった。Znの平衡電位より卑な電位域では,Znの部分電流密度100-300 A·m-2の電流密度域では,Znの析出は光沢剤を添加すると光沢剤の種類に関わらず抑制された。PQを添加すると,Zn電析の拡散限界電流密度が出現し,QAを共存させるとその拡散限界電流密度が低下した。Znの部分電流密度が300 A·m-2を超える高電流密度域では,IME,QAによるZn電析の抑制効果は特に見られなかった。

Partial polarization curves of Zn during Zn–Ni alloy deposition from solutions containing various additives.
Fig.3にZn-Ni合金電析におけるNi析出の部分分極曲線を示す。Znの平衡電位(-1.27 V)より貴な電位域では,Ni電析はIMEを添加すると最も大きく抑制されており,その次にPQ+QA, PQの順で抑制が大きかった。QA添加による抑制効果はNiの部分電流密度4 A·m-2以下ではほとんど見られなかったが,4 A·m-2を超えると抑制効果が見られた。一方,Znの平衡電位より卑な電位域ではNiの部分電流密度10 A·m-2以上の領域では,Niの析出は光沢剤を添加すると光沢剤の種類に関わらず抑制された。特にPQ,PQ+QAを添加するとNiイオンの拡散律速により部分電流密度が低くなる領域が見られたが,Zn電析の場合とは異なり,Niイオンの拡散限界電流密度には到達していなかった。

Partial polarization curves of Ni during Zn–Ni alloy deposition from solutions containing various additives.
Fig.4にZn-Ni合金電析における水素発生の部分分極曲線を示す。Zn-Ni合金浴からの水素発生は,Znの平衡電位より貴な領域では,光沢剤の有無に関わらず電位の卑な方向への移行とともに一旦減少し,Znの平衡電位より卑な領域になると増加に転じた。水素発生に及ぼす光沢剤の影響に着目すると,Znの平衡電位より貴な領域では,同一電流密度(10 A·m-2)における水素発生電位は,光沢剤添加により卑に移行していることが分かる。IMEを添加すると最も卑に移行しており,その次にPQ+QA, PQの順で移行しており,Zn, Ni析出に対する場合と同様の傾向を示した。一方,Znの平衡電位より卑な電位域では,水素の部分電流密度10-200 A·m-2の領域で,光沢剤による水素発生の抑制効果が見られ,特にQAによる抑制効果が大きかった。しかし,水素の部分電流密度が1000 A·m-2以上になると,光沢剤による水素発生の抑制効果は無くなり,逆に促進効果が見られた。
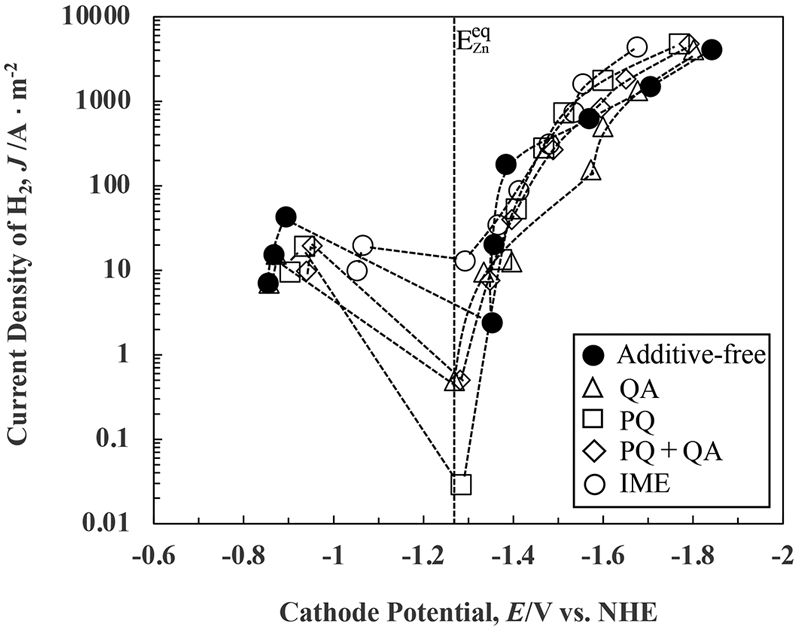
Partial polarization curves of H2 during Zn–Ni alloy deposition from solutions containing various additives.
Fig.5にZn-Ni合金電析におけるZn-Ni, Zn, Ni析出の電流効率と電流密度の相関関係を示す。以下に示すZn-Ni合金電析の電流効率は,Zn析出とNi析出の電流効率を足したものである。Fig.5(a)に示すように合金電析の電流効率は,光沢剤が無い場合,10~50 A·m-2の低電流密度域(Znの平衡電位より貴な領域)では15~30%程度と低かったが,電流密度が50 A·m-2を超えると急激に増加し,100 A·m-2(Znの平衡電位より卑で電荷移動律速の領域)で最大となり,電流密度が500 A·m-2以上(Znの平衡電位より卑でイオン拡散律速の領域)に増加すると電流効率は大きく低下した。一方,光沢剤を添加すると,その種類に関わらず,電流効率は電流密度20 A·m-2を超えると急激に増加し50 A·m-2で最大となり更に電流密度が増加すると低下した。光沢剤を添加すると,電流効率が急激に増加する電流密度が低電流側にシフトした。

Current efficiencies for Zn–Ni alloy deposition from solutions containing various additives. [(a) Zn-Ni, (b) Zn, (c) Ni]
光沢剤による相違に着目すると,10~20 A·m-2の低電流密度域(Znの平衡電位より貴な領域)では,IME,PQを添加すると電流効率はほぼゼロまで低下した。しかし,QA添加による電流効率の低下はほとんど見られなかった。50~500 A·m-2の中電流密度域(Znの平衡電位より卑で電荷移動律速の領域)では,IMEを添加すると電流効率は最も低下し,PQを添加するとその次に電流効率は低下した。1000 A·m-2以上の高電流密度域(Znの平衡電位より卑でイオン拡散律速の領域)では,PQ+QAの添加で電流効率の低下が最も大きく,その次にPQ添加で電流効率は低下した。なお,QAを添加すると,200 A·m-2以上の電流密度域で,無添加に比べ,電流効率が若干増加した。
合金電析の際のZn析出の電流効率(Fig.5(b))は,光沢剤が無い場合の10~50 A·m-2,光沢剤がある場合の10~20 A·m-2での低電流密度域では,非常に低かったが,それぞれ電流密度が50,20 A·m-2を超えると急増した。電流密度50 A·m-2以上の領域でのZn析出の電流効率に及ぼす光沢剤の影響は,先に述べたZn-Ni合金電析の電流効率に及ぼす場合と同一であった。合金電析の際のNi析出の電流効率に及ぼす光沢剤の影響は,特に10~20 A·m-2の低電流密度域で認められ,IME,PQを添加すると電流効率はほぼゼロまで低下した(Fig.5(c))。Fig.5(a),(b),(c)の比較より,Zn-Ni合金電析の電流効率は,光沢剤の有無に関わらず,低電流密度域(Znの平衡電位より貴な領域)ではNi析出の,中電流密度域(Znの平衡電位より卑で電荷移動律速の領域)および高電流密度域(Znの平衡電位より卑でイオン拡散律速の領域)ではZn析出の電流効率を反映したものである事が分かった。IME,PQは,低電流密度ではNi析出の電流効率に影響を及ぼし,中電流密度域および高電流密密度域ではZn析出の電流効率に影響を及ぼした。
Fig.6にZn-Ni合金電析膜のNi含有率に及ぼす電流密度の影響を光沢剤毎に示す。図中の破線は,Niについてその浴組成と合金組成が等しい場合を示す組成参照線(Composition reference line,以下CRLと略す)である。電析膜のNi含有率がこの線の上部に位置していれば,電気化学的に貴なNiが優先析出する正常型共析であり,下部に位置していれば卑なZnが優先析出する変則型共析となることを示す。Fig.6(a)に示すように,光沢剤が無い場合,Ni含有率は50~100 A·m-2の領域で大きく変化した。50 A·m-2以下ではNi含有率は90 mass%前後とCRLより上部にあり,正常型共析となるのに対して,100 A·m-2以上ではCRLを下回り変則型共析となった。電析挙動が正常型から変則型へ移行する電流密度は転移電流密度と称される35–37)。光沢剤を添加すると,その種類に関わらず,Ni含有率は20~50 A·m-2の領域で大きく変化し,100 A·m-2以上ではCRLを下回り変則型共析となった。すなわち,転移電流密度は,光沢剤の種類に関わらずそれを添加すると低下した。この転移電流密度は,光沢剤の有無に関わらず,Fig.1に示す全分極曲線の電位がZnの平衡電位より貴な領域から卑な領域に急激に移行する電流密度および合金電析の電流効率が大きく変化する電流密度(Fig.5)と一致している。光沢剤による相違に着目すると,10~20 A·m-2の低電流密度域では,Ni含有率はIMEを添加すると最も低下し,その次にPQ+QA, PQの順で低下しており,QA添加による影響は見られなかった。

(a) Ni contents in the Zn–Ni alloys deposited from solutions containing various additives. (b) Magnified view of the area of 0–14 mass% of the Ni content.
変則型共析となる領域のNi含有率を拡大した図をFig.6(b)に示す。50~500 A·m-2の電流密度域では,光沢剤を添加すると総じてNi含有率は若干低下した。しかし,PQ, PQ+QAを添加した溶液では,電流密度が1000 A·m-2以上になるとNi含有率が増加するという特徴的な挙動が認められた。
3・2 電析膜の外観,微細構造に及ぼす光沢剤の影響Fig.7に種々の光沢剤を含む溶液から200, 2000 A·m-2で得られたZn-Ni合金電析膜の外観を示す。なお,一部の供試材については,対面に置いた文字を撮影時に反射させたものを示しており,その文字が明瞭になるほど,光沢度が高いことを表している。光沢剤が無い場合,何れの電流密度においても電析膜は灰色で無光沢であった。QAを添加しても無添加の場合とほぼ同様であり,PQを添加すると2000 A·m-2において光沢が生じ,PQ+QAの添加で光沢は更に顕著となった。IMEを添加した場合には表面に光沢ムラが見られた。

Appearance of Zn–Ni alloy films deposited from solutions containing various additives. (Online version in color.)
Fig.8に中電流密度200 A·m2(Znの平衡電位より卑で電荷移動律速の領域)にて得られた電析膜の表面SEM像を示す。なお,200 A·m2は,変則型共析の領域にあり,光沢剤の有無,種類に関わらず電析膜のNi含有率は7.1~8.6 mass%であり,供試材毎の差は小さい(Fig.6(b))。光沢剤を含まない溶液から得られた電析膜(a)には,0.2 μm前後の粒状の結晶が見られた。電析膜(a)と比較してQA(b),PQ(c),PQ+QA(d)添加により結晶が微細化した。特にQA(b)添加による微細化が顕著であった。IMEを添加すると(e),平滑部の上に数μmサイズの大きな粒状結晶が見られた。この大きな粒状結晶は微細な結晶の集まりと考えられる。

SEM images of the Zn–Ni alloy films deposited at 200 A∙m−2 from the solution containing various additives. [(a) Additive-free, (b) QA, (c) PQ, (d) PQ + QA, (e) IME]
Fig.9に各種光沢剤を含む溶液において200 A·m-2で得られた電析膜(Ni含有率7.1~8.6 mass%)のX線回折図形を示す。光沢剤がない場合(a),メインピークはη-Zn相に由来するものであり,γ相(Ni2Zn11の金属間化合物)に由来する弱いピークも見られた。光沢剤QAを添加しても(b),無添加の場合と同様の傾向を示したが,γ相のピークが無添加の場合より強くなった。PQを添加すると(c),基板のFe以外は,γ相のピークのみとなり,η-Zn相のピークは見られなかった。PQ+QA(d),IME(e)を添加した場合も,PQを添加(c)した場合とほぼ同様の傾向を示した。電析膜のNi含有率は,光沢剤がない場合,QAを添加した場合でそれぞれ,8.0, 8.6 mass%であるのに対して,PQ, PQ+QA, IMEを添加した場合はそれぞれ7.1, 7.3, 7.8 mass%となっており,PQ, PQ+QA, IMEの添加では電析膜のNi含有率が低下するにも関らず,γ相のみが形成された。

X-ray diffraction patterns of the Zn–Ni alloy films deposited at 200 A∙m−2 from the solution containing various additives. [(a) Additive-free, (b) QA, (c) PQ, (d) PQ + QA, (e) IME] (○ Fe PDF # 65-4899, ● Zn[η] PDF # 87-0713, and ★ Ni2Zn11[γ] PDF # 65-5310) (Online version in color.)
Fig.10に高電流密度2000 A·m2(Znの平衡電位より卑でイオン拡散律速の領域)にて得られた電析膜の表面SEM像を示す。2000 A·m2にて得られた電析膜のNi含有率は6.3~9.3 mass%であった(Fig.6(b))。光沢剤を含まない溶液から得られた電析膜(a)は1 μm前後の粒状結晶から構成された。QA(b)を添加すると結晶が粗大化したが,PQ(c)を添加すると,結晶は微細となり,PQ+QA(d)を添加すると結晶は更に緻密となり平滑な表面形状を示した。IMEを添加すると(e),結晶は微細となったが,若干凹凸が見られた。ところで,光沢剤を含まない溶液からの電析膜の結晶サイズは高電流密度2000 A·m-2で1 μm前後(Fig.10(a))であるのに対して,中電流密度200 A·m-2では0.2 μm前後(Fig.8(a))と電流密度が高い方が結晶が大きくなった。通常,電流密度が高くなると核生成が優先し,結晶が微細化するが本研究の結果は逆の傾向を示した。Zn電析において,Zn2+イオンの拡散律速の条件下では,電析物の凸部に電流が集中し結晶サイズが大きくなることが報告されている38)。本研究の2000 A·m-2では,Zn, Ni析出がZnO22-, Niイオンの拡散律速となっており(Fig.1-3),このため結晶サイズが大きくなったと考えられる。

SEM images of the Zn–Ni alloy films deposited at 2000 A∙m−2 from the solution containing various additives. [(a) Additive-free, (b) QA, (c) PQ, (d) PQ + QA, (e) IME]
Fig.11に各種光沢剤を含む溶液において2000 A·m-2で得られた電析膜(Ni含有率6.3~9.3 mass%)のX線回折図形を示す。光沢剤がない場合(a),メインピークはη-Zn相に関するものであり,わずかにγ相(Ni2Zn11の金属間化合物)に関するピークも見られた。QAを添加すると(b),γ相のピークが主となりη-Zn相に関するピークも見られた。PQを添加すると(c),γ相のピークが主となりわずかにη-Zn相に関するピークも見られたが,PQ+QA添加では(d),基板のFe以外は,γ相のみのピークとなり,η-Zn相のピークは見られなかった。IMEを添加すると(e),γ相のピークが主ではあったが,η-Zn相に関するピークも見られた。なお,電析膜のNi含有率は,光沢剤がない場合,6.7 mass%であるのに対して,QA, PQ, PQ+QA, IMEを添加した場合はそれぞれ6.6, 8.0, 9.3, 6.3 mass%であった。

X-ray diffraction patterns of the Zn–Ni alloy films deposited at 2000 A∙m−2 from the solution containing various additives. [(a) Additive-free, (b) QA, (c) PQ, (d) PQ + QA, (e) IME] (○ Fe PDF # 65-4899, ● Zn[η] PDF # 87-0713, and ★ Ni2Zn11[γ] PDF # 65-5310) (Online version in color.)
以上のFig.9, 11の結果より,200, 2000 A·m-2で得られた電析膜は共に,光沢剤がない場合は,主にη-Zn相から構成されるが,PQ, PQ+QA, IMEを添加すると主にγ相から構成されることが分かった。QA添加の場合は,200 A·m-2に比べ2000 A·m-2で得られた電析膜の方がγ相が優勢となったが,無添加およびQA以外の光沢剤を添加した場合は,γ相の形成に及ぼす電流密度の影響は特に見られなかった。
アルカリジンケート浴からのZn-Ni合金電析挙動,電析膜の形態に及ぼす光沢剤の影響をまとめた結果をTable 3に示す。PQを添加すると,Zn電析の拡散限界電流密度が出現し,QAを共存させるとその拡散限界電流密度が低下した(Fig.2)。また,PQ,PQ+QAを添加するとNiイオンの拡散律速によりNi部分電流密度が低くなる領域が見られた(Fig.3)。すなわち,今回検討した光沢剤PQには,電解液中のZnO22-, Niイオンの拡散を抑制する効果があり,その効果はQAが共存すると更に顕著となった。一方,IMEは,電荷移動過程が律速となるZn部分電流密度100-300 A·m-2の領域およびNi部分電流密度10-20 A·m-2の領域において,Zn,Niの析出を抑制した(Fig.2,3)。すなわち,IMEには,Zn-Ni合金電析における電荷移動反応を抑制する効果が見られた。電析挙動が正常型から変則型に移行する転移電流密度,合金電析の電流効率,電析膜の組成,電析膜の形態に及ぼす光沢剤の影響はその種類により異なることが分かった。以下,その要因について低電流密度域(Znの平衡電位より貴で正常型共析の領域),中電流密度域(Znの平衡電位より卑で電荷移動律速,変則型共析の領域),高電流密度域(Znの平衡電位より卑でイオン拡散律速の領域)毎に考察する。
| QA | PQ | PQ + QA | IME | |
|---|---|---|---|---|
| Suppression effect | Charge transfer | Diffusion of ions | Diffusion of ions | Charge transfer |
| Transition C.D. | Decrease | Decrease | Decrease | Decrease |
| iLim of Zn | Not affected | Decrease | Decrease | Not affected |
| Ni % in deposit at C.D. < 1000 A∙m−2 at C.D. > 1000 A∙m−2 | Not affected Not affected | Decrease Increase | Decrease Increase | Decrease Decrease |
| Current Efficiency at C.D. < 1000 A∙m−2 at C.D. > 1000 A∙m−2 | Not affected Increase | Decrease Significantly decrease | Decrease Significantly decrease | Significantly decrease Decrease |
| Morphology at 2000 A∙m−2 | Coarsening | Smooth | Significantly Smooth | Smooth |
本研究のZn-Ni合金電析における転移電流密度は,光沢剤が無い場合は50~100 A·m-2であるのに対して,光沢剤を添加した場合はその種類に関わらず20~50 A·m-2となり,光沢剤の添加により大きく低下した(Fig.6(a))。ここで,Zn-Ni合金電析における転移電流密度は,水素発生が抑制されるほど低くなることが報告されている39–42)。H+の還元反応は吸着中間体Hadを経由した多段階還元機構により進行し,Hadが吸着できるサイトが制限されているため,Zn(OH)2が形成されると水素発生が抑制されることが報告されている39–42)。また,光沢剤としてIMEを添加すると水素発生が抑制され,転移電流密度が低下することも報告されている21–26)。
Znの平衡電位より貴な領域では水素発生は,PQ, PQ+QA添加により抑制されていることが分かる(Fig.4)。これは,Hadが吸着できるサイトが制限されているためZn(OH)2,IMEと同様にPQ, PQ+QAが水素発生を抑制すると考えられる。Zn-Ni合金電析においてPQ, PQ+QAを添加すると水素発生が抑制されるため,転移電流密度は低下したと考えられる。しかしながら,QA添加では,Znの平衡電位より貴な電位域において水素発生がほとんど抑制されていないにも関わらず(Fig.4),転移電流密度はPQ, IMEを添加した場合と同様に低下した。また,光沢剤の種類により水素発生の抑制の程度が異なるにも関わらず,光沢剤を含む溶液からの転移電流密度はほぼ同一となった(Fig.6(a))。この要因については現状不明である。
ところで,Fig.2に示すように光沢剤無しおよびQAを添加した溶液において,Znの平衡電位より貴な-0.9 V前後においてもZnが顕著に析出しており,見掛け上ZnのUnderpotential co-depositionが生じた。Zn-Ni合金電析におけるZnのUnderpotential co-depositionは,電析により安定な金属間化合物Ni5Zn21が形成され,電析膜のZnの活量係数がかなり小さくなるため生じることが報告されている42–45)。すなわち,ZnのUnderpotential co-depositionが生じるためにはNiの共析が必須となり,本研究においては,光沢剤無しおよびQAを添加した溶液においてZnの平衡電位より貴な-0.9 V前後においてもNiの析出が顕著であるため,ZnのUnderpotential co-depositionが進行したと考えられる。
4・1・2 中電流密度域(Znの平衡電位より卑で電荷移動律速,変則型共析の領域)Zn-Ni合金電析における電流効率に及ぼす光沢剤の影響については,PQ, IMEは,Zn, Ni電析の両方を抑制しており(Fig.2, 3),このため変則型共析の領域で電流効率が低下したと考えられる(Fig.5(a))。Znの部分電流密度300 A·m-2以下の電流密度域,すなわちZn電析の電荷移動過程律速の領域では,何れの光沢剤においてもZn電析に対する抑制効果がみられ,その抑制効果はIMEが最も大きかった(Fig.2)。全電流密度50~500 A·m-2の電荷移動過程律速の領域で,IMEを添加すると電流効率が最も低下したのは(Fig.5(a),(b)),Zn電析に対する抑制効果が最も大きいためと考えられる。
一方,電析膜組成に及ぼす光沢剤の影響については,PQ, PQ+QAを添加すると,Ni含有率は100~500 A·m-2において低下している(Fig.6(b))ことからNi析出の方がより強く抑制されることが分かる。光沢剤としてIMEを添加するとNi含有率が低下することが既に報告されている21–26)。Ni電析において中間体NiOHadが吸着できるサイトが制限されていると仮定すれば,IMEを添加した場合,その吸着により限定されたNiOHadの吸着サイトが封鎖され,Ni電析の方がより強く抑制されると考察されている21–26)。PQ,PQ+QAの添加においても同様のことが推察される。
4・1・3 高電流密度域(Znの平衡電位より卑でイオン拡散律速の領域)Znの部分電流密度300 A·m-2以上の高電流密度域では,光沢剤がない場合,Zn電析はZnO22-イオンの拡散律速となっており,その領域ではIME,QAによる分極効果が見られなくなった(Fig.2)。これは,IME,QAには,ZnO22-イオンの拡散を抑制する効果がないためと考えられる。それに対してPQ添加浴では,Znの部分電流密度200 A·m-2前後でZn析出が拡散限界電流密度に到達しており(Fig.2),PQはZnO22-イオンの拡散を抑制していることが分かる。PQにQAを加えるとZn析出の拡散限界電流密度は更に低下しており,PQとQAにはZnO22-イオンの拡散を抑制する相乗効果が見られた。Ni電析に及ぼす光沢剤の影響についても,Zn電析とほぼ同様の傾向が見られた(Fig.3)。PQ, PQ+QAを添加するとZn, Ni析出がZnO22-, Niイオンの拡散律速に到達し易くなっており(Fig.2, 3),このため1000 A·m-2以上の高電流密度域では電流効率がより低下したと考えられる(Fig.5)。なお,Znの平衡電位より卑な領域において,QAを添加した溶液では,水素発生が抑制されていた(Fig.4)。QAを添加した溶液で200~2000 A·m-2の中電流密度および高電流密度域においてZn-Ni合金電析の電流効率が増加した(Fig.5(a))のは,水素発生が抑制されるためと考えられる。
PQ,PQ+QAを添加した溶液では,電流密度が1000 A·m-2以上になると電析膜のNi含有率が増加するという特徴的な挙動が見られた(Fig.6(b))。これは,Niに対して優先析出するZnの方が先にZnO22-イオンの拡散限界となりNi析出はまだ拡散限界電流密度に到達していないため(Fig.2, 3),電流密度の増加に伴い,電析膜のNi含有率は増加したと考えられる。PQには,溶液中のイオンの拡散を抑制する作用があるため,このような電流密度の増加に伴いNi含有率が増加するという特徴的な挙動が生じたと考えられる。このPQ,PQ+QAの添加によりZnO22-イオンの拡散が抑制される挙動は,ジンケート浴からの純Znめっきにおいて報告されているものと同一であり27–30),Zn-Ni合金電析においても同様の傾向が見られた。ZnO22-イオンの拡散に及ぼすPQとQAの相乗効果の要因については,これまでに報告されておらず不明である。
PQは直鎖状高分子であり,QAは第四級アンモニウム塩の単体である。分子量の大きいPQは複数の吸着座を持ち陰極面の広いサイトに渡り吸着するのに対して,分子量の小さいQAは,局所的なサイトに吸着することが予想される。そのため,PQの吸着サイトの隙間にQAが吸着して添加剤の被覆率が増加している可能性がある。添加剤の被覆率が増加する,すなわち添加剤の濃度が高くなると仮定すれば,拡散層を含む陰極界面での溶液の粘度が上昇し拡散層でのイオンの拡散が抑制されると説明できる。
4・2 Zn-Ni合金電析膜の微細構造に及ぼす光沢剤の影響拡散限界電流密度下での電析では,通常,電析膜は粒状またはデンドライト状となることが報告されているが46),本研究のPQ+QAを添加した溶液からの電析では,ZnO22-イオンの拡散限界電流密度下(2000 A·m-2)での電析にも関わらず,平滑な外観を呈した(Fig.10)。PQ+QAは,合金電析における電荷移動過程を抑制することに加えて,溶液中のZnO22-, Niイオンの拡散を抑制している(Fig.2, 3)。その結果,電析膜の結晶成長が抑制され,核生成速度が相対的に速くなり,結晶が微細になったと考えられる。電荷移動過程を抑制するIMEを添加した場合も2000 A·m-2では,無添加の場合より平滑になったが(Fig.10),PQ+QA添加ほどではなかった。電析膜の平滑性向上には,溶液中のイオンの拡散抑制も寄与していると考えられる。
一方,電析膜の相構造については,光沢剤を添加すると,電析膜のNi含有率に関わらず,γ相が形成され易くなった(Fig.9, 11)。特に電析の過電圧を増加させるPQ, IMEを添加するとその傾向が顕著であった。Zn-Ni系2元系平衡状態図47)によると室温でのγ相の安定領域はNi 12.8~16.5 mass%である。PQ, IMEを添加した溶液から200 A·m-2にて得られた電析膜は,Ni含有率が7.1, 7.8 mass%であるにも関わらずγ単相となり,平衡状態図から予想される相とは異なっている。γ相の安定領域のNiよりも少ないNi含有率でγ相単相になる原因としては,γ相にZnが固溶していることが考えられるが詳細は不明である。電析においては,結晶化過電圧が高くなる,すなわち結晶化過程が抑制されると,還元された吸着原子が過飽和の状態で結晶化されるため急冷合金に類似した非平衡相(あるいは高温相)の膜が得られることが報告されている48)。光沢剤を添加すると電荷移動過程に加えて結晶化過程を抑制することが報告されている49)。本研究においては,光沢剤の添加により電析の結晶化過電圧が増加するため,還元されたZnとNiの吸着原子(Znad, Niad)がより過飽和になり,状態図とは異なる組成域でγ相が形成され易くなったと推察される。
各種光沢剤を含むアルカリジンケート浴(ZnO 0.15 mol·dm-3, NiSO4·6H2O 0.016 mol·dm-3, N(CH2CH2OH)3 0.34 mol·dm-3, NaOH 2.5 mol·dm-3, 303 K)からのZn-Ni合金電析挙動とその微細構造を調べた結果,以下のことが分かった。電析挙動が正常型から変則型に移行する転移電流密度は,光沢剤の添加により低下した。光沢剤の種類により水素発生の抑制の程度が異なるにも関わらず,光沢剤を含む溶液からの転移電流密度はほぼ同一となった。合金電析の電流効率は,Zn電析を抑制する効果がある光沢剤を添加すると大きく低下した。光沢剤は,Zn電析よりNi電析の方をより強く抑制するため,電析膜のNi含有率は,光沢剤を添加すると低下した。第四級アンモニウムカチオンが直鎖状に結合した高分子(PQ)を添加すると,溶液中のZnO22-, Niイオンの拡散が抑制され高電流密度域では電流密度の増加に伴い電析膜のNi含有率が増加するという特徴的な挙動が見られた。これは,Niに対して優先析出するZnの方が先にZnO22-イオンの拡散限界となった一方で,Ni析出は拡散限界に到らなかったためと考えられる。PQとベンゼン環を含む第四級アンモニウム塩を併せて添加すると,ZnO22-イオンの拡散限界電流密度下での電析において,膜の結晶は緻密となり平滑な表面形状が得られた。電析の過電圧を増加させる光沢剤を添加すると,電析膜のNi含有率に関わらず,γ相(Ni2Zn11金属間化合物)が形成され易くなった。