2022 Volume 62 Issue 12 Pages 940-945
2022 Volume 62 Issue 12 Pages 940-945
症例は53歳女性である.出生時に肺動脈狭窄と単心室症を合併したfalse Taussig-Bing奇形と診断された.手術は行われず,成人期まで保存的に加療されていた.二次性多血症と再発性脳梗塞の既往があり,抗血小板薬と抗凝固薬を内服していたが,4回目の脳梗塞で入院した.本患者のチアノーゼを伴う心奇形では,右左シャントを有し,凝固異常も伴うために奇異性脳塞栓症のリスクが高く,二次性多血症も有することから,病態を考慮しワルファリンとアスピリンを併用する方針とした.治療の進歩により,成人心奇形の患者は増加しており,これらの症例の脳梗塞予防については,今後更なる検討が必要と考えた.
The case was a 53-year-old woman. At birth, she was diagnosed with a false Taussig-Bing anomaly with pulmonary artery stenosis and a single ventricle. However, no cardiac surgery was performed, and conservative treatment was continued by a cardiovascular surgeon even after adulthood. Because of secondary polycythemia and a history of multiple cerebral infarctions, she took anti-platelet drugs and anti-coagulants. However, she was admitted with the diagnosis of cerebral infarction for the fourth time. It was considered that the patient was at high risk of paradoxical cerebral embolism due to cardiac malformation with cyanotic congenital heart disease accompanied by coagulation abnormalities. Considering the pathophysiology, we decided to use aspirin in combination with warfarin.
われわれは,false Taussig-Bing奇形,肺動脈弁狭窄,単心室症という複雑心奇形を持ちながら,手術を行うことなく成人まで生存し,心奇形に起因する脳梗塞を発症した症例を経験した.先天性心疾患は出生100人に1人の有病率とされ,心房中隔欠損のような単純心奇形から,本例のような複雑心奇形まであり,脳血管障害のリスクになる.肺動脈弁狭窄を伴うfalse Taussig-Bing奇形を含むファロー四徴症類縁疾患は,新生児期からチアノーゼを生じ,外科治療未施行の場合は1年生存率が75%,3年生存率が60%,10年生存率が30%と言われる1).類似の報告は過去になく,貴重な症例と考え報告する.
患者:53歳,女性,右利き
主訴:思うように言葉が出ない
既往歴:白内障,子宮筋腫.
生活歴:精神発達遅滞なし.無職.喫煙歴なし.
家族歴:特記事項なし.
現病歴:出生時にfalse Taussig-Bing奇形,肺動脈弁狭窄,単心室症と診断された.手術を勧められたが家族が拒否し,姑息手術及び根治手術は行われなかった.肺動脈弁狭窄を合併していたため,肺高血圧症に至らず生存可能であったと考えられ,近医心臓血管外科で保存的加療が継続されていた.脳梗塞発症前から低酸素血症による二次性多血症で,アスピリン100 mg/日の内服が開始された.今回の発症から20年前に1回目の脳梗塞を発症し,ジピリダモール100 mg/日が追加された.19年前に2回目の脳梗塞を発症し,さらにワルファリン2 mg/日が追加された.8年前に3回目の脳梗塞を発症し,上記3剤が継続され,5年前に詳細不明であるがアスピリン100 mg/日が中止され,以降ジピリダモール100 mg/日とワルファリン1 mg/日を内服していた.PT-INRは1.5~2.5の範囲でコントロールされていた.発症日,起床後より言葉がうまく出てこない様子の患者を家族が発見し,救急要請し,当院に搬送された.
診察時所見:身長152.8 cm,体重44.7 kg.体温36.6°C,血圧117/84 mmHg,脈拍62/分・整,SpO2 88%(酸素4 l)であった.以前から在宅酸素療法を行い,酸素2 l投与下で普段からSpO2は70~80%台であった.チアノーゼ,ばち指を認めたが,頸動脈雑音を聴取せず,他一般身体所見に異常はなかった.名前を答えられるが,日付,年齢,場所を答えられず,意識レベルはJapan Coma Scale 2,Glasgow Coma Scale E4V4 M5であった.自発語の減少はなかったが,聴覚理解・復唱の障害を認めた.語性錯語や言語性保続も認めた.聴覚理解が障害されており,失行,失認の正確な評価はできなかった.瞳孔は正円同大で対光反射は両側迅速,眼球運動障害はなく,顔面筋力低下,顔面感覚の左右差はなかった.以前の脳梗塞の後遺症としての構音障害を認めた.粗大な麻痺や四肢の痛覚鈍麻を認めなかった.腱反射は左右差なく正常で,Babinski反射は両側陰性であった.意識障害(年齢と日付),構音障害,失語からNational Institutes of Health Stroke Scaleは4点であった.
検査所見:血液検査ではBNP 2,591.2 pg/mlと上昇を認めた.総蛋白6.5 g/dl,AST 30 IU/l,ALT 13 IU/l,BUN 36 mg/dl,Cr 1.08 mg/dl,Crクリアランス(Cockcroft-Gaultの式)42.49 ml/minと腎機能低下を認めた.LDLコレステロール96 mg/dl,HDLコレステロール39 mg/dl,血糖73 mg/dl,HbA1c 6.0%と脂質異常症や糖尿病を認めなかった.赤血球631×104/μl,Hb 16.9 g/dl,Ht 55%,血小板23.1×104/μlと多血症を認めた.D-dimer 0.5 μg/mlと上昇なく,PT-INR 2.38であった.アンチトロンビンIII(ATIII)活性56%,プロテインC(PC)抗原量41%,PC活性27%,プロテインS(PS)抗原量44%,PS活性54%と低下を認めた.頭部MRIでは,拡散強調画像で左前大脳動脈,左中大脳動脈,左後大脳動脈の血流境界領域に急性期脳梗塞を認めた(Fig. 1A).また,両側の小脳,基底核およびその周囲に陳旧性脳梗塞が散在していた(Fig. 1B).頸動脈超音波検査,MRおよび3D-CTアンギオグラフィーで頸部と頭蓋内主幹動脈に狭窄はなく,ホルター心電図検査で心房細動を認めなかった.経胸壁心臓超音波検査では,出生時からの心奇形である両大血管右室起始,重症肺動脈弁狭窄,肺動脈弁下心室中隔欠損,心房中隔欠損,完全大血管転位,単心室が観察された(Fig. 2A~C).左心室も描出されたが,体循環と肺循環の双方を機能的に右室のみに依存していた.下肢静脈超音波検査で血栓はなかった.

Axial diffusion-weighted images showed the high intensity lesions in the boundary zones between left anterior cerebral artery, middle cerebral artery and posterior cerebral artery, where low signal changes were also demonstrated by ADC map, reflecting acute cerebral infarction (A). Multiple old cerebral infarctions were observed in both anterior and posterior circulation in axial fluid-attenuated inversion recovery images (B).
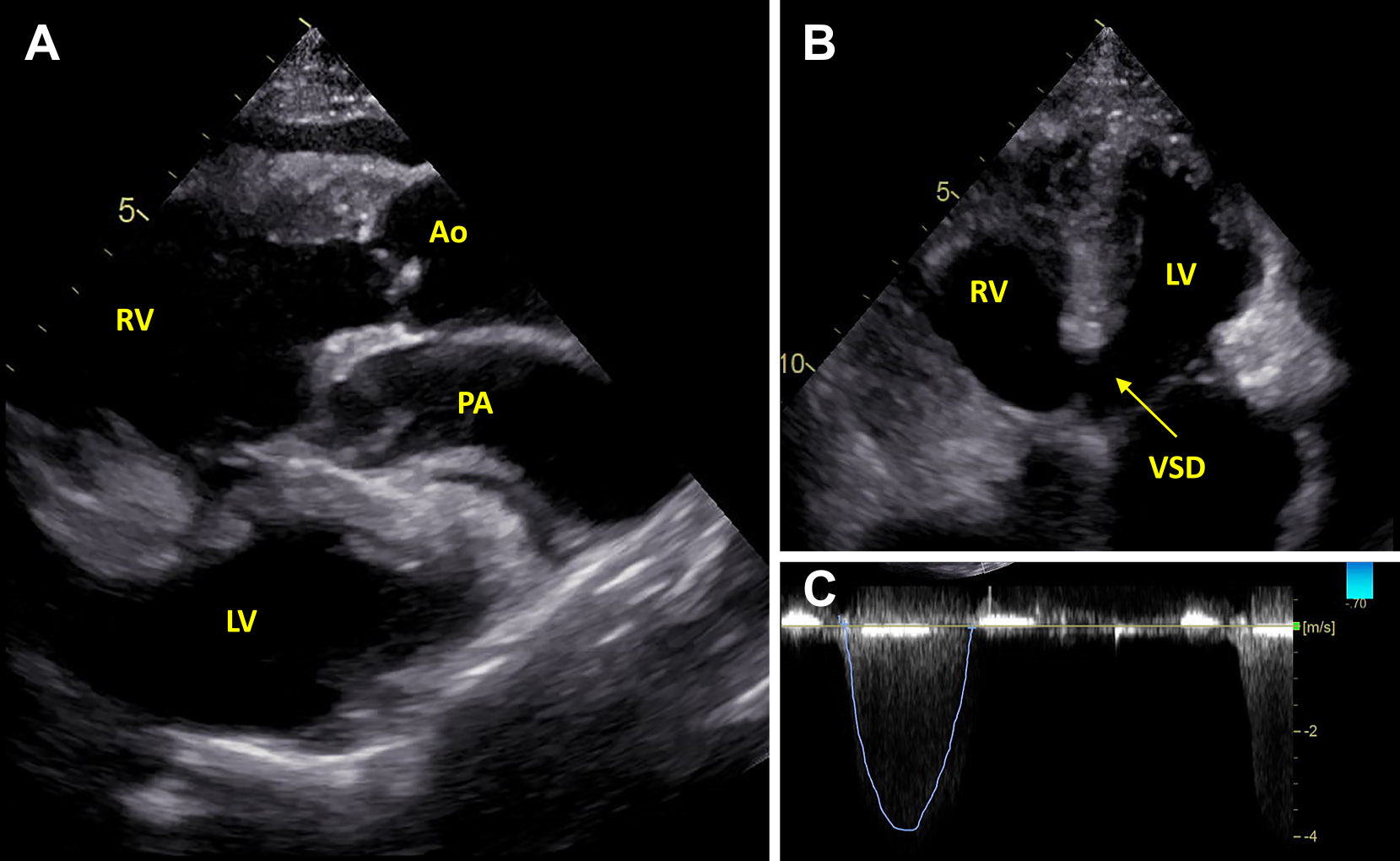
Both the aorta and the pulmonary artery originated from the right ventricle (A). The arrow with dotted line indicated ventricular septal detect, and left ventricle not functioning effectively was observed (B). Echocardiography with Doppler measurement detected the severe pulmonary stenosis (C). Abbreviations, Ao: aorta, LV: left ventricle, PA: pulmonary artery, RV: right ventricle, VSD: ventricular septal defect.
入院後経過:入院当日よりヘパリン10,000単位/日で加療を開始し,数日後にワルファリン内服に切り替えた.多血症に関しては,エリスロポエチン250 mIU/mlと高値で,JAK2 V617F遺伝子解析で遺伝子変異は陰性であり,心疾患に起因する二次性多血症と診断した.治療としては,原疾患の根治は期待できず,瀉血も継続が難しいために,抗血小板薬をジピリダモール100 mg/日から多血症に対して一般的に使用されるアスピリン100 mg/日に変更した.これまでの経過でワルファリン単独では脳梗塞の再発予防が困難であり,脳梗塞再発予防にはワルファリンとアスピリンを併用することが必要と結論した.ワルファリンはPT-INR 1.5~2.5の範囲でのコントロールを目指し,最終的に1.75 mg/日の内服とした.入院当初にみられた感覚性失語は,言語聴覚士によるリハビリテーションにより日常の大まかな言語理解は可能なまでに回復し,入院3週間で退院した.
先天性心奇形を持つ小児では脳梗塞の発症率が高く2),その機序は奇異性脳塞栓が主と考えられている3).単心室症や大血管転位症では特に脳梗塞の頻度が高く4)5),根治術後に新規脳梗塞を認めなくなったとの報告があるため6),心奇形患者の脳梗塞発症には,右左シャント等の解剖学的異常が大きく寄与していると推測される.さらに,先天性心奇形では解剖学的異常に加え,血液凝固異常を伴うとされる.塞栓症の重要な要因になると考えられ7),単心室症の根治術前の患者ではPC,PS,ATIIIといった抗血栓作用を持つ蛋白の血中濃度が健常児や術後の児よりも低下している8).その明確な機序は不明であるが,低酸素血症が大きく関連し,低酸素血症による二次性多血症が血管内ずり応力を高め,血管内皮細胞を活性化し,トロンボモジュリン-PC-PS経路が抑制されるためなどと推定されている9)10).
本例はfalse Taussig-Bing奇形に肺動脈弁狭窄,単心室症を合併し,根治術未施行であった.false Taussig-Bing奇形は両大血管右室起始症の一形態である.両大血管右室起始症は大動脈と肺動脈の二つの大血管のうち,どちらか一方の大血管が完全に,他方の大血管が50%以上右心室から起始する.そして,心室中隔欠損が肺動脈弁下に位置し,大血管転位を合併するものがfalse Taussig-Bing奇形と呼ばれる(Fig. 3A)11).本例では,加えて肺動脈狭窄を伴っていたが,脳梗塞の発症機序を考える上で重要である.すなわち,全身の静脈系から静脈血栓が右心室に流入した場合,肺動脈弁狭窄があることにより,静脈血栓は同じく右心室から起始している肺動脈より大動脈に流入しやすくなると考えられる(Fig. 3B).実際に両大血管右室起始症の症例で,肺血管絞扼術を施行した直後に脳梗塞を生じた報告がある12).また,本例で合併している単心室症のような心奇形では,前記のように解剖学的異常に加え,凝固異常も伴うことが示唆されており10),本例でも実際にPC,PS,ATIIIの低下を認めた.本例は採血時にワルファリンを内服していたため,凝固異常が全て心奇形に起因すると断定することはできない.しかし,ATIIIはビタミンK依存性蛋白ではないため,これら三つの蛋白の低下の原因をワルファリンのビタミンK拮抗作用のみに帰することはできず,本例には少なからず心奇形が関与する凝固異常があると考えた.

Abbreviations, Ao: aorta, ASD: atrial septal defect, BCA: brachiocephalic trunk, CCA: common carotid artery, LV: left ventricle, PA: pulmonary artery, PS: pulmonary stenosis, RA: right atrium, RV: right ventricle, SCA: subclavian artery, TGA: transposition of the great arteries, VSD: ventricular septal defect.
治療に関して,脳卒中治療ガイドライン2021では先天性心疾患を持つ患者の脳卒中に関する記述はなく,定まった治療は確立されていない13).成人先天性心疾患診療ガイドラインでは,チアノーゼ性先天性心疾患患者に脳梗塞が生じた場合,静脈血栓を認めれば奇異性脳塞栓症として抗凝固療法を行い,血栓を認めない場合でも原因不明の再発性脳梗塞をきたしている場合は抗凝固療法が推奨されている14).その根拠には,凝固異常の存在や静脈血栓が生じた場合の奇異性脳塞栓症の発症リスクの高さがあると考えられる.本例では,原因不明の脳梗塞患者において卵円孔開存がどの程度脳梗塞発症へ寄与するかを予測するRisk of Paradoxical embolism(RoPE)スコアが脳梗塞初発時に9点と高値であり15),複雑心奇形により右左シャント量も多く,実際に脳梗塞を再発しており,卵円孔開存を有し,その関与が疑われる塞栓源不明の脳塞栓症(embolic stroke of undetermined sources,以下ESUSと略記)に準じて治療方針を検討することとした.
卵円孔開存症の関与が疑われるESUSにおいて,静脈血栓症を認める場合には通常抗凝固療法を行う16).一方,静脈血栓症を認めない場合,その治療に関するエビデンスは確立していない.脳卒中治療ガイドライン2021でも,抗血小板薬,抗凝固薬,その中でもワルファリン,direct oral anticoagulants(DOAC)の位置づけに明確な優劣はない13).本例は先天性心奇形に起因する凝固異常にも介入が必要という観点から抗凝固薬を選択したが,ワルファリンとDOACの直接比較をした報告はない.卵円孔開存症を有する患者の治療をレビューし,間接的にその有用性を比較した報告ではワルファリンが有用性,安全性とも上回る結果であったが,今後の検討が必要である17).本例では,慢性腎臓病があること,本邦ではDOACは静脈血栓症を認めない場合は適応外使用となることなどから,ワルファリンを選択した.先天性心奇形のある患者にワルファリンを処方する場合,至適PT-INR値は定まっていない13).奇異性脳塞栓症にワルファリンを処方する際,PT-INRが1.5未満となると再発率が増加するという報告があることから,1.5以上,かつ出血リスクを考慮して2.5は超えないように管理することとした18).
さらに,本例では二次性多血症を認めたが,原疾患の根治が望めないため,多血症に対するアスピリンの内服が必要であった19).真性多血症の患者が静脈血栓症を発症した場合,抗血小板薬,抗凝固薬をそれぞれ単剤で投与するか,併用するか,そこに細胞減少療法を併用するかは定まっていないが,抗凝固薬のみでは血栓症の再発予防効果は十分ではないと評価されている20).本例はこれまでワルファリンとジピリダモールの併用下であっても複数回の脳梗塞を起こしていることを考慮し,ワルファリンのみでは脳梗塞予防は不十分と考えた.やや出血のリスクは高くなるものの,抗凝固薬と抗血小板薬を併用することの有用性を示唆する報告があり21),基本的に特定の禁忌がない限り,すべての真性多血症患者に低用量アスピリンによる抗血小板療法が推奨され22),骨髄増殖性疾患患者の門脈血栓症において,出血が起きるまではワルファリンとアスピリンの併用を行い,出血が起きた時点でアスピリンを中止するという対応をしている報告もある23).よって,本例では,これまでPT-INRが不安定になることなくワルファリンを長期に投与できており,抗血小板薬を併用しながらも出血合併症をきたしたこともなかったため,現時点ではワルファリンにアスピリンを併用することは,出血のリスクを考慮しても血栓症再発の予防のためには許容されると考えた.
生命予後不良な複雑先天性心奇形を持ちながら成人まで生存し,脳梗塞を発症した症例を経験した.治療については既存のガイドラインでは不十分であり,チアノーゼを伴う心奇形では,右左シャントを有し,凝固異常も伴うために奇異性脳塞栓症のリスクが高く,二次性多血症も有する特殊な病態を考慮して治療方針を決定した.外科的・内科的治療の発展により,先天性心奇形を持つ成人患者は増えつつある24).心奇形の解剖学的異常という脳梗塞のリスク因子は手術を行うことである程度修飾可能であるが,心奇形術後の成人であっても脳梗塞発症率は一般人口よりも高い25).これは,不整脈の合併,長期の瀉血による鉄欠乏13),そして長期の低酸素血症による内皮細胞障害17)など複数の因子が重なるためと考えられ,心奇形では複合的因子により脳梗塞のリスクが高いと考えられる.今後,本例のような先天性心疾患を伴う脳梗塞を診療する場面は増えると予想される.脳神経内科医も,先天性心奇形の血行動態を理解し,治療方針を個々に検討することが必要であると考えた.
謝辞:本患者の診療にあたり,福島県立医科大学循環器内科学講座の八重樫大輝先生,岩谷医院の岩谷文夫先生に終始適切な助言を賜りました.深謝いたします.
※著者全員に本論文に関連し,開示すべきCOI状態にある企業,組織,団体はいずれも有りません.