2023 Volume 63 Issue 8 Pages 505-512
2023 Volume 63 Issue 8 Pages 505-512
72歳男性.約10か月前から電子マネーカードのチャージや携帯電話の掛け方が分からないなどの症状が出現した.入院時には近時記憶障害,構成障害,失書,失計算など広汎な高次脳機能障害を認めた.頭部MRI T2*強調画像で脳表面をびまん性に縁取る低信号を認め,古典型脳表ヘモジデリン沈着症(cortical superficial siderosis,以下cSSと略記)と診断したが,小脳や脳幹へのヘモジデリン沈着がめだたない点が特徴的であった.123I-IMP-SPECT検査で左優位に前頭頭頂葉の血流低下を認めた.脳表限局性微小出血や脳表へのヘモジデリン沈着を認め,probable CAA(cerebral amyloid angiopathy:脳アミロイドアンギオパチー)と診断,CAAに伴うcSSと考えた.
A 72-year-old male developed neurological symptoms such as difficulty in charging his electronic money card and making his mobile-phone call ten months before admission. On admission, neurological examination revealed extensive higher brain dysfunction such as impairment in recent memory, executive function disorders, constructional disturbance, agraphia and acalculia. Brain MRI revealed a low intensity lesion on the surface of the cerebral cortex diffusely and symmetrically on T2*-weighted images. MRI images are consistent with superficial siderosis. However, the lack of hemosiderin deposition in the brain stem and cerebellar hemisphere was atypical of the classical type of superficial siderosis. 123I-IMP-SPECT revealed hypoperfusion dominantly in the left hemisphere, particularly in the left frontal and parietal lobes. According to the Boston criteria, the patient with the cerebral microbleeds and cortical superficial siderosis was diagnosed with probable CAA (cerebral amyloid angiopathy).
広汎な高次脳機能障害を呈した古典型脳表ヘモジデリン沈着症(cortical superficial siderosis,以下cSSと略記)の1例を報告する.古典型cSSにおいて,ヘモジデリンは小脳,聴神経,脳幹や脊髄に沈着を来しやすいとされる1)~3).こうした病態を反映して,小脳性運動失調,感音性難聴,ミエロパチーを呈する例が多く,初発症状としては,小脳性運動失調または感音性難聴が約90%を占めていたとの報告がある4).本例は臨床的には,近時記憶障害,遂行機能障害,構成障害,失書,失計算など広汎な高次脳機能障害を認めたが,小脳性運動失調や難聴はみられなかった.画像上は,頭部MRI T2*強調画像で脳表面を縁取る明瞭な低信号をびまん性・対称性に認めたが,脳幹や小脳へのヘモジデリン沈着はめだたない点が特徴的であった.
症例:72歳,男性
主訴:できないことが増えてきた
既往歴:高血圧症,2型糖尿病.
内服薬:ニルバジピン40 mg/日,シタグリプチンリン酸塩水和物50 mg/日.
教育歴:高校卒業.
生活歴・職業歴:右利き.62歳まで建築業に従事.退職後は毎日自宅の畑で野菜を育てたり,雑草を刈ったりしていた.日常的に書字や計算をする習慣はなかった.
家族歴:類症なし.
現病歴:X−1年夏頃電子マネーカードのチャージの仕方が分からず,買い物のときに現金で支払うようになった.また車のエンジンのかけ方やワイパーの動かし方が分からなくなった.秋頃から携帯電話の掛け方やテレビゲームの操作方法が分からなくなった.X年1月頃からテレビの録画予約ができなくなった.シャツをハンガーに掛けるときに,上下逆に掛けようとすることがあった.日常生活は自立し,物の置き忘れや探し物が増えたことはなかった.5月頃から日付が分からなくなっていることに家族が気づき,X年6月当科外来受診,7月に精査入院した.
一般身体所見に特記すべき所見は認めなかった.神経学的所見では,意識清明,時間の見当識障害がみられた.入院中の前日の検査や面会があったことを忘れることがあり,また,3物品名の遅延再生は難しく,近時記憶の障害がみられた.HDS-R 10点で,時間の見当識,計算,数字の逆唱および遅延再生の項目で減点し,言語流暢性の項目は1語のみ想起した.MMSE 11点で,3段階の口頭命令,復唱および文章書字の項目でも減点した.FAB 5点(概念化1点,行動プログラム1点,把握反応3点)であった.挙手敬礼やおいでおいでなどの口頭指示による慣習的動作は可能で,歯を磨く,櫛で髪をとかすなどの実物なしの身振りも可能であり,観念運動性失行はなかった.はさみや爪切り,箸,歯ブラシと歯磨き粉の使用に問題はなかった.しかし,便箋を封筒に入れて糊で封をするように指示すると,便箋や手に糊を付けようとした.複合的な行為の一部は障害され,観念性失行が疑われた.左右失認や手指失認はなかった.失計算がみられた.着衣ではボタンを掛け違えたり,上下や左右逆にシャツを着ようとすることがあった.立方体の模写や積み木構成は可能であったが,手指肢位模倣はキツネ,ハトが不能であり,構成障害が疑われた.聴理解は良好で,喚語障害はなく,失名辞は認めなかった.書字障害があり,特に平仮名と漢字の書字困難がめだち,自由文は全く書けなかった(Fig. 1A~C).読字や写字は可能であった.礼節は保たれ,性格変化はなく,口尖らし反射,強制把握等の前頭葉徴候はみられなかった.神経学的には,嗅覚低下,耳鳴・難聴なく,その他脳神経に特記なかった.腱反射は正常であり,運動系・協調運動系・感覚系,自律神経系に特記なかった.標準失語症検査では,「仮名・漢字の書字」の項目が0%と著明に低下し,計算の項目も40%と失計算がみられた(Fig. 2).
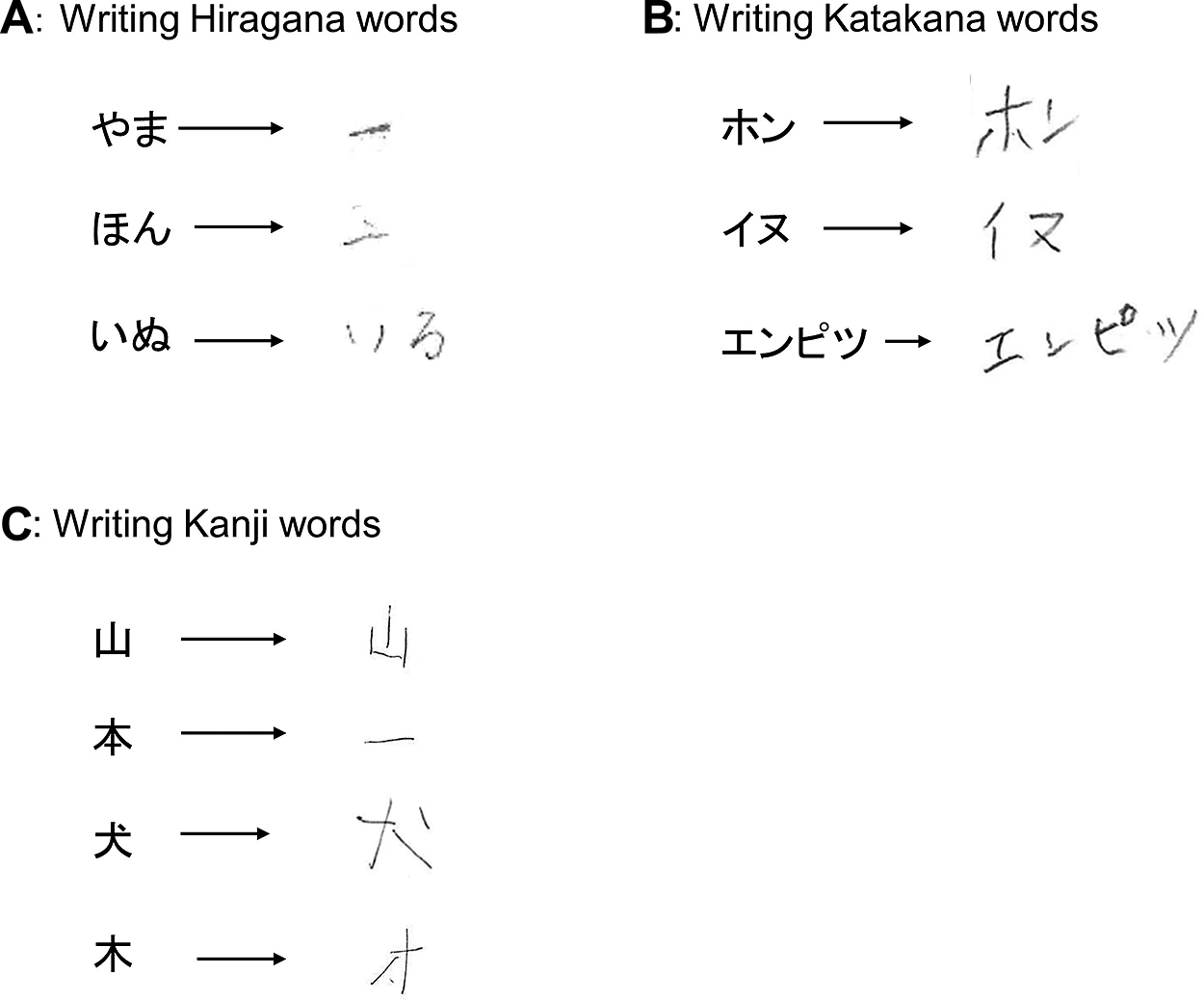
He had more difficulty in writing Hiragana words (A) than Katakana words (B). He had difficulty in writing Kanji words (C).

He had severe difficulty in the items on writing Hiragana as well as Kanji words on admission. While the SLTA questions for explaining picture stories and sentence repetition got worse, the items for writing Kana and Kanji words improved three months and a year after admission.
検査所見:血液生化学に特記なかった.HbA1cは5.6%,甲状腺機能は正常で,ビタミンB1,ビタミンB12,葉酸の欠乏はみられなかった.ApoE遺伝子型はε3/ε3型であった.髄液検査では細胞数3/μl,髄液蛋白45 mg/dlで軽度高値であった.髄液中のフェリチンは19.4 ng/ml(正常値12 ng/ml以下)と高値であった.髄液Aβ40 3,073 pg/ml(参考値4,003 ± 1,185),髄液Aβ42 305 pg/ml(参考値838 ± 253),Aβ40/Aβ42比10.1(参考値4.91 ± 1.13)であり,髄液Aβ42値が低値であった.髄液細胞診ではシデルファージは認めなかった.頭部MRIでは,全般性に大脳皮質の萎縮がめだち,右優位の海馬の軽度萎縮もみられた.皮質下に白質病変を認めた.T2強調画像で脳表を縁取るような線状の低信号を認めた.T2*強調画像では大脳皮質に沿って広範にほぼ左右対称性にヘモジデリン沈着を認め,脳表には ‘track-like appearance’ と呼ばれる特徴的な二重線状の信号変化がみられた.前頭頭頂葉や側頭葉に比べて,後頭葉へのヘモジデリン沈着は軽度であり,脳幹や小脳へのヘモジデリン沈着はめだたなかった.皮質や皮質下白質には脳表限局性微小出血が散在していた.また円蓋部などの脳溝に皮質性くも膜下出血(cortical subarachnoid hemorrhage,以下cSAHと略記)と思われる信号変化を認めた(Fig. 3).拡散強調画像では新鮮梗塞巣は認めず,造影MRIではあきらかな造影効果をみとめなかった.MRAでは特記なかった.MRI voxel-based specific regional analysis system for Alzheimerʼs disease(VSRAD)ソフトウェアをもちいvoxel-based morphometry(VBM)画像の検討を行ったところ,前頭頭頂葉を中心にT2*強調画像でヘモジデリン沈着がめだつ領域を中心に皮質萎縮を示唆する所見を認めた.また,AD用の設定された関心領域(ROI)のZ score 0.77と算出され,ADにみられる特異的な領域の萎縮は明らかではなかった(Fig. 4A).また,前部帯状回の萎縮が示唆された(Fig. 4B).全脊髄MRIではあきらかな脳脊髄液貯留や血管奇形・腫瘍性病変を認めず,T2強調画像およびT2*強調画像でもヘモジデリン沈着は認めなかった.123I-IMP-SPECT検査では,左優位に大脳半球の血流低下を認め,特に前頭葉から頭頂葉にかけての血流低下がめだった.Three-dimensional stereotactic surface projections(3D-SSP)画像では左優位に前頭葉の血流低下部位を認めた.楔前部,後部帯状回や小脳の血流低下はみられなかった(Fig. 5).
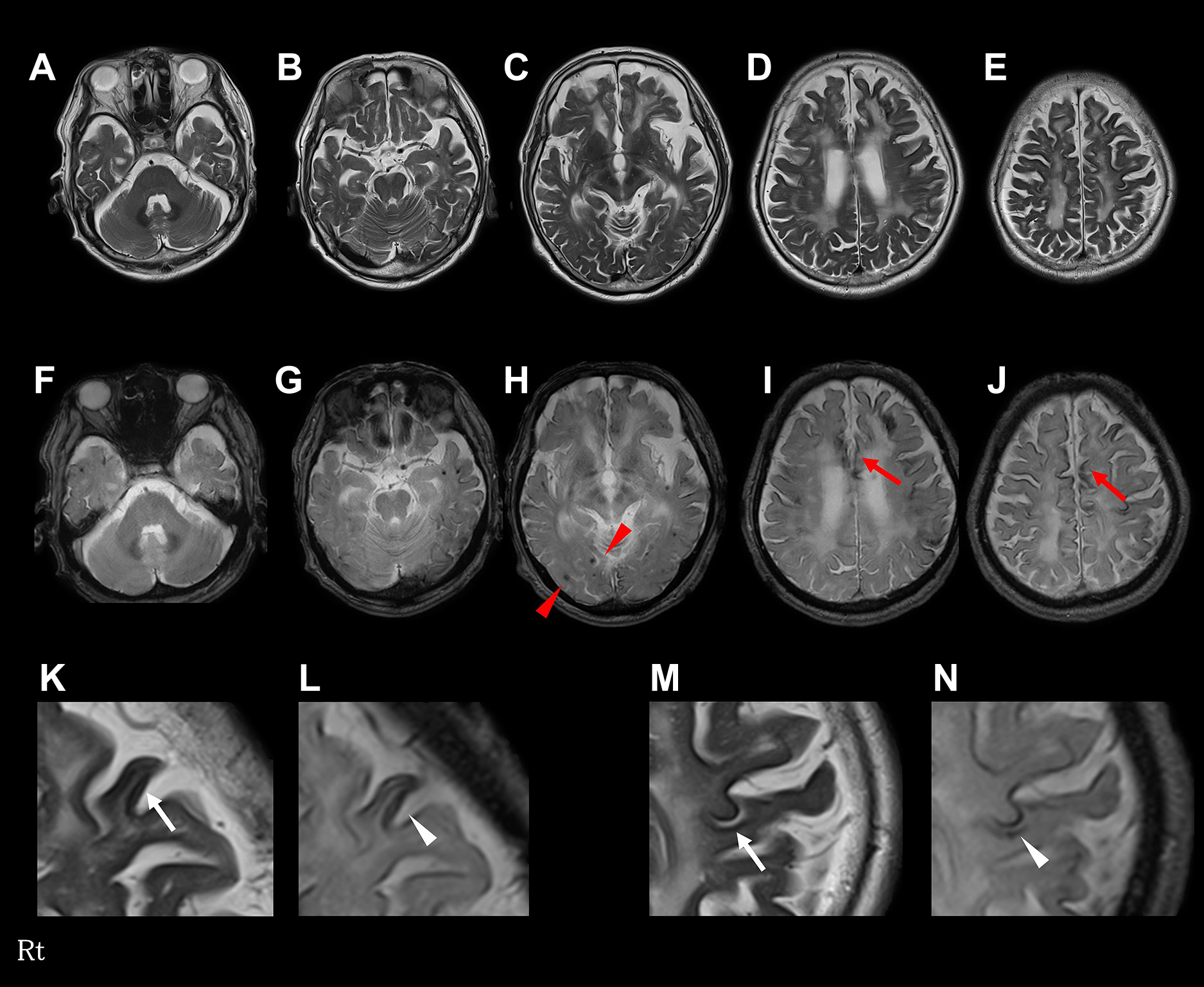
Axial T2-weighted brain MRI (3 T; TR 4,000 ms, TE 98 ms) (A–E, K, M) demonstrates a hypointense band surrounding the surface of the cerebral cortex (K, M, white arrows), together with mild cerebral cortex atrophy. Gradient echo T2*-weighted imaging (3 T; TR 615 ms, TE 12 ms) (F–J, L, N) of the axial sections shows low intensity lesions suggestive of hemosiderin deposition on the cerebral cortex (H–J), less on the surface of the brainstem and cerebellum (F, G). T2*-weighted imaging reveals convexity subarachnoid hemorrhage (I, J, red arrows). T2*-weighted imaging reveals characteristic bilinear ‘track-like’ appearance on the surface of the cerebral cortex suggestive of cortical superficial siderosis (L, N, white arrowheads).

Cortical atrophy was observed predominantly on the frontal and parietal lobe, less on the medial temporal lobe (A: axial view). In particular, the atrophy of the anterior cingulate gyrus was noticeable (B: 3D image).
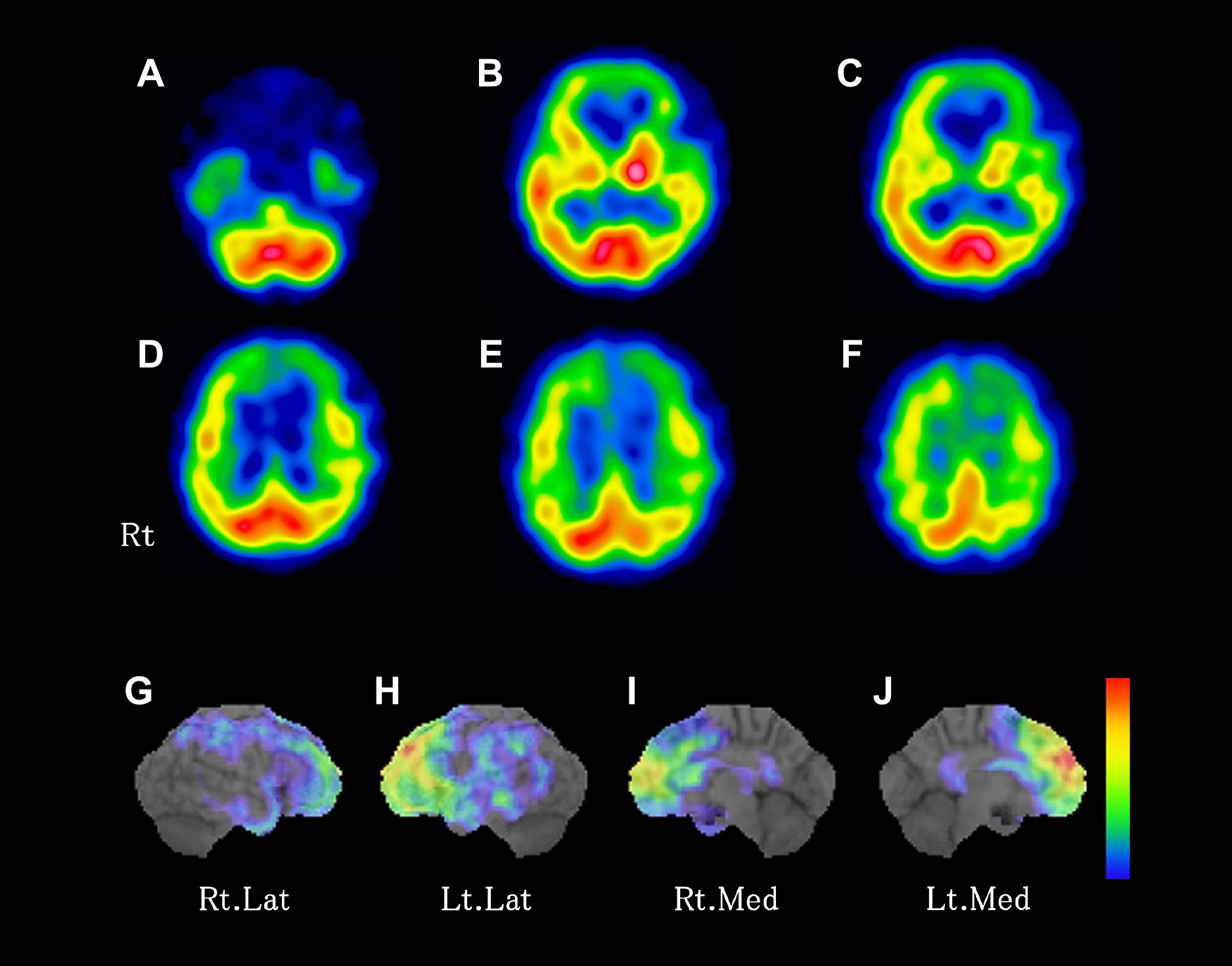
Cerebral blood flow decreased dominantly in the left hemisphere, particularly in the frontal and parietal lobes (A–F). Three dimensional-SSP SPECT images showed uptake reduction dominantly in the left frontal lobe (G–J).
臨床経過:本例は古典型cSSの診断基準の臨床症候のうち認知機能障害を満たし,また頭部MRI T2*強調画像にて脳表面を縁取る明瞭な低信号をびまん性,対称性にみとめることから古典型cSSの診断基準4)を満たした.しかし,小脳や脳幹など後頭蓋窩への沈着はめだたなかった.脳表限局性微小出血および脳表のヘモジデリン沈着を認め,また,他に原因となりうる病態は否定的であり,Modified Boston Criteria5)に基づき,probable CAA(cerebral amyloid angiopathy:脳アミロイドアンギオパチー)と診断した.脊髄腫瘍や硬膜欠損などcSSの原因となりうるその他の疾患は認めず,本例はCAAに伴うcSSと診断した.カルバゾクロム酸90 mg/日,トラネキサム酸1,000 mg/日の内服を開始した.X年10月(初回検査から3か月後)およびX+1年7月(初回検査から1年後)に標準失語症検査を行ったところ,失書の項目の改善がみられた一方で,語想起などの項目が悪化していた(Fig. 2).X+1年7月の頭部MRIでは脳表へのヘモジデリン沈着のあきらかな増悪はみられなかった.
本例は,広汎な高次脳機能障害を呈した古典型cSSの1例である.大脳皮質に沿って広範にヘモジデリン沈着を認めたが,小脳や脳幹への沈着はめだたず,小脳性運動失調,感音性難聴がみられない点が特徴的であった.
cSSでは,クモ膜下腔への反復性・持続性の出血により,脳脊髄液中のヘムが増加し,組織毒性のあるフェリチン合成が誘導される.最終的にヘモジデリンが形成され,小脳,脳幹,大脳,脊髄の軟膜下に沈着する.軟膜下へのヘモジデリン沈着は,反応性グリオーシスや脱髄を引き起こし6),神経細胞の機能障害や変性を引き起こす7)~9).こうした病態を反映し,髄液検査では赤血球の増加やキサントクロミー,鉄やフェリチンの上昇が報告されている10)11).特に髄液中のフェリチンは常に上昇しているとの報告があり12),本例では髄液での赤血球の増加やキサントクロミーはみられなかったが,髄液フェリチンが高値であった.また,本例の画像所見では,頭部MRI T2*強調画像での大脳皮質に沿ったヘモジデリン沈着に加え,脳表に ‘track-like appearance’ と呼ばれる特徴的な二重線状の信号変化がみられた.これは,正常のくも膜下腔の信号変化が,隣接する皮質の表層に沈着した線状のヘモジデリンによって両側性に縁取られることによる信号変化であり,慢性的にヘモジデリンが沈着するcSSで特徴的な所見とされる13).
cSSにおいて,小脳はフェリチン合成能の高いプルキンエ細胞層のBergmann gliaを有しているためヘモジデリンが沈着しやすく1)2),脳神経では特に聴神経がヘモジデリン沈着を来しやすいとの報告がある3).また,脳脊髄液に広範に接する脳幹・脊髄にも比較的ヘモジデリン沈着を来しやすい4).cSSは,小脳や脳幹など後頭蓋窩を中心に中枢神経系にびまん性・対称性に病変が生じる古典型と,限局型に分類される.本例は古典型cSSの診断基準5)14)の臨床症候のうち認知機能障害を満たし,また頭部MRI T2*強調画像にて脳表面を縁取る明瞭な低信号をびまん性,対称性に認めることから古典型cSSの診断基準5)14)を満たしたが,脳幹や小脳へのヘモジデリン沈着はめだたなかった点が特徴的であった.山脇らが報告した本邦の全国調査における古典型cSSの臨床症候は,病態を反映して,小脳性運動失調が83%,感音性難聴が74%,ミエロパチーが53%,認知症が23%,などであったと報告しており4),Levyらの270例の文献報告においても類似した頻度であった15).初発症状としては,小脳性運動失調または感音性難聴が約90%を占めていたとしている4).本例は初診時には既に広汎な高次脳機能障害がみられた.しかし,日常的に書字や計算をする習慣はなく,遂行機能障害が徐々に出現しても自宅での生活には支障がなく,病初期には近時記憶障害がめだたなかったため,家族は病的な高次脳機能障害があると考えていなかった.本例のように小脳性運動失調や感音性難聴を来さず,高次脳機能障害を呈するcSSでは,ヘモジデリンが沈着する領域によって様々な高次脳機能障害で発症する症例があり,また,本例のように本人や家族からの病歴と神経学的所見の間に乖離がみられることもあり,詳細な神経診察が必要と考える.
CAAは,クリアランス機構の破綻により血管壁に蛋白質が蓄積するprotein-elimination failure arteriopathiesと称される病態の関与が推定されている.間質液中の一部のAβは血管周囲リンパ排液路を経て髄液へ移行するとされるが,CAAではその排液路の駆動力が低下しAβの髄液移行が減少する16).特に易凝集性のAβ42は老人斑や毛細血管壁での沈着が主となり,髄腔内まで到達しにくくなると考えられる16).本例においても髄液中のAβ42は低値,Aβ40/Aβ42比が高値であり,CAAに伴うAβ42の髄液移行の低下が示唆された.そして,CAAにおけるAβの血管壁への沈着が微小動脈瘤様変化やフィブリノイド壊死を引き起こし,その結果,皮質微小出血やcSAH,脆弱な血管からの漏出によりくも膜下腔に血液が流出し,cSSを引き起こす原因となりうるとされる17).近年cSSの出血源として硬膜欠損部あるいは損傷部付近の脆弱な血管による慢性出血が原因となるduropathyという概念が提唱されている4)18)19)が,本例においては全脊髄MRIであきらかな異常所見は認めず,CAAに伴う皮質微小出血やcSAHが本例のcSSの原因となったと考えた.
本例でみられた円蓋部のcSAHは,cSSとの関与が示唆されており20),またCAAの画像マーカーとされる20).cSAHは軟膜上の破綻した細動脈から漏出した血液が脳溝内に血腫として描出されたものである21).probable CAAと診断した症例を円蓋部のcSAHがみられた群と頭蓋内出血を呈した群の2群に分けて後方視的に検討した報告では,cSSがみられた割合は,頭蓋内出血群(57.7%)に比してcSAH群(88.9%)で高かったと報告した20).この結果は,CAAを有する症例において,円蓋部のcSAHとcSSとの関連を示唆する所見であると報告している20).本例はprobable CAAの診断基準を満たしたが,後頭葉などに脳表限局性微小出血が多発していなかった一方で,円蓋部の脳溝にcSAHと思われる所見がめだち,このことが本例のヘモジデリン沈着が前頭葉にめだった原因と考えた.しかし,CAAの表現型として円蓋部のcSSがめだった一方で,脳表限局性微小出血が乏しかった本例に特徴的な背景に関しては不明である.軽微な外傷などの外的要因や,血管壁へのAβの沈着による脆弱な血管がなんらかの原因により前頭葉にめだった可能性などが考え得るが,今後の症例の蓄積による検討が必要と考える.
認知機能障害を呈したprobable CAAの症例を,cSSの有無で比較検討した報告では,cSSを伴う群では,より重度の認知機能障害を呈し,画像上,楔前部や後部帯状回,側頭頭頂葉や内側側頭葉の萎縮がみられ,アルツハイマー病(Alzheimer’s disease,以下ADと略記)の萎縮パターンに類似していたと報告している22).さらにアミロイドPET検査を施行した症例を検討すると,cSSを伴う群16例全例がアミロイドPET陽性であり,cSSを伴わない群17例中7例(41.2%)に比べて有意にアミロイドPET陽性率が高かったと報告している22).本例はcSSを伴うprobable CAAであり,ADを合併していた可能性はある.しかし,123I-IMP-SPECT検査で後部帯状回や楔前部の血流低下はみられず,MRI VSRADによるVBM画像での前頭葉を中心とした皮質萎縮がみられた領域は,T2*強調画像でヘモジデリン沈着がめだつ領域に一致していると考えた.Papez回路は,海馬,脳弓脚,脳弓体,脳弓柱,乳頭体,視床前核,帯状回へと連絡し,最終的に海馬に戻るという閉鎖回路を構成しており,エピソード記憶の記銘および再生に寄与していると考えられている23)24).本例における近時記憶障害の病巣に関しては,MRI VSRADの結果を考えると,Papez回路のうち,両側帯状回,特に前部帯状回の萎縮が影響していたと考えた.以上から,本例はアミロイドPETを施行していないが,広汎な高次脳機能障害を来し,前頭葉から頭頂葉にかけて血流低下を来した主病態はADではなく,cSSと考えた.本例における髄液中のAβ42低値,Aβ40/Aβ42比高値の所見を含め,本例の病態にADがどこまで関与しているのかは今後さらなる検討を要すると思われた.
APOE ε4は血管壁へのAβの沈着を増強し,AD発症における危険因子の一つである13)25).一方で,APOE ε2は血管壁の破壊性変化や血管炎症のリスクとなり,CAAに関連した脈管障害を促進し,cSSの頻度が高くなる13)26).CAAにcSSを伴う症例は,APOE ε4の頻度が高いとの報告がある22).しかし,本例はAPOE ε3/ε3であり,本例のApoE遺伝子多型と病態の関連は否定的であった.
本報告の要旨は,第109回日本神経学会中国・四国地方会で発表し,会長推薦演題に選ばれた.
※著者全員に本論文に関連し,開示すべきCOI状態にある企業,組織,団体はいずれも有りません.