2024 Volume 64 Issue 1 Pages 17-22
2024 Volume 64 Issue 1 Pages 17-22
レボドパ(levodopa,以下LDと略記)で治療中のパーキンソン病患者.LD/ドパ脱炭酸酵素阻害剤配合剤の変更で動きが悪化した既往があった.入院中,LDからLD/カルビドパ(carbidopa,以下CDと略記)に変更後,悪性症候群様症状(Parkinsonism-hyperpyrexia syndrome,以下PHSと略記)を呈した.LDに戻すと症状が改善した.空腸投与用LD/CDゲル(levodopa carbidopa intestinal gel,以下LCIGと略記)投与後に再びPHSを示した.敗血症と播種性血管内凝固症候群(disseminated intravascular coagulation: DIC)を併発し,血小板減少が遷延した.LDへの薬剤変更とステロイド投与で,病状が改善した.抗PAIgG陽性とLCIGに対する薬剤誘発性リンパ球刺激試験陽性(drug-induced lymphocyte stimulation test: DLST)で,CDに対するII型,IV型の薬剤アレルギーが疑われた.LD製剤変更時の不調の際,薬剤アレルギーを考慮する必要がある.
A 70-year-old male who has medical history of Parkinson’s disease for 26 years admitted to our hospital for trial of levodopa carbidopa intestinal gel (LCIG) therapy because of severe dyskinesia and frequent wearing-off. He developed deterioration when he was treated with one of the levodopa (LD) decacrboxylase inhibitor compounds in the past. Five days after LD had changed into equivalent dose of LD/carbidopa (CD), high fever with hyperCKemia appeared. He was diagnosed as having Parkinsonism-hyperpyrexia syndrome (PHS). Exchange of LD/CD to LD drugs improved the symptoms quickly. Four days after LCIG administration, PHS reappeared. Simultaneously, the patient developed sepsis and disseminated intravascular coagulation (DIC). Thrombocytopenia did not improve after recovery from infection and DIC. Anti-PA IgG and drug-induced lymphocyte stimulation test (DLST) against LCIG showed positive. Exchange of LCIG to LD drugs and intravenous methylprednisolone administration improved the symptoms and thrombocytopenia. CD induced type II and type IV allergy were suspected. This case offers a caution that physicians should be aware of drug allergy in cases of which unexpected symptoms occurred in altering one LD compound to another.
レボドパ(levodopa,以下LDと略記)製剤は,パーキンソン病(Parkinson’s disease,以下PDと略記)の治療の中心的薬剤である.一般にLDの副作用として,幻覚,嘔気といった副作用や,LDの急激な中断による悪性症候群様症状(Parkinsonism-hyperpyrexia syndrome,以下PHSと略記)などの有害事象が知られている.今回,我々は空腸投与用LD/カルビドパ(carbidopa,以下CDと略記)ゲル(levodopa carbidopa intestinal gel,以下LCIGと略記)によるアレルギー惹起例を経験した.PD患者は投与薬物に敏感な傾向があるが,担当医共々アレルギーへの認識が少なく,貴重な症例と考え報告した.
症例:70歳,男性 主訴:体動困難
既往歴:51歳時,胃癌手術 53歳時,鼠径ヘルニア手術
家族歴:弟がPD.
内服歴:入院時の内服薬をTable 1に示す.
| Medicine | Daily dose (mg/day) |
|
|---|---|---|
| Anti-Parkinson drug |
Levodopa | 1,750 |
| Entacapone | 100 | |
| Cabergoline | 3 | |
| Taripexole | 0.4 | |
| Zonisamide | 50 | |
| Others | Clonazepam | 0.5 |
| Midodrine | 4 | |
| Tamuslosin | 0.2 | |
| Mirabegron | 50 | |
| Ramelteon | 8 | |
| Dimethicone | 80 | |
| Sodium Picosulfate Hydrate 0.75% | as needed | |
| Magnesium Oxide | 1,980 | |
| Ambroxol Hydrochloride | 15 |
現病歴:26年前(44歳時),左手の使いにくさで発症した.某医によりPDと診断,抗PD薬が有効であった.9年前,首下がり,すくみ足が出現し,杖歩行となった.この頃,LD,ドパミンアゴニスト,抗コリン薬,アマンタジンで加療されていた.6~3年前,オフ時間が増加した.LDをLD/ドパ脱炭酸酵素阻害剤(DCI)配合剤に変更したところ動きが悪化し,LDに復し,これ以降漸次増量された.3年前,ゾニサミドが追加され,同時期から,ジスキネジアが出現した.2年前,右斜め徴候,起立性低血圧による失神が出現した.1年前,エンタカポンが開始された.10ヶ月前,幻覚のため,アマンタジンが中止された.半年前,ジスキネジアが悪化し,LD 3,000 mg/日から1,750 mg/日まで減量された.ジスキネジアは軽減したが,オフ時間が増加した.体動困難となり,車いすを使用するようになった.LD/CD持続経腸療法(以下,LCIG療法と略記)を希望し,当院に紹介となり,精査入院した.
入院時所見:一般身体所見:身長162.5 cm,体重52.8 kg,BMI 20 kg/m2.血圧103/71 mmHg,脈拍72/分,体温35.8°C.
神経学的所見:意識清明,認知機能は正常範囲で,幻覚はなかった.仮面様顔貌,小声,振戦,動作緩慢,前傾姿勢,小刻み歩行,すり足歩行などを認めた.レム睡眠行動障害,便秘がみられた.Hoehn-Yahr重症度分類は,オン時は3度,オフ時は4度であった.ジスキネジアは認めなかった.
入院時の検査所見:血算,生化学,血液ガス,感染症検査,胸部X線,心電図検査で異常を認めず,頭部MRIでは軽度の脳萎縮を認めた.Dopamine transporter(DAT)シンチグラフィーは両側線条体で高度に取り込み低下が認められた.Meta-iodobenzylguanidine(MIBG)シンチグラフィーでは,心縦隔比が早期像1.70,後期像1.33と低下を認めた(Fig. 1).
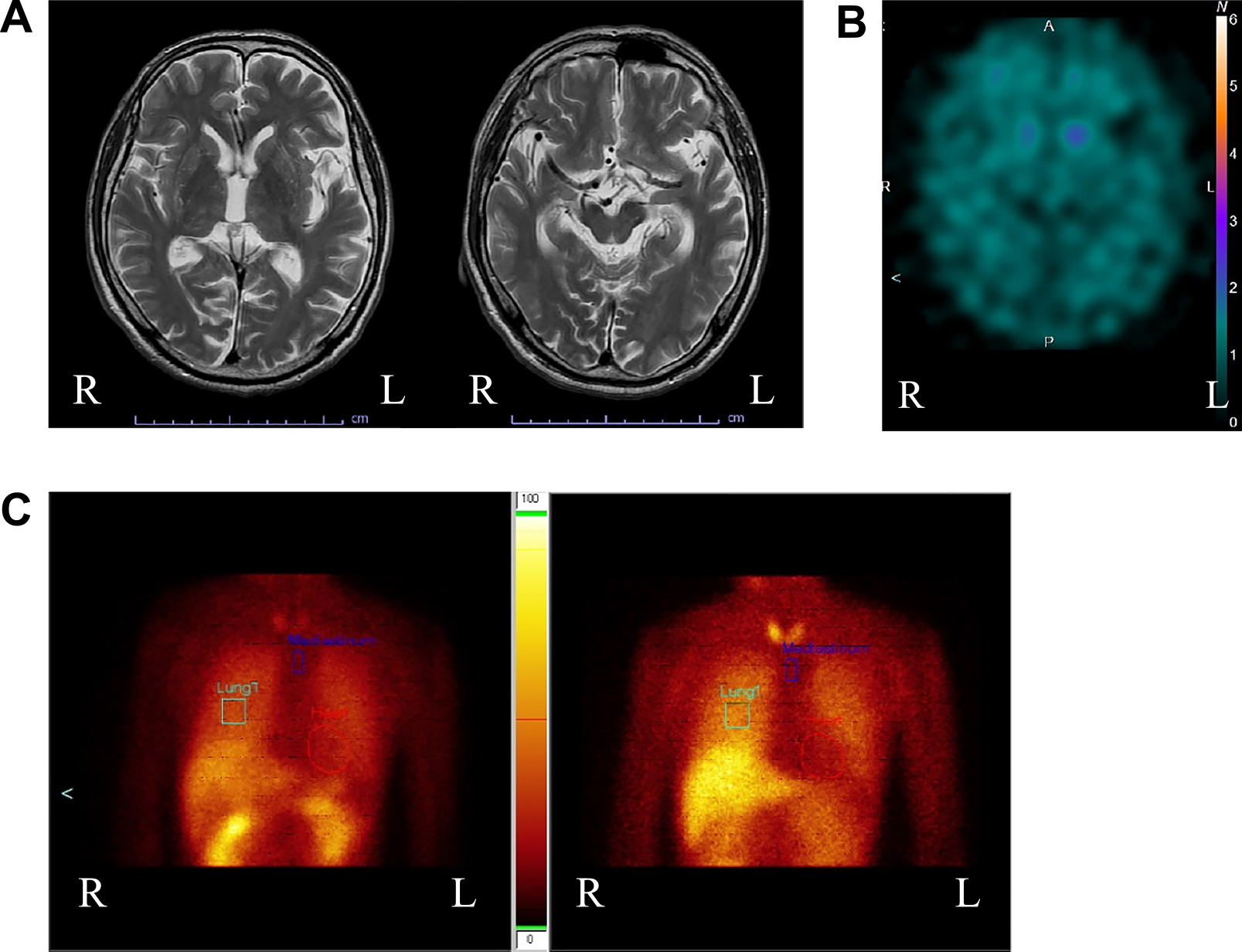
(A) Brain MRI at the level of striatum (left) and the substantia nigra (right) show no remarkable findings. (B) DAT scintigraphy at bilateral striatum demonstrates severe loss of uptake. (C) MIBG scintigraphy of early (left) and delayed (right) display decreased H/M ratio and increased washout ratio. The early and the delayed H/M ratio are 1.70, and 1.33 respectively. The heart washout ratio is 44.9%.
入院後経過:入院第9日目に,LD 1,750 mg/日を含むすべての抗PD薬を,レボドパ換算量から計算しLD/CD配合剤700 mg/日に変更した(Fig. 2).第14日目から高熱,混迷,筋強剛,発汗,CK値2,645(基準値59~248 IU/l)と上昇がみられた.PHSの可能性を考え,LD 1,750 mg/日に戻し,ダントロレンの投与を開始した.解熱傾向となり,CK値も正常化したが,閉塞性無呼吸発作が出現し,II型呼吸不全となった.LD 2,100 mg/日に増量し,第23日目より非侵襲的陽圧換気(noninvasive positive pressure ventilation,以下NPPVと略記)を開始した.オフ症状による閉塞性無呼吸発作を疑い,第32日目,経鼻空腸管よりLCIG 1,275 mg/日投与を開始した.直後から高熱と,高CK血症1,532 IU/lが出現し,PHSの再発と考えた.第34日目,肺炎,敗血症性ショック,急性腎不全を併発した.続いて血小板減少,出血傾向がみられた.播種性血管内凝固症候群(disseminated intravascular coagulation,以下DICと略記)スコア 厚労省基準 9点(カットオフ 7点以上)急性期DIC診断 6点(カットオフ 4点以上)であり,DICと診断した.抗生剤,昇圧剤,新鮮凍結血漿による治療で,感染徴候,CK値は改善した.遷延する血小板減少に対して,血小板輸血を続けていた.無呼吸発作の頻発で,呼吸状態が不安定となったため,LD/CDのアレルギー反応を疑い,第39日目にLCIG療法を中止した.LD 2,100 mg/日を再開したが,心房粗動,徐脈,頻脈を繰り返した.第42日目,ステロイドパルス療法(メチルプレドニゾロン500 mg/日,3日間静脈内投与),続いて経口プレドニゾロンによる後療法を開始したところ,血小板数は急激に改善した.第39日目に行った血小板関連IgG(以下,PA IgGと略記)抗体が,400(基準値:0~46 ng/107 cell)と上昇していたことがわかった.経過中に皮疹は認めなかった.薬物アレルギー反応および自己免疫機序の関与を考え,諸検査を行った.ハプトグロビン,ADAMST13活性は基準値内,直接Coombsと間接Coombsは陰性であった.抗核抗体が40倍と境界値で,Homogeneous,Speckled型を示し,ds-DNA IgG抗体32x(基準値:0~12倍)と軽度上昇していた.抗DNA抗体,抗RNP抗体,抗SM抗体,抗SS-A抗体,抗Scl-70抗体,抗Jo-1抗体,PR3-ANCA,MPO-ANCA,カルジオリピン抗体,ループスアンチコアグラント,血小板結合性IgG(PB IgG)は陰性であった.KL-6,IgG,IgA,IgM,C3,C4,CH50は基準値内であった.LCIGに対する薬剤誘発性リンパ球刺激試験(drug-induced lymphocyte stimulation test,以下DLSTと略記)が321%(陽性>180%)と陽性であった.第54日目,著明な徐脈が出現し,心静止となった.心臓マッサージで心拍再開した.LD 2,450 mg/日に増量したところ,全身状態が改善し,経口摂取を再開した.第80日目,NPPVを離脱した.第182日目に,Hoehn-Yahr 4度で自宅退院となった.後日施行した,LD/ベンセラジド(benserazide,以下BZと略記)のDLSTは陰性であった.
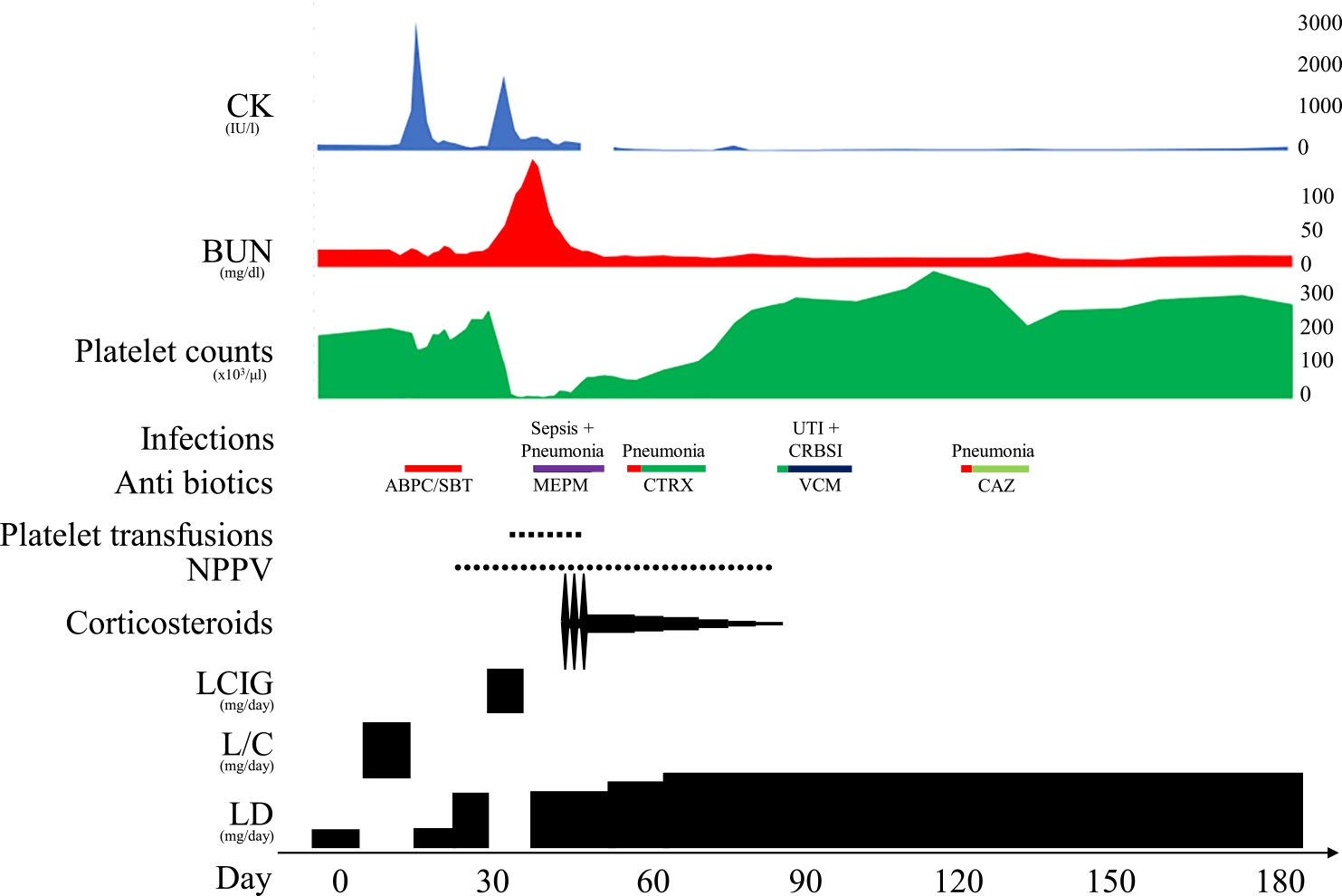
LD 1,750 mg/day and other anti-parkinsonian drugs were converted to LD/CD 700 mg/day on day 9. High fever, confusion, hyperhidrosis, and hyper CKemia were appeared and parkinsonism-hyperpyrexia syndrome (PHS) was diagnosed on day 14. After reconversion LD/CD to LD 1,750 mg/day and administration of dantrolene, body temperature and serum CK level returned to normal. Type 2 respiratory failure due to frequent obstructive apnea attacks occurred. NPPV was administrated on day 23. Nasojejunal intubation was performed under endoscopic procedure. Immediately after LCIG 1,275 mg/day was administrated, PHS with high fever and hyper CKemia was recurred on day 32. Pneumonia, septic shock and acute renal failure occurred on day 34. Subsequently, subcutaneous hemorrhage and thrombocytopenia appeared. He was diagnosed as having DIC. He was treated by antibiotics, catecholamines, fresh frozen plasma transfusion. Platelet transfusions were continued for persistent thrombocytopenia. LCIG was discontinued and LD 2,100 mg/day was readministered on day 39. Intravenous pulse Steroid therapy was performed from day 42 to 44. After LD dose was increased up to 2,450 mg/day, general condition was stabilized. He was weaned from NPPV on day 80 and discharged home on day 182. LD: levodopa, LD/CD: levodopa/carbidopa, LCIG: levodopa carbidopa intestinal gel, CK: Creatine phosphokinase, BUN: blood urea nitrogen, NPPV: Noninvasive Positive Pressure Ventilation, DIC: Disseminated Intravascular Coagulation, UTI: Urinary tract infection, CRBSI: Catheter related blood stream infection.
本例では,LDからLCIGに変更後,PHSと血小板減少を認めた.LCIGの中止,LDの再開,副腎皮質ステロイドホルモン治療によって,良好な転帰を得た.抗PA IgG陽性,LCIGに対するDLST陽性より,II型,IV型の薬剤アレルギーと判断した.LCIGに先行して投与されたLD/CD配合剤でも,PHSが生じ,これも薬剤アレルギーと考えた.
薬剤アレルギーは,I~IV型に分けられるが,LD製剤の薬剤アレルギーには,II型とIV型の報告が多い(Table 2).I型アレルギーとして,LD/CD導入直後に結膜充血,鼻汁,発汗,血圧上昇などの自律神経症状と皮疹を認めた報告があり,抗原としてCDが疑われた2).II型アレルギーとしては,溶血性貧血3)~6)や,血小板減少7)~9)の報告が多数あり,原因として,LD4)5)7)8),CD3)9),BS6)が示唆されている.溶血性貧血で,直接Coombs,温式抗体,冷式抗体が陽性を示した症例3)や,血小板減少では,抗PAIgG陽性を示した症例がみられた7)~9).アレルギー発症までの期間は,暴露から1~2年と長期経過している報告もあった8)9).III型アレルギーとしては,LD/CDによる紫斑,関節痛,血尿,蛋白尿を来し,皮膚生検で血管炎が証明され,Henoch-Schönlein syndromeと診断された報告がある10).IV型アレルギーについては,いずれも皮疹を呈しており11)~14),抗原として,LD製剤に添加された黄色色素とする報告11)~13)が多いが,LDとした報告14)もあった.薬剤投与から発症までの期間は3日から6か月,中止から改善までの期間は3週間から6か月と幅広く,長い潜伏期間の要因として,継続による薬剤の蓄積が示唆された13).薬剤アレルギー発症後のPD治療として,LD製剤間での薬剤変更,ドパミンアゴニストへの変更8)9),ステロイド併用でのLD製剤使用継続3)7)が行われていた.
| Type | Medicine | Symptoms | Reference |
|---|---|---|---|
| I | Carbidopa | drowsiness, heartburn, excessive sweating, tearing, conjunctival injection, rhinorrhea, blood hypertension, tachycardia, skin rash | 2 |
| II | Levodopa/Carbidopa | autoimmune hemolytic anemia, positive for direct Coombs test, and/or cold antibody | 3 |
| Levodopa | hemolytic anemia | 4, 5 | |
| Levodopa/Benserazide | autoimmune hemolytic anemia | 6 | |
| Levodopa | autoimmune thrombocytopenia positive for PA IgG, hematomas* | 7, 8* | |
| Levodopa/Carbidopa | gross hematuria, thrombocytopenia positive for PA IgG | 9 | |
| Carbidopa | thrombocytopenia positive for PA IgG | This case | |
| III | Levodopa/Carbidopa dose dependent | palpable purpura, edema, arthralgia, cramp, leucocytoclastic vasculitis, microhematuria, proteinuria, hypergammaglobulinemia, Henoch- Schönlein syndrome | 10 |
| IV | Yellow dye D&C Yellow 10** FD&C Yellow 6** |
maculopapular rashes | 11, 12**, 13 |
| Levodopa | pruritic erythematous maculopapular rash | 14 | |
| Carbiodpa | positive for DLST | This case |
Symptoms marked *, ** are only reported in the article with the same marks.
このように,LD,CD,BS,添加色素を抗原としたLD製剤アレルギーの報告があるが,DLSTが行われた報告はなかった.DLSTによる原因薬剤の同定感度は53.9%,特異度61.5%である15).本例は,LCIGによるアレルギーの初報であると共に,LD製剤によるアレルギーをDLSTで証明した初報である.DLSTにはLCIGを用いたため,LD,CD,添加物のカルメロースナトリウムが抗原となり得る(Table 3).本例では,LD/CDでもPHSが出現した経過から,両者の共通成分であるCDが抗原と考えた.本邦ではCD単剤の入手は困難であり,CDによるDLSTは不可能だった.なお,後日行ったLD/BSに対するDLSTは陰性であった.急性期のDLSTに関しては擬陽性を示す可能性も否定できず,慢性期に再検することが望ましい.
本例における血小板減少について薬剤アレルギー以外にDIC,特発性血小板減少性紫斑症(idiopathic thrombocytopenic purpura,以下ITPと略記),全身性エリテマトーデス(systemic lupus erythematosus,以下SLEと略記)が鑑別にあげられた.DICとしては,敗血症改善後も血小板減少が遷延した経過が矛盾した.ITPについては,疾患特異性の低いPA IgG抗体のみ陽性で,PB IgG抗体は陰性であった.SLEについては,抗核抗体とds-DNA抗体陽性,二系統の血球減少,急性期に精神症状が認められ,2012年に作成されたSLEの国際診断基準Systemic lupus international collaborating clinicsを満たす.しかし,ステロイド治療が1か月半と短期間で中止できておりITP,SLEとも否定的であった.以上より,薬剤アレルギーと結論づけた.
本例において,PHSを呈した機序として,アレルギー性の腸管障害による血中ドパミン濃度の急激な低下,およびアレルギーによる発熱の双方が考えられる.本例では,一度目のPHS後,アレルギーに考慮が及ばず,胃切除後の吸収障害を疑い,LCIGを1,275 mgまで増量した.十分と思われたがPHSを再燃したため,アレルギー反応によるPHSと考えた.セロトニン症候群も鑑別にあがるが,モノアミン酸化酵素阻害薬,抗うつ剤の服用歴はなく,深部腱反射亢進は認めず,否定的であった.
CDに対するII型,IV型薬剤アレルギーの症例を報告した.LD製剤の開始・変更後に,PD症状の悪化や,異変があった場合,薬効成分や,添加物に対するアレルギーの可能性を考慮し,配合剤の種類(LD/CD,LD/BS)や,LD,ドパミンアゴニストなどへの変更を検討する必要がある.投与早期だけでなく,数年後に発症するという報告もあるため,定期的に血液検査でモニターする必要がある.
本報告の要旨は,第240回日本神経学会関東・甲信越地方会で発表し,会長推薦演題に選ばれた.