2024 Volume 64 Issue 2 Pages 109-112
2024 Volume 64 Issue 2 Pages 109-112
症例は74歳女性.30歳代で重症筋無力症(myasthenia gravis,以下MGと略記)を発症し,翌年に胸腺腫を摘出したがMG症状が安定せず,fast-acting treatment strategy(FT)目的の頻回な入院治療が必要だった.X−2年3月よりエクリズマブを開始し,MG症状が軽快したため外来で経過観察していた.X年2月に全身倦怠感,発熱が出現しSARS-CoV2 PCR検査で陽性となり胸部CTで軽度の肺炎像を認め,入院した.入院中はMGとCOVID-19関連肺炎の症状は重症化しなかったが,その際にエクリズマブがそれぞれの病態に良好に作用した可能性があるため文献的考察を踏まえて報告する.
A 74-year-old woman developed myasthenia gravis (MG) at the age of 32. She had a thymoma removed the following year, but her MG symptoms did not stabilize, and she required frequent hospitalization for fast-acting treatment (FT). She started eculizumab in March of two years ago and was followed up on an outpatient basis as her MG symptoms became milder. In February of this year, she was admitted to our hospital due to mild COVID-19-associated pneumonia with general malaise and fever. Her COVID-19-associated pneumonia was treated with intravenous sotrovimab, dexamethasone, and unfractionated heparin, and oral therapy for MG stayed the same. Eculizumab was not administered during hospitalization due to the combination of stable MG symptoms and the fact that the drug is not paid for by the Japanese insurance system. The patient’s MG and COVID-19-associated pneumonia were not severe during hospitalization. However, the risk of myasthenic crisis and death is high when patients with MG develop COVID-19-associated pneumonia. Several reports suggest that the condition of patients with eculizumab-treated MG who develop COVID-19-associated pneumonia is not severe, and that that inhibition of the complement pathway with eculizumab is effective for COVID-19-associated pneumonia. Complement deposition in organ microvessels has been observed in patients with COVID-19, which suggests that complement overload may be a risk factor for COVID-19-associated pneumonia. Excessive complement activation may be involved in the pathogenesis; thus, eculizumab may function by inhibiting this pathway. In this case, eculizumab was discontinued while the patient had COVID-19-associated pneumonia, however, CH50, which is an indicator of complement, was suppressed during hospitalization due to the COVID-19-associated pneumonia. Therefore, eculizumab may have interfered with this course of events. This case demonstrates that eculizumab may be safe for and tolerated by patients with MG and COVID-19-associated pneumonia, but more cases need to be accumulated to support this conclusion.
重症筋無力症(myasthenia gravis,以下MGと略記)は神経筋接合部のシナプス後膜上にあるいくつかの標的抗原に対して自己抗体が神経筋接合部の刺激伝達を障害することによって生じる自己免疫疾患である.原因となる自己抗体としては抗アセチルコリン受容体(acetylcholine receptor,以下AChRと略記)抗体,抗筋特異的チロシンキナーゼ(muscle-specific receptor tyrosine kinase: MuSK)抗体が判明しており,近年では抗低密度リポ蛋白質受容体関連蛋白質4(low-density lipoprotein receptor-related protein 4: LRP4)抗体の関与の可能性も検討されている.
抗AChR抗体陽性の難治性全身型MGに対して本邦では2017年より抗C5モノクローナル抗体であるエクリズマブ(ソリリス®)の使用が認可された.エクリズマブは発作性夜間ヘモグロビン尿症に関して承認されて以降,非典型溶血性尿毒症症候群,MG,視神経脊髄炎スペクトラム障害などにも適応が拡大されている薬剤であるが,最近ではCOVID-19関連肺炎に対してその重症化を防ぐ可能性が示唆されている.エクリズマブを使用しているMG患者がCOVID-19関連肺炎を続発した1例を経験し,その治療経過や転機について,文献的考察を踏まえ報告する.
症例:74歳,女性
主訴:呼吸困難感
既往:71歳より骨髄異形成症候群,2型糖尿病,糖尿病性腎症,高血圧,頸椎症性脊髄症,狭心症,下肢深部静脈血栓症.
現病歴:30歳代でMGを発症し,その翌年に拡大胸腺摘出術を施行された.X−10年頃にMG症状は安定していたため,プレドニゾロン(prednisolone,以下PSLと略記)を中止された.X−6年頃からMG症状の増悪を繰り返すようになり,X−6年からX−3年の3年間で7回に及ぶ免疫グロブリン静注療法(intravenous immunoglobulin,以下IVIgと略記)やステロイドパルス療法(intravenous methylprednisolone: IVMP),血漿浄化療法といったfast-acting treatment strategy(FT)目的に入院していた.MG症状が不安定で難治性であるため,X−2年3月よりエクリズマブを使用開始した.以降はMG治療目的の入院はなく,外来経過観察のみでMG症状は安定していた.X年2月に全身倦怠感と発熱が出現,その3日後に家族のSARS-CoV2 PCR陽性が判明し,38.6°Cの発熱,SpO2 90~91%であり当院に救急搬送され入院した.
入院時現症:身長158.6 cm,体重83 kg,BMI 33.2,血圧123/59 mmHg,脈拍71 bpm,体温37.5°C,SpO2 97%(2 l/min,経鼻カニューレ).軽度の咽頭発赤を認めた.肺野に肺雑音を聴取しなかった.
神経学的所見:意識清明.複視なく,両眼瞼下垂が常時ではないが毎日見られ,嚥下機能は軽度低下していた.四肢筋力は易疲労性がなく正常で,感覚障害や小脳運動失調は認めなかった.自律神経系の異常所見を認めなかった.固形物の咀嚼で疲労,体動時の息切れあり,MG activity of daily living scale(MG-ADL)は5点であった.
検査所見:白血球9,000/μl,CRP 7.0 mg/dlと炎症反応が高値で,D-dimer 1.8 μg/mlと軽度の血栓傾向を認めた.BUN 40 mg/dl,クレアチニン3.48 mg/dlで高度の腎機能障害が見られ,空腹時血糖321 mg/dl,HbA1c(NGSP)9.6%で糖尿病のコントロールは不良であった.入院日から直近(X年1月)の抗AChR抗体は2.7 nmol/l,CH50は検出感度以下,来院時SARS-CoV2 PCRは陽性であった.胸部CTでは右肺下葉,左肺上葉に淡い濃度上昇を認め,軽度の肺炎所見であった.胸腺は摘出済みであった(Fig. 1).

There was a pale frosted shadow in the lower lobe of the right lung (↓).
入院後経過:入院時,MGに対して,ピリドスチグミン120 mg/日,PSL 6 mg/日,シクロスポリン50 mg/日を内服していた.入院期間中にエクリズマブの投与予定があったが,入院医療費制度を考慮し延期した.入院後,COVID-19関連肺炎に関しては,ソトロビマブ500 mgを単回投与し,デキサメタゾン6.6 mg/日を7日間静注,未分画ヘパリン10,000単位/日の15日間静注を併用した.入院第10病日には酸素需要が消失し,第16病日に退院した.入院期間中,MG症状は安定しており,MGの治療薬は同量で継続した.退院1週間後の外来診察で,MG-ADLは3点(嚥下,呼吸,眼瞼下垂の項目で1点ずつ加点)で入院時点より悪化はなく,抗AChR抗体は2.7 nnmol/lで不変,CH50は36.0 U/mlで正常値の下限程度で,その後エクリズマブを外来で再開した.一連の臨床経過を図に示した(Fig. 2).
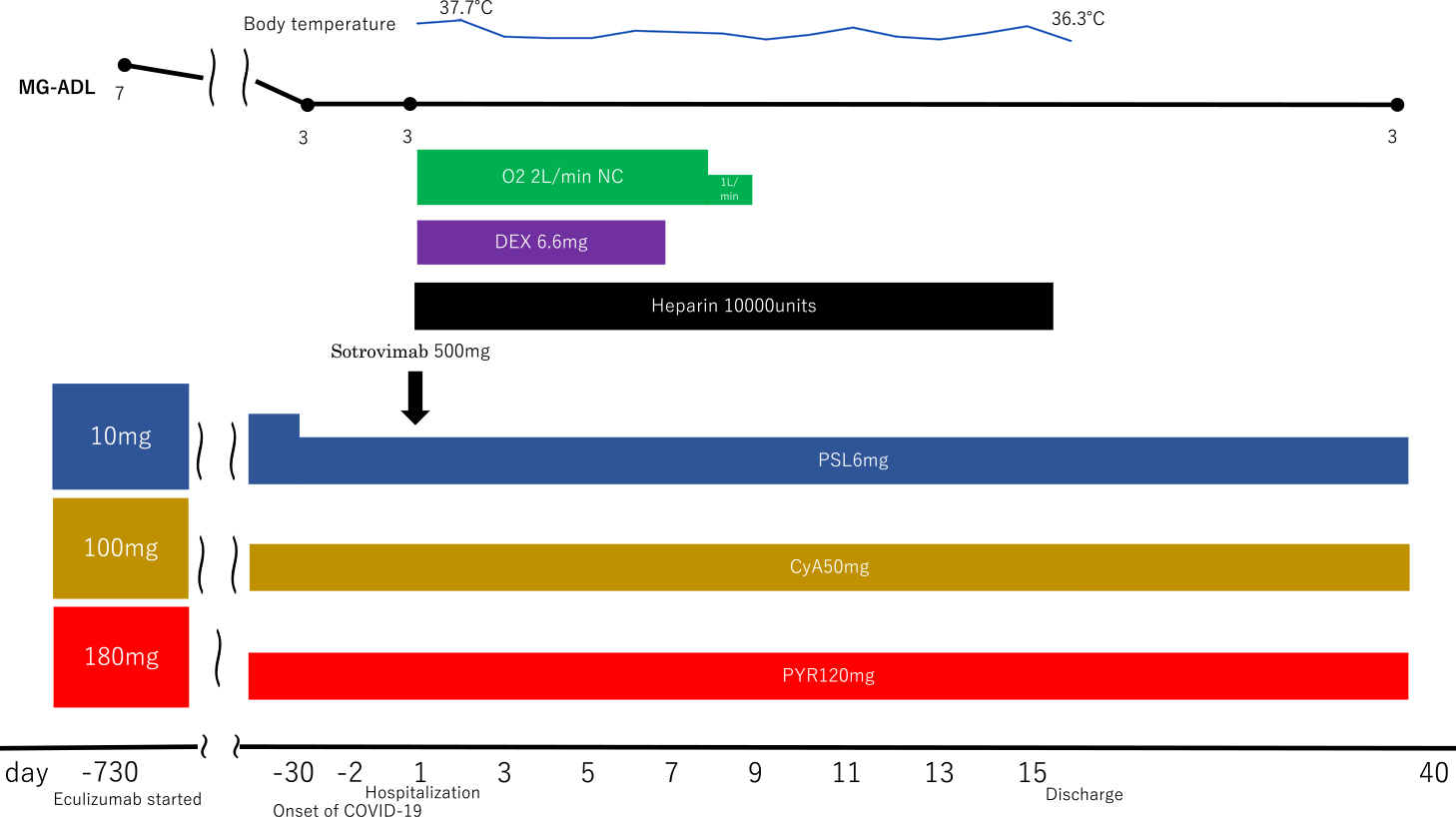
MG-ADL improved from the time eculizumab was introduced two years ago in March, and oral prednisolone, cyclosporine, and pyridostigmine doses were reduced. Oral medications were the same as before the onset of COVID-19. Ach-R ab: anti acetylcholine receptor antibody, CyA: cyclosporine A, DEX: dexamethasone, MG-ADL: myasthenia gravis activities of daily living, PSL: prednislone, PYR: pyridostigmine bromide.
エクリズマブは難治性MGにおいて使用されるが実際は,Quantitative MG score(QMG),MG-ADLなどのMGの評価スケールが有意に改善するのは60%程度と言われている1).本症例においてはX−2年にエクリズマブ導入するまでは頻回な入院治療を要していたが,導入後はMG悪化による入院,レスキュー治療は行われていない.Minimal Manifestations with PSL 5 mg or better(MM-5 mg)の達成までは至っていないが,経口ステロイドや免疫抑制薬の用量は減量傾向で治療経過は導入前後で明らかに改善している.
MG患者がCOVID-19に罹患した場合MGの増悪や筋無力症クリーゼ発症の危険性がある.MuppidiらはCOVID-19を罹患したMG患者91例の40%でMGの増悪または筋無力症クリーゼを,24%に死亡をもたらす2)と報告しているが,一方,2023年のThomasらの39例の報告ではそれぞれ12.8%,10.5%3)と述べられている.これらの報告は,MG患者がCOVID-19に感染した場合に普遍的なリスクは存在しているが,治療やワクチンの開発により改善している可能性を示唆している.また,米国のElectoronic Health Record datasetを解析した研究によるとCOVID-19を発症したMG患者377例のうち38.5%が入院,12.7%がICU管理と報告され,これは非MG患者よりも有意に多かった4).同研究では年齢が75歳以上,嚥下機能障害を有することが死亡リスクである4)と示唆しているが,COVID-19発症前にMyasthenia Gravis Foundation of America classification(MGFA)≧IVの患者では,COVID-19が重症化しやすく,ICU入院を必要とする場合が多いと指摘する既報も認め5),MGの重症度が転帰に影響する可能性が考察されている.MGの速効性治療や免疫療法自体はCOVID-19の重症化には関係しないようで6),COVID-19発症中にMG症状が増悪した場合は,IVIgや血液浄化療法といったFTの施行により良好な転帰をとりやすい6)~8).本症例ではCOVID-19の経過中にMGの増悪を認めなかったため,MGに対する治療介入の必要性はなかった.
本症例では入院前のMGの病勢が安定していたことと,本邦の保険制度の関係によりエクリズマブは継続されなかった.エクリズマブは補体を介して免疫を抑制するためにNeisseria meningitidesによる髄膜炎や上気道感染症のリスクを認め,COVID-19感染下の使用が有益かどうか明確ではない.一方でMimoriらの報告では,二度の筋無力症クリーゼの既往がある治療抵抗性のMG患者が,COVID-19に罹患した際にエクリズマブの投与を継続したところ,MG症状の悪化やクリーゼを認めず,COVID-19が悪化せずに従来通りに治療可能であったため,COVID-19発症下においてもエクリズマブの投与を慎重に継続することを推奨していた9).Alisらの報告では,エクリズマブ以外の免疫療法に対して抵抗性のMG患者において,エクリズマブ投与中にCOVID-19感染症を発症したが,肺炎には至らなかった.感染中にMG症状の指標であるQMG,MG-ADLの悪化が見られ,IVIgを施行,速やかにMG症状が改善し,最終的にクリーゼを起こさず,COVID-19感染症は治癒した10).
COVID-19患者において様々な臓器の微小血管に補体の沈着が観察される場合があり,補体の過剰な活性化が病態へ関与している可能性が示唆されており,エクリズマブがCOVID-19の転帰を改善する可能性があると報告されている11)~14).本症例でMGが重症化しなかった要因の一つに,外来でエクリズマブを定期使用していたことが挙げられる.エクリズマブは抗C5抗体であるためCH50を抑制するが,本症例ではCOVID-19発症直前のCH50は検出感度以下にまで抑制されていた.そのため,エクリズマブの定期投与を一度中断したものの,エクリズマブがCOVID-19の治療経過に関与している可能性が高いと推察した.
エクリズマブがCOVID-19に影響せず,単にMG症状に対して寄与したのみで,COVID-19治療薬により重症化しなかったと推測することもできるが,我々はエクリズマブ投与により入院前のMG症状を良好にコントロールしていたこと,加えてCOVID-19における補体経路の阻害の両面で良好な転機に影響したと考察している.エクリズマブとCOVID-19感染症の関係について,我々が渉猟した範囲では報告が少なく,今後さらなる症例の蓄積が期待される.