要旨
症例は69歳女性.2005年からプロトンポンプ阻害薬を内服しており,2015年にHelicobacter pyloriを除菌した.2017年10月の上部消化管内視鏡検査で,胃内多発ポリープの1つから生検でGroup 4,胃癌疑いと診断された.同ポリープは経時的にサイズが増大し,頂部に不整陥凹を伴っていたため,腺癌の発生を疑って2018年1月にEMRを行った.切除病変は病理学的に非萎縮性胃粘膜に生じた胃底腺ポリープであったが,連続した腺窩上皮に高分化型腺癌が発生していた.今回われわれは胃底腺ポリープに腺癌が併存した貴重な1例を経験した.腺癌の併存が疑われる場合は慎重な経過観察や適切な治療を行う必要がある.
Abstract
A 69-year-old woman had been taking a proton pump inhibitor (PPI) for reflux esophagitis since 2005 and also succeeded to Helicobacter pylori(H. pylori) eradication in 2015. EGD revealed multiple gastric polyps in 2017, one of them was suspected to be malignant based on biopsy findings. The polyp gradually enlarged with an irregular depression on its surface; therefore, endoscopic mucosal resection was performed for further diagnosis and treatment. Histopathological assessment confirmed adenocarcinoma on the fundic gland polyp (FGP); however, findings suggestive of gastric mucosal atrophy or H. pylori infection were absent. Gastric adenocarcinoma arising from a PPI-related FGP is rare. Thus, when adenocarcinoma on an FGP is suspected, carefully follow-up and endoscopic resection are recommended.
Ⅰ 緒 言
胃底腺ポリープ(fundic gland polyp:FGP)は組織学的に胃底腺の過形成や囊胞状拡張を特徴とする隆起性病変である
1).一般的にHelicobacter pylori(H. pylori)感染がなく,萎縮のない胃底腺領域に発生し,癌の合併は極めて稀であることが知られている
1),2).近年,プロトンポンプ阻害薬(proton pump inhibitor:PPI)の長期投与やH. pylori除菌によってFGPが発生ないし増大するという報告が散見される
3)~5).今回,われわれはPPI長期服薬中にFGPが増大し,一部に高分化型腺癌の発生を認めた1例を経験したので,文献的考察を加えて報告する.
Ⅱ 症 例
患者:69歳 女性.
主訴:なし.
既往歴:高血圧症,子宮筋腫術後.
内服薬:ランソプラゾールOD錠15mg,アムロジピンベシル酸塩錠5mg,エナラプリルマレイン酸塩錠10mg.
現病歴:2005年に逆流性食道炎に対してランソプラゾールの内服を開始した.2015年にH. pyloriの除菌を受けた.2017年10月,健康診断の上部消化管内視鏡検査で,胃内の多発ポリープの1つから生検でGroup 4,胃癌疑いと診断されたため精査加療目的に当院を紹介され,受診した.
初診時現症:身長 151cm,体重 57kg.バイタルサインに異常はない.眼球および眼瞼結膜に異常を認めない.腹部は平坦・軟で圧痛は認めない.下腹部正中に手術瘢痕を認めた.
臨床検査成績:血中H. pylori抗体は陰性(<3.0U/mL)であった.その他,一般血液検査で異常は認めなかった.
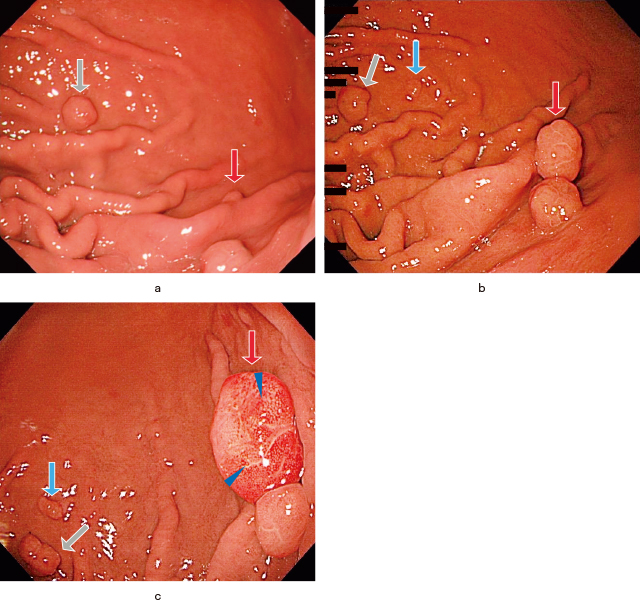
上部消化管内視鏡所見:軽度の萎縮胃粘膜を背景とし,FGPと思われるポリープが多発していた.ポリープは経時的に数が増加し,サイズが増大しているものを複数認めた(Figure 1-a~c).胃体下部大彎のポリープは表面にわずかな陥凹を伴っており,陥凹部より生検を施行された(Figure 1-c).
前医生検結果:胃底腺粘膜のごく一部に異型腺管を認め,免疫染色で一部にp-53陽性を示し,Ki-67陽性細胞とβ-catenin核内移行を認めた.高分化型腺癌が疑われたが検体量がごく少量であり確定診断には至らずGroup 4と診断された.
当院で再検した上部消化管内視鏡検査では,木村・竹本分類C-1相当の萎縮を認めた.当該病変は立ち上がりが明瞭な10mm大の赤色調の隆起性病変で,頂部に辺縁不整の陥凹を認めた.隆起部は表面平滑で背景粘膜と同様の円形の腺管開口部を認め,FGPに合致する所見であった(Figure 2-a).Narrow Band Image(NBI)観察でも陥凹以外には均一でやや大きな円形開口部を認めFGPとして矛盾しなかった.NBI拡大観察所見では陥凹内には腺管開口部や腺窩辺縁上皮と思われる構造物を認めたが不規則なパターンを呈しており,走行が不整な異常血管が観察された(Figure 2-b).
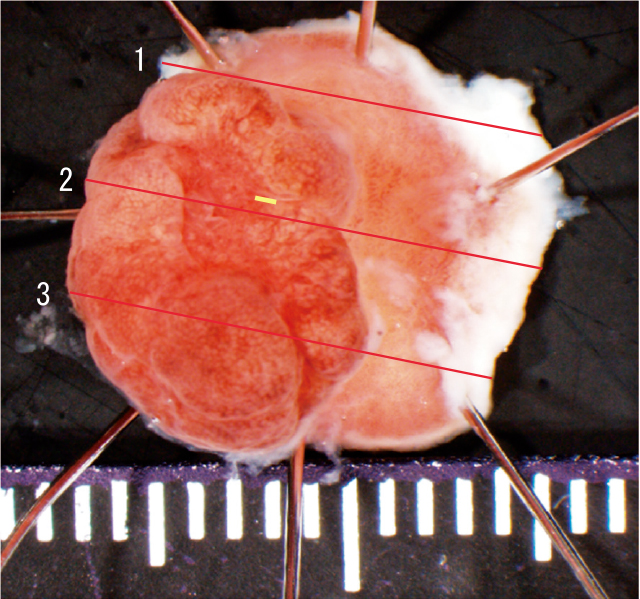
臨床経過:内視鏡で癌領域を明確に指摘できなかったが,前医生検結果からポリープの陥凹部に胃癌が存在することが示唆され,粘膜内病変と考えられたため内視鏡的粘膜切除術(EMR)で一括切除した(Figure 3).
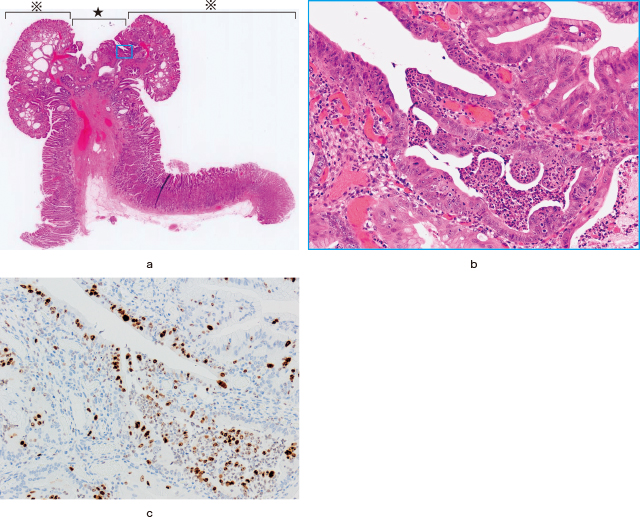
切除標本の病理組織学的所見:背景は炎症所見の乏しい萎縮のない胃底腺粘膜であった.隆起部は腺管の房状分枝や固有胃腺の小囊胞状拡張が見られFGPに合致する所見であった(Figure 4-a).FGPに連続した陥凹部の間質には炎症細胞浸潤が目立ち,表層には粘液が豊富で大小不同の異型腺管が開口しているが,腺管を構成する核の極性は保たれており大部分が再生異型と考えられた.一方,陥凹の一部には形状不整を示した異型腺管の増生を認め,異型腺管を構成する細胞の核は腫大し,類円形を呈しており,高分化型腺癌の所見であった(Figure 4-b).再生異型と思われる陥凹部は内視鏡で表面構造が不明瞭化している部位に一致していると考えられたが,高分化型腺癌の領域は小さく表面への露出もないため内視鏡所見から癌と認識することは困難であったと考えられた.免疫染色では癌部においてKi-67陽性細胞が増加を認めた(Figure 4-c).β-cateninは陽性細胞が多く出現しており,核内移行が観察された.p-53の過剰発現は認められなかった.粘液形質はMUC5ACとMUC6が部分陽性で,MUC2が陰性であり胃型粘液形質であった.また,非腫瘍部の固有層内の壁細胞数は増加しており,拡張した胃底腺において壁細胞の細胞質が突出する,いわゆるparietal cell protrusion(PCP)が認められた.
術後経過:治癒切除が得られたと考え経過観察中である.この他のポリープに関して,概ね10mm以上のものを計3つEMRで切除した.すべて病理学的にFGPと診断され,PCPを認めたが悪性腫瘍は伴っていなかった.また下部消化管内視鏡検査では家族性腺腫性ポリポーシス(familial adenomatous polyposis:FAP)の所見は認められなかった.
Ⅲ 考 察
FGPは組織学的に胃底腺の過形成や囊胞状拡張を特徴とする非腫瘍性の隆起性病変である
1).FAP症例の26~43%に発生するとされ
6),以前はFAPに合併する病変と考えられていた.しかし近年,散在性FGPが多く診断されるようになり,報告によって差はあるが一般人口における頻度は1.8~5.9%で
7),8),中年女性に好発するとされる
8).
1992年にGraham
9)はPPIの長期投与中にFGPが新たに発生した症例を初めて報告し,その後の研究でPPI長期投与例においてはFGPが発生ないし増大することが明らかになっている
3),4).鎌田ら
10)は,PPI長期投与によるFGPの形態変化について検討しており,FGPはPPI長期投与によって表面にやや凹凸を伴い,亜有茎性で馬鈴薯様または水腫様の形態に変化することが特徴的であるとしている.増大の要因として,胃酸分泌低下に対するnegative feedbackで生じる高ガストリン血症やPPIの直接作用が挙げられている
10)が,明確な機序は未だ不明である.組織学的には,腺管の著明な拡張と間質の浮腫
4),10),PCPが認められることがある.PCPは壁細胞が長軸方向に膨化し,病理標本で壁細胞が管腔側に突出して見える現象であり,PPI長期投与で生じる高ガストリン血症に対する代償性の変化だと考えられている
11).
FAP随伴FGPは高頻度(25~44%)にdysplasiaを伴うことが報告されている
6)が,散在性FGPにおいてその頻度は非常に稀である.山本ら
2)は組織学的に診断したFGP 477例と過形成性ポリープ 562例を比較検討した研究の中で,FGPが悪性化した症例は1例も認められず,FGPは悪性化することのない良性疾患であると述べている.Levyら
12)は組織学的にFGPと診断した35,732例のうち,62例の散在性FGPにlow grade dysplasiaを伴っていたが,high grade dysplasiaおよびadenocarcinomaは認められなかったと報告している.
H. pylori感染によって胃底腺が萎縮することでFGPが消失する
13),除菌によって出現ないし増大する
14)という報告もあり,一般にFGPはH. pylori感染のない萎縮性変化の乏しい胃底腺粘膜に生じ,FGPの存在自体が胃癌発生の低リスク因子であると考えられてきた.しかし近年,FGPに悪性所見を伴う症例の報告が散見されるようになってきた
15)~22).それらの症例に自験例を含め一覧を示す(Table 1).性別においては女性に多かった.FGPのサイズは3mm程度から20mm程度とばらつきが見られたが,これまでの報告と同様にPPI投与例ではサイズが大きく,水腫様もしくは馬鈴薯様の形態を示す傾向があった.癌の発生は3mmから12mmのFGPで認められ,癌とサイズとの関連性は明らかではなかった.多くの症例で胃粘膜萎縮とH. pylori感染はなかった.
本症例では血中ガストリン値を測定できなかったため詳細な検討は困難だが,除菌直前である2015年の上部消化管内視鏡検査を施行した時点で既に当該病変が増大傾向で,PCPが認められたことからPPIが何らかの影響を及ぼしていた可能性は否定できないと思われた.PPIの長期投与はFGPのみならず,胃癌のリスクも上昇させる可能性があるという報告がある
23),24).しかし,いずれもFGP内の癌の発生については言及しておらず,PPI,FGP,癌という三者の関連性は解明されていない.また,過去のH. pylori感染が交絡因子として影響している可能性もあり,今後のさらなる研究が期待される.
内視鏡所見に関しては,FGPに合併したadenocarcinomaの部位で不整な陥凹や発赤を認め,内視鏡的に診断し得た症例が報告されている.Togoら
19)はNBI拡大観察を行うことで不規則な微小血管構造や表面構造を認識してdemarcation lineを同定することができたと報告している.本症例では癌の領域が小さく表面への露出もなかったため,拡大観察でも癌としての認識は困難であったと考えるが,炎症性変化によると思われる再生異型により発赤や陥凹,表面構造の不明瞭化を呈したため診断的治療を行い,微小な癌を発見・治療することができた.稀ではあるがFGP内に癌が発生する可能性があるということを念頭に置き,FGPが疑われる病変であったとしても,発赤や陥凹を伴う病変に関しては拡大内視鏡を用いた詳細な観察を行い,必要に応じて診断的治療を検討することが望ましいと考えられた.
Ⅳ 結 語
H. pylori除菌後,PPI服薬中に増大したFGPに高分化型腺癌の併存を認め,内視鏡的切除を行った1例を経験した.特に発赤や陥凹を伴うFGPは癌が併存している可能性を考慮して慎重な経過観察や適切な治療を行う必要がある.
文 献
- 1. 上村 直実, 向井 俊一, 山口 修司ほか.胃底腺ポリープ症例の背景胃粘膜に関する臨床的検討 特に胃癌症例との対比について.Gastroenterol Endosc 1993;35:2663-71.
- 2. 山本 明子, 市川 正章, 高原 理ほか.胃底腺性ポリープの臨床的検討.日消誌 1998;95:1101-9.
- 3. 山元 隆文, 松元 淳, 小斉平 智久ほか.omeprazole長期投与により発症したと思われる多発性胃底腺ポリープの1例.日消誌 2003;100:421-5.
- 4. 菅原 通子, 今井 幸紀, 齊藤 詠子ほか.プロトンポンプ阻害薬長期投与中に増大した胃底腺ポリープの検討.Gastroenterol Endosc 2009;51:1686-91.
- 5. 鎌田 智有, 井上 和彦, 青木 利佳ほか.胃ポリープの自然史とmalignant potential―胃底腺ポリープ.胃と腸 2012;47:1227-34.
- 6. 八尾 隆史, 三富 弘之, 日高 康博ほか.【胃ポリープの意義と鑑別】胃ポリープの病理学的分類・鑑別診断と臨床的意義.胃と腸 2012;47:1192-9.
- 7. Kinoshita Y, Tojo M, Yano T et al. Incidence of fundic gland polyps in patients without familial adenomatous polyposis. Gastrointest Endosc 1993; 39:161-3.
- 8. Genta RM, Schuler CM, Robiou CI et al. No association between gastric fundic gland polyps and gastrointestinal neoplasia in a study of over 100,000 patients. Clin Gastroenterol Hepatol 2009; 7:849-54.
- 9. Graham JR. Gastric polyposis:onset during long-term therapy with omeprazole. Med J Aust 1992; 157:287-8.
- 10. 鎌田 智有, 山中 義之, 松本 啓志ほか.【食道・胃・十二指腸ポリープの鑑別診断】PPI長期投与による胃底腺ポリープの形態変化.消化器内視鏡 2015;27:83-92.
- 11. 山形 寿文, 幡地 正輝, 中山 沙映ほか.PPI長期内服患者の胃壁細胞腫大に関する検討.Prog Dig Endosc 2016;88:42-5.
- 12. Levy MD, Bhattacharya B. Sporadic Fundic Gland Polyps With Low-Grade Dysplasia:A Large Case Series Evaluating Pathologic and Immunohistochemical Findings and Clinical Behavior. Am J Clin Pathol 2015; 144:592-600.
- 13. Watanabe N, Seno H, Nakajima T et al. Regression of fundic gland polyps following acquisition of Helicobacter pylori
.Gut 2002; 51:742-5.
- 14. Okano A, Takakuwa H, Matsubayashi Y. Development of sporadic gastric fundic gland polyp after eradication of Helicobacter pylori
. Dig Endosc 2008; 20:41-3.
- 15. Jalving M, Koornstra JJ, Gotz JM et al. High-grade dysplasia in sporadic fundic gland polyps:a case report and review of the literature. Eur J Gastroenterol Hepatol 2003; 15:1229-33.
- 16. Kawase R, Nagata S, Onoyama M et al. A case of gastric adenocarcinoma arising from a fundic gland polyp. Clin J Gastroenterol 2009; 2:279-83.
- 17. 青井 健司, 安永 祐一, 松浦 倫子ほか.【胃ポリープの意義と鑑別】プロトンポンプ阻害薬長期服用中に発生した胃底腺ポリープ内にdysplasiaを認めた1例.胃と腸 2012;47:1270-4.
- 18. Jeong YS, Kim SE, Kwon MJ et al. Signet-ring cell carcinoma arising from a fundic gland polyp in the stomach. World J Gastroenterol 2014; 20:18044-7.
- 19. Togo K, Ueo T, Yonemasu H et al. Two cases of adenocarcinoma occurring in sporadic fundic gland polyps observed by magnifying endoscopy with narrow band imaging.World J Gastroenterol 2016; 22:9028-34.
- 20. 樋貝 詩乃, 保坂 稔, 落合田 鶴枝ほか.プロトンポンプ阻害薬長期服薬中に胃底腺ポリープにHigh-Grade Dysplasiaを生じた1例.ENDOSC FORUM digest dis 2017;33:14-20.
- 21. Shibukawa S, Wakahara Y, Ouchi S et al. Synchronous Three Gastric Fundic Gland Polyps with Low-grade Dysplasia Treated with Endoscopic Mucosal Resection after Being Diagnosed to Be Tubular Adenocarcinoma Based on a Biopsy Specimen. Intern Med 2019; 58:1871-5.
- 22. Yasuda T, Tatsushi O, Yagi N. Fundic Gland Type Adenocarcinoma in Fundic Gland Polyps. Intern Med 2020; 59:455-6.
- 23. Cheung KS, Leung WK. Long-term use of proton-pump inhibitors and risk of gastric cancer:a review of the current evidence. Ther Adv Gastroenterol 2019; 12:1-11.
- 24. Tran-Duy A, Spaetgens B, Hoes AW et al. Use of Proton Pump Inhibitors and Risks of Fundic Gland Polyps and Gastric Cancer:Systematic Review and Meta-analysis. Clin Gastroenterol Hepatol 2016; 14:1706-19.