2017 Volume 50 Issue 1 Pages 26-32
2017 Volume 50 Issue 1 Pages 26-32
症例は73歳の男性で,腹部超音波検査で胆囊腫大を指摘され,腹部造影CTおよびMRIにて肝門部領域胆管に全周性壁肥厚と造影効果を伴った腫瘤を認めた.肝門部領域胆管癌の診断にて肝左葉尾状葉切除,亜全胃温存膵頭十二指腸切除,門脈切除再建術を施行した.病理組織学的には腫瘍の角化傾向がみられ,免疫染色検査で扁平上皮のマーカーであるCK5/6,p63が腫瘍全体に発現しており,扁平上皮癌と診断した.腫瘍に腺癌の成分は確認されなかった.術後3年9か月経過した現在,無再発で外来通院中である.肝門部領域胆管扁平上皮癌の術後長期生存の報告はまれである.
胆道癌は日常臨床の現場で比較的よくみられるが,多くは腺癌であり,まれに一部扁平上皮癌の成分を有する腺扁平上皮癌がみられることがあるが,胆道系原発の扁平上皮癌は極めてまれである1).今回,我々は肝門部領域原発の扁平上皮癌の1例を経験した.これまでの肝外胆管原発の扁平上皮癌の報告10例に自験例を加えて,臨床的特徴を検討したので報告する.
患者:73歳,男性
主訴:特になし.
家族歴,既往歴:右腎癌(60歳時に右腎摘出術施行)
現病歴:右腎癌術後の定期検査の腹部超音波検査で胆囊腫大を指摘され,当院泌尿器科より紹介となった.
入院時現症:身長170 cm,体重64 kg.
腹部は平坦・軟で特記すべき身体所見は認めなかった.
血液検査所見:生化学検査でCre 1.13 mg/dlと軽度腎機能障害を認めた.腫瘍マーカーはCEA・CA19-9ともに基準値内であった.
腹部造影CT所見:肝門部領域胆管を中心に壁肥厚と造影効果を伴った35 mmにわたる全周性の壁肥厚を伴った腫瘤を形成し,一部門脈に接していた.肝門部から膵上縁に至るまで胆管壁の造影効果を認めた.肝内胆管の拡張は認めなかったが,膵上縁から肝門部に至るまで胆管内腫瘤圧排による胆管狭窄を疑う所見を認めた(Fig. 1).

a, b: Abdominal enhanced CT revealed that the tumor was located in the perihilar bile duct, and contact with the portal vein.
ERCP所見:肝門部胆管を主座に腫瘤を形成し,上流側は左右肝管合流部,下流側は膵上縁に接していた(Fig. 2).ERCP時に施行した管腔内超音波検査(intraductal ultrasonography;以下,IDUSと略記)では左右肝管分岐部から腫瘤を認めた.深達度は粘膜層にとどまると思われ,生検を腫瘤部下端,左右肝管分岐部,左肝管から行った.HE標本では明らかな癌であったが,特定の分化を示さず組織分類が困難な癌であった.
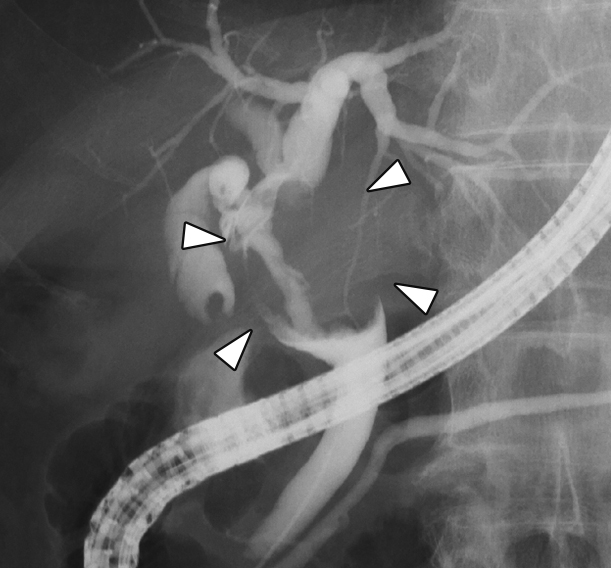
ERCP showed the perihilar bile duct tumor. The tumor progressed to the middle bile duct from the left and right hepatic duct confluence section.
以上より,結節型で広範進展を有する肝門部領域胆管癌の術前診断で,根治切除には肝左葉・尾状葉切除,亜全胃温存膵頭十二指腸切除,門脈切除再建術が必要と判断し,手術を施行した.術前ICG-R15値は9.1%と良好であった.
手術所見:腫瘍を肝十二指腸間膜内に固く触知した.固有肝動脈,左右肝動脈には明らかな肉眼的浸潤を認めなかったが,門脈本幹への肉眼的浸潤は認めた.腫瘍は膵内まで進展しており,根治切除として肝左葉・尾状葉切除,亜全胃温存膵頭十二指腸切除,門脈切除再建術を施行した.門脈は2 cm合併切除し端々吻合を行った.胆管は前区域・後区域の2孔となり,再建はWhipple法にて行った.手術時間は420分,出血量は850 ml,輸血は施行しなかった.
摘出標本肉眼所見:胆管の割面では壁全層に肥厚を認め,4×3 cmの腫瘍を認めた.腫瘍は白色・辺縁不整で結節浸潤型と診断した(Fig. 3).

The macroscopic specimen finding was that the tumor accounted for all layers of the perihilar bile duct wall.
病理組織学的検査所見:病理組織的に腫瘍はクロマチンの増加した大小不同のある異型核を持つ細胞が充実性に浸潤増殖していた.標本内のほぼ腫瘍全体に角化傾向がみられ,腫瘍に腺癌の成分は認められず,扁平上皮癌で占められていた.
免疫染色検査では扁平上皮癌を特異的に発現するCK5/6,p63で陽性を示した.腫瘍の角化傾向があまりみられない箇所でも発現しており,腫瘍全体に扁平上皮癌の成分が含まれていると考えられた(Fig. 4).胆道癌取扱い規約第6版による組織学的分類では,squamous cell carcinoma,Bp,pT1a,int,INFβ,ly1,v1,pn2,s0,hinf0,ginf0,panc0,Du0,PV0,A0,pHM0,pDM0,pEM0,pT1N0M0 stage Iであった.

a: HE×200. Histopathological findings showed that the keratinization was observed throughout the tumor. Tumor were occupied by components of the squamous cell carcinoma. b: CK5/6 ×200, c: p63 ×200. Immunohistochemical examination showed expression of squamous epithelial markers.
術後経過:膵液瘻(Grade B)を合併したが保存的に軽快し,術後第45病日に退院した.術後3年9か月経過した現在,再発は認めていない.
肝外胆管原発の扁平上皮癌は報告例も少なく,その臨床像にいまだ不明な点も多い.剖検例からの発生頻度をみると,肝外胆管の悪性腫瘍(全悪性腫瘍例中の1.3~1.4%)の中では,腺癌が94.0~94.8%とほとんどを占め,腺扁平上皮癌が1.7~3.8%,扁平上皮癌は0~1.4%と極めて少ない1).
肝外胆管原発の扁平上皮癌の報告は1930年のCabot2)の総胆管における扁平上皮癌の剖検例が第1例である.このCabot2)の報告例を含め,PubMedおよび医中誌Webで「胆管癌(bile duct cancer)」,「扁平上皮癌(squamous cell carcinoma)」をキーワードとしてPubMedは1950年から2015年1月まで,医中誌Webは1977年から2015年1月までの検索期間で検索した結果,自験例を含めると11例2)~11)の報告しかなく極めてまれな疾患である(Table 1).
| No. | Author | Year | Age/Sex | Jaundice | Tumor location (bile duct) | Surgery | Survival time (month) |
|---|---|---|---|---|---|---|---|
| 1 | Cabot2) | 1930 | 58/M | N/A | superior (Bs) | autopsy | unknown |
| 2 | Burger3) | 1978 | 24/F | N/A | inferior (Bi) | PD | 8m death |
| 3 | Aranha4) | 1980 | 56/M | + | porta hepatis (Bp) | biliary drainage | 3m death |
| 4 | Clements5) | 1990 | 73/M | + | porta hepatis (Bp) | autopsy | unknown |
| 5 | Heianyama6) | 1990 | 68/M | + | middle (Bm) | PD | 3m |
| 6 | Sakata7) | 1991 | 68/M | + | inferior (Bi) | PD | 27m |
| 7 | Shibata8) | 1994 | 50/M | + | porta hepatis (Bp) | Lt. hepatectomy | 10m |
| 8 | Nakasaki9) | 1996 | 75/M | + | inferior (Bi) | PD | 6m |
| 9 | Cho10) | 2000 | 64/M | + | inferior (Bi) | PD | 6m |
| 10 | Sewkani11) | 2005 | 60/M | + | inferior (Bi) | PD | unknown |
| 11 | Our case | 73/M | − | middle (Bm) | HPD+PVR | 45m |
PD: pancreatoduodenectomy, HPD: hepatopancreatoduodenectomy, PVR: portal vein resection, N/A: not applicable
胆管の粘膜は1層の円柱上皮からなっており,正常では扁平上皮細胞は存在しない7).そのため胆管に原発した扁平上皮癌の組織発生に関して,早渕ら12)の報告を引用すると以下の四つに大別される.
①異所性扁平上皮の癌化
②未分化基底細胞由来の癌
③先行する腺癌細胞の扁平上皮化生
④扁平上皮化生の癌化
①の異所性扁平上皮の癌化説,②の未分化基底細胞由来の癌説は報告例がなく,現在のところは否定的である.③の先行する腺癌細胞の扁平上皮化生説においては,純粋な扁平上皮癌よりも比較的報告例の多い腺扁平上皮癌で,腺癌成分と扁平上皮癌成分の境界部に両者の移行像が認められたという報告13)~16)もあることから,従来より腺扁平上皮癌の報告例においてこの仮説が支持されていることが多い.しかし,本症例においては摘出標本の全割連続切片からは腺癌の部分が全く存在しなかった.さらに,免疫染色検査において,扁平上皮癌を特異的に発現するマーカーであるCK5/6,p63を用いても,角化傾向が明らかでない部分にも発現が認められ,腫瘍全体に扁平上皮癌の成分が含まれていた.このことからも本症例においては③の可能性は低いと考えられる.腫瘍部位こそ異なるが,Boswellら17)は胃の扁平上皮癌の検討において,純粋な扁平上皮癌は腺癌の化生によって発生したものではないと推論している.Karasawaら18)も胆囊における純粋な扁平上皮癌は,腺扁平上皮癌にみられるような腺癌の扁平上皮化生とは異なった組織発生を考えるべきであると述べている.本症例において最も考えられる可能性は④の扁平上皮化生の癌化である.肝外胆管原発の扁平上皮癌の最初の報告者であるCabot2)も長期にわたる炎症性刺激による胆管粘膜の扁平上皮化生からの癌化説を提唱した.湯浅ら19)も下部胆管の腺扁平上皮癌の非癌部胆管上皮に散在性に扁平上皮化生を認めたと報告しており,扁平上皮化性の癌化の可能性を示唆している.いずれにしろ症例数が極めて少ない現時点で,その発生過程に関して明確な説明は困難であるが,本症例のような純粋な扁平上皮癌と腺扁平上皮癌では,初期の発生過程は異なると考えられる.
自験例を含めた11例中2)~11),10例は男性症例であった.腫瘍の胆管狭窄による黄疸での発症は記載があるもので8例4)~11)で認めた.自験例は黄疸発症ではなく,腎癌術後の定期腹部超音波検査で胆囊腫大を指摘され精査で診断された.定期検査がなければ,自験例もいずれは腫瘍増大による胆管狭窄で黄疸を来していたと思われる.
予後については,従来予後不良とする報告3)~5)が多い.その理由の一つとして内藤ら20)は,扁平上皮癌は腺癌の2倍の速さで成長するため,腺癌から腺扁平上皮癌に変わると悪性度が高くなるというものである.その他にも,病理組織学的な予後不良因子として膵浸潤,リンパ節転移,curabilityが悪いと悪性度が高いとする報告21)もある.ただこれらは胆管原発の腺扁平上皮癌について述べているものであり,発生過程が異なると思われる純粋な扁平上皮癌にそのまま当てはめて考えることには疑問が残る.
胆管癌は解剖学的位置関係から,しばしば門脈や肝動脈に浸潤するが,近年血管合併切除再建が積極的に行われるようになった22)~24).水平方向への進展が広範である症例に対してhepatopancreatoduodenectomy(HPD)が唯一の根治切除となりうる症例もあり24),本症例においても術中所見で肝十二指腸間膜と門脈本幹への浸潤を疑い,根治性を高めるために肝左葉・尾状葉切除,亜全胃温存膵頭十二指腸切除,門脈切除再建術を施行した.
予後不良な報告が多い中で,本症例は治癒切除後3年9か月経過している.今後とも慎重な経過観察のもと,長期予後を期待している.
利益相反:なし