Abstract
先天性第VII因子欠乏症(以下,第VII因子欠乏症と略記)は,まれな疾患である.第VII因子欠乏症併存胃癌症例に対し,遺伝子組換え活性型第VII因子製剤(以下,rFVIIaと略記)を投与し胃切除術を施行した.症例は58歳の男性で,B型肝炎治療のため検査を施行し,第VII因子欠乏症併存胃癌と診断された.プロトロンビン時間が18.0秒(control 12.7秒)と延長し,第VII因子活性は10%と低下していた.上部消化管内視鏡検査では胃角部前壁に胃癌を認めた.以上より,第VII因子欠乏症併存胃癌と診断し,術直前にrFVIIa 1.2 mg(18 μg/kg)を静脈注射し幽門側胃切除術を施行した.術後も第VII因子活性を測定しながら第4病日までにrFVIIa 1.2 mgを計13回静脈注射した.第VII因子欠乏症の手術報告例は少なく,第VII因子活性の測定およびrFVIIaの投与により安全に施行できた.
Translated Abstract
Congenital factor VII deficiency is a rare disease. We performed gastrectomy safely in a gastric cancer case with congenital factor VII deficiency after administering recombinant activated factor VII (rFVIIa) preoperatively. The patient, who was a 58-year-old man, underwent examination to treat hepatitis B and was given a diagnosis of gastric cancer with congenital factor VII deficiency. Prothrombin time was prolonged to 18.0 seconds (control 12.7 seconds), and factor VII activity was reduced to 10%. Upper gastrointestinal endoscopy showed gastric cancer on the anterior wall of the gastric angle. We performed distal gastrectomy after intravenous injection of rFVIIa 1.2 mg (18 μg/kg) preoperatively. After distal gastrectomy, 1.2 mg of rFVIIa was injected intravenously for a total of 13 times by postoperative day 4, after measuring factor VII activity. Few cases of congenital factor VII deficiency have been reported in surgery, and distal gastrectomy was performed safely by measuring factor VII activity and administering rFVIIa.
はじめに
先天性第VII因子欠乏症(以下,第VII因子欠乏症と略記)は,常染色体劣性遺伝形式のまれな疾患であり,手術報告例も極めて少なく1),1951年に初めて報告された2).今回,我々は第VII因子欠乏症併存胃癌症例に対し,遺伝子組換え活性型第VII因子製剤(以下,rFVIIaと略記)を投与し胃切除術を施行,安全に術後管理ができた症例を経験したので報告する.
症例
症例:58歳,男性
既往歴:12歳時:虫垂炎手術.13,17歳時:中耳炎手術.18歳時:副鼻腔炎手術.2か月前から慢性B型肝炎に対しエンテカビルの内服治療を開始(感染時期は不明であるが,30歳頃にB型肝炎を指摘)していた.現在までに止血凝固異常や出血傾向を指摘されたことはなかったが,口腔内血腫は自覚することがあった.ビタミンK拮抗薬などの経口抗凝固薬の服用はしていない.
家族歴:出血傾向を示唆するような家族歴はなし.
嗜好品:アルコールは2合ほぼ毎日
現病歴:前医にて慢性B型肝炎の治療を行うにあたり,各消化器系検査を施行した.上部消化管内視鏡検査では早期胃癌が疑われたが,血液凝固学検査でプロトロンビン時間(以下,PTと略記)の延長を認め,凝固因子異常が疑われたために胃生検ができず,血液凝固学精査および消化器系精査のため当院に紹介された.
初診時身体所見:身長172 cm,体重67 kg,血圧112/68 mmHg,眼瞼結膜の貧血や眼球結膜の黄疸は認めなかった.体表リンパ節は触知しなかった.腹部は平坦,軟,肝脾およびその他の腫瘤も触知しなかった.女性化乳房,クモ状血管腫,手掌紅斑,皮下出血なども認めなかった.
血液凝固学検査結果:前医ではPT 36.3秒(INR 1.79)と延長,活性化部分トロンボプラスチン時間(以下,APTTと略記)は30.8秒と正常,プロトロンビン活性62.9%,第V因子活性75.2%,第VII因子活性11.8%,第X因子活性55.9%,PIVKA-II 11 mAU/ml(基準値範囲)であり,またビタミンK補充によるPT-INRの変化は1.70から1.61と改善しなかった.当院臨床検査医学科での精査結果を示す(Table 1).当院での検査結果も前医と同様にPT 18.0秒(INR 1.61)と延長,APTTは正常,第VII因子活性は10%と低値を示した.フィブリノゲンおよびアルブミン定量は基準値範囲であり,肝合成能は問題ないと判断した.また,抗リン脂質抗体およびループスアンチコアグラントを確認したが,抗カルジオリピン抗体および抗カルジオリピンβ2GPI抗体は陰性,またループスアンチコアグラント中和法およびdRVVTは正常であった.さらに,患者血漿に正常血漿を一定の割合で混和してPT測定するPTクロスミキシングテストでは因子欠乏の補正パターンであった(Fig. 1).検査結果から第VII因子抗体を含めた後天的凝固因子阻害は否定的で先天性第VII因子欠乏症と診断した.胃生検施行時には内視鏡検査の前後でrFVIIa 1.2 mg(18 μg/kg)の静脈投与を行い止血異常はなかった.後日,臨床検査医学科で遺伝子解析を行った結果,第VII因子遺伝子(F7)のエクソン1のシグナルペプチド領域のチミンからシトシンへの1塩基置換c.38t>c,p.Leu13Proによるミスセンス変異がホモ接合体で検出した.
Table 1
Blood biochemical findings on initial presentation and detailed examination of hemostasis
| WBC |
3,400/ul |
AST |
37 U/l |
PT-pt |
18.0 sec |
| RBC |
4.42×104/ul |
ALT |
39 U/l |
PT-cont |
12.7 sec |
| Hb |
13.9 g/dl |
LDH |
179 U/l |
INR |
1.61 |
| Ht |
40.90% |
γ-GTP |
42 U/l |
APTT-pt |
27.5 sec |
| PLT |
13.8×104/ul |
T-Chol |
150 mg/dl |
APTT-cont |
27.6 sec |
|
|
TP |
6.7 g/dl |
Fib |
229 mg/dl |
| CEA |
2.6 ng/ml |
ALB |
4.2 g/dl |
FDP |
1.3 μg/ml |
| CA19-9 |
34.5 U/ml |
T-Bil |
0.75 mg/dl |
|
|
| CA72-4 |
5.7 U/ml |
BUN |
8.9 mg/dl |
Coagulation factor II |
62% (80~120) |
|
|
CRTN |
0.69 mg/dl |
Coagulation factor V |
86% (80~120) |
| HBs antigen |
>2,000.0 COI |
Na |
141 mEq/l |
Coagulation factor VII |
10% (80~120) |
| HBs antibody |
(−) |
Cl |
104 mEq/l |
Coagulation factor X |
74% (80~120) |
| HBe antigen |
(−) |
K |
4.0 mEq/l |
|
|
| HBe antibody |
100% INH |
CRP |
<0.3 mg/dl |
anti-β2-glycoprotein I antibody |
(−) |
| HBc antibody |
98.2×200% INH |
|
|
anticardiolipin antibody |
(−) |
| HBV-DNA |
<3.7 LGE/ml |
|
|
LA(SCT) |
<0 (≤6.3) |
|
|
|
|
LA (dRVVT) |
0.98 (<1.3) |

生化学検査結果:肝機能は正常であったが,ICG15分値は16.2%であった.腫瘍マーカーはCEA,CA19-9は正常値であったが,CA72-4 5.7 U/ml(4.0 U/ml以下)と高値であった.HBs抗原,HBe抗体,HBc抗体はいずれも陽性,HBV-DNA定量は3.7 LGE/ml未満であった(Table 1).
消化器系検査結果
上部消化管造影検査所見:腫瘍は不明瞭で確認できなかった.
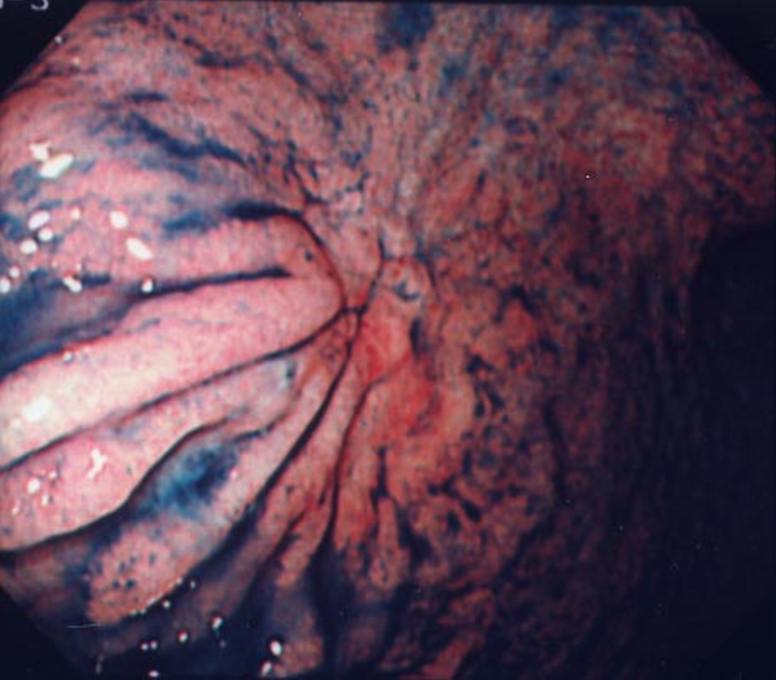
上部消化管内視鏡検査所見:食道胃静脈瘤は認めなかった.胃角部前壁にひだの融合と棍棒状変化を伴う0-IIc病変を認めた.深達度はSMと診断した(Fig. 2).生検結果は低分化腺癌であった.
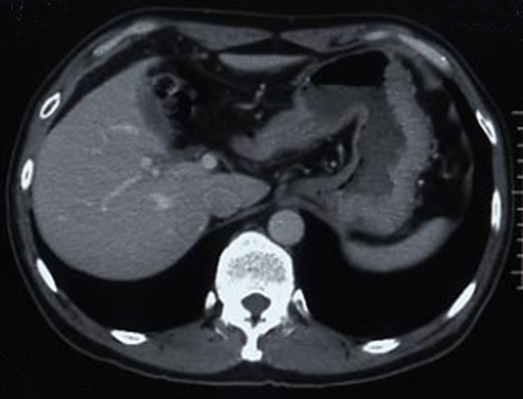
腹部造影CT所見:食道および胃周囲の静脈拡張は明らかでなかった.腫大リンパ節,遠隔臓器転移,腹水は認めなかった.また,肝臓・脾臓にも異常は認めなかった(Fig. 3).
本症例診断時の胃癌取扱い規約第13版に準じ,L-Ant c T1(SM)N0 H0 P0 CYx M0 cStage IAと診断した.
術前カンファレンス:臨床検査医学科とのカンファレンスの結果,周術期にrFVIIaを投与することにより手術リスクを低下させることが可能であると判断した.治療方針は同時期の胃癌治療ガイドライン第2版に準じた.腹腔鏡下胃癌手術の導入前であったため,開腹手術を施行した.出血が危惧されたので硬膜外麻酔は行わず,術後疼痛管理目的に経静脈患者管理鎮痛(IVPCA)を使用した.
手術所見:腹腔内に転移を疑う所見は認めなかった.肝臓表面は凹凸であり,肝線維症の病態であった.幽門側胃切除,D1+β郭清,B-I再建術を施行した(胃癌取扱い規約第13版).確実な止血を目的として通常より結紮を多用した(エネルギーデバイスは使用しなかった).術中明らかな噴出性の出血はなかったが,脾被膜損傷による脾臓からの出血と脆弱な組織からのoozingが多く,出血量が増加した.輸血は行わなかった.手術時間は230分,出血量は1,255 mlであった.
摘出標本の肉眼および病理組織学的検査所見:L-Antに0-IIc病変を認めた.摘出胃の大網には術中に生じた血腫が形成されていた.
組織型はpor2,深達度M,リンパ節に転移は認めなかった.以上より,f T1(M)N0 H0 P0 CYx M0;fStage IAと診断した.
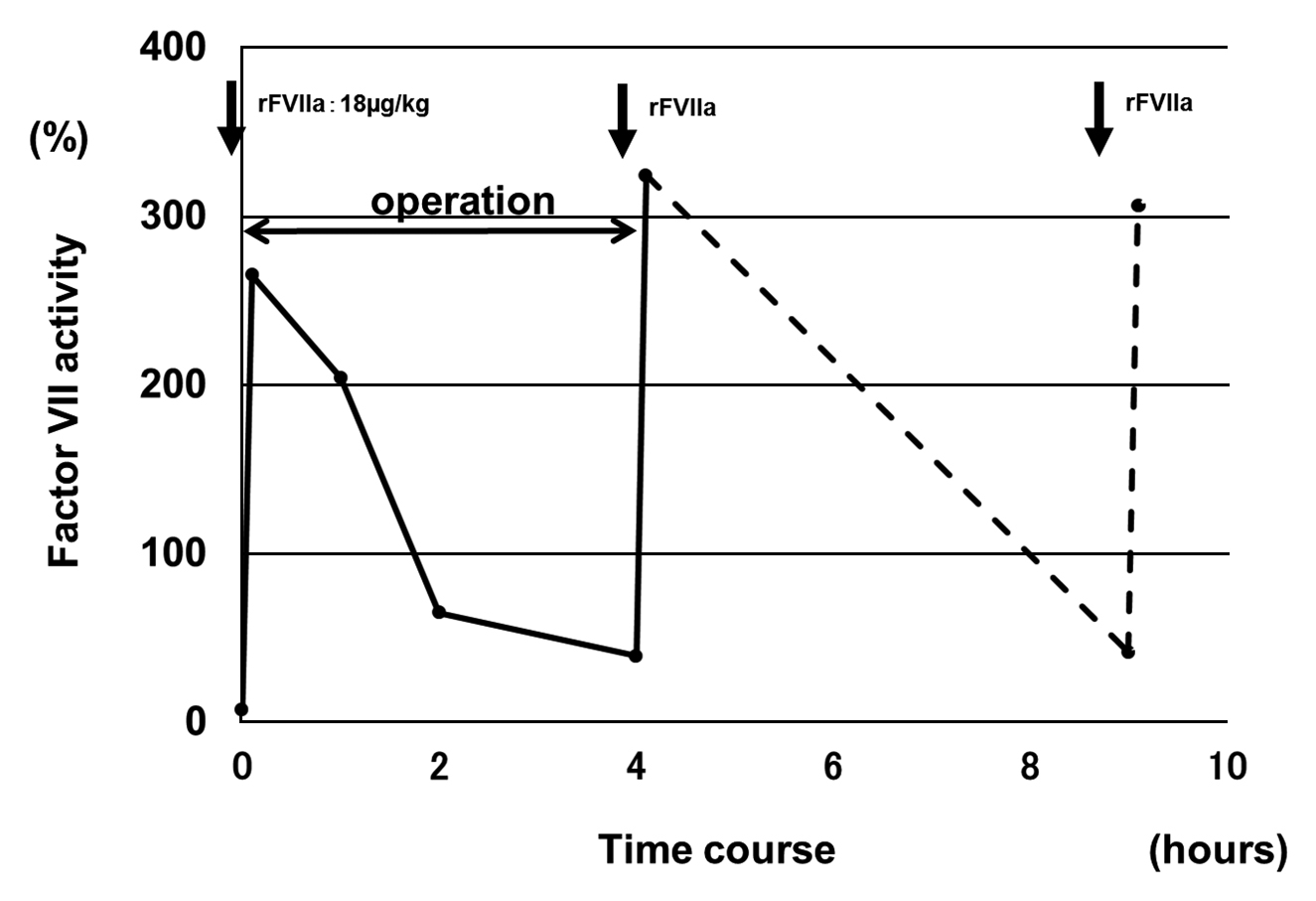
術中および術後経過:第VII因子活性は臨床検査医学科がACL9000(IL社)によって随時測定した.執刀直前および手術終了時(初回投与時より4時間後)にrFVIIaを1.2 mg(18 μg/kg)ずつ静脈投与した.rFVIIaの初回投与15分後には第VII因子活性値は7.12%から265%まで速やかに上昇し,その後1時間後に204%,2時間後に64.7%,4時間後には39.0%まで低下し,2回目のrFVIIaを投与し直後324%まで上昇した(Fig. 4).その後は5時間後にrFVIIaを1.2 mg投与し,以後8時間ごとに術後4日目までrFVIIaを1.2 mgずつ合計13回静脈投与した.13回目の投与に合わせてドレーンを抜去し,出血症状はなかった.術後第2病日と第4病日のPT(INR)はそれぞれ13.9秒(1.17),12.3秒(1.00)と正常を推移した.術後出血は認めず順調に経過し,血栓症状も出現しなかった.第5病日より経口摂取を開始,第11病日に軽快退院した.退院後は外来に5年通院し,以降の外来通院は終了とした.その期間中の肝炎の経過観察は紹介医が行っており,その期間中に出血のエピソードなどはなかった.
考察
第VII因子は血液凝固反応で働く重要な酵素前駆体で,止血栓,病的血栓の形成に不可欠な蛋白質である1).第VII因子欠乏症は1951年にAlexanderら2)により初めて報告された.常染色体劣性遺伝形式で,発症頻度は地域によって異なるようであるが,発症頻度は50万人に1人という極めてまれな疾患であり1),2001年時点では277例が登録されている3).臨床的には第VII因子活性の低下に基づくPTの延長が見られる.出血症状は極めて多彩といわれており,鼻出血,歯肉出血,皮下出血などである.重症例では関節内出血,中枢神経系出血も合併し,女性では過多月経が見られる1).出血症状と凝固活性が乖離することがあるが,その原因は検査試薬の違いが関与していると考えられている1).
本症例は凝固検査においてPT延長が精査のきっかけとなった.APTTも延長している場合には,後天性としてはdisseminated intravascular coagulation(以下,DICと略記)による凝固因子の消費,ビタミンK欠乏によるビタミンK依存性凝固因子の低下,経口ビタミンK拮抗剤の服用,重症肝障害にともなう肝合成能の低下による凝固因子の産生障害が考えられる.また,共通系凝固因子である第V因子,第X因子,プロトロンビン(第II因子),フィブリノゲンの低下によっても起きる.本症例はAPTTが正常であるため,これらの病態は考えにくい.ビタミンK拮抗薬の服用はなく,精査の結果ではDIC,ビタミンK欠乏や肝合成能障害を示さなかった.共通系凝固因子も有意な低下は見られていない.本症例のようにPT延長,APTT正常の場合には,まず外因系凝固因子である第VII因子の欠乏が考えられ,先天性もしくは後天性に分類される.その鑑別方法としてPTクロスミキシングテストによって,正常血漿を混和しても補正されない場合には,阻害物質の存在が考えられる.第VII因子抗体(インヒビター)やPT試薬に対する阻害物質として,抗リン脂質抗体やループスアンチコアグラントが考えられるが,正常血漿の混和によりPTは補正され,またその他の検査結果からもそれらを示唆する結果は得られなかった.以上より,本症例は過去に出血傾向がみられていないが,先天性第VII因子欠乏症と診断した.後日行った遺伝子解析でもF7遺伝子エクソン1のミスセンス変異をホモ接合体で検出されている.
第VII因子活性は10%以上なら出血症状はほとんどないとされ1),本症例も10%程度の活性値をもっているので,これまでは大きな止血異常はなかったと考えられる.大手術に際しては安全のためトラフ値を20%程度に維持することを目標とする.また,Zimmermannら4)は第VII因子活性が10%以下の手術では補充療法が必要であり,特に術後3日間は15%以上に保つべきと述べている.
以前は第VII因子欠乏症において止血を目的とする保険適応の薬剤がなく,従来は第VII因子を含むプロトロンビン複合体製剤を使用していた.しかし,欧米ではrFVIIaが適応となっており,15~30 μg/kgの4~6時間毎投与が推奨されている.これをもとに花房ら5)によりrFVIIaの使用臨床試験が13例に行われた.本薬剤との因果関係は不明だが使用症例のうち,使用後凝固能亢進が1例にみられたが他の副作用はなく,安全性が確認された.現在は本邦でも第VII因子欠乏症に対してrFVIIaの使用が承認されている.
凝固因子の中で第VII因子は半減期が4~6時間とビタミンK依存性凝固因子の中で最も短い1)6).また,rFVIIaの半減期は2.82~3.11時間と報告されている5).海外では,第VII因子欠乏症へのrFVIIaの投与により抗第VII因子同種抗体の発現も報告されており注意が必要である1).また,Ingerslevら7)は,第VII因子欠乏症において血栓症発現の報告している.原因としてプロトロンビン複合体製剤の補充で他の凝固因子活性が上昇したことにより凝固能が亢進したため,または第VII因子欠乏症自体が血栓傾向を出現させる可能性も考えられているが,明らかなことはわかっていない7).本症例では血栓症歴はなく,また周術期での血栓症発症もみられなかった.インヒビター保有血友病症例においてrFVIIaの使用による血栓塞栓症の報告はあるが,第VII因子欠乏症に対してのrFVIIaの使用では血栓形成は現在のところ報告されていない8).
rFVIIaの手術時の適正使用方法を検討するために術前にrFVIIaの投与試験を施行した報告がある6)9).この試験によりrFVIIaの投与後の第VII因子活性値の減衰変化を確認し,術中術後の投与方法を決定する.本症例においては,rFVIIaの半減期がおよそ3時間であることから,臨床検査医学科の協力のもと術中術後に第VII因子活性を測定し,rFVIIaの適正な投与量と投与間隔を決定した.初回投与前の活性値は7.12%であったが,rFVIIa 18 μg/kgの投与15分後には活性値が265%まで速やかに上昇し,投与4時間後の活性値は39%まで低下した(Fig. 4).術後活性値を測定し,8時間毎の投与により活性値を十分に保てると判断した.以降術後4日目まで8時間毎に投与を継続した.術後4日目にドレーン抜去直前に13回目のrFVIIaを投与し,出血することなく抜去でき,以降rFVIIaの投与なく経過良好であった.現時点まで第VII因子欠乏症に対するrFVIIaの投与による血栓形成の報告はないものの,投与量の増加により血栓形成の可能性は高くなると思われる.前述のように術後3日間は15%以上に保つべきとあり4),本症例のような術後の出血がなく,侵襲的な処置がない場合には,投与を終了とすることも選択肢の一つと考える.
第VII因子欠乏症の手術の報告は少なく,1964年から2019年4月までの医学中央雑誌で「先天性第VII因子欠乏症」をキーワードとして検索した(会議録除く)結果,消化器手術の報告は5例のみであった5)10)~12).消化器疾患でない報告は21例あった5)6)9)13)~23)(Table 2).2000年以前の症例ではrFVIIaを使用していなかった.花房ら5)は消化器疾患では2例のrFVIIaの使用経験を報告している.1例はS状結腸切除術で,術後のoozingに対しrFVIIaを2回投与した.もう1例は胃切除術中術後にrFVIIaを6~12時間毎に13回使用していた.2例ともに良好な経過であった.我々は8時間毎のrFVIIaを合計13回使用し,良好な経過であった.欧米では4~6時間毎の投与が推奨使用方法であるが,本症例においては活性値を測定することにより推奨時間より長い8時間毎の投与で対応が可能であった.本症例は8時間毎の投与で安全に周術期が管理できたのは,当院で第VII因子活性が約30分と迅速に測定可能であったためと考えられる.頻回に測定できない場合や結果判定に時間を要する場合には,前述のように術前に投与試験を行い,投与量と投与間隔の計画を立てることも一つの手段として考えるべきであろう.
Table 2
Reported surgery cases for congenital factor VII deficiency
| No |
Author |
Year |
Age/Sex |
Pre ope VII (%) |
PT (%) |
PT (sec) |
History of bleeding |
Operation |
Bleeding (ml) |
Blood preparation |
Dose (μg/kg) |
Dosing interval (h) |
VII range (%) |
Last day of administration |
| 1 |
Nakagawa10) |
1990 |
76/M |
8 |
40 |
29.8 |
− |
stomach |
270 |
PPSB |
|
|
|
POD7 |
| 2 |
Hanabusa5) |
2006 |
59/M |
<3 |
|
100.6 |
− |
colon |
50 |
rFVIIa×2 |
23 |
|
|
|
| 3 |
Hanabusa5) |
2006 |
55/M |
10 |
|
20.6 |
− |
stomach |
263 |
rFVIIa×13 |
15 |
|
|
|
| 4 |
Mino11) |
2015 |
68/M |
44.1 |
31.1 |
19.6 |
+ |
colon |
160 |
rFVIIa×92 |
30 |
4–24 |
48.2 |
POD16 |
| 5 |
Nakano12) |
2015 |
32/M |
17 |
32 |
|
− |
duodenum |
2,082 |
rFVIIa×4 |
15 |
4–6 |
|
POD1 |
| 6 |
Our case |
|
58/M |
10 |
|
18 |
− |
stomach |
1,255 |
rFVIIa×13 |
17 |
8 |
7.12–324 |
POD4 |
| 7 |
Hayashi14) |
1974 |
59/F |
2–12 |
|
29 |
+ |
tooth |
|
Konyne |
|
|
|
|
| 8 |
Umehara15) |
1996 |
42/M |
12 |
|
32.5 |
+ |
kidney |
|
PROPLEX ST |
|
|
|
|
| 9 |
Takahashi6) |
2003 |
68/F |
1.1 |
13.4 |
|
+ |
hip joint |
662 |
rFVIIa×9 |
|
8–12 |
41.8–330.2 |
POD3 |
| 10 |
Niikura9) |
2005 |
68/F |
1.1 |
13.4 |
|
+ |
hip joint |
662 |
rFVIIa×9 |
28.6 |
12 |
32.1–39.9 |
POD3 |
| 11 |
Satoh16) |
2006 |
17/F |
<3 |
25 |
|
|
tooth |
|
rFVIIa×1 |
20 |
|
61–336 |
|
| 12 |
Hanabusa5) |
2006 |
32/F |
<3 |
|
|
|
tooth |
0 |
rFVIIa×1 |
21 |
|
61–336 |
|
| 13 |
Hanabusa5) |
2006 |
11/M |
|
|
|
|
tooth |
0 |
rFVIIa×2 |
35 |
4 |
|
|
| 14 |
Hanabusa5) |
2006 |
69/M |
|
|
|
|
prostatic biopsy |
— |
rFVIIa×1 |
23 |
|
|
|
| 15 |
Hanabusa5) |
2006 |
67/M |
|
|
|
|
hernia |
<10 |
rFVIIa×1 |
24 |
|
|
|
| 16 |
Hanabusa5) |
2006 |
68/F |
1.1 |
|
|
+ |
hip joint |
662 |
rFVIIa×8 |
29 |
8–12 |
42–330 |
POD3 |
| 17 |
Hanabusa5) |
2006 |
78/F |
11 |
|
|
|
hip joint |
1,160 |
rFVIIa×1 |
30 |
|
|
|
| 18 |
Hanabusa5) |
2006 |
33/F |
|
30.6 |
|
|
Cesarean |
1,000 |
rFVIIa×4 |
10–20 |
5 h |
|
|
| 19 |
Hanabusa5) |
2006 |
60d/ |
|
30 |
|
|
heart |
442 |
rFVIIa×2 |
30 |
2–3 |
|
|
| 20 |
Koeda17) |
2007 |
20/M |
42 |
47.4 |
15.5 |
− |
mandible |
0 |
— |
|
|
|
|
| 21 |
Jodai18) |
2009 |
65/M |
47 |
34.3 |
16.9 |
− |
lung |
770 |
rFVIIa×1 |
19.7 |
|
|
|
| 22 |
Fukuyama19) |
2010 |
43/M |
10.1 |
25.1 |
20.5 |
+ |
tooth |
|
|
|
|
|
|
| 23 |
Jinbo13) |
2014 |
18/M |
46 |
55 |
15.3 |
+ |
lung |
|
rFVIIa×5 |
|
5 |
|
|
| 24 |
Yoshioka20) |
2014 |
58/F |
<3 |
|
56.4 |
+ |
uterus |
342 |
rFVIIa×16 |
18 |
4–12 |
|
POD3 |
| 25 |
Kurihara21) |
2014 |
23/M |
10 |
|
|
|
tooth |
|
rFVIIa×4 |
|
3–16 |
|
POD1 |
| 26 |
Miyata22) |
2016 |
61/M |
31 |
|
14.6 |
− |
lung |
165 |
rFVIIa×3+continuous |
20 |
|
|
POD5 |
| 27 |
Sawai23) |
2017 |
70/F |
|
|
|
|
knee |
|
rFVIIa×9 |
|
|
|
|
PPSB: heat-treated prothrombin complex concentrates
検索しえた報告例を検討するとrFVIIaの使用方法はさまざまであった.投与量は10~35 μg/kgで投与間隔は2~24時間であった.最長の24時間の投与は定期投与でなく徐々に間隔を延長した投与方法であり,同様に投与間隔を徐々に延長する方法が散見された.三野ら11)の報告は複合型の凝固異常症例であるが,術後のrFVIIaの投与間隔を延長したところ後出血がみられ,投与間隔を再度短縮し良好な止血効果が得られたとしている.また,止血不十分のため持続投与に変更し,その後良好な止血が得られた報告もあった22).神保ら13)は,術後出血に対してrFVIIaを使用し,止血可能であったと述べている.本症例の活性測定結果より,rFVIIaを投与すると早急に活性値が上昇するため,これらの症例は投与直後より止血効果が得られたと考えられた.
rFVIIaの使用方法に関しては,第VII因子欠乏症症例が少ないため明言はできない.しかし,今回の検討では多くの報告で欧米の推奨量・間隔で投与されていた.また,rFVIIa投与後の血栓症などの合併症は報告されておらず,現時点での投与方法は欧米の推奨法に準ずるのが妥当と考える.ただし,止血困難な状況では増量,持続なども検討は必要であろう.術後3日間は活性値を15%以上に保つことを推奨されているが4),大手術であってもrFVIIaを数回だけの投与の症例も散見され,第VII因子欠乏症の程度および止血異常の程度が症例によって異なるため,統一した見解はない.また,実臨床で活性値が常時15%以上保っているかを確認することも困難である.現状としては,まず推奨法で投与し,その後個々の症例に合わせた投与を検討せざるをえない.
第VII因子欠乏症はまれであるため,手術時のrFVIIaの使用方法もいまだ確立されていない.今後,症例が集積され,rFVIIaの使用方法が確立されることが望まれる.
謝辞 稿を終えるにあたり,第VII因子欠乏症について指導,助言を頂いた東京医科大学臨床検査医学科の先生方に深く感謝申し上げます.
利益相反:なし
文献
- 1) 一瀬 白帝.血液症候群II 凝固・線溶異常による出血傾向 血友病および類縁疾患 VII因子欠損症/異常症.別冊日本臨牀.1998;21:460–463.
- 2) Alexander B, Goldstein R, Landwehr G, Cook CD. Congenital SPCA deficiency: a hitherto unrecognized coagulation defect with hemorrhage rectified by serum and serum fractions. J Clin Invest. 1951;30:596–608.
- 3) 高宮 脩, 沖本 由理.先天性第VII因子欠乏症.日本血栓止血学会誌.2001;12:320–327.
- 4) Zimmermann R, Ehlers G, Ehlers W, von Voss H, Göbel U, Wahn U. Congenital factor VII deficiency: a report of four new case. Blut. 1979;38:119–125.
- 5) 花房 秀次, 大山 和成, 渡辺 智, 榊原 謙, 平松 祐司, 新福 玄二,ほか.先天性第VII因子欠乏症患者に対する遺伝子組換え活性型第VII因子製剤(注射用ノボセブン)の有効性と安全性.日本血栓止血学会誌.2006;17:695–705.
- 6) 高橋 完靖, 西川 哲夫, 三枝 康宏, 藤代 高明, 今堀 正也, 黒坂 昌弘.全人工股関節置換術を施行した先天性第VII因子欠乏症の1例.臨床整形外科.2003;38:679–681.
- 7) Ingerslev J, Kristensen HL. Clinical picture and treatment strategies in factor VII deficiency. Haemophilia. 1998;4:689–696.
- 8) 桑原 光弘.Factor VIIa製剤の過去・現在・未来.日本血栓止血学会誌.2014;25:475–481.
- 9) Niikura T, Nishikawa T, Saegusa Y, Fujishiro T, Yoshiya S, Kurosaka M. Total hip arthroplasty in severe congenital factor VII deficiency: successful use of recombinant activated factor VII for hemostasis. J Arthroplasty. 2005;20:396–400.
- 10) 中川 国利, 古沢 昭, 桃野 哲, 佐々木 陽平, 氏家 紀一.胃切除を施行した先天性第VII因子欠乏症の1例.日本外科学会雑誌.1990;91:771–773.
- 11) 三野 和宏, 服部 優宏, 後藤 順一, 土橋 誠一郎, 安本 篤史, 玉置 透,ほか.複合型の先天性凝固因子欠乏症患者に発症した結腸憩室出血の1例.日本消化器外科学会雑誌.2015;48:60–67.
- 12) 中野 順隆, 寺島 秀夫, 真船 太一, 塚本 俊太郎, 朴 秀吉, 今村 史人,ほか.出血性十二指腸gastrointestinal stromal tumorに対して膵頭十二指腸切除を施行した先天性凝固第VII因子欠乏症の1例.日本消化器外科学会雑誌.2015;48:23–30.
- 13) 神保 充孝, 郷良 秀典.先天性第VII因子欠乏症患者の自然気胸術後の止血に第VII因子製剤の投与が有効であった1例.日本呼吸器外科学会雑誌.2014;28:183–187.
- 14) 林 久智, 佐々木 雅英, 吉岡 溥夫, 新谷 憲治, 半沢 敦正, 喜多嶋 康一.先天性第VII因子欠乏症の1例.臨床血液.1974;15:1042–1048.
- 15) 梅原 次男, 北村 寛, 三宅 正文, 中沢 修, 飯塚 惇三.先天性第VII因子欠乏症に発症した両側腎結石に対する治療経験.泌尿器外科.1996;9:501–504.
- 16) Satoh K, Okamoto M, Torimura A, Taguchi R, Mineno Y, Mizutani H. Successful hemostasis after dental extraction with the use of recombinant activated factor VII in a factor VII deficient patient. Oral Sci Int. 2006;3:10–12.
- 17) 小枝 聡子, 稲原 英恵, 根井 仁志, 鈴木 孝裕, 後藤 哲, 川村 仁.先天性第VII因子欠乏症を伴った骨格性下顎前突症患者に対し下顎枝矢状分割術を施行した1例.日本顎変形症学会雑誌.2007;17:42–50.
- 18) 城台 環, 上田 純二, 加藤 雅人.左肺摘除術を施行した先天性第VII因子欠乏症の1例.日本呼吸器外科学会雑誌.2009;23:101–104.
- 19) 福山 裕子, 鈴木 正二, 星野 都, 井上 勝元, 福田 正勝, 坂下 英明.先天性第VII因子欠乏症の抜歯経験.有病者歯科医療.2010;19:33–37.
- 20) 吉岡 智子, 高橋 直人, 白澤 弘光, 藤本 俊朗, 澤田 賢一.術前検査にて診断され補充療法が奏功した先天性第VII因子欠乏症.東北止血・血栓研究会会誌.2014;XXVI:13–16.
- 21) 栗原 由貴, 石井 宏昭, 笠原 英生.先天性出血性素因を有する患者に対する抜歯経験.有病者歯科医療.2014;23:186–191.
- 22) Miyata N, Isaka M, Kojima H, Maniwa T, Takahashi S, Takamiya O, et al. Continuous infusion of recombinant activated factor VII for bleeding control after lobectomy in a patient with inherited factor VII deficiency. Gen Thorac Cardiovasc Surg. 2016;64:177–180.
- 23) 澤井 龍生, 高木 陽平, 大井 雄紀, 土山 耕南, 藤岡 宏幸, 吉矢 晋一.先天性第VII因子欠乏症を有する変形性肩関節症に対し肩人工骨頭置換術を施行した1例.中部日本整形外科災害外科学会雑誌.2017;60:755–756.