2021 Volume 54 Issue 8 Pages 523-530
2021 Volume 54 Issue 8 Pages 523-530
症例は85歳の女性で,局所進行膵頭部癌(上腸間膜動脈,門脈浸潤)に対し,化学放射線療法後に亜全胃温存膵頭十二指腸切除術,門脈合併切除再建術を施行した.術後経過は良好であったが3か月目に下血と貧血を認めた.CTで肝外門脈閉塞(extrahepatic portal vein obstruction;以下,EHOと略記)と肝管空腸吻合部周囲に増生した側副血行路を認めた.ダブルバルーン小腸内視鏡検査で静脈瘤を肝管空腸吻合部に認め,同部からの出血と診断した.門脈圧減圧による出血予防を目的に部分的脾動脈塞栓術(partial splenic embolization;以下,PSEと略記)を施行した.その後は出血を認めていない.EHOにより生じる異所性静脈瘤出血は診断・治療の困難な致命的な合併症であるが治療法は確立していない.PSEは肝管空腸吻合部静脈瘤出血に対し一考すべき治療法である.
An 85-year-old woman was diagnosed with locally advanced pancreatic carcinoma involving the superior mesenteric artery and portal vein. She underwent subtotal stomach-preserving pancreaticoduodenectomy with portal vein resection after chemoradiotherapy. The postoperative course was uneventful. However, she was readmitted to our hospital with anemia and melena 3 months postoperatively. CT showed an obstructed portal vein and formation of collaterals adjacent to the hepaticojejunostomy site. Double-balloon endoscopy revealed red color sign-positive varices around the hepaticojejunostomy site, and hemorrhage from the varices was diagnosed. Endoscopic therapy was not possible because it was difficult to maintain a table position for endoscopy. Therefore, partial splenic embolization (PSE) was performed to reduce portal venous pressure and control the hemorrhage. Melena and anemia have not occurred after PSE. Ectopic variceal hemorrhage caused by extrahepatic portal vein obstruction is a lethal complication after intraperitoneal surgery, and early detection and treatment of the hemorrhagic source remain difficult. No guidelines for variceal hemorrhage around the hepaticojejunostomy site have been established. This case suggests that PSE should be considered as treatment for variceal hemorrhage around the hepaticojejunostomy site.
腹部消化管手術後の肝外門脈閉塞(extrahepatic portal vein obstruction;以下,EHOと略記)による門脈圧亢進症により小腸などに生じる異所性静脈瘤出血は診断・治療に難渋することが多く,致命的な合併症の一つである1).今回,膵頭十二指腸切除(pancreatoduodenectomy;以下,PDと略記)・門脈合併切除術後の肝外門脈閉塞が原因で生じた肝管空腸吻合部静脈瘤出血に対し,部分的脾動脈塞栓術(partial splenic embolization;以下,PSEと略記)により門脈圧を低下させることでコントロールを得られた症例を経験したので報告する.
患者:85歳,女性
主訴:黒色便
既往歴:高血圧,高脂血症,骨粗鬆症
現病歴:閉塞性黄疸で前医受診,切除不能な局所進行膵頭部癌(cT4,cN0,M0:cStage III2),門脈・上腸間膜動脈浸潤)の診断となった(Fig. 1a).化学放射線療法(重粒子線照射12回,gemcitabine+nab-paclitaxel 2コース)が著効し,腫瘍縮小効果を認めたため(Fig. 1b),conversion手術として亜全胃温存膵頭十二指腸切除術(Child変法)+門脈合併切除再建を施行した.手術時間は548分,出血量は800 mlであった.膵臓切離後,上腸間膜動脈右側組織の硬結が疑われた.術前より下腸間膜静脈は脾静脈に流入していることを確認しており,脾静脈は上腸間膜動脈右側の視野確保のため上腸間膜静脈と下腸間膜静脈間で切離し,左胃静脈も切離した.腫瘍の門脈浸潤を認めたため脾静脈分岐部よりも中枢側門脈約2 cm長の門脈合併切除を施行した(Fig. 2).門脈再建は5-0PROLENEを両端にかけ2点支持とし,連続縫合(後壁:intraluminal suture method,前壁:over and over method)で施行した.術後経過は良好であり術後25日目に退院となった.退院前に撮影した腹部造影CTでは明らかな異常所見は認めなかった.病理診断はinvasive ductal carcinoma,T1b,N0,M0:Stage Ib2),組織学的治療効果はGrade 32)であった.

(a) A pancreatic head tumor was diagnosed as locally advanced pancreatic carcinoma involving the superior mesenteric vein (★) and artery (☆), and was judged to be unresectable based on initial CT. (b) After chemoradiotherapy, the tumor was diagnosed as borderline resectable pancreatic carcinoma because it was reduced in size after chemoradiotherapy.

Schematic diagram showing the relationships of the pancreatic head tumor and veins during the operation. The portal vein (PV), superior mesentric vein (SMV), splenic vein (SV), right gastric vein (RGV), and the pancreatic head tumor were detected. The veins were cut as shown in this schema and the PV was reconstructed.
術後3か月目に黒色便を認め受診,採血で貧血の進行も認めた.
来院時採血所見:貧血の進行(Hb:7.2 g/dl)とBUN(28.1 mg/dl)/CRE(0.65 mg/dl)比の上昇を認め,主訴と併せて消化管出血が疑われた.その他に特記すべき異常所見はなかった.
来院時腹部造影CT所見:肝管空腸吻合部近傍腸管壁に強い造影効果を認め,またEHO,側副血行路の発達を認めた(Fig. 3).

CT at the time of observation of anemia and melena. (a) Extrahepatic portal vein obstruction (arrow). (b) Irregular high density area around the hepaticojejunostomy site (arrow).
上部下部消化管内視鏡検査所見:明らかな出血の原因となる所見は認めなかった.
来院後経過:禁食と赤血球濃厚液の輸血を計6単位投与後に軽快し退院となるも,その1か月後に再度黒色便と貧血の進行を認めた.同様に禁食と赤血球濃厚液の輸血を計4単位投与後に軽快したが,今後も繰り返すと思われたため肝管空腸吻合部の静脈瘤からの出血を疑い,ダブルバルーン小腸内視鏡検査を施行した(Fig. 4).肝管空腸吻合部にred color sign陽性の静脈瘤を複数認め,ここからの出血が繰り返す貧血の原因と思われた.内視鏡的止血は手技的に困難であると判断し,薬物療法として門脈圧(静脈瘤圧)低下目的にβ遮断薬を投与したが効果は不十分であった.そこで血行動態の検索のために血管造影を施行した.
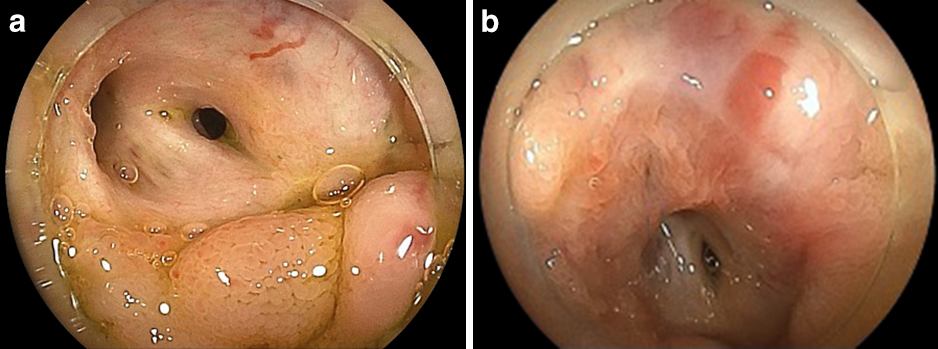
(a, b) Double-balloon endoscopy showed red color sign-positive varices around the hepaticojejunostomy site.
血管造影検査所見:上腸間膜動脈造影門脈相にて門脈は造影されず,求肝性の側副血行路を経由して肝門部より肝内門脈に流入していた.この側副血行路は挙上空腸の腸間膜静脈と診断した.脾動脈造影では,脾静脈は途絶し下腸間膜静脈を逆流して上腸間膜静脈に入り挙上空腸の腸間膜静脈を経由して肝門部より肝内門脈に流入していた.よってPSEによる脾静脈血流量の減少が門脈圧(静脈瘤圧)低下に寄与すると思われた.脾動脈分岐3本を選択し塞栓し,約7割程度の塞栓域を確認し処置を終了した(Fig. 5).PSEによる明らかな合併症は認めなかった.

Abdominal angiography. (a) Venous phase of superior mesentric artery angiography: the portal vein was obstructed and a hepatic hilar cavernous transformation supplied blood flow to the intrahepatic portal vein. (b) Arterial phase of splenic artery angiography. (c) Venous phase of splenic artery angiography: the splenic vein was interrupted, but the splenic venous blood flow was backward toward the inferior mesenteric vein and there was flow into hepatopetal collaterals via the superior mesenteric vein. (d) Celiac artery angiography after partial splenic embolization: the spleen was embolized in the range of about 70%.
PSE施行後は1年3か月間,貧血の進行や黒色便は認めていない.CT上も静脈瘤の増悪は認めず,脾臓は萎縮し一部造影不良域を持っていた(Fig. 6).

CT at one year and 3 months postoperatively. (a) Varices around the hepaticojejunostomy site showed no change. (b) Half of the spleen was atrophied and a partial contrast area was present.
EHOは肝前性門脈圧亢進症に分類され,肝門部を含めた肝外門脈の閉塞により門脈圧亢進症に至る症候群と定義される3).EHOは原因不明の一次性と,血液疾患,腫瘍,胆道炎,膵炎,臍炎,手術などが原因となる二次性がある4).また,PD後の良性閉塞としては術後の組織癒着や繊維化・炎症性変化による門脈閉塞,術中放射線照射例,本症例のような門脈合併切除再建後の閉塞がある5).また,門脈の切除長が3 cm以上の場合,術後1年目の開存率が低いという報告がある6).本症例の術後経過は良好であったため,門脈閉塞の原因は再建の手技であると推測され,一般的な門脈再建操作中に生じる問題は以下のものが挙げられるが本症例に関しては明らかでない.①運針が前・後壁に貫通する,②血管壁の全層ではなく一部にかけてしまう,③薄い門脈壁のため糸の貫通部で裂傷が生じる,④縫い代と間隔が乱れる,⑤最後の結紮をやや締め込んでしまう,などがある7).また,周辺臓器やドレーンなどによる外部からの圧迫で門脈が狭小化する場合もあり7),今後の手術の際には留意したい点である.
Lebrecら1)は門脈圧亢進症で食道と胃以外に発生した静脈瘤を異所性静脈瘤と定義した.EHOの約70%に消化管出血が見られ,腹部消化器手術既往例では食道・胃静脈瘤出血以外に異所性静脈瘤からの出血が多い.異所性静脈瘤は遠肝性と求肝性に分類される.遠肝性は一般的に肝硬変に伴うもので,求肝性は主に門脈閉塞の場合に出現し,閉塞した門脈の遠位部から側副血行路が肝十二指腸,肝結腸靭帯,胆囊周囲を通って肝臓まで網目状に発達する.外観が海綿状血管腫に似ていることからcavernous transformation of the portal veinと称されている8).しかし,PD後の門脈閉塞では肝十二指腸靭帯郭清により同部の側副血行路の発達は期待できず,門脈系血流は挙上空腸の腸間膜静脈を逆流し,肝管空腸吻合部の静脈叢を通り求肝性に流入するため,吻合部粘膜下の静脈瘤は発達して破裂,出血を引き起こす9).出血部位の特定が困難な場合もあるが,本症例のようにダブルバルーン小腸内視鏡や上部消化管内視鏡検査で観察できた報告もある10).
術後のEHOによる肝管空腸吻合部静脈瘤からの出血の治療法は外科的治療,内視鏡的治療,interventional radiology(以下,IVRと略記),薬物治療などがある.外科的治療には静脈シャント術,出血部空腸切除・再吻合術の報告がある8)9)11).しかし,本症例ではPD後の腹腔内の状態から外科的治療は手技的に困難であると判断した.内視鏡的治療には,内視鏡的静脈瘤硬化療法(endoscopic injection sclerotherapy;以下,EISと略記),内視鏡的静脈瘤結紮術,内視鏡的クリッピング術があるが,本症例のように手技的に困難である場合がある12).特にEISの場合,血管内に注入した硬化剤が肝内に流入することが危惧される.IVRでは経回腸静脈静脈瘤塞栓術(transileocolic vein obliteration;以下,TIOと略記)が静脈瘤へのアプローチ法として選択される12).しかし,本症例では求肝性側副血行路が静脈瘤を形成していることから,注入した硬化剤が肝内に流入し肝門部の虚血の危険性がありTIOの選択は断念した.Hiyoshiら13)は門脈ステントの開存期間の中央値は14か月(2~84か月)と良好であったと報告しているものの,血栓形成による早期ステント閉塞などの合併症もあり,一定した長期成功例は報告されていない14).薬物治療では門脈圧(静脈瘤圧)を下げる目的でβ遮断薬や硝酸薬が使用されるが15),本症例では効果は不十分であった.
PD術後のEHOによる肝管空腸吻合部静脈瘤出血の治療報告例を医学中央雑誌において「肝管(胆管)空腸吻合部静脈瘤」で1986年~2019年の間で検索(会議録を除く)したところ,自験例を含めて12例の報告例があった(Table 1)9)~12)14)16)~20).PDの再建法はIIA法が最も多く,門脈合併切除例は6例,出血の発症時期は術後3か月から4年と幅広かった.治療法は門脈ステント留置術,シャント手術,経回結腸静脈的塞栓術,内視鏡的処置の報告があるが,PSEでの加療は本症例のみであった.本症例では下腸間膜静脈は切離した脾静脈分岐であり,脾動脈造影をした際に,脾静脈から下腸間膜静脈を逆流し,結腸間膜辺縁静脈,上腸間膜静脈を経由して挙上空腸腸間膜静脈から肝門部へ流入する側副血行路が確認できたため,PSEによる門脈圧(静脈瘤圧)の減圧が見込まれた.近年PSEはステロイドの使用や脾内動脈の選択的塞栓などで合併症を減らす工夫がなされている21)22).処置後の発熱や疼痛の大半は非ステロイド性抗炎症薬でコントロール可能であり,重篤な合併症は少なく,門脈圧亢進症に対する低侵襲な治療法の一つである21)22).今回の症例に対しても低侵襲で有効な治療であったと考えられる.似たような病態として,PD後の左側門脈圧亢進症による膵空腸吻合部静脈瘤出血に対しPSEで治療した報告23)や一次性EHOによる胃静脈瘤出血に対しPSE併用で治療した報告24)などがある.いずれもPSE後の明らかな合併症は認めず,また静脈瘤の再出血を認めておらず低侵襲で効果的な治療法であったと思われる.本症例の場合,通常は門脈閉塞や静脈瘤に対する治療が検討されることが多い中で,患者背景や当施設の機能を考慮し第一に選択された治療がPSEであった.しかし,一般的にPSEの治療過程において,脾動脈の血流量には個人差があり脾動脈の塞栓範囲を規定することは困難である.さらに,脾静脈の血流量が門脈閉塞に伴う側副血行の血流量や静脈瘤からの出血に与える影響を定量化することは困難であり,門脈閉塞を有する全ての患者において,PSEに一定の治療効果を期待することは難しいかもしれない.そのため,本症例では幸いにもPSEの効果が継続しているが,2回目以降のPSEやPSE併用で別の治療も考慮すべきである.
| No | Author | Year | Age/Sex | Primary disease | Operation | PV reconstruction | Duration from surgery to bleeding | Treatment | Outcome |
|---|---|---|---|---|---|---|---|---|---|
| 1 | Koike16) | 2002 | 39/F | Pancreatic NET | PPPD | + | 5 m | PV metal stenting | No recurrence (21 m) |
| 2 | Yamamoto11) | 2009 | 61/M | Pancreatic cancer | PD-IIA | – | 18 m | Splenic-left portal shunt | No recurrence (12 m) |
| 3 | Kosono10) | 2009 | 49/F | Pancreatic cancer | PPPD-IIA | + | 24 m | PV metal stenting | No recurrence (18 m) |
| 4 | Hirota17) | 2010 | 63/F | Bile duct cancer | PD-IIA | + | 13 m | PV metal stenting | No recurrence (3 m) |
| 5 | Senda18) | 2010 | 67/F | Pancreatic cancer | PPPD-IIA | + | 11 m | EIS | No recurrence (18 m) |
| 6 | Kubokawa19) | 2010 | 68/M | Bile duct cancer | PD | – | 35 m | PV metal stenting →Failure | Recurrence (35 m) Death (48 m) |
| 7 | Kubokawa19) | 2010 | 70/M | Bile duct cancer | SSPPD | + | 10 m | No treatment | Recurrence (12 m) Death (16 m) |
| 8 | Kubo14) | 2013 | 49/F | Pancreatic cancer | PPPD-IIA | + | 20 m | PV metal stenting | None |
| 9 | Saeki20) | 2013 | 59/F | Duodenal cancer | PD | – | 36 m | TIO | No recurrence (12 m) |
| 10 | Matsui9) | 2016 | 58/F | IPMC | PD-III | – | 48 m | Splenectomy and CSRS | No recurrence (96 m) |
| 11 | Kanesada12) | 2018 | 80/M | Bile duct cancer | PPPD-IIA | – | 3 m | Endoscopic clipping | No recurrence (18 m) |
| 12 | Our case | 83/F | Pancreatic cancer | SSPPD-IIA | + | 3 m | Partial splenic embolization | No recurrence (15 m) |
PV: portal vein, PPPD: pylorus-preserving pancreaticoduodenectomy, PD: pancreaticoduodenectomy, EIS: endoscopic injection sclerotherapy, SSPPD: subtotal stomach-preserving pancreaticoduodenectomy, TIO: transileocolic vein obliteration, CSRS: central splenorenal shunt
脾静脈切離を伴うPDでは術後の左側門脈圧亢進症がしばしば問題となる.Mizunoら25)の報告では,術後3年以内に左側門脈圧亢進症で生じた静脈瘤からの出血は4.2%であった.本症例は門脈閉塞が主な原因と考えられるが,左胃静脈や中結腸静脈,副右結腸静脈が切離された症例では左側門脈圧亢進症予防に脾静脈再建も考慮するという報告26)もある.この病態に関してはまだ不明確な点もあり,今後さらなる研究が望まれる.
PSEはPD術後のEHOによる肝管空腸吻合部静脈瘤出血に対し,一考すべき治療法の一つであると考えられた.今後のPSEによるさらなる治療報告や検討が望まれる.
本論文の要旨は第26回門脈圧亢進症学会(2019年9月,山口)にて発表した.
利益相反:なし