2026 Volume 53 Issue 1 Pages 49-55
2026 Volume 53 Issue 1 Pages 49-55
【目的】大腿骨近位部骨折(hip fractures:以下,HFs)患者における入院時血清アルブミン値と退院時歩行自立度との関連を,ポリファーマシーの有無・程度別に検討した。【方法】75歳以上のHFs術後患者243例を対象に,常用薬数によって非ポリファーマシー群,ポリファーマシー群(6剤以上),ハイパーポリファーマシー群(10剤以上)の3群に分類した。退院時functional ambulation category(以下,FAC)スコア3以上を歩行自立と定義し,血清アルブミン値との関連を多重ロジスティック回帰分析によって患者層ごとに評価した。【結果】血清アルブミン値はポリファーマシー群(OR 2.49)とハイパーポリファーマシー群(OR 3.59)においてのみFACスコア3以上と有意に関連した。【結論】入院時血清アルブミン値は,ポリファーマシー患者においてこそ,退院時歩行自立を予測する有用な指標となる。
Objective: This study aimed to clarify the association between serum albumin levels at hospital admission and ambulatory independence at discharge in older patients with hip fractures (HFs), stratified by the presence and degree of polypharmacy.
Methods: We retrospectively analyzed 243 postoperative patients aged ≥75 years who underwent surgery for HFs. Patients were stratified into three groups based on the number of regularly prescribed oral medications: non-polypharmacy (<6 drugs), polypharmacy (≥6 drugs), and hyper-polypharmacy (≥10 drugs). Ambulatory independence was defined as achieving a Functional Ambulation Categories (FAC) score of ≥3 at discharge. Multivariable logistic regression analyses were conducted separately within each group, and odds ratios (ORs) with 95% confidence intervals (CIs) were calculated. Receiver operating characteristic curve analysis was performed to evaluate predictive performance, summarized by the area under the curve (AUC).
Results: The proportion of patients achieving FAC scores of ≥3 at discharge was 47.1% in the non-polypharmacy group, 39.9% in the polypharmacy group, and 39.7% in the hyper-polypharmacy group. Serum albumin levels were significantly associated with achieving FAC scores ≥3 in the polypharmacy group (OR, 2.49; 95% CI, 1.35–4.80) and the hyper-polypharmacy group (OR, 3.59; 95% CI, 1.31–11.54), but not in the non-polypharmacy group. The highest predictive accuracy was observed in the hyper-polypharmacy group (AUC=0.67).
Conclusion: Serum albumin levels at admission may have limited predictive value in patients without polypharmacy but appear to be particularly informative for predicting ambulatory independence, defined as achieving FAC scores of ≥3 at discharge, among older patients with polypharmacy or hyper-polypharmacy.
わが国における大腿骨近位部骨折(hip fractures:以下,HFs)は,80歳以上の患者が全体の7割以上を占める主要な加齢関連疾患である1)2)。急性期病院は,高齢患者の早期歩行能力回復を支援し,スムーズな転院調整を提供する必要がある3)。そのため,入院時の限られた情報に基づき退院時の機能的転帰を予測することは,不良転帰が予測される症例への重点的な介入計画を可能にするため,その臨床的意義は大きい。そのような背景のなか,血清アルブミン値(以下,アルブミン値)は,HFs患者の術後合併症の発症や死亡率4)5),さらには急性期退院時の歩行自立度(以下,退院時歩行自立度)との関連が指摘されている6)7)。多くの先行研究では,入院時に採取された血液検体によるアルブミン値が予後予測に用いられており,臨床の早期段階で得られる指標として有用性が期待されている。
しかしながら,高齢者では多疾患併存状態が一般的であり8),その影響による慢性炎症の持続は,非栄養学的要因によるアルブミン値低下を招くことが知られている9)10)。先行研究ではこの点を十分に考慮しておらず,アルブミン値の予後予測因子としての一般化可能性は限定的である。また,併存疾患負担の指標として広く用いられるCharlson Comorbidity Index(以下,CCI)は,フレイルやサルコペニアといった高齢者特有の健康状態を反映しない11)。そのため,CCIでは高齢者の併存疾患負担を適切に評価できるとは言いがたい。このように,アルブミン値に対する併存疾患負担の影響はこれまで定量的に評価されておらず,アルブミン値の予後予測能には限界があると考えられる。
そこで本研究では,併存疾患負担を反映する可能性のある指標として常用薬数に着眼した。わが国の高齢者は複数の慢性疾患を背景に多剤併用状態(以下,ポリファーマシー)にあることが多い12)。ポリファーマシーは,薬物有害事象リスクの増大や服薬アドヒアランス低下との関連が指摘されており13–15),高齢者医療における重要な課題である。加えて,ポリファーマシーは転倒,日常生活動作能力の低下,嚥下障害といった不良転帰の増加とも関連し16–18),高齢者の併存疾患負担を間接的に反映する指標となることが期待される。本研究の目的は,高齢HFs術後患者をポリファーマシーの有無と程度に基づいて層別化し,入院時アルブミン値の退院時歩行自立度に対する予測能の違いを検討することである。
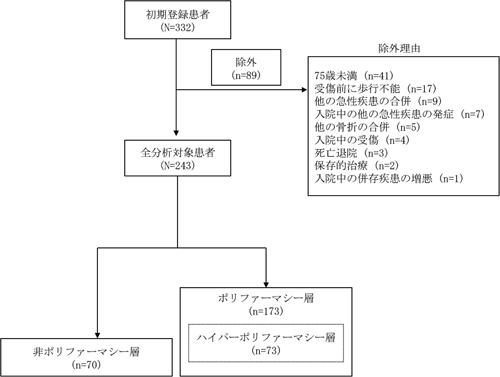
本研究は,後方視的コホート観察研究として実施した。対象は,2017年4月から2023年8月の間に,320床を有する急性期総合病院である地方独立行政法人大牟田市立病院(以下,当院)に入院したHFs患者332例とした。除外基準は,1)75歳未満,2)受傷前に歩行不能であった患者,3)頭部外傷性疾患などの他の急性疾患の合併,4)入院中に新たな急性疾患を発症した場合,5)他部位の骨折の併発,6)当院入院中の受傷,7)死亡退院,8)保存的治療を受けた場合,9)入院中に併存疾患の増悪が認められた場合とした。除外基準に該当した89例を除外し,最終的に243例を解析対象とした。本研究では後方視的デザインの特性上,あらかじめサンプルサイズの算出は行わず,解析可能な全症例(n=243)を対象とした(図1)。
手術は,骨接合術または人工骨頭置換術(bipolar hip arthroplasty:以下,BHA)が行われた。当院のクリニカルパスでは,手術翌日から理学療法を開始し,骨接合術では術後2日目,BHAでは術後4日目から全荷重による歩行練習を許可している。一般的にはBHAの方が早期荷重が可能とされるが,当院では術後の脱臼リスクを回避する目的から,クリニカルパスに基づきBHAを術後3日目まで免荷とする運用を行っている。加えて,関節可動域運動,筋力増強運動,心肺持久力運動などを,疼痛や身体状況に応じて段階的に実施した。栄養管理については,基礎疾患の有無や種類に応じた標準食または治療食を基本とし,必要に応じて補液や静脈栄養が行われた。アルブミン製剤の投与は,主治医の臨床判断に基づき限られた症例にのみ実施された。
2. ベースラインデータの収集データは,整形外科領域で5年以上の臨床経験を有する理学療法士3名が分担して収集し,ダブルチェックにより検証された。これにより測定バイアスの最小化を図った。収集したベースライン項目は,先行研究に基づき,退院時歩行自立度に影響を及ぼす可能性があるものとした。具体的には,年齢,性別,body mass index(以下,BMI),受傷前の歩行補助具の使用有無(以下,歩行補助具の使用),骨折型,受傷から手術までの日数(time to surgery:以下,TTS),術式,併存疾患の有無,アルブミン値,入院時の推定糸球体濾過量(estimated glomerular filtration rate:以下,eGFR),老年栄養リスク指数(geriatric nutritional risk index:以下,GNRI)および常用薬数である19–23)。
歩行補助具については,使用の有無のみを記録し,その種類の分類は行わなかった。骨折型は,大腿骨頸部骨折と大腿骨転子部骨折の2種類に分類し,各型における臨床的重症度の評価は実施しなかった。術式は骨接合術とBHAの2種類に分類したが,手術時間,出血量,麻酔方法,使用インプラントの種類については,調査対象外とした。併存疾患については,代表的な慢性疾患である高血圧(hypertension:以下,HT)に加え,HFs術後の不良転帰との関連が報告されている2型糖尿病(type 2 diabetes mellitus:以下,T2DM),慢性心不全(chronic heart failure:以下,CHF),慢性腎臓病(chronic kidney disease:以下,CKD)および血液透析(hemodialysis:HD)の有無を調査したが24–28),それらの臨床的重症度評価は行わなかった。アルブミン値は,受傷による影響を最小限に抑えるために,入院1日目の採血によって得られた検体から当院の標準検査法により測定したが,受傷から測定までの期間は調査しなかった。GNRIは,先行研究に基づく計算式にしたがって算出した29)。常用薬数は,入院時に患者が持参した薬剤のうち,2週間以上継続して処方されている内服薬の品目数と定義し,その数をカウントした。点眼薬,点鼻薬,吸入薬,外用薬,注射薬,解熱鎮痛薬などの頓用薬,ならびに市販薬やサプリメントなどの非処方薬は除外した。なお,先行研究を参考に,常用薬が6剤以上の場合をポリファーマシー,10剤以上の場合をハイパーポリファーマシーと定義した30–32)。
3. アウトカムの設定歩行能力の評価には,HFs患者を対象とした先行研究で汎用されているfunctional ambulation category(以下,FAC)スコアを使用した33)34)。FACスコアは,歩行時に必要とされる身体的介助の程度に基づき,0から5の6段階で評価される臨床指標であり,スコアが高いほど歩行の自立度が高いことを示す34)。FACスコア3は,体重を支えるような直接的な身体的介助なしに歩行が可能な状態を指すが,安全確保のための他者による監視を必要とする場合を含む34)。本研究におけるアウトカムは,退院時に身体的介助を要さない歩行能力への到達とし,FACスコア3以上に設定した35)。
4. 統計学的処理本研究では,ベースライン項目およびアウトカムにおける欠損データは認められなかったため,すべての症例を完全データとして解析に含めた。まず,対象者を常用薬数に基づき,非ポリファーマシー群およびポリファーマシー群の2群に分類した。次に,ポリファーマシー群のうち,10剤以上の常用薬を有する群をハイパーポリファーマシー群として追加分割し,最終的に3群(非ポリファーマシー群,ポリファーマシー群,ハイパーポリファーマシー群)に層別化した。
続いて,各群におけるベースライン特性とアウトカムの要約統計量として,数値変数は平均値または中央値,カテゴリ変数は割合を算出した。数値変数の正規性はShapiro–Wilk検定により判定し,正規分布が認められた場合には平均値を,非正規分布の場合には中央値を採用した。最後に,アルブミン値と退院時歩行自立度との関連を検討するため,群別に多重ロジスティック回帰分析を実施した。従属変数はFACスコア3以上,独立変数はすべてのベースライン項目とした。解析は,非ポリファーマシー群をモデル1,ポリファーマシー群をモデル2,ハイパーポリファーマシー群をモデル3として,それぞれの群に限定したロジスティック回帰分析を行った。モデル構築にはAkaike’s information criterionに基づくステップワイズ法を用いた。
モデルの有意性は尤度比検定により評価し,抽出された各因子についてオッズ比(odds ratio:以下,OR)および95%信頼区間(95% confidence interval:以下,95%CI)を算出した。多重共線性の評価にはvariance inflation factor(以下,VIF)を用い,5以上の場合を多重共線性ありと判定した。モデルの適合度はHosmer–Lemeshow検定により評価した。receiver operating characteristic(以下,ROC)曲線分析では,アルブミン値が有意因子として抽出された群において,area under the curve(以下,AUC), Youden指数に基づくカットオフ値,感度および特異度を算出した。
すべての統計解析は,R(バージョン4.3.1, CRAN)およびR Commander(バージョン2.9-1)を使用して実施した。Hosmer–Lemeshow検定にはResource Selectionパッケージを用いた。すべての検定における有意水準はp<0.05とした。
5. 倫理的配慮本研究は,大牟田市立病院倫理審査委員会の承認を得て実施した(承認番号:第2324号)。全ての研究手続きでは,ヘルシンキ宣言を遵守し,患者の個人情報保護に配慮して匿名化を行った。後ろ向き研究であり,侵襲的な介入や患者への直接的な接触を伴わないため,書面によるインフォームドコンセントは取得せず,研究実施に関する情報を公開し,患者が研究参加を拒否できるオプトアウトの機会を保障した。
本研究のフローチャートを図1に示す。非ポリファーマシー群は70例,ポリファーマシー群は173例であり,後者のうち73例はハイパーポリファーマシー群に該当した。各群におけるベースライン特性およびアウトカムの要約統計量を表1に示す。アルブミン値の中央値は3.5~3.65 g/dLの範囲であり,ポリファーマシー群およびハイパーポリファーマシー群では相対的に低値を示した。退院時にFACスコア3以上を達成した割合は,非ポリファーマシー群で47.1%,ポリファーマシー群で39.9%,ハイパーポリファーマシー群で39.7%であり,ハイパーポリファーマシー群で最も低かった。
| 全分析対象患者 (N=243) |
非ポリファーマシー群 (n=70) |
ポリファーマシー群 (n=173) |
ハイパーポリファーマシー群 (n=73) |
|
|---|---|---|---|---|
| ベースラインデータ | ||||
| 年齢 | 88(84–92) | 88.5(82–93) | 88(84–92) | 88(84–90) |
| 女性(%) | 198(81.5) | 56(80.0) | 142(82.1) | 59(80.8) |
| BMI (kg/m2) | 19.4(17.5–21.8) | 18.3(16.9–20.2) | 19.6(17.8–22.4) | 20.1(18.2–23.5) |
| 受傷前の歩行補助具の使用(%) | 152(62.6) | 36(51.4) | 116(67.1) | 51(69.9) |
| 頚部骨折(%) | 133(54.7) | 37(52.9) | 96(55.5) | 36(49.3) |
| TTS(日) | 5(3–7) | 5(3–7) | 5(3–7) | 4(3–7) |
| 術式 | ||||
| BHA (%) | 88(36.2) | 23(32.9) | 65(37.6) | 24(32.9) |
| 併存疾患 | ||||
| T2DM (%) | 50(20.6) | 9(12.9) | 41(23.7) | 22(30.1) |
| HT (%) | 151(62.1) | 34(48.6) | 117(67.6) | 50(68.5) |
| CHF (%) | 50(20.6) | 9(12.9) | 41(23.7) | 19(26.0) |
| CKD (%) | 38(15.6) | 4(0.1) | 34(19.7) | 22(30.1) |
| HD (%) | 1(1.4) | 0(0) | 1(0.6) | 1(1.4) |
| 血清アルブミン値(g/dL) | 3.6(3.1–3.9) | 3.65(3.2–3.9) | 3.5(3.1–3.9) | 3.5(3.1–3.9) |
| eGFR (mL/min/1.73m2) | 58.5(40.9–72.1) | 64.4(51.2–76.4) | 52.8(36.6–70.3) | 47.6(25.3–65.3) |
| GNRI | 94.2±11.1 | 92.5±11.0 | 94.9±11.1 | 95.9±12.5 |
| 常用薬数 | 8(5–10) | 3(1–4) | 9(7–11) | 12(10–13) |
| アウトカム | ||||
| 退院時FACスコア3以上(%) | 102(42.0) | 33(47.1) | 69(39.9) | 29(39.7) |
正規分布が確認された変数は「平均値±標準偏差」,正規分布に従わない変数は「中央値(四分位範囲[25%–75%])」で示した.BMI:body mass index, TTS: time to surgery, BHA:bipolar hip arthroplasty, T2DM: type 2 diabetes mellitus, HT: hypertension, CHF: chronic heart failure, CKD: chronic kidney disease, HD: hemodialysis, eGFR: estimated glomerular filtration rate, GNRI: geriatric nutritional risk index, FAC: functional ambulation category.
多重ロジスティック回帰分析の結果を表2に示す。非ポリファーマシー群に対する解析(以下,モデル1)では,年齢(OR 0.88, 95%CI 0.79–0.95, p<0.01)およびeGFR(OR 0.97, 95%CI 0.93–0.99, p<0.05)が有意な関連因子として抽出されたが,アルブミン値は抽出されなかった。一方,ポリファーマシー群およびハイパーポリファーマシー群に対する解析(以下,モデル2およびモデル3)では,アルブミン値が有意変数として抽出され,モデル2ではOR 2.49(95%CI 1.35–4.80, p<0.01),モデル3ではOR 3.59(95%CI 1.31–11.54, p<0.05)であった。いずれのモデルにおいても,抽出された全変数のVIFは5未満であり,多重共線性は認められなかった。モデルごとの尤度比検定はいずれも有意(p<0.01)であり,Hosmer–Lemeshow検定の結果も,モデル1:p=0.71,モデル2:p=0.17,モデル3:p=0.18と,すべて良好な適合性を示した。アルブミン値の退院時FACスコア3以上に対するROC曲線分析の結果を表3に示す。モデル3におけるアルブミン値のカットオフ値は3.35 g/dLであり,AUCは0.67,感度86.2%,特異度52.3%を示し,3モデル中で最も高い予測精度を有していた。
| p値 | OR | 95% CI | VIF | ||
|---|---|---|---|---|---|
| 下限 | 上限 | ||||
| モデル1 | |||||
| 年齢 | 0.004 | 0.88 | 0.79 | 0.95 | 1.14 |
| CKD | 0.112 | 0.11 | 0.004 | 1.45 | 1.24 |
| eGFR | 0.024 | 0.97 | 0.93 | 0.99 | 1.35 |
| HT | 0.152 | 0.45 | 0.15 | 1.34 | 1.02 |
| モデル2 | |||||
| 血清アルブミン値 | 0.005 | 2.49 | 1.35 | 4.80 | 1.00 |
| 頚部骨折 | 0.070 | 1.81 | 0.96 | 3.48 | 1.00 |
| モデル3 | |||||
| 血清アルブミン値 | 0.020 | 3.59 | 1.31 | 11.54 | 1.07 |
| 年齢 | 0.124 | 0.93 | 0.85 | 1.02 | 1.00 |
| 頚部骨折 | 0.067 | 2.82 | 0.94 | 8.85 | 1.02 |
| 常用薬数 | 0.054 | 0.68 | 0.44 | 0.97 | 1.09 |
各モデルにおけるモデルχ2検定の結果はいずれもp<0.01であり,統計学的に有意であった.Hosmer–Lemeshow検定の結果は,モデル1: p=0.71, モデル2: p=0.17, モデル3: p=0.18であり,いずれも良好な適合性を示した.OR: odds ratio, CI: confidence interval, VIF: variance inflation factor, CKD: chronic kidney disease, eGFR: estimated glomerular filtration rate, HT: hypertension.
| モデル2 | モデル3 | |
|---|---|---|
| カットオフ値(g/dL) | 3.45 | 3.35 |
| 感度(95% CI) | 69.6 (58.7–80.4) | 86.2 (73.7–98.8) |
| 特異度(95% CI) | 53.8 (44.3–63.4) | 52.3 (37.5–67.0) |
| AUC (95% CI) | 0.64 (0.56–0.73) | 0.67 (0.54–0.80) |
CI: confidence interval, AUC: area under the curve.
本研究では,高齢HFs術後患者を対象に,退院時の歩行自立度に関連する因子を,常用薬数によって層別化して検討した。その結果,ポリファーマシー群およびハイパーポリファーマシー群において,入院時のアルブミン値が退院時の身体的介助を要さない歩行能力(FACスコア3以上)への到達と有意に関連していた。一方,非ポリファーマシー群ではこの関連は認められなかった。これらの結果は,アルブミン値がすべての患者に対して一律に有効な予後指標というよりも,多剤併用を要するような重症度の高い患者群において,特にその予測的意義が高まることを示唆するものである。
ポリファーマシー群およびハイパーポリファーマシー群では,HT, T2DM, CHF, CKDなどの慢性疾患が多く併存していた。これらの疾患は,慢性炎症を介してアルブミン値の低下を引き起こすことが知られている9)10)。さらに,骨折や手術に伴う急性炎症も,炎症性サイトカインの産生を通じて肝臓でのアルブミン合成を抑制し,アルブミン合成を直接的に抑制する36)。加えて,こうした慢性疾患や高齢そのものがサルコペニアのリスク因子でもあり,筋タンパク異化や慢性微小炎症がアルブミン値をさらに低下させる要因となる37–40)。本研究において,これらの疾患を多く有するポリファーマシー群でアルブミン値が相対的に低値であったことは,こうした複合的な病態を反映していると考えられる。また,先行研究では75歳以上の日本人高齢者におけるサルコペニアや死亡リスクの上昇と関連するアルブミン値のカットオフ値は3.8 g/dLとされている41)。本研究で算出されたカットオフ値は3.35~3.45 g/dLとこれを下回っており,対象者がすでに臨床的に意義のある低アルブミン血症の状態にあった可能性がある。アルブミン値は,低栄養状態,慢性疾患,炎症,サルコペニアなど,複数の病態を反映する包括的なバイオマーカーであり,特に併存疾患負担が高い患者群においては,退院時の歩行自立度を予測するうえで有用な臨床情報となりうる。
本研究にはいくつかの限界がある。第一に,後方視的コホート研究であるため,観察された入院時アルブミン値と退院時歩行自立度との関連は因果関係を示すものではない。また,ポリファーマシー群とハイパーポリファーマシー群の一部重複により,厳密な群間比較は困難であった。第二に,情報収集上の限界がある。受傷前の歩行能力についてFACスコアでの評価ができず,歩行補助具の使用有無を代替指標としたが,これにより歩行能力の実態を過小評価した可能性がある。さらに,認知機能,リハビリテーション実施量,薬剤の内容や有害事象,サルコペニアの評価といった,歩行自立度に影響しうる重要な交絡因子が十分に調整されていなかった点も,本研究の解釈上の重要な制約である。加えて,ROC解析におけるアルブミン値のAUCは最大でも0.67と予測精度は限定的であった。これは,対象者の年齢中央値が88歳と極めて高齢であったことから,加齢に伴う身体機能の多様性が予測モデルの精度に影響を与えた可能性がある。第三に,バイアスの影響が否定できない。アルブミン値の測定に関しては,受傷から採血までの期間にばらつきがある可能性があり,この点が測定値に影響を及ぼした可能性がある。また,本研究では院内受傷例を除外しており,これに伴う選択バイアスの影響も考慮する必要がある。さらに,アルブミン値を連続変数として解析した一方で,カテゴリ変数としての検討や,異なるカットオフ値を用いた感度分析を実施しておらず,これらの不実施は本研究におけるモデルの頑健性を制限する可能性がある。第四に,外的妥当性に関する限界がある。本研究は単施設で実施され,対象が極めて高齢の日本人患者に限定されているため,他施設や異なる年齢層への一般化には慎重な解釈が求められる。今後は,認知機能,サルコペニア指標,リハビリテーション実施量などの交絡因子を包括的に考慮した多因子予測モデルの構築,カットオフ値の感度分析を含む多角的な統計的検証,および多施設共同による前向き研究を通じて,外的妥当性と臨床応用性の高い知見の蓄積が求められる。
入院時のアルブミン値は,多疾患併存状態をはじめとした高齢者特有の健康状態を反映する包括的な指標として,高齢HFs患者における退院時歩行自立度の予測に有用である可能性がある。特に,10剤以上の薬剤を常用するハイパーポリファーマシー群において,その予測的意義は最も高かった。
本研究の実施にあたり,ご協力いただいた対象者ならびに関連施設の職員の皆様に深く感謝申し上げる。
本研究に関して開示すべき利益相反はなく,特定の研究助成も受けていない。