2015 Volume 57 Issue 6 Pages 275-285
2015 Volume 57 Issue 6 Pages 275-285
目的:がん治療に使用される抗がん剤の多くのものは健常者にとって有害な物質である.近年抗がん剤による医療従事者への職業性曝露,健康障害が危惧および報告されている.著者等は使用頻度や有害性が比較的に高い抗がん剤10種について,医療従事者の曝露に繋がる可能性の高い病院内汚染を把握するため,床や机に残留する抗がん剤を拭き取りLC/MSにより一斉分析する方法を開発した.対象と方法: 使用頻度や有害性が比較的に高い抗がん剤パクリタキセル,ビンクリスチン,ドセタキセル,ビノレルビン,イリノテカン,メトトレキサート,オキサリプラチン,ゲムシタビン,シクロホスファミド,フルオロウラシルを対象とした.多くの病院の床と同じ素材であるP-タイル上の抗がん剤を少量のメタノールに浸したセルロースろ紙またはポリプロピレン不織布で拭き取り,ヒドラジン一水和物含有メタノール5 mlで抽出およびろ過した.抽出とろ過を2回繰り返し,ろ液を1 mlまで濃縮しLC/MSにて測定した.また,安全キャビネット等と同じ素材であるステンレスプレートについても検討した.結果: P-タイル上に散布した対象の抗がん剤10物質のうちフルオロウラシルを除く9物質の回収率は37~101%,相対標準偏差1.8~19%であった.ステンレスプレート上からは対象10物質の回収率は35~111%,相対標準偏差は1.3~11%であった.考察と結論:対象とした抗がん剤10種は,分子量,オクタノール/水分配係数(logPow)等の物理化学的性状が多様であるため,1つの拭き取り素材では良好な回収率を得られなかった.しかし,拭き取りにセルロースろ紙とポリプロピレン不織布を対象物質によって使い分けることで,P-タイルではフルオロウラシルを除く対象抗がん剤9物質,ステンレスプレートでは対象10物質すべてについて汚染を定量的に把握,またはそれには劣るが床およびステンレス表面に残留する抗がん剤量を十分推定できる分析法の開発に至ったと考えられる.
抗がん剤を使用し治療する薬物療法は,がんの三大療法の1つであり,近年は入院患者のみではなく外来患者にも行われている1).
他方,抗がん剤の多くは健常者にとって有害な物質である.米国国立労働安全衛生研究所(NIOSH)2)は,保健医療現場において有害な医薬品を使用することや,その付近で作業をすることで皮膚発疹,不妊症,流産,先天性異常,白血病その他のがんを発症する恐れがあると警告している.抗がん剤の発がんリスクについては,国際がん研究機関IARC3)の分類によると,シクロホスファミド,エトポシド等がGroup 1(ヒトへの発がん性を有する),ドキソルビシン,カルムスチン等がGroup 2A(ヒトへの発がん性を高い確率で有する),ブレオマイシン,ダカルバジン等がGroup 2B(ヒトへの発がん性を有する可能性がある),フルオロウラシル,ビンクリスチン等がGroup 3(実験動物では発がん性の十分な証拠があるが,ヒトにおいては不十分な証拠であり,分類できない)に指定されている.加えて,タキサン系抗がん剤(パクリタキセル,ドセタキセル等)やビンカアルカロイド系抗がん剤(ビンクリスチン,ビノレルビン等)は組織障害性が高い.
また,抗がん剤を扱う医療従事者への職業性曝露が報告されている.Falckら4)は,1979年に抗がん剤を扱う看護師の尿中から変異原性物質が検出されたことを報告した.これ以降,欧米では抗がん剤による職業性曝露への関心が高まり,上記以外にも職業性曝露の報告や研究5,6,7)がされてきた.
職業性曝露の予防策として,抗がん剤の取り扱いに関するガイドラインが各国で制定されている.1980年代から1990年にかけてオーストラリア,カナダ,イギリス,アメリカ等の諸外国においてガイドラインが制定され,日本でも1991年に日本病院薬剤師会によって勧告された8).欧米ではガイドラインを遵守するよう国や各種医療団体が勧告している9).日本では近年まで国レベルの施策はなかったが,2014年5月に厚生労働省労働基準局安全衛生部の化学物質対策課長からの通知,「発がん性等を有する化学物質を含有する抗がん剤等に対するばく露防止対策について,基安化発0529 第2 号」が出され,行政による曝露防止の取り組みが始まった10).
抗がん剤の分析法について,Sessinkら11)がGC/MSを用いた尿中のシクロホスファミドの分析法を報告している.病院内汚染の評価については,吉田ら12)が0.03M水酸化ナトリウム水溶液とティッシュ(JKワイパー)を用い,シクロホスファミド,フルオロウラシル,白金製剤,ゲムシタビンを対象とした拭き取り調査を行っている.その他にも,松本ら13)はドキソルビシンを中心にアントラサイクリン系の抗がん剤を対象としHPLC蛍光法を用いて定量限界1.5 ng/100 cm2で調査しており,濱らは,シクロホスファミド測定を行っている公的機関および民間分析機関両者に拭き取りキットに染み込ませたシクロホスファミドの測定を依頼し,分析精度比較をしている14).
抗がん剤の使用頻度について,本研究で対象とした抗がん剤は,様々ながん種のキードラッグ(効果が明らかである薬剤)となっているものが多く,罹患率の高いがん種に使用される汎用性の高い抗がん剤である.フルオロウラシルは大腸,食道といった消化器がんおよび頭頸部がん,ゲムシタビンは膵がん,パクリタキセルとドセタキセルは乳がんおよび卵巣がん,イリノテカンとオキサリプラチンは大腸がんのキードラッグとして使用されている.その他にもビンクリスチンはリンパ腫,ビノレルビンは乳がんおよび肺がんの治療で使用されている.
著者等は使用頻度や有害性が比較的に高い抗がん剤10物質について,医療従事者への曝露に繋がる可能性が高い病院内汚染を把握するため,床,机等に残留する抗がん剤を拭き取りにより採取しLC/MSにより一斉分析する方法を開発したので報告する.
使用した試薬および有機溶媒は,以下のとおりである.
メタノール(HPLC用)はメルク製(Whitehouse Station, NJ. USA)を,アセトニトリルはシグマアルドリッチ製(Saint Louis, MO. USA)を,ギ酸(特級,純度98.0%以上),蒸留水(HPLC用)は関東化学製(Tokyo,Japan)を,ヒドラジン一水和物(純度79.0%以上)は東京化成工業製(Tokyo, Japan)を使用した.
また,対象物質である抗がん剤10種の分子構造をFig. 1に示す.使用した抗がん剤10種のうちフルオロウラシルを除く9種は実際に医療現場で使用しているものを,フルオロウラシルは標準品を使用した.抗がん剤10種の詳細は以下の通りである.

Chemical structures, molecular weights and logPow values of the anti-cancer drugs.
パクリタキセル(パクリタキセル点滴専用)およびビンクリスチン(オンコビン注射用)は日本化薬製(Tokyo, Japan),ドセタキセル(ワンタキソテール点滴静注液)およびイリノテカン(トポテシン点滴静注液)は第一三共製(Tokyo, Japan),ビノレルビン(ナベルビン注射用)は協和発酵キリン製(Tokyo, Japan),メトトレキサート(メソトレキセート点滴静注液)はファイザー製(New York, NY. USA),オキサリプラチン(エルプラット点滴静注液)はヤクルト製(Tokyo, Japan),シクロホスファミド(エンドキサン注射用)は塩野義製薬製(Osaka, Japan),ゲムシタビン(ジェムザール注射用)はイーライリリー製(Indianapolis, IN. USA),フルオロウラシル(5-フルオロウラシル特級)は和光純薬工業製(Osaka, Japan)である.
上記抗がん剤10種の二次標準液,およびそれらの混合標準液は,メタノールで溶解し調製した.
2. 器具と装置およびLC/MS測定条件拭き取り実験用素材として,セルロースろ紙(5C, 110 mm, ADVANTEC, Tokyo, Japan)とポリプロピレン不織布(マスクフィルター用不織布,以下「不織布」と称する,倉敷繊維加工,Osaka, Japan)を使用した.ろ紙および不織布からの抽出には超音波洗浄機(アズワン,Osaka, Japan)を用い,抽出後の溶媒のろ過にメンブレンフィルター(DISMIC-13HP, ADVANTEC)を使用した.濃縮は窒素吹付器を用いた.
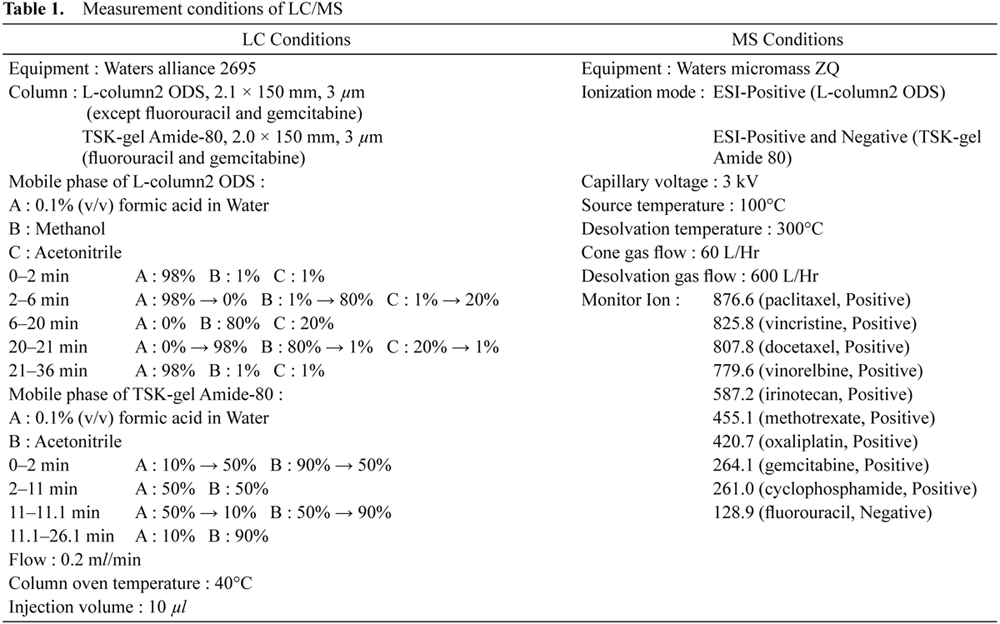
LC/MS測定には,Alliance2695/Micromass ZQ(Waters, Milford, USA)を用いた.LC/MS測定条件をTable 1に示す.カラムはL-Column2 ODS(化学物質評価研究機構,Tokyo, Japan),TSK-GEL Amide-80(東ソー,Tokyo, Japan)を使用した.フルオロウラシル,ゲムシタビンを除く8種をL-Column2 ODSを用いた逆相モードで,上記2種をTSK-GEL Amide-80を用いたHILICモードで測定をした.対象物質はすべてESIによりイオン化し,選択イオン検出(SIM)法で測定,定量した.
拭き取り分析法のスキームをFig. 2に示す.多くの病院の床と同じ材質であるP-タイル,安全キャビネット等と同じ材質であるステンレスプレートに抗がん剤10種の各10 mg/l混合標準液を10 µl添加し10分程度放置後,少量のメタノールに浸したセルロースろ紙または不織布で拭き取った.拭き取りは同じ素材を2枚使用し,同じ箇所をそれぞれ1回ずつ,計2回拭き取る方法で行った.拭き取ったろ紙または不織布を風乾後ハサミで細かく切断し,0.01%(v/v)ヒドラジン一水和物含有メタノール5 mlに浸して超音波抽出(40°C,10分)を2回行った.その後抽出した液をメンブレンフィルターに通し,ろ液を窒素吹き付けにより1 mlとし,LC/MSで測定した.
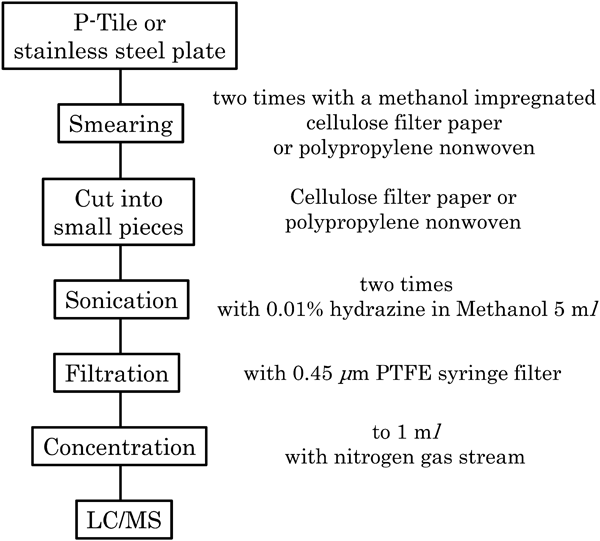
Analysis scheme of the anti-cancer drug residues.
P-タイル上に添加した抗がん剤をセルロースろ紙,不織布により拭き取る検討を行った.その回収率をTable 2に示す.Table 2に記載したMDLは,Carolynらの報告15)を参考にMDL = t (a)×σ (t (a): 片側危険率5%のt値,σ : 添加回収率の標準偏差)で算出した.
| Recovery (%) (SD (%)) | MDL* (ng) |
Recovery (%) (SD (%)) | MDL* (ng) |
|
|---|---|---|---|---|
| with cellulose filter paper | with polypropylene nonwoven | |||
| vincristine** | 45 (16) | 14 | 36 (9.6) | 6.7 |
| oxaliplatin** | 82 (19) | 30 | 13 (3.1) | 0.8 |
| gemcitabine** | 73 (15) | 21 | 10 (1.5) | 0.3 |
| fluorouracil** | 18 (2.8) | 1.0 | 13 (2.4) | 7.8 |
| paclitaxel*** | 85 (13) | 21 | 101 (13) | 26 |
| docetaxel*** | 38 (10) | 7.4 | 74 (5.5) | 7.9 |
| vinorelbine*** | 15 (2.6) | 0.8 | 41 (1.8) | 1.4 |
| irinotecan*** | 23 (4.0) | 1.8 | 44 (2.7) | 2.3 |
| methotrexate*** | 18 (3.5) | 1.2 | 37 (7.5) | 5.3 |
| cyclophosphamide*** | 42 (9.6) | 7.8 | 83 (6.2) | 10 |
*5% error. **by smearing P-tile surface with cellulose filter paper. ***by smearing P-tile surface with polypropylene nonwoven.
対象とした抗がん剤10物質は,分子量が130~854,logPowが–1.28~3.54と幅広く,物理化学的性状が多様であるため,拭き取りにセルロースろ紙と不織布を対象物質によって使い分けることで,拭き取りはフルオロウラシルを除く9物質の汚染を把握できる拭き取り効率を得た.すなわち,ビンクリスチン,オキサリプラチン,ゲムシタビン,フルオロウラシルはセルロースろ紙で,パクリタキセル,ビノレルビン,イリノテカン,メトトレキサート,ドセタキセル,シクロホスファミドは不織布で拭き取る方法とした.パクリタキセル,ドセタキセル,シクロホスファミドはP-タイル上に散布した50%以上が回収され(以下「回収率」と称す),その相対標準偏差は10%前後であった.ビノレルビン,イリノテカン,メトトレキサートは,回収率が40%程度であったが,相対標準偏差は10%未満であった.ビンクリスチン,オキサリプラチン,ゲムシタビンは,回収率は45~82%だが,相対標準偏差が15%以上であった.フルオロウラシルは回収率が20%未満と顕著に低かった.このように,対象とした抗がん剤10物質の拭き取りによる回収率の標準偏差は1.8~19%で,フルオロウラシルを除く9物質については,標準偏差が10%を超えるものの定量精度は高くないが,P-タイル表面に残留するいずれの抗がん剤の量も推定できると考えられる.オキサリプラチン,ゲムシタビンは標準偏差が19%,15%とそれぞれ高く,拭き取りの回収率と4. 2で記述する溶媒によるP-タイルからの直接抽出の回収率が,t検定(5%危険率)により有意差がないとされた(Table 3).このため,標準偏差が10%を超えるものの中でも特に定量精度は低いが,汚染の濃度レベルは推定できると考えられる.フルオロウラシルを汚染の評価ができる物質から除いた理由および拭き取り分析法の効率についての詳細は4. 2で記述する.また,2. 1で記述したようにフルオロウラシルのみ標準試薬を使用したため,医薬品で使用される際の添加物の影響はこの結果に反映していない.
| t value* | p value** | |
|---|---|---|
| paclitaxel | 0.0367 | 1.86 |
| docetaxel | 0.514 | 1.86 |
| vincristine | 0.000 | 1.86 |
| vinorelbine | 5.11 | 1.86 |
| irinotecan | 0.463 | 1.86 |
| methotrexate | 5.04 | 1.86 |
| oxaliplatin | 0.491 | 1.86 |
| gemcitabine | 0.505 | 1.86 |
| cyclophosphamide | 0.685 | 1.86 |
| fluorouracil | 4.27 | 1.86 |
*t = {(recovery in the smearing analysis) – (recovery in the rinsing analysis)} / [{(population variance in the smearing analysis recovery) ^2 / (number of samples in the smearing analysis)} + {(population variance in the rinsing analysis recovery) ^2 / (number of samples in the rinsing analysis)}] ^0.5.
**5% error degree of freedom = (number of samples in the smearing analysis) + (number of samples in the rinsing analysis) – 2 .
ステンレスプレートは安全キャビネット等に使用され汚染の可能性は高いが,曝露の対象者,場所が限られるため,ステンレスプレートの拭き取り効率は3回の実験で評価した.
ステンレスプレートの拭き取りではメトトレキサート以外の9物質をセルロースろ紙で,メトトレキサートのみを不織布で拭き取ることで,10物質の汚染を把握できる回収率を得た(Table 4).
| Recovery (%) (SD (%)) | ||
|---|---|---|
| with cellulose filter paper |
with polypropylene nonwoven |
|
| paclitaxel* | 75 (5.2) | 54 (17) |
| docetaxel* | 83 (6.8) | 79 (7.8) |
| vincristine* | 74 (11) | 66 (14) |
| vinorelbine* | 35 (2.9) | 17 (0.42) |
| irinotecan* | 51 (6.6) | 23 (0.17) |
| oxaliplatin* | 74 (6.1) | 59 (8.9) |
| gemcitabine* | 111 (9.4) | 32 (0.69) |
| cyclophosphamide* | 81 (2.8) | 71 (6.5) |
| fluorouracil* | 47 (1.3) | 22 (4.9) |
| methotrexate** | 29 (1.6) | 61 (4.7) |
*by smearing stainless steel plate surface with cellulose filter paper. **by smearing stainless steel plate surface with polypropylene nonwoven.
ステンレスプレートの拭き取りはP-タイル拭き取りよりも全体的に回収率が高かった.このことは,ステンレスプレートでは浸透や酸化分解等の影響を受けにくいためと考えられる.
1)セルロースろ紙によるP-タイル上の抗がん剤の拭き取り
セルロースろ紙は分子構造に親水性(OH基)部分を多く有するが,疎水性の構造も持つ素材である.そのため,添加した抗がん剤は疎水性相互作用および静電相互作用によりセルロースろ紙に保持されると考えられる.セルロースろ紙の拭き取りでは,親水性物質のオキサリプラチン,ゲムシタビンが高い回収率であった.これはセルロースろ紙のOH基と対象物質との静電相互作用による効果と考えられる.パクリタキセル,ドセタキセル,シクロホスファミドはセルロースろ紙の疎水性部分が捕集に寄与し74~102%の拭き取り回収率が得られたと考えられるが,他方,セルロースろ紙は不織布よりも疎水性が低いため,不織布による拭き取りと比べ回収率が低かったと考えられる.同じく親水性物質であるイリノテカン,メトトレキサート,フルオロウラシルの3物質と疎水性物質のビノレルビンは回収率が20%程度と低かった.ビノレルビンの低回収率については,セルロースろ紙の性質からでは十分説明できない.
これら4物質を含め抗がん剤の拭き取り素材,床材上等における挙動については4. 3で考察する.
2) ポリプロピレン不織布によるP-タイル上の抗がん剤の拭き取り
ポリプロピレン不織布は疎水性の素材で,表面積も比較的小さいため,logPowが高い物質や分子量の大きい物質を保持し,そこから溶媒抽出できると考えられる.不織布の拭き取りではフルオロウラシル,ゲムシタビンの回収率が顕著に低かった.この2物質は不織布に抗がん剤を直接添加し抽出した場合も同様の傾向があった.炭素鎖のみからなる分子構造の不織布は疎水性が高く,logPowが低いフルオロウラシルとゲムシタビンは素材に保持することが難しいと考えられる.他方,パクリタキセル,ドセタキセル,シクロホスファミドは対象とした抗がん剤10物質の中では比較的logPowが高く,セルロースろ紙よりも不織布のほうが高い回収率を得たため,不織布との疎水性相互作用が捕集に大きく寄与したと考えられる.logPowが低いにもかかわらずセルロースろ紙よりも回収率が高かったイリノテカンとメトトレキサートは,フルオロウラシル,ゲムシタビンと比較して分子量が大きく,分子内に比較的広く分布する疎水性構造部分とポリプロピレンとの相互作用により捕集されたと考えられる.
2. P-タイルおよびステンレスプレートに添加した抗がん剤の溶媒による直接抽出効率P-タイルに添加した抗がん剤の拭き取り分析法の効率を,溶媒で直接抽出する方法と比較した(Fig. 3).
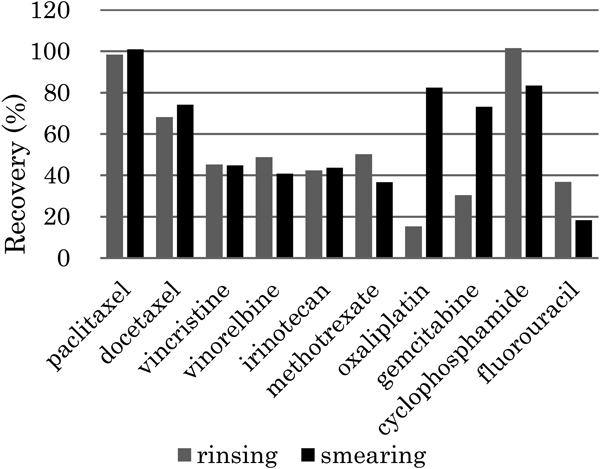
Comparison of anti-cancer drug recoveries from a P-tile by rinsing and smearing with cellulose filter paper and polypropylene nonwoven.
P-タイル拭き取りでは,ビンクリスチン,ビノレルビン,イリノテカン,メトトレキサートの拭き取り回収率が40%程度であったが,溶媒による直接抽出でも同程度の回収率であった.詳細は4. 3で考察するが,これらの物質は添加量の4割程度がP-タイル表面に残留していたと考えられ,残りはP-タイルへの浸透や分解等により失われたと考えられる.したがって本拭き取り分析法によりP-タイル表面に残留するこれら4物質は,ほぼ全量回収できたと考えられる.フルオロウラシルはP-タイルの拭き取り回収率が18%と顕著に低く,溶媒による直接抽出の回収率も37%と低かった.詳細は4. 3. 4で考察するが,P-タイルの拭き取りで,フルオロウラシルの残存量の評価は難しいと考えられる.
ステンレスプレートの拭き取り回収率とステンレスプレートを溶媒で直接抽出した回収率の比較をFig. 4に示す.ビノレルビン,フルオロウラシルは拭き取りで50%前後しか回収できなかった.原因については4. 3. 3および4. 3. 4で考察するが,直接抽出の回収率から表面の残留の約半分は拭き取ることができていること,拭き取りの標準偏差が低い(3%未満)ことから,この2物質の大凡の汚染レベルは評価できると考えられる.
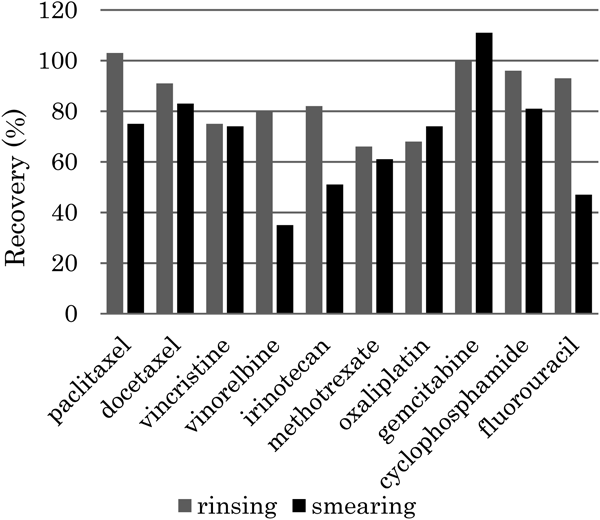
Comparison of anti-cancer drug recoveries from a stainless steel plate by rinsing and smearing with cellulose filter paper and polypropylene nonwoven.
P-タイルからの拭き取り回収率について,それに影響する可能性が考えられる抗がん剤の分子構造,分子量,π電子,分子に占める酸化されやすいアミノ基(後述する)の割合について考察する.P-タイルからの拭き取り回収率と抗がん剤の分子に占める酸化されやすいアミノ基の割合,π電子の保有数の関係を示したグラフをFig. 5に示す.

Correlations of three elements. Recoveries from P-tile by smearing; π electrons and amine-N, except that in aromatic rings, and low reactivity of lone-pair electrons /molecular weights of anti-cancer drugs.
P-タイルから高い拭き取り回収率を得られた抗がん剤(Fig. 5では径の大きい円で示されている)は,分子量200~400程度のオキサリプラチン,ゲムシタビン,シクロホスファミドおよび800以上のパクリタキセル,ドセタキセルである.一般に分子量が小さいとP-タイルの内部への浸透が多く,P-タイルとの分子間力は小さいと考えられ,分子量が大きいとその反対になると考えられる.対象とする10種の抗がん剤で,分子量が200~400程度の物質で低い拭き取り回収率の物質はなかった.他方,分子量800前後では,拭き取り回収率が40%台の物質(ビンクリスチン,ビノレルビン)も存在した.
π電子はπ-π相互作用の対象となり,π電子の保有数が多い物質ほどP-タイル表面や添加物との吸着を起こしやすいと考えられる.しかしながら,必ずしもπ電子の保有数と回収率の相関が見られたわけではなかった.
酸化されやすいアミノ基が分子に占める割合が高い物質は,全ての物質が当てはまるわけではなかったが,回収率が低い傾向が見られた.酸化分解物を確認したわけではないため可能性の域ではあるが,酸化分解を起こしている可能性が高いと考えられる.対象の抗がん剤はアミノ基を含むものが多いが,アミノ基のN原子が非共有電子対を持つものであれば酸化されやすいと考えられる.N原子が芳香環に含まれる,あるいは他の原子と接触し共役している場合,またはN原子の非共有電子対が金属原子に配位して安定となっている場合(オキサリプラチンのような形)は,酸化の影響を受けにくいと考えられる.
拭き取り回収率への分子構造,物理化学的性状等の影響について,物質ごとに考察する.
1) パクリタキセル,ドセタキセル,シクロホスファミド
パクリタキセルとシクロホスファミドは,P-タイル拭き取りの回収率がそれぞれ101%と83%,直接抽出の回収率が98%と102%で,拭き取りと直接抽出どちらも回収率が80%以上であった.P-タイルはポリ塩化ビニルからなり,不織布と同じく疎水性であるが不織布よりもソフトであることから,可塑剤等の添加物が含まれ,分子と分子の間隔が大きいと考えられる.パクリタキセルは分子量853と分子が大きく,P-タイルの分子と分子の隙間に入りにくいため浸透しにくいと考えられる.また,パクリタキセルは分子に占める酸化されやすいアミノ基の割合は低く,酸化分解の影響も受けにくいと考えられる.シクロホスファミドは分子量261と分子は小さいが,対象の抗がん剤の中でπ電子の数が最も少ない.このことからP-タイルとの相互作用は比較的小さくなり,吸着しにくいと考えられる.一方で,シクロホスファミドの分子に占める酸化されやすいアミノ基の割合は他物質と比べて高いほうだが,拭き取りおよび直接抽出の回収率は80%以上であった.原因については定かではないが,何らかの理由でアミノ基があまり酸化されず,分解されなかったことが考えられる.
ドセタキセルはP-タイル拭き取り回収率が74%,直接抽出の回収率が68%で,拭き取りと直接抽出の回収率はTable 3のt検定による有意な差はなかった.また,分子構造が良く似たパクリタキセルよりも回収率が低かった.この両者の分子構造は,Fig. 1の円で示したa,bの2箇所以外は同じである.ドセタキセルとパクリタキセルの回収率を比較すると,ステンレスプレートの拭き取りおよび直接溶媒で抽出した回収率については有意な差は見られないが,P-タイル上では有意な差が見られる.このことから,P-タイルとの相互作用に相違があると考えられる.また,P-タイルと同様に疎水性である不織布からの抽出率は110%であるから,P-タイルの不織布による拭き取りの違いが回収率に影響していると考えられる.すなわち,P-タイルの素材であるポリ塩化ビニル,それに添加された可塑剤,安定剤等の添加物と部分構造の違いが影響していると思われるが,原因を明らかにできる結果は得られていない.
2) オキサリプラチン,ゲムシタビン
オキサリプラチン,ゲムシタビンの2物質は,P-タイルから溶媒による直接抽出の回収率が拭き取りの回収率よりも顕著に低かった.この2物質はセルロースろ紙からは概ね抽出されており,また分子中に酸化されやすいアミノ基が占める割合が少ないため,酸化の可能性も低いと考えられる.したがって,この2物質は拭き取る物理的効果が回収率向上に寄与したと考えられる.オキサリプラチンとゲムシタビンは極性官能基を複数有し,さらに,オキサリプラチンには白金との共有結合性の低い結合,ゲムシタビンには複数のOH基があり,P-タイルと静電相互作用があると考えられる.それらの相互作用の結果,溶媒で洗い流すだけでは回収されず,セルロースろ紙による拭き取りでこすり取られたと考えられる.
3) イリノテカン,メトトレキサート,ビンクリスチン,ビノレルビン
イリノテカン,メトトレキサート,ビンクリスチン,ビノレルビンの4物質は,P-タイル拭き取り回収率が37~45%,溶媒によるP-タイルからの直接抽出の回収率が42~50%と,どちらも低回収率であった.これらの物質は対象物質の中でも分子量454~825と比較的分子が大きく,P-タイル内部へ浸透する可能性は低いと考えられる.
イリノテカン,ビンクリスチン,ビノレルビンは分子に占める酸化されやすいアミノ基の割合が他物質と比較して高く,π電子の保有数も多い.これらの物質は酸化分解もしくはP-タイル表面への吸着により,回収率が低かった可能性が考えられる.さらに,ビノレルビンは浸透,吸着の少ないステンレスプレートで,溶媒による直接抽出の回収率は80%と高かったが,拭き取り回収率は35%と低かったため,拭き取り素材にうまく移行していない可能性も考えられる.
メトトレキサートは酸化されやすいアミノ基を含む割合が少ないが,π電子の数はイリノテカンと同程度である.したがって,メトトレキサートのP-タイル上での低回収率はπ-π相互作用によるP-タイル表面への吸着による可能性が考えられる.
4)フルオロウラシル
フルオロウラシルは,P-タイル拭き取り回収率が18%,P-タイルからの溶媒による直接抽出の回収率が37%と,顕著に低かった.
セルロースろ紙からの抽出は54%と概ね5割抽出されたことと合わせて考えると,P-タイル表面には添加したフルオロウラシルの40–50%が残留し,それをセルロースろ紙で概ね5割抽出したと考えられる.ステンレスプレートについても同様に,拭き取りが47%,直接抽出が93%であることから,ステンレスプレートの存在量をほぼ拭き取り,そのおよそ半分がセルロースろ紙から抽出されたと考えられる.P-タイルとステンレスプレートについて,溶媒による直接抽出の回収率を比較すると,P-タイルの回収率が顕著に低かった.拭き取りでもP-タイルの回収率がステンレスプレートより低い傾向が同様に認められた.フルオロウラシルは分子中に含まれる酸化されやすいアミノ基の割合が高く,浸透に加えて酸化分解が起こっている可能性も考えられる.ステンレスプレートの溶媒による直接抽出が100%近く回収されたのは,拭き取りよりも溶媒による抽出のほうが空気に触れる時間が短いため,酸化の影響をあまり受けなかったことが考えられる.また,フルオロウラシルは分子が小さいため,P-タイルの分子と分子の隙間に入り込みやすいと考えられ,P-タイル上で浸透の影響を受けた可能性も考えられる.
4. 分析方法に関するその他の検討セルロースろ紙と不織布以外の拭き取り素材の検討を行った.その結果について4. 3. 1で述べる.また,拭き取り素材からの抽出液の濃縮過程における抗がん剤の分解とその防止方法に関する検討結果を4. 3. 2に示す.
1)その他の拭き取り素材の検討
石英繊維ろ紙(QR-100,ADVANTEC製),ナイロンろ紙(Nylon Membrane,メルクミリポア製,Darmstadt,Germany),キムワイプ(ワイパー200,日本製紙クレシア製,Tokyo, Japan)に抗がん剤10種の各10 mg/l混合標準液を10 µl直接添加し,0.01%ヒドラジン含有メタノールによる抽出率を評価した.これらの抽出率とセルロースろ紙,不織布からの抽出率をTable 5に示す.
| Recovery (%) (SD (%)) | |||||
|---|---|---|---|---|---|
| cellulose filter paper | polypropylene nonwoven | quartz fiber filter | nylon filter paper | Kimwipe | |
| paclitaxel | 61 (11) | 89 (9.0) | 27 (9.1) | 64 (3.9) | 66 (7.0) |
| docetaxel | 60 (5.4) | 110 (4.0) | 57 (4.4) | 90 (6.5) | 104 (2.6) |
| vincristine | 85 (11) | 69 (5.0) | 72 (3.4) | 67 (8.0) | 104 (18) |
| vinorelbine | 78 (4.6) | 53 (1.4) | 38 (3.5) | 20 (2.9) | 33 (3.0) |
| irinotecan | 30 (7.6) | 67 (2.5) | 61 (5.3) | 61 (2.0) | 84 (5.6) |
| methotrexate | 34 (1.7) | 69 (6.0) | 27 (4.3) | 70 (5.5) | 25 (1.0) |
| oxaliplatin | 73 (12) | 64 (5.5) | 44 (9.0) | 7.5 (0.70) | 79 (1.3) |
| gemcitabine | 69 (12) | 40 (2.9) | 57 (4.6) | 5.9 (0.22) | 40 (11) |
| cyclophosphamide | 66 (6.5) | 79 (5.4) | 66 (3.8) | 70 (3.2) | 99 (0.33) |
| fluorouracil | 54 (1.2) | 36 (5.1) | 64 (9.2) | 16 (1.2) | 33 (1.9) |
| number of experiments | n=5 | n=5 | n=3 | n=3 | n=3 |
石英繊維ろ紙ではlogPowが低い物質の抽出率は比較的高かったが,logPowが高いパクリタキセル,ドセタキセルの抽出率が低かった.logPowが低い物質は石英繊維ろ紙のシラノール基との静電相互作用により保持され,それにメタノールを加えることにより抽出されたと考えられる.一方logPowが高い物質は,石英繊維ろ紙との親和力が小さいことが,素材での保持が非常に小さかった原因と考えられる.また,石英繊維ろ紙は壊れやすいため,拭き取りには不向きであった.
ナイロンろ紙ではlogPowの低いオキサリプラチン,ゲムシタビン,フルオロウラシルの3物質の抽出率が低かった.ナイロンは分子内にアミド構造を有しているが,分子構造は概ね疎水性であると考えられる.ナイロンろ紙はセルロースろ紙と比べると親水性相互作用が弱く,logPowの低い物質の抽出率が低くなったと考えられる.
キムワイプはパルプからなるため,主成分はセルロースである.しかし,ゲムシタビンとフルオロウラシルの抽出率がセルロースろ紙よりも低かった.この原因は不確かではあるが,キムワイプはセルロースろ紙と異なり,加工の際に使用された添加物の影響,セルロースろ紙よりも薄く物質を保持する表面積が少ないことが考えられる.
2)試料抽出液の濃縮過程における抗がん剤の分解とその防止方法に関する検討
試料抽出液を窒素吹き付け濃縮する際,試料抽出液の液温が50°Cでは10物質すべて回収率が低かった.対象物質の酸化等の何らかの分解,揮散が原因として考えられたため,酸化防止剤として抽出溶媒にヒドラジン一水和物を添加し,さらに濃縮時の液温を30°Cとすることで濃縮時の回収率低下を改善した.
なお,酸化防止剤としてヒドラジン一水和物の他にL-アスコルビン酸,4-アミノフェノールも検討した.アスコルビン酸は抽出溶媒のメタノールに溶解しにくく,LC/MS測定時に析出してしまう可能性が考えられ,4-アミノフェノールは使用するとオキサリプラチンとゲムシタビンの抽出率が低化したため,ヒドラジン一水和物を選択した.
医療従事者の曝露に繋がる可能性が高い抗がん剤の病院内汚染を把握するため,床,机等に残るそれらを拭き取り,LC/MSで分析する方法を検討した.その結果,セルロースろ紙とポリプロピレン不織布を対象物質によって使い分けることで,床材として使用されることが多いP-タイル上の9種類の抗がん剤を37~101%,相対標準偏差1.8~19%で,安全キャビネット等に使用されるステンレスプレート上の10種類の抗がん剤を回収率35~111%,相対標準偏差1.3~11%で,汚染を定量的に把握またはそれには劣るが汚染を十分推定できる分析法を開発した.また,一般的にUVと比べてMSは2~3桁感度が高いと考えられることから,MSを検出手段としている本分析法のMDLは,UVを検出手段としている方法と比較して2桁程度以上低いと考えられる.阿部らの報告1)では,調査結果でフルオロウラシルについて,「ND(5-FU < 20 ng/ml)」とされており,このNDレベルを計算すると3,200 ngと推察される.方法が異なり一概に比較はできないが,これを本分析法のフルオロウラシルのMDL(7.8 ng)と比較すると,本法のMDLが3桁程低いレベルであった.また,本分析法と同じくMSを検出器として使用した濱らの報告16)では,測定の対象がバイアル表面の拭き取りで本分析法と異なるが,シクロホスファミドの単一成分の分析でMDLが16 ng(GC/MS/MS),10 ng(LC/MS/MS)とされている.本分析法は10物質の多成分一斉分析で,シクロホスファミドのMDLは10 ngと同程度のMDLで,シクロホスファミド以外の9物質も同レベルのMDLで分析できる.本分析法によって病院内の抗がん剤汚染の把握が進むことを念じている.
一方で,実際の病院内の薬剤調製室等では高濃度の抗がん剤が扱われている.そのため,医療従事者の作業環境では,それらの漏れ等による高濃度の抗がん剤汚染が危惧される.現在施されている汚染対策の1つとして,クローズドシステムがある.大阪府立公衆衛生研究所の報告17)によると,クローズドシステムは抗がん剤のバイアルと抜き取るシリンジの間に特別な部品を装着することで抗がん剤の調製時の漏れを防止するもので,これによって汚染が導入前より約80%減少したという.神戸市立医療センター中央市民病院では,クローズドシステムのBD PhasealTM(Becton, Dickinson and Company, Franklin Lake, New Jersey)の導入によってシクロホスファミドの汚染を低レベルに抑えられるとの報告16)があるが,完全な除去には至らないという.また,BD PhasealTMはすべてのバイアルの規格に対応していないという問題も報告されている18).
抗がん剤汚染の防止および除去方法の研究は今後の重要な課題であり,分析方法および調査の充実も含め,抗がん剤曝露の低減研究が進むことが望まれる.