2015 年 101 巻 12 号 p. 645-652
2015 年 101 巻 12 号 p. 645-652
Kinetics of iron carburization via CaO-SiO2-Al2O3 slag containing sulfur at 1723 K was investigated. The simulated blast-furnace (B.F.) slag (CaO/SiO2=1) containing sulfur and high basicity slag (CaO/SiO2=7.6) containing sulfur were prepared. The rate of carburization of iron through the high basicity slag containing sulfur was higher than the rate of carburization of iron through the simulated blast-furnace slag containing sulfur. Furthermore, the rate of carburization of iron through the slag containing sulfur was higher than the rate of carburization of iron through the slag without sulfur. On the other hand, the rates in the middle stage of carburization of iron through the slag containing sulfur were k=6.15×10–5 mol/m2·s (the simulated blast-furnace slag) and k=1.35×10–4 mol/m2·s (the high basicity slag), and were much higher than the other stages, and were influence by the existence of sulfur in the slag. The rates in the last stage of carburization of iron through the slag containing sulfur were k=2.95×10–5 mol/m2·s (the simulated blast-furnace slag) and k=6.21×10–5 mol/m2·s (the high basicity slag), and were closed to the rates carburization of iron through the slag without sulfur, and were not influenced by the existence of sulfur in the slag.
至近の良質資源の枯渇と価格の急騰を背景に,鉄鋼業においても鉄鉱石および石炭などの原燃料の価格変動に対応していく新たな技術開発が不可欠となっている。特に,高炉用コークス製造に適した粘結炭は石炭資源の3割に過ぎないため,将来,良質な粘結炭の確保が困難となることが予想される。劣質炭は粘結性が著しく低く,コークス強度を大幅に低下させるため,現在の技術ではコークス炉での多量使用が不可能である。このような問題を解決するため,鉄鋼業では新たな高炉装入物として粘結性が低い劣質炭でも使用できる炭材内装塊成鉱の開発に取り組み始めている。
炭材内装塊成鉱は焼結鉱および鉄鉱石ペレットと比較して,1273 K以上の高温域において高速還元の可能な製鉄原料である。また,炭材内装塊成鉱を用いた手法では,焼結などの高温前処理をすることなく,粉鉱石や炭材粉が利用できること,還元材として石炭,ダスト粉などが利用できること,炭材と鉱石粉を密に混合できるため生産性の向上が望めることなどのメリットを期待できる1)。これまで炭材内装塊成鉱を使用する対象プロセスとしては,主に還元鉄を製造するため,ロータリーハース炉内で加熱・還元する,FASTMET,INMETCOなどが検討されてきた。これらのプロセスでは還元速度が非常に速いこと,およびSL/RN法に比べ,還元材比が低いという利点を有している2)。最近では,1273 K以上の高温域で還元反応が高速に進行する特性を生かし,短時間で還元鉄を製造するプロセスがダスト処理の用途で実用化されている3)。また,セメントをバインダーとしてコールドボンドペレットやブリケットが一部の高炉で少量使用されている4,5)。高炉で多量使用できない理由として,結晶水や付着水の影響によるシャフト上部での昇温・還元遅れ,スラグ比の増加および高温強度の低下による通気性の悪化などが問題とされている。それゆえ,これらの問題を克服するために,被還元性の向上および適度な強度を有する炭材内装塊成鉱の開発が求められている6)。このような背景から,炭材内装塊成鉱を高炉に装入し,シャフト部における反応の高速化,低温化を目指した種々の基礎研究が実施された。炭材内装塊成鉱を用いた場合,鉄鉱石と炭材がミクロに接触しているため,還元とブドワー反応が同一場で進行すると共に,カップリング反応効果によって低温から還元反応が活発化し,還元平衡温度が低温化すること,およびCOガス利用率の向上により,還元材比の大幅な低減が期待できる。一方,内装炭材による酸化鉄の還元後,スラグ成分の溶融,還元鉄の浸炭,溶融の順に反応が進むと考えられる。しかし,スラグ・メタルの分離が起きにくいことが,問題点として挙げられる7)。その原因として,以下のことが考えられる。炭材内装塊成鉱の鉱石粒子は,酸化鉄と脈石成分により構成されている。高炉と同条件で炭材内装塊成鉱を昇温,還元すると,まず内装炭材により,酸化鉄の還元がおこり酸化鉄はメタルになる。さらに昇温すると,脈石成分の軟化,溶融が開始する。その後,さらに昇温すると,メタルが溶融する。メタルの溶融後,スラグ(表面張力:200~400(×10−3 N/m))とメタル(表面張力:1600~1800(×10−3 N/m))の表面張力の差により8),メタルが中心に凝集しスラグが周囲に押し出され,メタル表面にスラグ相が形成される。このような過程で反応が進むことで,メタルがスラグ中に保持される。
この問題を解決する方法の一つとして,メタルへの浸炭反応の促進が考えられる。メタル粒子への浸炭が進むことで,メタルの凝集粗大化がおこり,スラグ・メタルの分離につながることが報告されている9,10)。すなわち還元鉄への浸炭,溶融を促進させることで,スラグ・メタルの分離を促進することが期待できる。
そこで本研究では,浸炭反応の低温高速化へ向けたスラグ設計の基礎として,スラグを介した炭素の移動現象に着目し,炭素がスラグ中に溶解し,スラグ/メタル反応を通して鉄中へ浸炭する反応速度について,初期検討を行い,報告した11)。本報では,スラグを介した浸炭反応における硫黄の影響について検討したので報告する。
CaO-SiO2-Al2O3系状態図を基に本実験で使用した硫黄を含まないスラグ試料の組成をTable 1およびFig.1に示す。高炉を模擬したスラグ(塩基度1)と高塩基性スラグ(塩基度7.6)の2つのスラグを用いた。これらのスラグは低融点の組成を有する。これらの2種類のスラグ試料を基に,硫黄含有スラグ試料を作製した。作製方法としては,試薬CaCO3を1273 Kで12 hか焼して作製したCaOおよび試薬SiO2,Al2O3,CaSをTable 2で示す所定割合で混合した。ここで,2.2 mass%のCaSの添加は1 mass%相当のS添加したことを意味する。その後,黒鉛坩堝(36 mm×42 mm×80 mm)に入れ,1723 K,Ar:200 cm3/min(s.t.p.),CO:20 cm3/min(s.t.p.)雰囲気中で20 h保持し,スラグ中に溶解させた。その後,炉から取り出し,急冷した。スラグの表面を削り取った後,粉砕し,スラグ試料とした。

Composition of pre-melted slag plotted on CaO-SiO2-Al2O3 phase diagram.
| CaO | SiO2 | Al2O3 | |
|---|---|---|---|
| Simulated B.F. slag | 40 | 40 | 20 |
| High basicity slag | 50 | 6.6 | 43.4 |
| CaO | SiO2 | Al2O3 | CaS | |
|---|---|---|---|---|
| Simulated B.F. slag | 38.1 | 39.8 | 19.9 | 2.2 |
| High basicity slag | 48.8 | 6.5 | 42.5 | 2.2 |
炉から取り出したスラグ中の炭素・硫黄濃度については,日鉄住金テクノロジー(株)に依頼し,燃焼−導電率法12,13)・熱分解−ヨウ素酸カリウム滴定法14,15)によって分析した。
2・2 スラグを介した浸炭反応速度の測定スラグ相を介した浸炭に及ぼす硫黄の影響を知るために,炭素相およびスラグ相に硫黄を含有させた実験を行った。
まず,Table 3で示す組成の実炉コークスを用いることで,炭素相に硫黄を含有させた実験を行った。粒度は45 μm以下のものを使用した。MgO坩堝(23 mm×30 mm×50 mm)に純鉄薄板((株)ニラコ,純度99.5 mass%,14 mm×14 mm×0.5 mm)を入れ,その上に作製したスラグ7.5 gを置いた。その坩堝を,黒鉛粉末を敷き詰めた黒鉛ホルダー(36 mm×42 mm×80 mm)の中に入れ,炉内に装入した。Ar雰囲気中で室温から昇温し,1723 Kに達したところで,15 min保持し,溶融したスラグの上に実炉コークス0.25 gを乗せた。その後,Ar:200 cm3/min(s.t.p.),CO:2 cm3/min(s.t.p.)雰囲気中で所定時間(1~25 h)保持し,炉から取り出した。
| Ash | VM | FC | S | C | H | N | O |
|---|---|---|---|---|---|---|---|
| 11.97 | 0.97 | 87.10 | 0.60 | 84.60 | 0.26 | 1.22 | 0.35 |
一方,作製した硫黄含有スラグ試料を用いて,上記と同様な条件で浸炭反応実験を行った。炭素源としては硫黄を含まない黒鉛粉末(和光純薬工業(株),純度98 mass%,粒度45 μm以下)を使用した。
上述の通り,炭素相/スラグ相/メタル相の3相におけるスラグ相を介した浸炭実験は,本報では条件II,IIIを新たに追加して行った。
条件I:黒鉛粉末/硫黄非含有スラグ/純鉄薄板(Onoらの実験条件11))
条件II:実炉コークス/硫黄非含有スラグ/純鉄薄板
条件III:黒鉛粉末/硫黄含有スラグ/純鉄薄板
実験後,鉄中炭素濃度については,日鉄住金テクノロジー(株)に依頼し,高周波燃焼赤外線吸収法によって分析した。
Table 4に作製した硫黄含有スラグ中炭素濃度と硫黄濃度を示す。炭素濃度,硫黄濃度ともに高炉模擬スラグに比べて,高塩基度スラグの方が濃度は高かった。
| mass%C | mass%S | |
|---|---|---|
| Simulated B.F. slag | 0.011 | 0.49 |
| High basicity slag | 0.017 | 0.81 |
溶融スラグ上に実炉コークスを置いた条件IIでの保持時間に対する鉄中炭素濃度分析結果をFig.2に示す。両スラグとも時間の経過とともに鉄中炭素濃度は増加した。また,高塩基度スラグの方が,浸炭反応速度は大きいことがわかった。硫黄を含まないスラグ試料を用いた条件Iと条件IIでの鉄中炭素濃度変化を比較するために,高炉模擬スラグを用いた鉄中炭素濃度の推移をFig.3に,高塩基度スラグを用いた鉄中炭素濃度の推移をFig.4に示す。どちらのスラグを用いた場合でも,条件Iと条件IIでの鉄中炭素濃度の推移に顕著な違いはみられなかった。
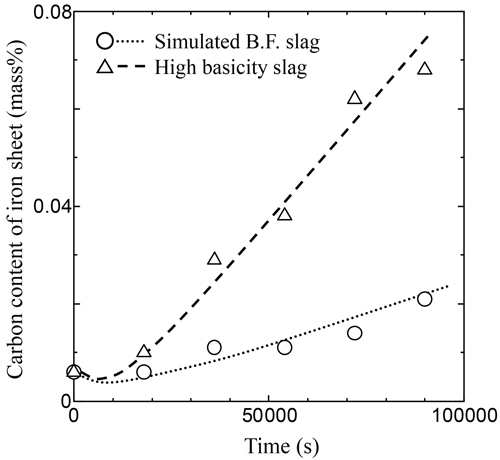
Variation of carbon content of iron sheet with time under experimental condition (II).

Comparison between variation of carbon content of iron sheet with time under experimental condition (I)11) and that under experimental condition (II).
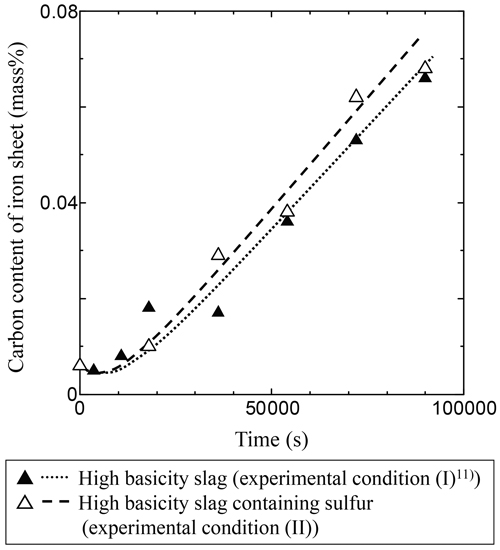
Comparison between variation of carbon content of iron sheet with time under experimental condition (I)11) and that under experimental condition (II).
次に,硫黄含有スラグを用いた条件IIIでの保持時間に対する鉄中炭素濃度分析結果をFig.5に示す。条件I,IIと同様に,両スラグとも時間の経過とともに鉄中炭素濃度は増加する傾向が見られた。また,高塩基度スラグの方が,浸炭反応速度は大きいことがわかった。
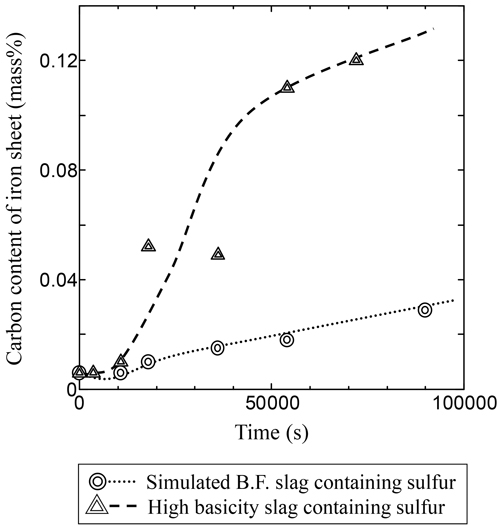
Variation of carbon content of iron sheet with time under experimental condition (III).
条件Iと条件IIIでの鉄中炭素濃度変化を比較するために,各条件における高炉模擬スラグを用いた鉄中炭素濃度の推移をFig.6に,高塩基度スラグを用いた鉄中炭素濃度の推移をFig.7に示す。硫黄非含有スラグを介した条件に比べて,硫黄含有スラグを介した条件の方が,鉄中炭素濃度は高かった。この差異は,硫黄非含有スラグを用いた場合に比べて,浸炭反応中期(およそ10800~18000 s付近)での鉄中炭素濃度の増加が,急激であったことによることがわかる。また,一旦鉄中炭素濃度が減少する浸炭反応初期(0~10800 s付近)においては,硫黄の影響は判断できるほど大きいものではなかった。

Comparison between variation of carbon content of iron sheet with time under experimental condition (I)11) and that under experimental condition (III).
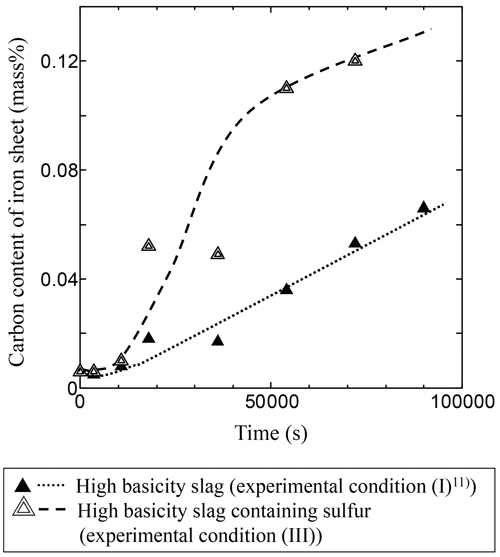
Comparison between variation of carbon content of iron sheet with time under experimental condition (I)11) and that under experimental condition (III).
また,保持時間が最も長い試料(高炉模擬スラグでは25 h,高塩基度スラグでは20 h)の鉄中の硫黄濃度分析結果をTable 5に示す。初期の鉄中硫黄濃度は,0.012 mass%であったが,実験終了後は,ともに0.001 mass%であり,初期濃度より減少しており,鉄中に硫黄はほとんど溶解していなかった。硫黄を含む系でのスラグ相を介した浸炭に関しても,実験後の純鉄薄板の炭素濃度は低く,均一液相領域である1.04 mass%まで浸炭は進んでいなかった。
| mass%S | |
|---|---|
| Simulated B.F. slag | 0.001 |
| High basicity slag | 0.001 |
スラグ中に溶解している硫黄は,以下の(1,2)式で示される反応により,サルファイドイオン(S2−),サルフェイトイオン(SO42−)の形をとると考えられる。
| (1) |
| (2) |
硫黄がスラグ中に溶解する際,前述のようにサルファイドイオンおよびサルフェイトイオンとして存在する。サルファイドイオンとサルフェイトイオンの飽和濃度は次式で表すことができる。
| (3) |
| (4) |
スラグ中の硫黄吸収能は,(3),(4)式中にも示されているサルファイドキャパシティCS2−およびサルフェイトキャパシティCSO42−により評価される。サルファイドキャパシティとサルフェイトキャパシティは,(1),(2)式の平衡定数を用いて,次式で表すことができる。
| (5) |
| (6) |
スラグへの硫黄溶解度が低い範囲では,硫黄の溶解についてヘンリーの法則が適合することが知られており,カーボネートキャパシティとカーバイドキャパシティと同様に,サルファイドキャパシティとサルフェイトキャパシティも,温度とスラグ組成のみの関数である。
一方,Onoらがすでに,自由酸素イオン(O2−)を多く含むスラグは炭素の溶解に有利であり,つまり塩基度の高いスラグほど炭素はスラグ中に溶解しやすいことを報告している11)。そのため,硫黄についても塩基度の高いスラグほど硫黄はスラグ中に溶解しやすいことが示唆される。また,(1)式の反応は,酸素分圧が10−6 atm以下で,(2)式の反応は,酸素分圧が10−4 atm以上で起こるとされている16)。つまり,本実験では,Onoらの実験条件11)と同じ酸素分圧PO2=9.28×10−21 atmであるため,スラグ中に溶解する硫黄はサルファイドイオンであり,スラグ中の硫黄溶解度はサルファイドキャパシティにより評価できることが示唆される。
4・2 スラグ中硫黄の溶解度本実験では,スラグ中の硫黄濃度は,サルファイドキャパシティで評価する。(5)式からもわかるように,本実験条件でのサルファイドキャパシティの決定は難しいが,これまでに報告された多くのサルファイドキャパシティに関する文献17,18,19,20,21)から,CaO-SiO2-Al2O3系スラグ中では,スラグ中CaOモル分率NCaOが大きいものほど,またスラグの塩基度の高いものほど,サルファイドキャパシティは大きな値をとることがわかっている。つまり,高炉模擬スラグに比べ,高塩基度スラグの方がサルファイドキャパシティの値は大きくなり,スラグへの硫黄の溶解度は大きいと考えられる。
Table 4に示したように,硫黄含有スラグ中の硫黄濃度は,高炉模擬スラグにCaSを添加したスラグでは0.49 mass%であり,高塩基度スラグでは0.81 mass%であった。両者を比較すると,今回の実験条件では上述した文献17,18,19,20,21)も踏まえて,高塩基度スラグの方が硫黄の溶解量は大きく,塩基度の高いスラグの方が硫黄はスラグ中に溶解しやすい可能性が明らかになった。しかし,Al2O3の濃度の影響については検討しなかったため,今後,塩基度を統一して,Al2O3の濃度の影響についても検討する必要がある。また,両スラグ共,スラグ作製過程で硫黄成分が空気中の水分と反応し,硫化水素等のガスに変化したことで,スラグ中の硫黄濃度は混合時の1 mass%以下になったことが示唆される。
4・3 スラグを介した浸炭反応に及ぼす硫黄の影響Onoらの報告11)から,1723 Kにおいて溶融CaO-SiO2-Al2O3系スラグの炭素吸収能を表すカーバイドキャパシティの測定ならびにスラグを介した固体鉄への浸炭実験を行ったところ,カーバイドキャパシティは,高炉模擬スラグに比べ,高塩基性スラグの方が大きいことがわかった。また,スラグ相を介した鉄への浸炭反応速度は,直接浸炭やスラグ相に酸化鉄を含む場合と比べて非常に小さいが,使用したスラグ相については高塩基性の方が浸炭反応速度は大きくなることが報告された。われわれはこれらの結果を踏まえて,スラグを介した浸炭反応に及ぼす硫黄の影響を考察した。
まず,条件IIではコークス中の硫黄は,無機硫黄および炭素−硫黄固溶体として存在する。無機硫黄は,FeS,CaSといった硫化物硫黄を主体とし,CaSO4,FeSO4などの硫酸塩硫黄,遊離硫黄として存在するが,コークス中硫黄の主体を成すのは,炭素−硫黄固溶体であると報告されている22)。また,黒鉛粉末がハニカム構造のグラフェンが層状に積層した結晶構造をもつのに対し,実炉コークスは,無定形炭素から黒鉛化度の高い結晶性の炭素まで様々な結晶構造を有している23)。また,黒鉛粉末と実炉コークスの粒度は共ともに45 μm以下であり,ほぼ同程度であるため,粒度による反応界面積の差による反応性の差はないと仮定した。さらに,スラグとの黒鉛とコークスの濡れ性についても,炭素の溶解反応に影響すると考えられるが,Fig.3, 4において浸炭速度がほぼ同じ値であったため,本論文では接触角等の物性値を考慮しなかった。
Onoらが報告した(7)式を用いて11),
| (7) |
既知の値と,実験結果から求めた時間t[s]における鉄中炭素量nC,tおよび鉄中炭素のモル分率NCを代入し,左辺を縦軸に,保持時間t[s]を横軸にとり,Fig.8に示す。実炉コークスを用いた場合でも,Onoらの報告11)と同様に,浸炭反応初期段階で負の値をとることと考えられるので,t=0[s]の値を除外し,最小二乗法により,回帰直線を引いた。ここで,浸炭反応初期段階で浸炭速度が負の値を取る理由として,以下のことが考えられる。初期段階はスラグ中にまったく炭素が存在しないので,黒鉛やコークスからの炭素のスラグ中への溶解反応が生じる。同時に純鉄薄板中の微量の炭素もスラグ中へと溶解する。そのため,初期段階のみ負の値をとる。一方,初期段階以降,スラグが炭素飽和に達すると,純鉄薄板中への浸炭反応が開始する。
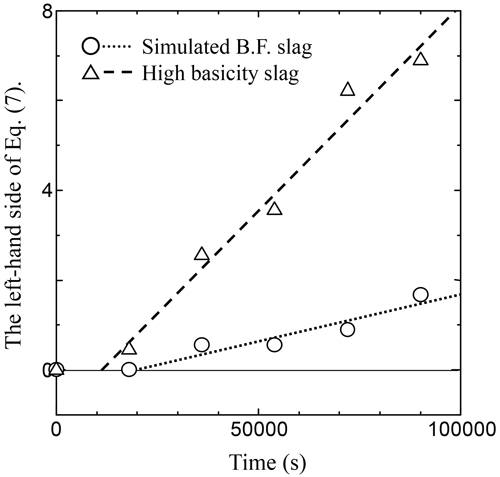
Relation between time and the left-hand side of Eq.(7) under experimental condition (II).
この直線の傾きから条件IIにおける浸炭反応速度定数kを求めた。高炉模擬スラグ:k=2.03×10−5[mol/m2・s],高塩基性スラグ:k=9.20×10−5[mol/m2・s]が得られ,高塩基性スラグの方が,反応速度定数の値は大きいことがわかる。また,浸炭反応速度定数は,Onoらの報告した硫黄を含まないスラグを用いた値がTable 6で示す高炉模擬スラグ:k=2.71×10−5[mol/m2・s],高塩基性スラグ:k=8.00×10−5[mol/m2・s]であり,各スラグであまり差がなかった。このことは,初期状態でスラグ中に硫黄を溶解していない場合,炭材/スラグあるいはスラグ/メタル界面での交換反応S2−+C=S+C2−が起きないためであると示唆される。スラグ中の硫黄の影響と浸炭のメカニズムについては最後に後述する。
| Experimental condition | Simulated B.F. slag | High basicity slag | |
|---|---|---|---|
| (I)11) | 2.71 × 10–5 | 8.00 × 10–5 | |
| (II) | 2.03 × 10–5 | 9.20 × 10–5 | |
| (III) | middle stage | 6.15 × 10–5 | 1.35 × 10–4 |
| last stage | 2.95 × 10–5 | 6.21 × 10–5 | |
次に,条件IIIにおいても(7)式を用いて実験結果から求めた時間t[s]における鉄中炭素量nC,tおよび鉄中炭素のモル分率NCを代入し,左辺を縦軸に,保持時間t[s]を横軸にとり,Fig.9に示す。Table 5に示したように,浸炭実験の保持時間が高炉模擬スラグでは25 h,高塩基度スラグでは20 h後の鉄中の硫黄濃度は,ともに0.001 mass%であり,初期の鉄中の硫黄濃度0.012 mass%より低い。つまり,硫黄含有スラグを用いた条件IIIでは,保持時間が長くなると,硫黄の影響は小さくなり,条件Iにおける浸炭速度とほぼ等しくなると考えられる。Fig.10に高炉模擬スラグと硫黄含有高炉模擬スラグを用いて行った浸炭実験の保持時間と(7)式の左辺の関係を示す。また,Fig.11に高塩基度スラグと硫黄含有高塩基度スラグを用いて行った浸炭実験の保持時間と(7)式の左辺の関係を示す。

Relation between time and the left-hand side of Eq.(7) under experimental condition (III).
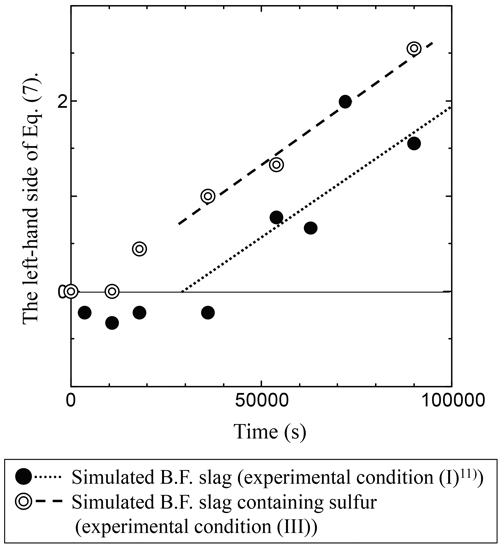
Relation between time and the left-hand side of Eq.(7) under experimental condition (I)11) and (III).
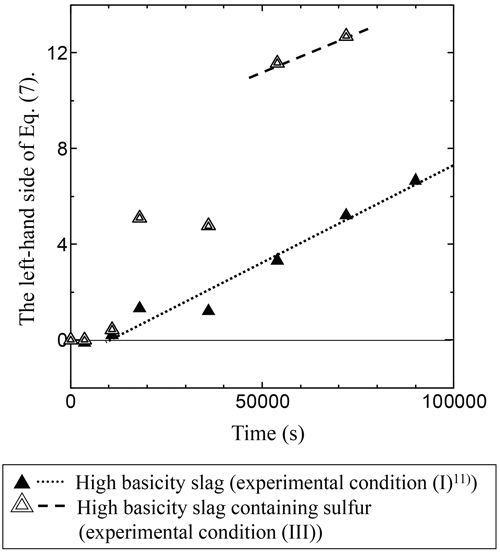
Relation between time and the left-hand side of Eq.(7) under experimental condition (I)11) and (III).
条件Iの浸炭反応速度定数kは,高塩基性スラグ:k=8.00×10−5[mol/m2・s]である11)。硫黄含有高塩基度スラグを用いた実験の後半における浸炭反応速度定数が,この値に近づくように検討すると,Fig.11の実験点54000 s以降を,スラグ中の硫黄の影響を無視できると考えることができ,最小二乗法により,回帰直線を引くと,k=6.21×10−5[mol/m2・s]と求めることができる。この段階を以下,この段階を「浸炭反応後期段階」と呼ぶ。同様に,条件Iの浸炭反応速度定数kは,高炉模擬スラグ:k=2.71×10−5[mol/m2・s]である11)。硫黄含有高炉模擬スラグを用いた浸炭反応後期段階における浸炭反応速度定数が,この値に近づくように検討すると,Fig.10の36000 s以降の実験点に関して,スラグ中の硫黄の影響を無視できると考えることができ,最小二乗法により,回帰直線を引くと,k=2.95×10−5[mol/m2・s]と求めることができる。
浸炭反応後期段階以前は,時間の経過のともにスラグ中硫黄濃度は増加している段階であると考えられる。この段階を以下,この段階を「浸炭反応中期段階」と呼ぶ。浸炭反応中期段階では,スラグ中の硫黄濃度が一定でないため,カーバイドキャパシティの値は,時間とともに変化していると考えられるが,暫定的にこの段階でも上述と同様に回帰直線の傾き(Fig.12)から浸炭反応速度定数を求める。高炉模擬スラグ:k=6.15×10−5[mol/m2・s],高塩基性スラグ:k=1.35×10−4[mol/m2・s]が得られ,浸炭反応速度は条件I,IIと比べて大きいことがわかる。浸炭反応中期段階は,スラグ中の硫黄の影響を無視できる段階(スラグ中の炭素・硫黄濃度が平衡に達したと考えられる段階)に比べて,スラグ中の炭素溶解度が大きい,つまりカーバイドキャパシティが大きいため,浸炭速度は大きいと考えられる。
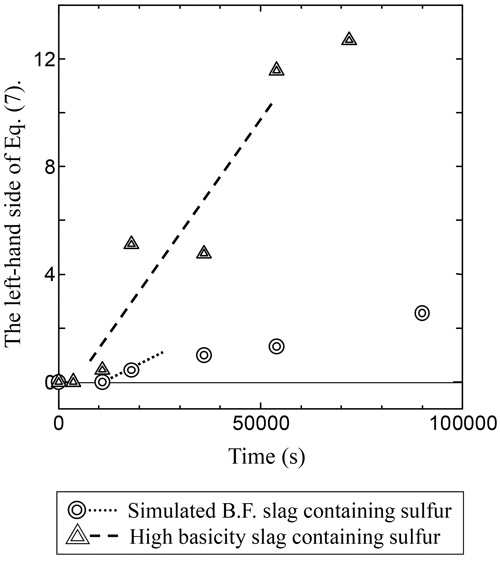
Relation between time and the left-hand side of Eq.(7) under experimental condition (III).
各条件における浸炭反応速度定数についてはTable 6に示している。浸炭反応速度は,実炉コークスを用いた条件IIでは,条件Iとあまり大きな差異は見られなかった。一方,硫黄含有スラグを用いた条件IIIでは,浸炭反応中期段階に硫黄の影響を受けることで,硫黄非含有スラグを介する条件Iに比べて反応速度は大きいが,保持時間が長くなった場合,スラグ中の硫黄濃度の平衡到達とともに,硫黄非含有スラグを介する場合と同等の反応速度を示した。
以上のことを踏まえて,硫黄含有スラグを介した浸炭反応のメカニズムの概念図をFig.13に示す。浸炭反応の初期においてスラグ中の硫黄は純鉄薄板中へ,黒鉛と純鉄薄板中の炭素はスラグ中へ交換反応S2−+C=S+C2−で移動するが,中期になると,純鉄薄板中に一旦移動した硫黄が鉄とスラグ界面で再度交換反応S2−+C=S+C2−が起こり,炭素がスラグを介して急激に鉄中に移動する。後期においてスラグ中の硫黄濃度が変化しなくなったため,炭素の移動は硫黄の影響を受けなくなることが示された。

Mechanism of iron carburization via CaO-SiO2-Al2O3 slag containing sulfur at 1723 K under experimental condition (III).
1723 Kにおいて,溶融CaO-SiO2-Al2O3系スラグ相を介した浸炭に対する硫黄の影響について検討し,以下の結論を得た。
1)CaO-SiO2-Al2O3系状態図を基に調整した硫黄含有高炉模擬スラグ(塩基度1)と硫黄含有高塩基度スラグ(塩基度7.6)を用いた浸炭実験で,高塩基度スラグの方が浸炭反応速度が大きいことがわかった。
2)硫黄を含有しないスラグ試料と比較したところ,硫黄を含有させたスラグの方が浸炭反応速度が大きいことがわかった。また,浸炭反応過程において反応中期は浸炭反応速度は大きくなるが,反応後期は浸炭反応速度は硫黄を含まないスラグの値に近づくことがわかった。
記号
PS2:硫黄(g)分圧(N/m2)
PO2:酸素(g)分圧(N/m2)
CS2–:サルファイドキャパシティ(−)
γS2–:サルファイドイオンの活量係数(−)
γC:鉄中炭素の活量係数(−)
K:反応の平衡定数(−)
aO2–:酸素イオンの活量(−)
nC,0:初期の鉄中炭素量(mol/m3)
nC,t:時間t[s]における鉄中炭素量(mol/m3)
A:純鉄薄板の反応界面積(m2)
NC:鉄中炭素のモル分率(−)
k:浸炭反応の総括速度定数(mol/m2・s)