2021 年 107 巻 10 号 p. 814-824
2021 年 107 巻 10 号 p. 814-824
Although it has been pointed out that corrosion products are the preferred scaling site, the detail research has not been conducted. In this study, the initial scaling sites on carbon steel with corrosion product were investigated and scaling mechanisms were discussed. Carbon steel sheets were i mmersed in a solution supersaturated condition for magnesium silicate under normal standard state. Scaling at a corroded part on carbon steel was easier to occur than that at non-corroded part on carbon steel. The corrosion product was comprised of Fe2O3 (Hematite), Fe3O4 (Magnetite), and β-FeOOH (Akaganeite). When the particles of Fe2O3, Fe3O4, and β-FeOOH were individually i mmersed in the solution, the formation of magnesium silicate occurs only on β-FeOOH. One of the preferred scaling sites for magnesium silicate was β-FeOOH. The physical and chemical interactions were investigated. The physical interactions were evaluated by zeta potential, and the results suggested that the repulsion occurs between them. On the other hand, the chemical interaction was evaluated by IR and Raman analyses. Only IR spectrum of β-FeOOH changed. The change was derived from absorption range of Fe-OH in β-FeOOH. The OH group in β-FeOOH may react with silanol group by the dehydration-condensation reaction.
地下水や地熱水は多くの鉱物成分を含むため,温度変化や蒸発による濃縮等で鉱物相が溶液中で過飽和状態となり水中に析出し,スケール,いわゆる“湯あか”が生じる。配管や熱交換器の伝熱面へのスケーリングは流量の減少や熱抵抗となり,系全体の熱効率を著しく低下させるため問題となっている。スケールとして沈着する代表的な鉱物相として炭酸カルシウムやシリカ・シリケートがある1,2)。これら鉱物相の付着を抑制する技術開発をするためには,汎用的に使用されている炭素鋼におけるスケーリング優先サイトを理解しておく必要がある。過去の報告で,Demadis3)は腐食生成物が鉱物相のスケーリングサイトとなると報告しているが,実験的な検証はされておらず経験的な議論しかなされていない。これまでの研究では,長崎県雲仙市小浜温泉にて形成した炭素鋼管上のスケールが,炭素鋼内壁から腐食生成物,シリケート,炭酸カルシウムの順で層構造となっており,腐食生成物がシリカ・シリケートのスケーリングサイトになっていた組織解析の報告があるのみである4–6)。なお,腐食生成物上に形成されたシリケートはマグネシウムを含んでおり,マグネシウムシリケートと同定された4,5)。本研究では,この実環境において腐食生成物上での形成が観察されたマグネシウムシリケートを対象にして,マグネシウムシリケートの炭素鋼上のスケーリングに及ぼす腐食生成物の影響を理解するために,室温でマグネシウムシリケートが析出する溶液を合成し,その溶液中に腐食させた炭素鋼と腐食させていない炭素鋼を浸漬させ,両炭素鋼のスケーリング性を評価した。そして,マグネシウムシリケートの付着形態観察および組織解析を行い,腐食生成物を起点としたマグネシウムシリケートのスケーリングをラボ環境で実証した。また,スケーリングサイトになった腐食生成物内の鉄系酸化物あるいは水酸化物を明らかにするため,本研究の系において発生した腐食生成物とマグネシウムシリケート間の物理的相互作用や化学的相互作用を評価し,初期スケーリングサイトとなる腐食生成物とその初期スケーリング過程を考察した。
炭素鋼(SPCC)を供試材とした。Table 1に化学組成を示す。試料の大きさは60 mm×60 mm×1 mmtであった。腐食させた炭素鋼は20 mg/Lの塩化ナトリウム水溶液に25°Cで24時間浸漬させることにより作製した。
| C | Mn | P | S | Si | |
|---|---|---|---|---|---|
| Carbon steel | 0.15 | 0.60 | 0.10 | 0.050 | ー |
Fe2O3(Hematite),Fe3O4(Magnetite),β-FeOOH(Akaganeite)の粉末試料を供試材とした。Fe2O3,Fe3O4は,それぞれ市販の標準試薬である,酸化鉄(III)および酸化二鉄(III)鉄(II)を用いた。β-FeOOHは塩化鉄(III)六水和物(FeCl3・6H2O)を27.03 g/Lの溶液とし,40°Cの恒温槽内に8日間静置し合成した。なお,試験前のサンプルについては湿度が十分に低い状態で保管し,すぐに取り出し測定した。
2・2 スケーリング試験2・2・1 板材試料に対するスケーリング試験マグネシウムシリケート合成溶液中に板材試料を浸漬し,試料のスケーリング性を評価した。合成溶液には,塩化マグネシウム六水和物(MgCl2・6H2O)とケイ酸ナトリウム九水和物(Na2SiO3・9H2O)の濃度が共に100 mg/Lとなるよう調整した溶液を用いた。25°Cの恒温槽内で溶液中に各試料を24時間浸漬した。試料のスケーリング性は試料の試験前後の重量を計測して評価した。
2・2・2 経時変化観察マグネシウムシリケート合成溶液を入れたシャーレに腐食していない炭素鋼試料を浸漬し,スケーリングの経時変化を観察した。腐食やスケーリングを顕著にさせるため塩化マグネシウム六水和物(MgCl2・6H2O)とケイ酸ナトリウム九水和物(Na2SiO3・9H2O)の濃度が共に板材試料に対するスケーリング試験の2倍の濃度である200 mg/Lとなるよう調整した溶液を用いた。観察には実体顕微鏡を用いて60分毎に同一箇所を板材盤面方向より,板材端面と溶液の境界付近を観察した。観察結果には,観察箇所で腐食が生じなかった場合と生じた場合の代表的な観察結果を示した。
2・2・3 粉末試料に対するスケーリング試験塩化マグネシウム六水和物(MgCl2・6H2O)とケイ酸ナトリウム九水和物(Na2SiO3・9H2O)をそれぞれ100 mg/Lの濃度で調整したマグネシウムシリケート合成溶液中に各粉末試料を30 mg/L入れて撹拌し,スケーリング性を評価した。実験条件は板材試料に対するスケーリング試験(2・2・1)と同様に25°Cの恒温槽内でスケーリング溶液中に各試料を24時間浸漬した。β-FeOOHのスケーリング試験に関してはpHの低下によってマグネシウムシリケートの析出を抑制してしまうため,ホウ酸緩衝液を用いてpH緩衝を行った。ホウ酸緩衝液はホウ酸(H3BO3)と四ホウ酸ナトリウム十水和物(Na2B4O7・10H2O)を,それぞれ74.2 mg/Lおよび76.3 mg/Lで溶解させた。
2・3 組織解析スケーリング箇所の形態観察にはSEM/EDSを用いた。板材試料の観察では,試料にポンチを打ち,試験前後で同一箇所を観察した。
腐食生成物の同定やスケーリング試験前後の相変態の有無の評価にはXRDを用いた。X線源としてCu線源を用い,kβフィルターを挿入した検出器には高速1次元半導体検出器を使用し,波高分析器を用いたPHA法によりX線の単色化を行い,Fe元素からの蛍光X線の影響を低減した。管電圧と管電流をそれぞれ40 kVと15 mAとし,スキャン速度4.0 deg/min,ステップ幅を0.02 degとした。発散スリットは0.625 deg,受光スリットは8.0 mm,散乱スリットはOpenとした。また,分子結合解析には,フーリエ変換赤外分光法(FT-IR)およびラマン分光法を用いた。FT-IRはATR法を用いてIRスペクトルを取得した。測定条件は,波数を400~4000 cm-1,分解能を2 cm-1,積算回数40回とし,検出器として温度調節機構付きDLATGS検出器を用いた。ラマンスペクトルは励起波長532 nmのグリーンレーザーを出力1 mW,露光時間を40秒,積算回数3回で,約3 cm-1の分解能で50~1800 cm-1の波数領域を記録した。試料はKBrで20倍程度に希釈し,レーザー光を100倍の対物レンズ用いて約1 μmのスポット径で照射・検出した。
2・4 ゼータ電位測定静電気的な物理的相互作用を調査するため,25°C,pH=11の水溶液中の粉末試料についてゼータ電位を測定した。レーザードップラー法を用いて,平均電場約16 V/cmのセル内5か所,積算回数3回で移動度を測定した。真の移動度は森・岡本の式より計算し,ゼータ電位をSmoluchowskiの式より求めた。
Fig.1は板材試料に対するスケーリング試験前後における試料の質量変化を示した図で,Fig.2はその外観写真である。マグネシウムシリケート合成液では,腐食させていない炭素鋼の質量は0.50 g/m2減少した。腐食させた炭素鋼においては質量が5.28 g/m2増加した。腐食させていない炭素鋼もスケーリング試験中に一部腐食生成物が形成されており,わずかに腐食していた。腐食させた炭素鋼においては,試験前に形成されていた腐食生成物の分布は試験後も変化がなかったが,一部腐食が進んでいた。
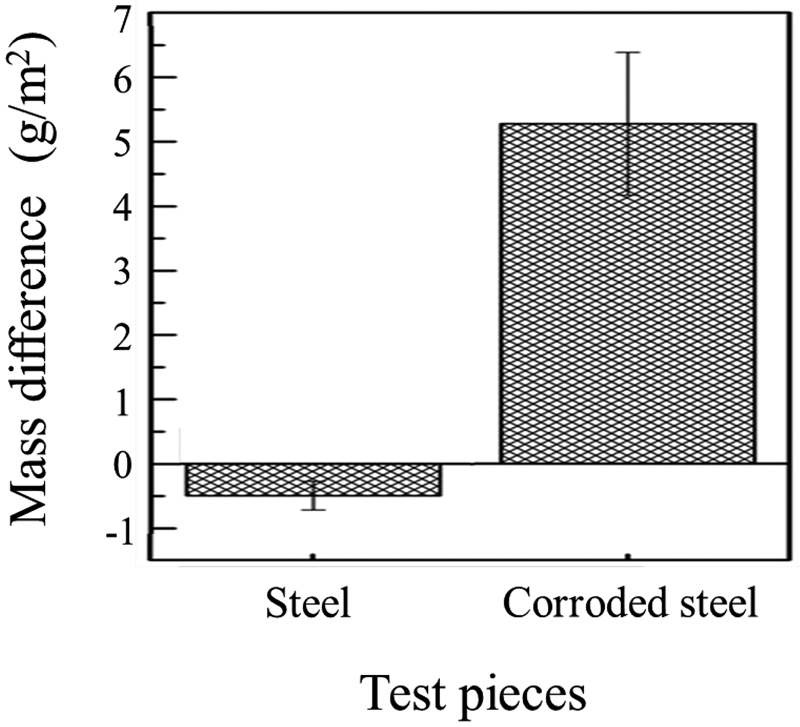
Mass difference between specimens before and after the scaling test.

Photographs of SPCC and corroded one before and after scaling test. (Online version in color.)
経時変化観察試験の結果をFig.3に示す。白い点線で炭素鋼と溶液の境界を示した。腐食の生じなかった箇所では,600分後においてもマグネシウムシリケートが付着しなかった(Fig.3(a))。一方,炭素鋼の腐食が生じた箇所では,120分後までに腐食生成物が発生し,240分後にマグネシウムシリケートが腐食生成物全面を覆うように付着し,その後,マグネシウムシリケートが成長することで厚みを増した(Fig.3(b))。なお,腐食の生じなかった部分(Fig.3(a))の600分後の写真で炭素鋼表面の色味が白く変化しているのは,撮影機材の自動露出機能によるもので,実際には変化していなかった。

Temporal changes of optical photographs at (a) non-corroded part and (b) corroded one on the carbon steel immersed in the test solution. (Online version in color.)
板材試料に対するスケーリング試験において,試験前の腐食させた炭素鋼表面から採取した腐食生成物のXRD回析パターンをFig.4に示す。腐食生成物はFe2O3,Fe3O4,β-FeOOHの3種類の腐食生成物から構成されていた。Fig.5(a)に腐食させた炭素鋼のスケーリング試験前のSE像およびEDSによる同一場所の元素マッピングを示す。Oが分布している部分は鉄の腐食生成物が生成されており,基材ままの部分があることを確認出来る。

X-ray diffraction profiles of corrosion products sampled from the corroded carbon steel before the scaling test.

SE images and element maps of corroded carbon steel surface (a) before and (b) after the scaling test. (Online version in color.)
Fig.5(b)に腐食させた炭素鋼の板材試料に対するスケーリング試験後のSE像および元素マッピングを示す。試験後,Siは腐食生成物上全体に分布していた。Si濃度の低い部分ではMgを検出することができなかったが,Si濃度の高い部分ではMgが検出された。高倍で観察した結果,Si濃度の低い部分では,スケール等の物質を確認できなかった。したがって,腐食生成物とマグネシウムシリケート合成溶液が反応したためSiが検出された,あるいは粒子が非常に小さく確認できなかった,のいずれかである。Fig.6に板材試料に対するスケーリング試験と同じ条件で合成した溶液から取り出したマグネシウムシリケート粉末の高倍率のSEM写真と,板材試料に対するスケーリング試験後のSi濃度の高い部分で観察されたマグネシウムシリケートのSEM写真を示し,比較した。マグネシウムシリケート粉末では粒子が連なった形態であった(Fig.6(a))。腐食させた炭素鋼の腐食生成物上でも同様に連なったマグネシウムシリケートが観察され,腐食生成物を覆うように付着していることが確認でき(Fig.6(b)),そこではSiとMgが検出された(Fig.6(c))。

High magnified SE images of (a) magnesium silicate precipitated in the test solution and (b) magnesium silicate scale on corrosion product, and (c) the element maps in figure (b). (Online version in color.)
Fig.7は粉末試料に対するスケーリング試験後の各腐食生成物のSiの検出された部分をピックアップしたSEM/EDS像である。全ての腐食生成物上で,SiとOを主成分とする物質が存在する箇所を確認することができた。Fe2O3ではSiとOを主成分とする,Fe3O4ではSi,Al,Oを主成分とするなだらかな表面と扁平状の物質であった。β-FeOOHでは,Mg,Si,Oから構成され,表面は複数の粒子が連なった様に凹凸形状であった。

SE images and element maps of (a) Fe2O3, (b) Fe3O4 and (c) β-FeOOH after the scaling test. (Online version in color.)
粉末試料に対するスケーリング試験前後の各腐食生成物のXRD回析プロファイルをFig.8に示す。各試料について,試験前後でピーク位置に変化はなく,溶液中で相変態は生じていなかった。Fe2O3とFe3O4は,試験前後でピーク強度に変化はなく,結晶度も変化しなかった。一方,β-FeOOHは試験後の方が試験前よりもピーク強度が高かった。また,スケーリング溶液のpH緩衝で使用した緩衝液のみの溶液中にβ-FeOOHを浸漬して取り出した時,ピーク強度が更に低下し,結晶度が下がっており,β-FeOOHは緩衝溶液中で分解した。

X-ray diffraction patterns of Fe2O3, Fe3O4 and β-FeOOH before and after the scaling test. (Online version in color.)
粉末試料に対するスケーリング試験前後の試料のIRスペクトルの指紋領域をFig.9に,官能基領域をFig.10に示す。指紋領域について,514 cm-1および472 cm-1のピークはFe2O3におけるFe-O結合振動に起因するピークである7)。Fe3O4に見られる535 cm-1のピークもFe-O結合振動の吸収ピークである8)。β-FeOOHの840 cm-1のピークはFe-O-H間の曲げ振動,640 cm-1はFe-OもしくはFe-OHの対称延伸振動か格子振動に関する吸収ピークである9)。試験前後でβ-FeOOHのみスペクトルに変化があった。指紋領域では840,640 cm-1のピーク強度の減衰,800 cm-1に新しいピークが現れた。官能基領域の3300 cm-1から3400 cm-1へのピークのシフトと強度の減衰がみられ,この吸収帯は内部のOH基に由来するものである10)。β-FeOOHの指紋領域のピークについて,Ramanスペクトルを取得した結果をFig.11に示す。310,390,720 cm-1の強いピークはβ-FeOOHに特徴的なピークであり,この内390 cm-1のピークは390 cm-1と430 cm-1の2つから,720 cm-1は720 cm-1と680 cm-1のショルダーピークから成る11)。IR活性部以外について539 cm-1,392 cm-1でピークの減衰がみられた。低波数領域は,Fe-O延伸振動およびFe-OH曲げ振動に関係しており,IRの測定結果と同様であった。IR活性と一致する変化では,680,840 cm-1のピークの減衰と800 cm-1に発生した新しいピークをRamanスペクトルでも確認できた。
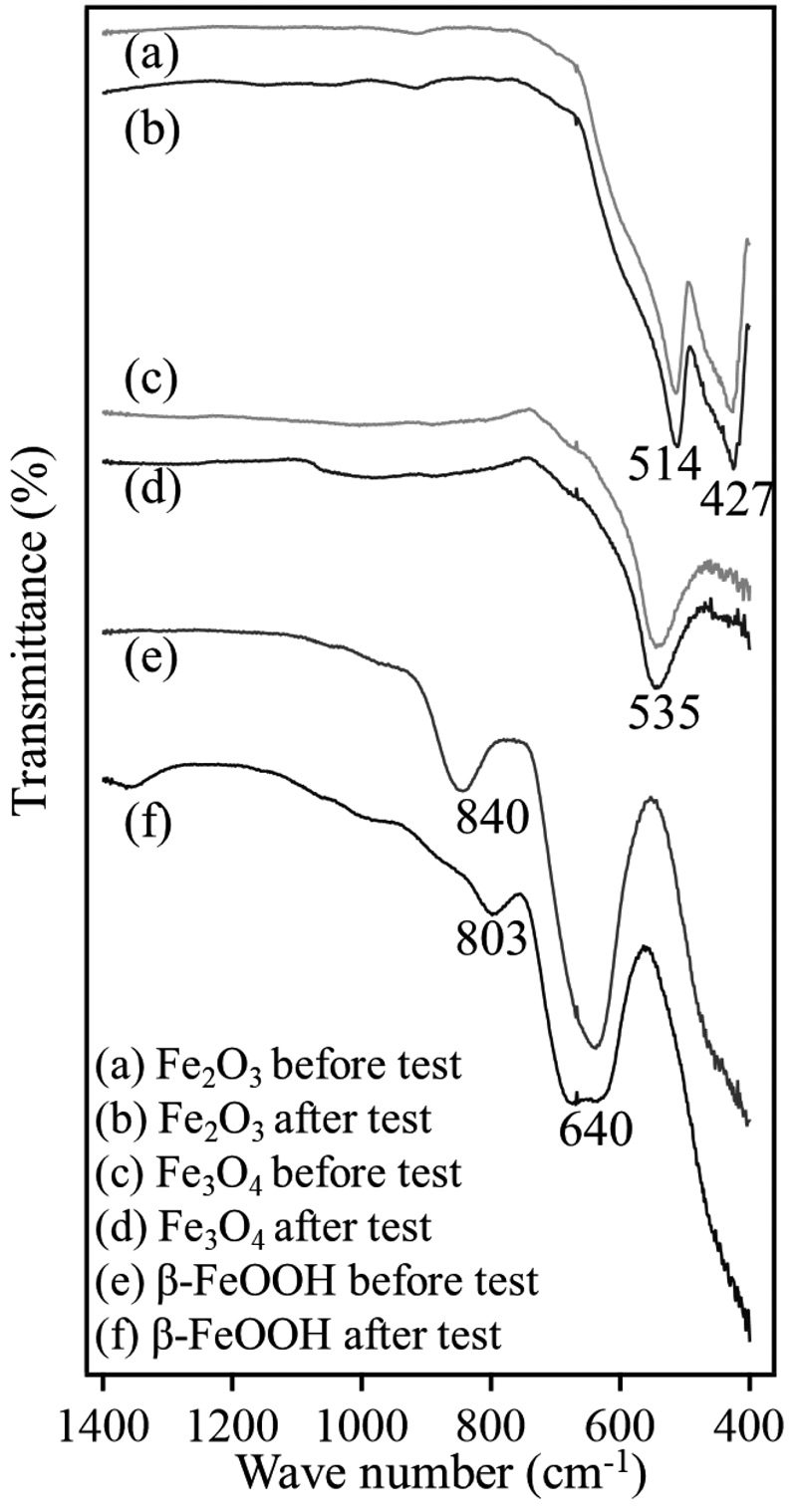
IR spectra in fingerprint region of Fe2O3, Fe3O4 and β-FeOOH b before and after the scaling test.
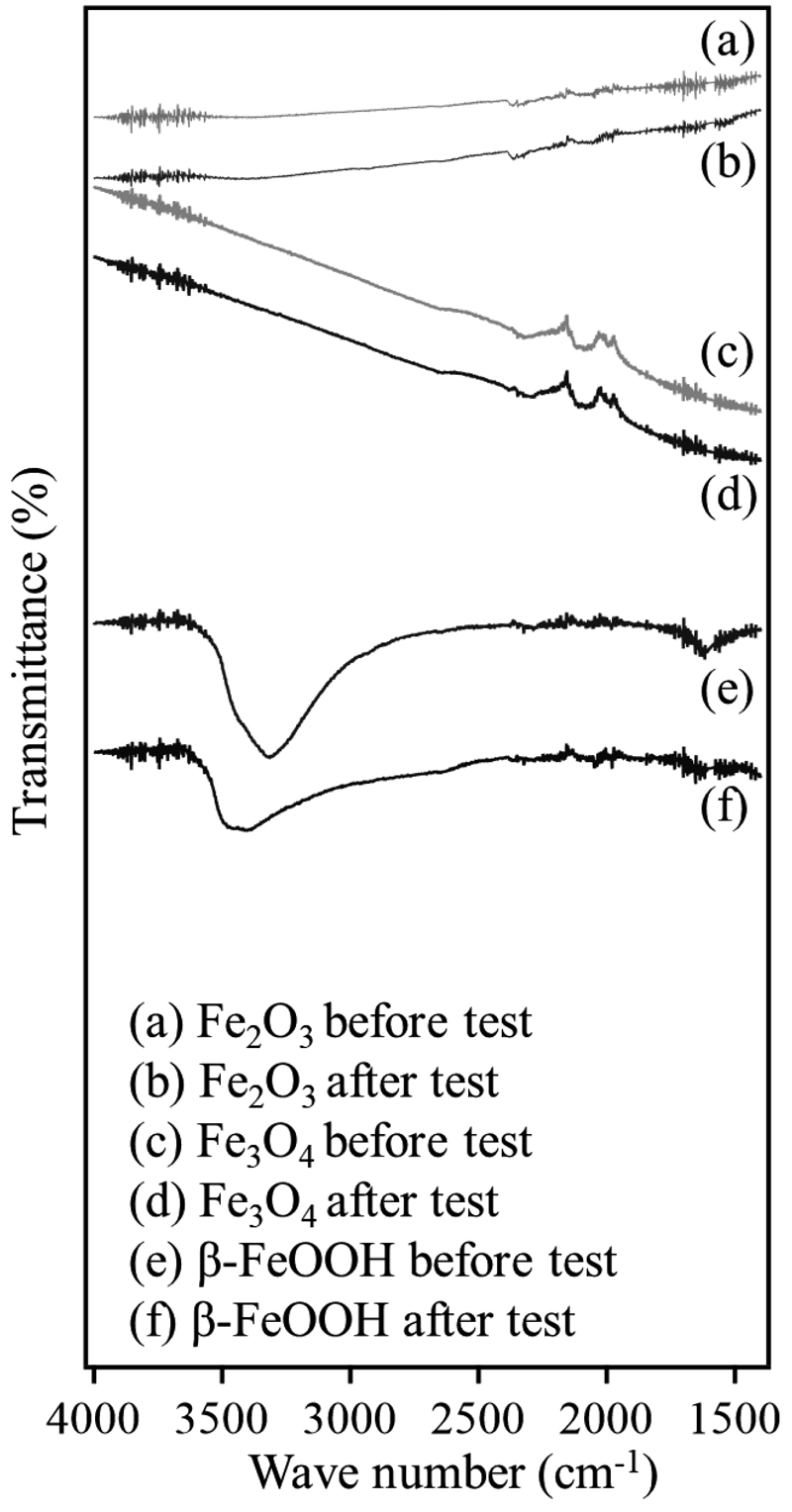
IR spectra in functional group region of Fe2O3, Fe3O4 and β-FeOOH before and after the scaling test.
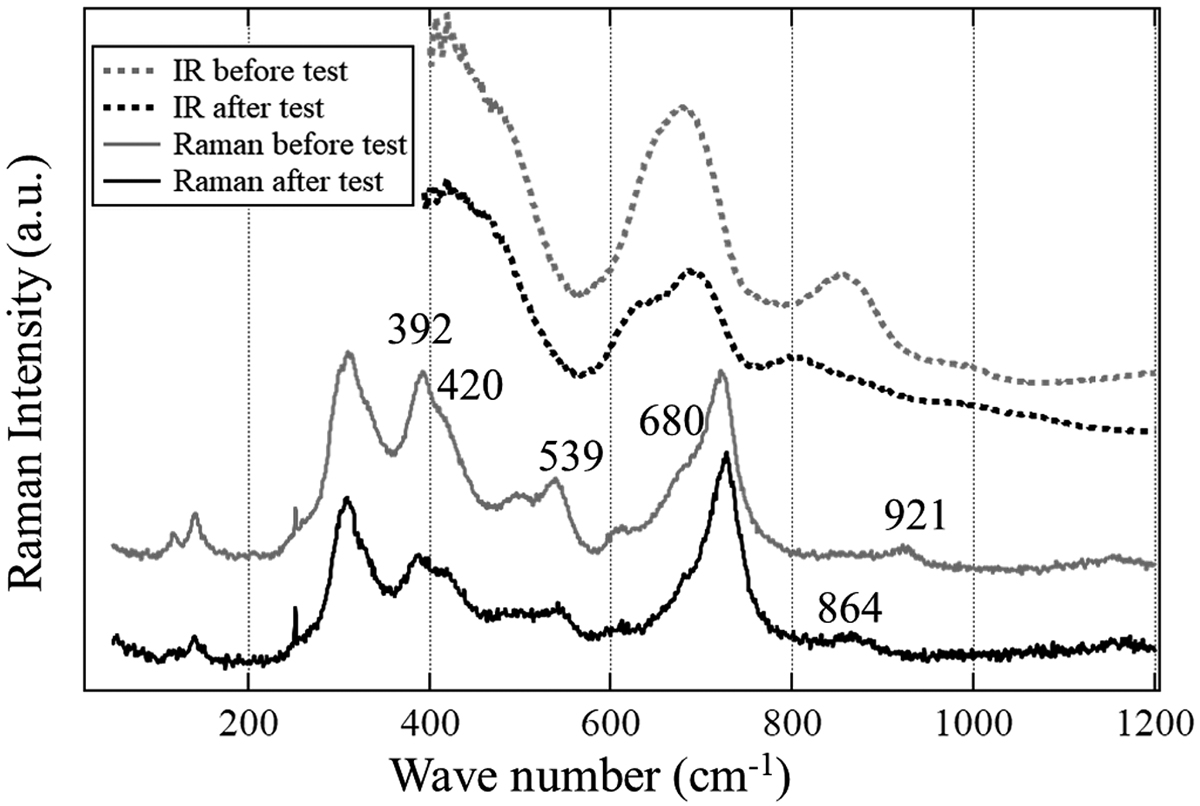
Raman and IR spectra of β-FeOOH before and after the scaling test.
Table 2にpH=11における各腐食生成物とマグネシウムシリケートのゼータ電位を示す。腐食生成物として確認されたFe2O3,Fe3O4,β-FeOOHのゼータ電位はそれぞれ-42.2,-33.9,-35.2 mVで負の電荷であった。本実験で行ったMg/Si比を保ちながら濃度を増して加速させて析出させたマグネシウムシリケートのゼータ電位は-7.0 mVであり,マグネシウムシリケートもまた負の電荷を示した。
| Sample | Zeta potential (mV) |
|---|---|
| Fe2O3 | −42.2 |
| Fe3O4 | −33.9 |
| β-FeOOH | −35.2 |
| Magnesium silicate | −7.0 |
経験的にスケールは腐食生成物上に形成容易と考えられてきた3)。腐食させた炭素鋼はスケーリング試験後に重量増加がみられ(Fig.1),その腐食生成物上ではスケーリングが確認された(Fig.5)。一方,腐食させていない試験片では,腐食量はわずかであり,重量が減少した。腐食生成物生成による重量増加やスケール形成による増加量よりも腐食による減量が優位であったため重量減少したといえる。したがって,腐食させた炭素鋼上での重量増加はスケーリングによるものと考えられる。スケール合成溶液中に浸漬した炭素鋼の経時変化を観察した結果からも,基材ままの部分にはスケーリングせず,腐食が生じた部分では優先的にスケーリングし成長したことが観察された(Fig.3)。このように本研究において実験的に腐食生成物上にスケーリング容易であることが示された。腐食生成物の種類は様々あるが,主に酸化鉄とオキシ水酸化鉄に分類できる。本研究では,腐食させた炭素鋼板を準備し,その腐食生成物は酸化鉄としてFe2O3,Fe3O4,オキシ水酸化鉄としてβ-FeOOHを含んでいた(Fig.4)。これらの腐食生成物のいずれかがスケーリングに関与していると考えられる。Fe2O3,Fe3O4とオキシ水酸化鉄に対して行ったスケーリング試験では,全ての粉末においてSiの存在を確認できた(Fig.7)。Fe2O3上では扁平状のSiとOから構成されるシリカであった(Fig.7(a))。その形状は板材試験片上で見られたスケーリングした物質の形態とは異なっていた(Fig.6(b))。また,スケーリング試験前後においてFe2O3の結晶構造および分子構造の変化は認められず,シリカや溶液と反応はしていなかった(Figs.8-10)。腐食させた炭素鋼板上でSi元素のみの存在が確認できた腐食生成物上では粒子状の物質は確認できなかった(Fig.5(b))。したがって,Fe2O3上で確認されたシリカは標準試薬に含まれていた不純物であると考えられる。Fe3O4の粉末試料に対するスケーリング試験では,Alを含む扁平な形状のアルミノシリケートが確認された(Fig.7(b))。しかし,この実験系においてはアルミニウムを添加していないため,アルミニウムシリケートの析出は起こりえない。また,不純物のアルミニウムが溶け出し,溶液と反応した場合を考えたとしても,標準状態でのアルミノシリケートの溶解度は10 mg/Lであり12),本実験で調整したスケーリング溶液ではこれを上回らない。したがって,粉末試料の純度に起因する不純物であると考えられる。Fe2O3,Fe3O4のスケーリング試験前の試料に対しEDS像を確認したところ,SiおよびAlの混入が見られた。β-FeOOHでは,Si,O,Mgを同位置に含み,形態が粒子の連なったような形状をしているシリケートが観察された(Fig.7(c))。この形態はマグネシウムシリケートのみを析出させた時の形態と一致していた(Fig.6(a))。スケーリング試験後のβ-FeOOHはピーク強度が向上していた(Fig.8(e)and(f))。また,β-FeOOHをアルカリ緩衝液中に浸漬して取り出した場合,回析ピーク強度が低下していことから結晶度が下がっていた(Fig.8(g))。β-FeOOHはアルカリ環境下でα-Fe2O3へ転化していくことが知られている13)。Fe(OH)3からβ-FeOOHを経てα-Fe2O3へと転化するとき,低結晶度であるβ-FeOOHから転化することから14),結晶度の高いβ-FeOOHは結晶度が低下した後にα-Fe2O3へと転化すると考えられる。本試験で用いたβ-FeOOHは大気中の水分を含みやすいことを確認しており,XRD解析時にも大気中の水分を含みα-Fe2O3へ転化し続け,結晶度が低下したと考えられる。一方,スケーリング試験後のβ-FeOOHはシリケート溶液中に浸漬したことにより転化が抑制され安定化した。結果,β-FeOOHままの結晶度と比較して,スケーリング試験後のβ-FeOOHの結晶度が見かけ上高くなったと考えられる。腐食させた炭素鋼板のスケーリング試験後,腐食生成物上ではSi元素が検出された(Fig.5(b))。しかし,シリカ粒子等は観察されなかった。アモルファスシリカの溶解度は標準状態で115 mg/Lであり12),今回の試験条件ではシリカ粒子が析出することはなかった。このことから,β-FeOOHはシリカ粒子と反応したわけではなく溶液中のイオンと反応したといえる。β-FeOOHにおいてはスケーリング試験前後でIRスペクトルに変化がみられた(Figs.9 and 10)。この結果もまたスケーリング溶液中のイオンとβ-FeOOHが反応したことを示唆する。Kwonら14)はシリケートイオンが存在することによるβ-FeOOHの転化の阻害は,β-FeOOH表面に溶液中のシリケートイオンが吸着することによると指摘している。本研究の結果は,その結果と一致しており,Fig.5(b)で検出されたSiはシリケートイオンとβ-FeOOHが反応した結果と考えられる。
以上のことから,腐食生成物中のFe2O3とFe3O4はマグネシウムシリケートのスケーリングサイトではなく,β-FeOOHがスケーリングサイトであった。
4・2 腐食生成物上でのマグネシウムシリケートスケーリング機構本実験で用いたような系でのスケール形成機構として,溶液中で析出した微粒子のマグネシウムシリケートと鉄系酸化物との物理的な相互作用によるものと,溶解状態のシリケートが鉄系酸化物と化学的な反応でマグネシウムシリケートが鉄系酸化物上に析出する2通りの場合が考えられる。物理的相互作用については物理的吸着が挙げられる。重力等の影響による停滞によっても生じるが,本研究では実験系として撹拌を行っており,重力の影響を無視して電気的な吸着性のみで議論する。通常電気的な吸着性はDLVO理論で表されるが,Ohsako and Wu15)によると,ゼータ電位の電荷の符号が違えば引力を,同じであれば斥力というように,粒子系の分散・凝縮性をゼータ電位による静電的な相互作用の概念で説明することができる。いずれの鉄系酸化物も負の電位をもっており,マグネシウムシリケートもまた負の電位を持っていた(Table 2)。このことから鉄系酸化物とマグネシウムシリケートは斥力を持つことが分かる。同符号であれば,電位差が大きいほど強い斥力が働く。このことから,物理的にはFe2O3,β-FeOOH,Fe3O4の順でマグネシウムシリケート粒子と接近容易で無い。実験結果においてはβ-FeOOHで最もスケーリング容易であり,スケーリングの難易に静電気的な相互作用はほとんど関与していなかった。一方,化学的相互作用については,溶液中での物質の相変態や,腐食生成物とスケールとなる物質の官能基同士の反応が挙げられる。Fe2O3とFe3O4は結晶相ならびに分子結合の両方で変化はなく,化学的相互作用を起こさなかった(Figs.8 and 9)。一方,β-FeOOHはFe-OH間の結合に由来する吸収ピークと官能基領域での3300 cm-1以降の大きなピークで変化が見られた(Fig.10)。特に,Fe-OH結合についてはIR分光法とラマン分光法の両方で明確な変化が現れており(Figs.9 and 11),β-FeOOHのFe-OH結合で化学反応が生じたといえる。先述したようにスケーリング試験後の観察よりシリケートイオンが存在することによって溶液中のシリケートイオンとβ-FeOOHが反応したことが示唆された。β-FeOOHのIRスペクトルを規格化して官能基領域を比較したものをFig.12に示す。スケーリング試験後のピークの減衰はOH基の減少を示す。ゆえにβ-FeOOH表面のFe-OHのOH基とシリケートイオンの持つ水酸基が脱水縮合反応したと考えられる。
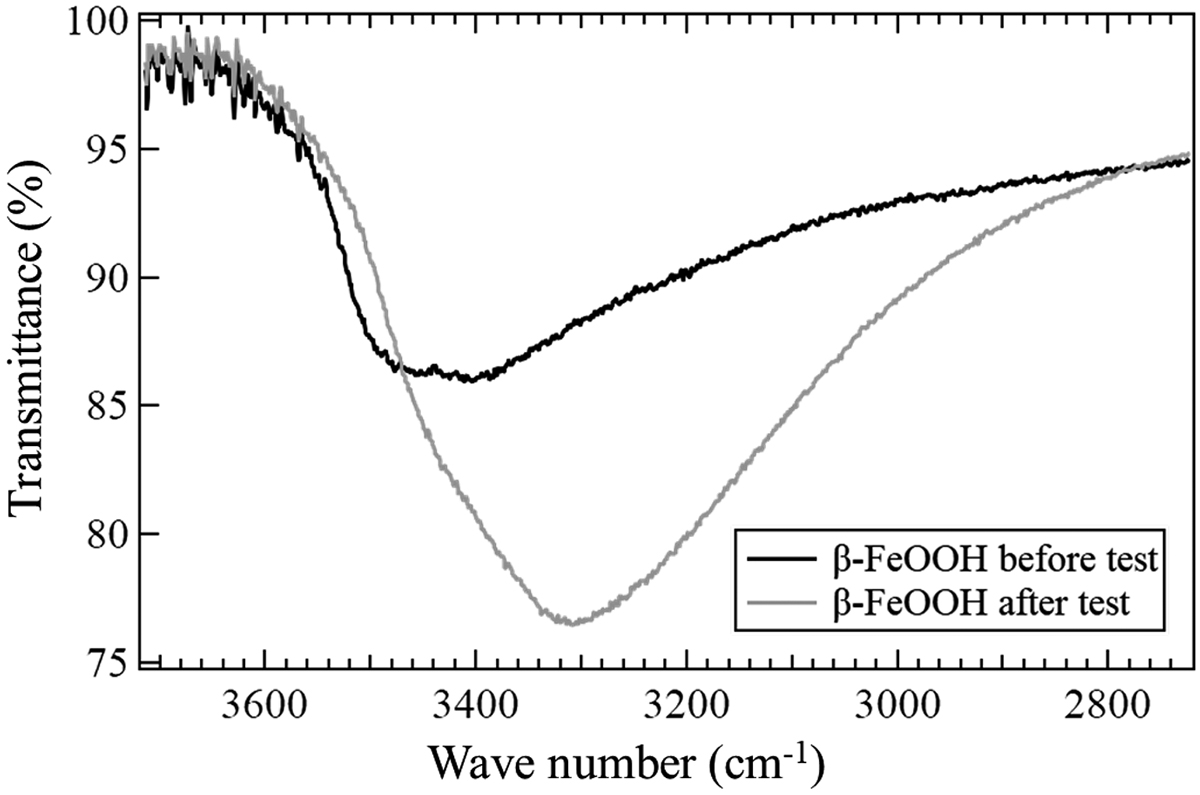
IR spectra of β-FeOOH before and after the scaling test.
腐食させた炭素鋼板上へのスケーリング試験では腐食生成物上でSi元素のみの部分が全体的に検出され,マグネシウムシリケートの形成は一部であった。一方,加速して行った経時変化の試験では,腐食生成物全体を覆うようにマグネシウムシリケートのスケーリングが進行していた。上記の結果から,本研究における炭素鋼上の初期のスケーリング過程を下記のように整理できる。
(1)炭素鋼上で腐食が生じ,β-FeOOHを含む腐食生成物が生成する。
(2)β-FeOOHとシリケートイオンが脱水縮合反応する。
(3)反応した部分を生成サイトとし,マグネシウムシリケートが腐食生成物を覆うように成長する。
このようにβ-FeOOHに対しシリケートイオンが反応した部分でマグネシウムシリケートの生成サイトとなった。腐食生成物を制御することでスケーリングを鈍化させられる可能性が示唆された。
炭素鋼上のスケーリングに及ぼす腐食生成物の影響を理解するために,室温でマグネシウムシリケートが析出する溶液を合成し,その付着形態観察および組織解析を行い,腐食生成物上に生じるその初期スケーリング過程を考察した。その結果以下のことが分かった。
(1)腐食させていない炭素鋼とステンレス鋼は同程度のスケーリング性であったが,腐食させた炭素鋼は高いスケーリング性を示した。腐食生成物上ではスケーリング容易である。
(2)Fe2O3(Hematite),Fe3O4(Magnetite),β-FeOOH(Akaganeite)の3種の中で,マグネシウムシリケートのスケーリングが顕著であったのは,β-FeOOH(Akaganeite)であった。
(3)Fe2O3,Fe3O4,β-FeOOHの3種とマグネシウムシリケートの静電気的な相互作用を評価した結果,それら3種とマグネシウムシリケートの間では斥力が働いていた。腐食生成物上でのスケーリングは物理的な相互作用が要因ではない。
(4)マグネシウムシリケートが析出する溶液中にFe2O,Fe3O4,β-FeOOHを浸漬した結果,Fe2O3とFe3O4で化学的反応は生じなかった。β-FeOOHではFe-OHとシリケートイオンが脱水縮合反応した。この反応したβ-FeOOHがスケーリングの初期生成サイトであると考えられる。
本研究の一部はJSPS科研費19H02453とクボタ若手研究者研究奨励制度(金属材料分野)の助成を受けて行われたものである。ここに謝意を表する。