2022 年 71 巻 2 号 p. 294-300
2022 年 71 巻 2 号 p. 294-300
新型コロナウイルス感染症(COVID-19)において,polymerase chain reaction(PCR)検査は確定診断に用いられている。当院では2020年4月から順次,定期検査用としてAmpdirectTM2019-nCoV検出キット(Ampdirect法)を,緊急検査用としてGeneXpert Xpress SARS-CoV-2「セフィエド」(GeneXpert法)およびFilmArray呼吸器パネル2.1(FilmArray法)を導入した。各検査法の検出率について,導入から同年12月までにGeneXpert法で測定した161検体およびFilmArray法で測定した493検体を対象とし,Ampdirect法と比較した。検出率は発症10日以内ではいずれも90%以上となった。また同年7月から12月までに測定した8,416検体をCOVID-19患者対応診療科(COVID-19診療科)とその他の一般診療科に分け,検査実績を評価した。陽性率(定期検査/緊急検査)はCOVID-19診療科で11.6%/29.9%,一般診療科で0.13%/3.50%となった。緊急検査の陽性率は定期検査よりも高く,陽性時の迅速な結果判明は入院や転院の判断,感染拡大防止の一助となった。また検査法を使い分けることにより,感染拡大に伴う検査件数の急増に対応することができた。COVID-19流行下における検査体制について,複数のSARS-CoV-2核酸検出キットをそれぞれの特徴を活かして運用することは大変有用であると考えられた。
In COVID-19 assay, the polymerase chain reaction (PCR) test is used for a definitive diagnosis. We have introduced the use of the AmpdirectTM2019-nCoV detection kit (Ampdirect method) for regular examinations, GeneXpert Xpress SARS-CoV-2 “Cepheid” (GeneXpert method), and FilmArray Respiratory Panel 2.1 (FilmArray method) in this sequence for emergency examinations from April 2020. The detection rates of these test methods for 163 samples measured by the GeneXpert method and 493 samples measured by the FilmArray method from their introduction to December 2020 were compared with those measured by the Ampdirect method. The detection rate within 10 days from onset was 90% and above. By focusing on the COVID-19-specialized clinical department and the general clinical department, the tests of 8,416 samples measured from July to December 2020 at our hospital were evaluated. The positivity rates (regular examinations/emergency examinations) were 11.6%/29.9% in the COVID-19-specialized clinical department and 0.13%/3.50% in the general clinical department. The positivity rate of the emergency examinations was higher than that of the regular examinations, and it was considered that the rapid result indicating positivity helped in deciding whether a patient requires admission in a general hospital or transfer to a COVID-19-specialized clinical department, thereby preventing the spread of infection. By using different test methods, we were able to quickly obtain the results and respond to the rapid increase in the number of cases to be tested. Regarding the testing system during the COVID-19 epidemic, it was considered very useful to apply multiple SARS-CoV-2 nucleic acid kits to make the best use of their respective characteristics.
2019年12月頃に報告された新型コロナウイルス感染症(COVID-19)1)の急速な拡散による世界的な流行は2021年になっても収束しておらず,医療現場を逼迫するなど社会的な問題となっている。本邦においては2020年1月に最初の感染者が報告され,同年2月に指定感染症となった2)。当院は感染症指定医療機関ではなかったが,厚生労働省の定める「行政検査としてCOVID-19に係る検査を実施する医療機関」3)に該当するため,感染拡大に伴い同年4月より重症および中等症のCOVID-19患者を対象とした専用病棟を設け,入院患者の受け入れを開始した。また,8月に地域の医療施設からのCOVID-19疑い紹介患者の診察を行う地域外来・検査センターを,12月には重症患者専用病棟である大阪コロナ重症センターを開設し,大阪府のCOVID-19医療において重要な役割を担っている。
2. SARS-CoV-2核酸増幅検査の院内導入COVID-19において,polymerase chain reaction(PCR)検査は確定診断に用いられている4)。PCR検査は当初保健所で行政検査として実施されていたが,民間検査機関の検査能力増強を見込んで3月に「SARS-CoV-2核酸検出」が新規保険収載項目となった5)。当院でも2020年4月からのCOVID-19入院患者の受け入れ開始に伴い,栄研化学のLoopamp® SARSコロナウイルス検出試薬キット(LAMP法)6)を導入し,院内検査を開始した。当初は入院中のCOVID-19患者の退院時や処置前の陰性確認といった限られた用途での試験的な運用であった。しかし入院時や手術前など検査対象が増加したことから,6月に島津製作所のAmpdirectTM2019-nCoV検出キットとロシュ・ダイアグノスティックス社のLightCycler96を用いたreal-time RT-PCR法(Ampdirect法)7)に切り替え,平日2回(午前10時30分と午後2時)の定期検査として運用を開始した。検査材料は当初より鼻腔拭い液のみとし,採取容器はコパンUTM(コパンジャパン)またはウイルス輸送液VTM(スギヤマゲン)を用いた。検体採取は外来の専用採取室,またはCOVID-19患者を取り扱う診療科にて行った。
更に7月になると,救急診療科へ運ばれてきた患者がCOVID-19であれば受け入れ,非COVID-19であれば転院するといったコロナトリアージが始まり,定期検査以外の時間帯や夜間休日の緊急検査の需要が高まった。そのため,少数検体迅速測定装置であるベックマン・コールター社のGeneXpert Xpress SARS-CoV-2「セフィエド」(GeneXpert法)8)を7月に,ビオメリュー社のFilmArray呼吸器パネル2.1(FilmArray法)9)を8月に導入し,この2法を緊急検査として用いた24時間対応を開始した。なお,GeneXpert法とFilmArray法の使い分けは試薬の供給状況に応じて行った。FilmArray法はSARS-CoV-2以外の感染症項目も同時に測定するが,結果報告はGeneXpert法に合わせてSARS-CoV-2のみとした。以後,当院の検査体制はAmpdirect法による平日2回の定期検査とGeneXpert法またはFilmArray法による24時間対応の緊急検査で運用している。なお,臨床症状などから偽陽性または偽陰性が疑われる場合は別法で再検している。よって,GeneXpert法およびFilmArray法は緊急依頼時だけではなく,Ampdirect法で測定済み検体の再検査にも使用している。また,初検と再検で結果が乖離した場合はinfection control docter(ICD)と協議の上,結果を報告している。
当院で導入したAmpdirect法,GeneXpert法,FilmArray法の比較および,この3法を用いた定期検査と緊急検査の検査実績について評価したので報告する。
本検討は,大阪急性期・総合医療センター臨床医学倫理審査委員会の承認(試験番号:2020-028)を得て実施した。
導入後から2020年12月までに緊急検査法で測定した654検体(GeneXpert法:161検体,FilmArray法:493検体)を対象とし,Ampdirect法と検出率を比較した。検査材料は全て鼻腔拭い液で,提出後24時間以内(冷蔵保存)に測定した。
COVID-19の確定診断基準は,感染が疑われる患者においてSARS-CoV-2が検出されることである4)。本検討では,COVID-19疑いなどでPCR検査を行った結果SARS-CoV-2陽性となった検体と,すでに確定診断されており他院からの転院時などに当院でPCR検査を行った検体を「COVID-19患者検体」と定義する。
GeneXpert法で測定した161検体の内訳はCOVID-19患者検体26件(発症10日以内18件,発症11日以降4件,発症日不明1件,無症状3件),非COVID-19患者検体135件であった。FilmArray法で測定した493検体の内訳はCOVID-19患者検体87件(発症10日以内45件,発症11日以降35件,発症日不明1件,無症状6件),非COVID-19患者検体406件であった。なお,発症10日以内の区分は,発症から約10日後はウイルスがほとんど分離されず,感染性が低いと考えられていることから設定した10)。
1) Ampdirect法最大96件同時測定可能,必要検体量は5 μL,結果報告までに要する時間は2時間(前処理30~50分(RNA抽出は不要),LightCycler96による核酸増幅70分)である。検出対象はN(Nucleocapsid)遺伝子の2領域(N1, N2)である。
2) GeneXpert法当院では4 UNIT × 2台所持しており,最大8件同時測定可能,必要検体量は300 μL,結果報告までに要する時間は55分(前処理5分,核酸増幅50分)である。各UNITが独立しているため測定中に検体を追加することができる。検出対象はE(Envelope)遺伝子とN遺伝子(N2)の2領域である。
3) FilmArray法当院では2 UNIT所持しており,最大2件同時測定可能,必要検体量は300 μL,結果報告までに要する時間は50分(前処理5分,核酸増幅45分)である。各UNITが独立しているため測定中に検体を追加することができる。検出対象はS(Spike)遺伝子とM(Membrane)遺伝子の2領域である。
2. 検査実績の評価平日2回の定期検査(Ampdirect法)と24時間対応の緊急検査(GeneXpert法またはFilmArray法)による運用を開始した2020年7月から12月までのSARS-CoV-2核酸増幅検査の実施件数は8,416件であった。ここから依頼元別にCOVID-19患者に対応する診療科(COVID-19診療科)とCOVID-19以外の患者に対応する診療科(一般診療科)に分け,実施件数と陽性率を集計した。また,同時期の大阪府全体の陽性数の推移とも比較した。
COVID-19患者検体26件におけるAmpdirect法の検出率は発症10日以内94%(17/18),11日以降100%(4/4),発症日不明100%(1/1),無症状67%(2/3)となった。GeneXpert法の検出率は10日以内100%(18/18),11日以降100%(4/4),発症日不明100%(1/1),無症状67%(2/3)となった。非COVID-19患者検体135件は2法ともすべて陰性となった。
発症日数は10日以内18検体が平均3.5日,11日以降4検体は平均17.0日,最長24日であった。GeneXpert法陽性でAmpdirect法陰性となった2件は,発症2日目と無症状患者の検体であった。GeneXpert法陰性でAmpdirect法陽性となった1件は,無症状患者の検体であった(Figure 1)。

n = 26
COVID-19患者検体87件におけるAmpdirect法の検出率は発症10日以内98%(45/46),11日以降74%(26/35),無症状83%(5/6)となった。FilmArray法の検出率は10日以内98%(44/45),11日以降77%(27/35),発症日不明100%(1/1),無症状100%(6/6)となった。なお,発症30日以降の8検体で2法ともまたはいずれかで陽性となったのは6件あり,これらは治療中または治療後に転床や転院前の検査として提出された検体であった。非COVID-19患者検体406件は2法ともすべて陰性となった。発症日数は10日以内45検体が平均4.5日,11日以降35検体は平均24.2日,最長44日であった。FilmArray法陽性でAmpdirect法陰性となった5件は,発症1日目,23日目,29日目,44日目と無症状,FilmArray法陰性でAmpdirect法陽性となった3件は発症2日目,30日目,41日目の検体であった(Figure 2)。
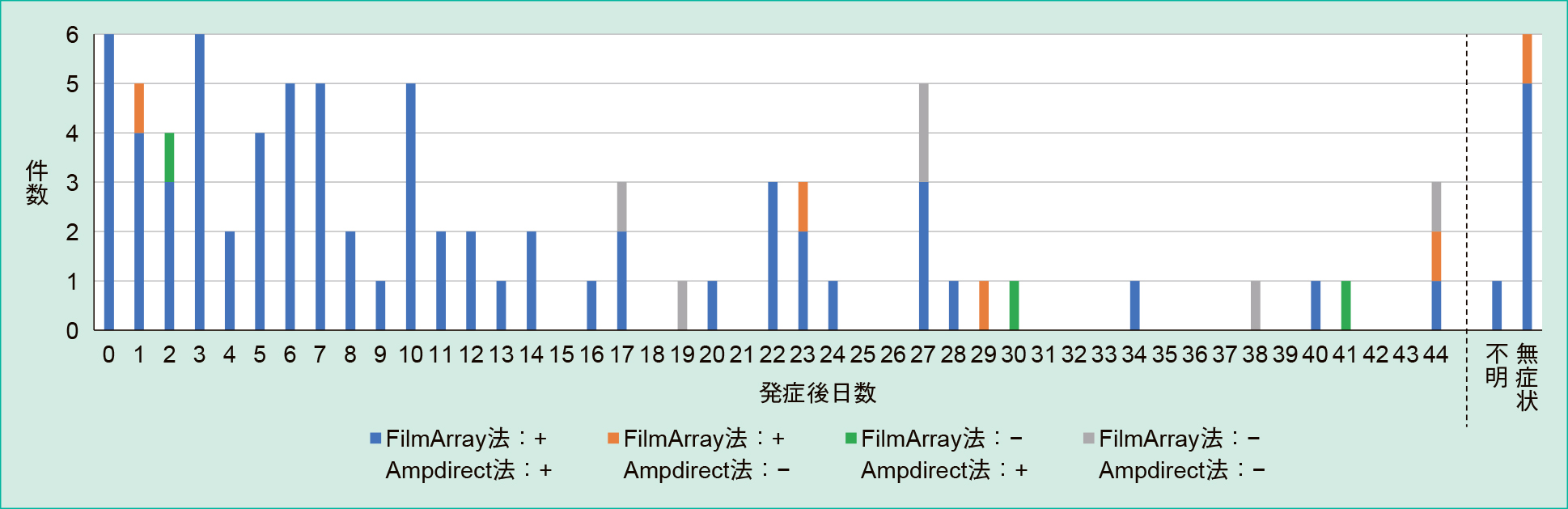
n = 87
当院と大阪府全体の陽性数の推移は同一傾向にあり,大阪府の陽性数の増減に合わせて当院の陽性数も推移していた(Figure 3)。
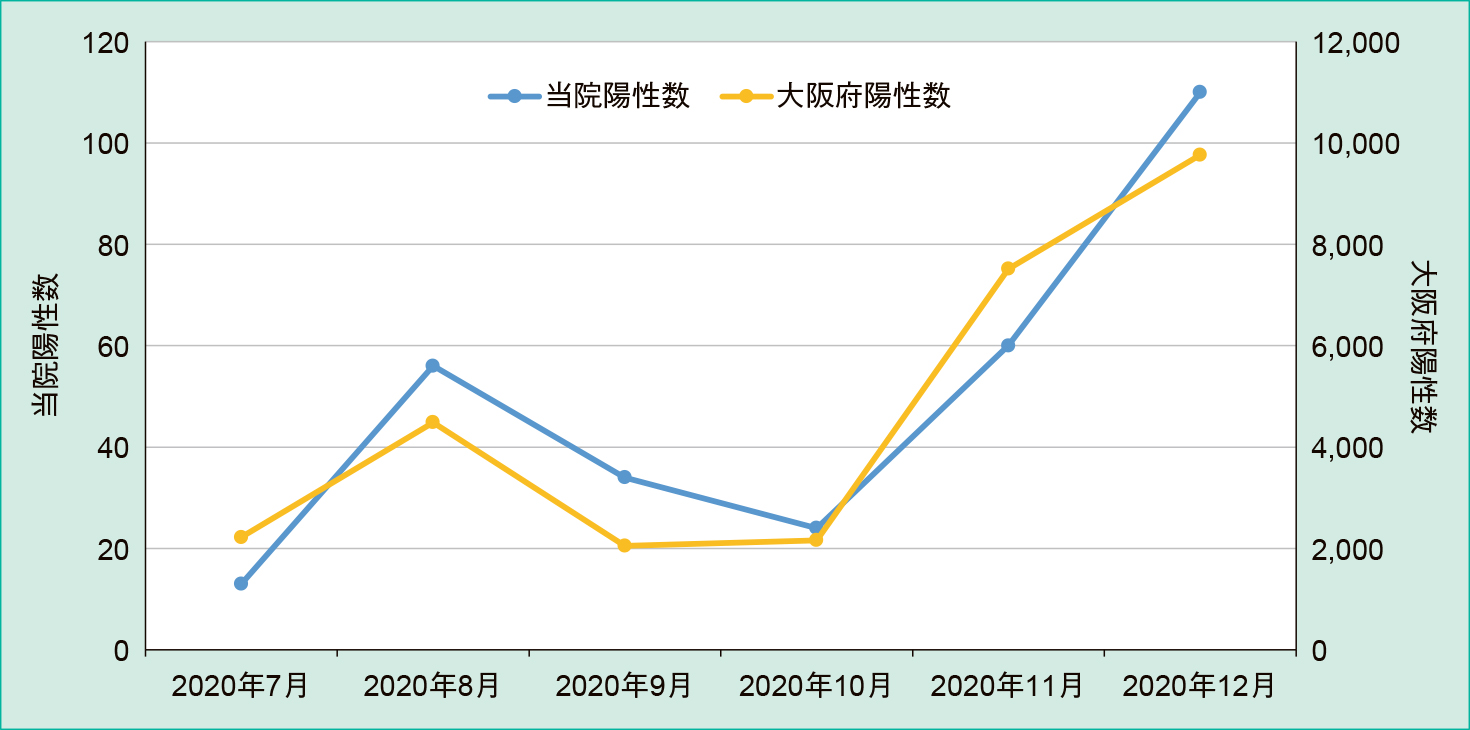
依頼総数1,783件(陽性274件,陽性率15.4%),定期検査1,419件(陽性165件,陽性率11.6%),緊急検査364件(陽性109件,陽性率29.9%)であった(Table 1)。月別の陽性率は流行に応じて上昇していた。定期検査と緊急検査の陽性率について,定期検査は11.6%,緊急検査は29.9%であった。
| 総数 | 定期検査 | 緊急検査 | ||||
|---|---|---|---|---|---|---|
| 件数 | 陽性(%) | 件数 | 陽性(%) | 件数 | 陽性(%) | |
| 2020年7月 | 195 | 13(6.7%) | 185 | 13(7.0%) | 10 | 0(0.0%) |
| 2020年8月 | 386 | 55(14.2%) | 350 | 46(13.1%) | 36 | 9(25.0%) |
| 2020年9月 | 304 | 31(10.2%) | 240 | 21(8.8%) | 64 | 10(15.6%) |
| 2020年10月 | 321 | 24(7.5%) | 256 | 8(3.1%) | 65 | 16(24.6%) |
| 2020年11月 | 286 | 57(19.9%) | 185 | 18(9.7%) | 101 | 39(38.6%) |
| 2020年12月 | 291 | 94(32.3%) | 203 | 59(29.1%) | 88 | 35(39.8%) |
| 総計 | 1,783 | 274(15.4%) | 1,419 | 165(11.6%) | 364 | 109(29.9%) |
n = 1,783
定期検査:Ampdirect法 緊急検査:GeneXpert法/FilmArray法
依頼総数6,633件(陽性23件,陽性率0.35%),定期検査6,208件(陽性8件,陽性率0.13%),緊急検査428件(陽性15件,陽性率3.5%)であった(Table 2)。定期検査で陽性となった8検体の内訳は,手術前スクリーニング1件,入院時スクリーニング4件,有症状3件であった。定期検査と緊急検査の陽性率について,定期検査は0.13%,緊急検査は3.50%であった。
| 総数 | 定期検査 | 緊急検査 | ||||
|---|---|---|---|---|---|---|
| 件数 | 陽性(%) | 件数 | 陽性(%) | 件数 | 陽性(%) | |
| 2020年7月 | 1,035 | 0(0.00%) | 1,034 | 0(0.00%) | 1 | 0(0.00%) |
| 2020年8月 | 1,047 | 1(0.10%) | 1,036 | 1(0.10%) | 11 | 0(0.00%) |
| 2020年9月 | 1,128 | 3(0.27%) | 1,071 | 1(0.09%) | 57 | 2(3.51%) |
| 2020年10月 | 1,252 | 0(0.00%) | 1,170 | 0(0.00%) | 82 | 0(0.00%) |
| 2020年11月 | 1,175 | 3(0.26%) | 1,056 | 1(0.09%) | 119 | 2(1.68%) |
| 2020年12月 | 996 | 16(1.61%) | 841 | 5(0.59%) | 158 | 11(6.96%) |
| 総計 | 6,633 | 23(0.35%) | 6,208 | 8(0.13%) | 428 | 15(3.50%) |
n = 6,633
定期検査:Ampdirect法 緊急検査:GeneXpert法/FilmArray法
なお緊急検査実施件数(792件)が検査法比較対象件数(654件)と異なるが,これは試薬の供給状況や業務上の都合によりGeneXpert法およびFilmArray法で測定した検体すべてをAmpdirect法と比較した訳ではないためである。
検査法を比較した結果,3法とも発症10日以内の検出率は90%以上となった。Ampdirect法とGeneXpert法およびFilmArray法で結果が乖離した検体は,発症2日以内または23日以上であった。また,結果が乖離した検体のThreshold Cycle(Ct値)はすべて35以上であった。測定法が異なるためCt値のみでウイルス量を比較することはできないが,Ct値が高いほどウイルス量が少ないという報告があり11),乖離した検体はウイルス量が少ないと考えられた。SARS-CoV-2模擬ウイルスの希釈溶液(7種:43,000,17,000,4,300,1,700,430,170,0コピー/mL)を用いたRNA検出率の比較結果によると,430コピー/mL・170コピー/mLにおける検出率はGeneXpert法とFilmArray法ではともに100%・100%,Ampdirect法では83%・33%となったことから,GeneXpert法とFilmArray法はAmpdirect法よりも検出感度が高いといえる12)。また,測定に用いる検体量がGeneXpert法とFilmArray法が300 μLであるのに対し,Ampdirect法は5 μLと少なく,手技による影響を受けやすい。従って,検出感度や手技の差,サンプリング時のウイルスの偏在が乖離の要因と考えられた。
発症11日以降の検出率について,Ampdirect法とGeneXpert法を比較した4検体では2法とも100%となったが,Ampdirect法とFilmArray法を比較した35検体ではAmpdirect法が74%,FilmArray法が77%であった。発症日数とウイルス量の関係について,患者上気道検体中のウイルス量は発症後時間経過に伴い低下するという報告がある13)。本検討においてAmpdirect法とGeneXpert法の比較では件数が少なく評価困難だが,Ampdirect法とFilmArray法の比較結果では発症11日以降の検出率は発症10日以内と比べて低下しており,発症日数の経過とともに検体中のウイルス量が低下していることが考えられた。しかし発症30日以上経過しても陽性となった例もみられた。発症8日以降に採取した検体からはウイルスが分離されなかったという報告があることから14),PCR検査陽性と感染性は必ずしも一致しないことが示唆された。
検査実績を評価した結果,緊急検査の陽性率はCOVID-19診療科,一般診療科ともに定期検査よりも高値となる傾向であった。これは,COVID-19が疑われる場合は,定期検査ではなく緊急検査依頼になるためと考えられた。緊急検査による迅速な結果判明は,入院や転院の判断,感染拡大の防止の一助となっている。
COVID-19診療科依頼における月別の陽性率は流行に応じて上昇しているが,12月の定期検査で陽性率が急増したのは,感染者の増加に加え,12月に開設した重症患者専用病棟である大阪コロナ重症センター入院患者の検査を行っていたためである。一般診療科依頼における定期検査において,手術前および入院時スクリーニングで陽性となったのは6,208件中5件(0.08%)と数字としては少ないが,陽性患者への曝露リスクを考えると1件でも検出できたことに意義があったと考えられた。
各検査法の特徴を活かし,処理能力の高いAmpdirect法を定期検査に,操作が簡便なGeneXpert法とFilmArray法を緊急検査として用いることで,検査対象の拡大および再流行に伴う検査依頼の急増への対応が可能となった。
COVID-19流行下における検査体制について,複数のSARSコロナウイルス核酸キットをそれぞれの特徴を活かして運用することは大変有用であると考えられた。
本論文に関連し,開示すべきCOI 状態にある企業等はありません。