2013 年 46 巻 9 号 p. 647-653
2013 年 46 巻 9 号 p. 647-653
症例は64歳の女性で,つかえ感を主訴に来院された.内視鏡検査では胸部中部食道に亜有茎性の1型の腫瘍を認め,生体組織検査では癌肉腫および神経内分泌癌の所見が得られた.CTでは胸部中部食道に32 mm大の腫瘍を認め,噴門周囲にリンパ節の腫大を認めた.右開胸開腹胸部食道切除,胸骨後経路胃管再建術を施行した.切除標本では中部食道に40×30 mmの1型病変を認めた.病理組織学的検査所見ではその9割を占める腫瘍はsynaptophysinおよびchromogranin A陽性で神経内分泌癌で,胞巣間の間質には腫大し異型な核を有する紡錘形の腫瘍細胞が錯綜し浸潤増殖していた(癌肉腫成分).また,腫瘍内部には腺様成分の混在を認め,さらに腫瘍の基部には表在性に進展する扁平上皮癌を認めた.以上より,癌肉腫,扁平上皮癌,腺様成分を伴った食道神経内分泌癌は非常にまれであり,文献的考察を含め報告する.
食道における神経内分泌癌は非常にまれな腫瘍で,日本食道学会のComprehensive Registry of Esophageal Cancer in Japan, 2003によれば神経内分泌癌の頻度は食道癌の0.6%とされる1).一方,癌肉腫も非常にまれな食道腫瘍で,食道癌の0.2%とされる1).今回,癌肉腫,扁平上皮癌および腺様成分を伴った食道神経内分泌癌を経験したので,それぞれの腫瘍成分の形質発現を含めて報告する.
現病歴:症例は64歳の女性で,食事のつかえ感のため近医を受診した.上部消化管内視鏡検査にて,中部食道に3 cm大の1型病変を指摘された.生体組織診断で神経内分泌癌あるいは癌肉腫と診断され,当科に紹介となった.
既往歴・生活歴:特記すべき事項なし.
現症:胸部および腹部に異常所見を認めず,体表リンパ節を触知しなかった.
入院時検査所見:貧血はなく,生化学検査にも異常を認めなかった.腫瘍マーカーはSCC 1.4 ng/ml,CA19-9 23.0 ng/ml,p53Ab <0.40と正常であったが,CEA 4.7 ng/ml(正常範囲0~3.5 ng/ml),NSE 11 ng/ml(正常範囲0~10.0 ng/ml)とProGRP 102.05 pg/ml(正常範囲0~70.0 pg/ml)は高値であった.
上部消化管造影検査:胸部中部食道(Mt)左壁に,45 mm大の比較的明瞭な境界を有する1型病変を認めた.
上部消化管内視鏡検査:切歯より28~32 cmの中部食道に1型病変を認め,周辺にわずかな随伴IIb病変を認めた(Fig. 1).ヨード染色では隆起性病変は染色されなかった.超音波内視鏡検査では食道壁第3層の断裂を認め,深達度T1bと判断された.生体組織診断でのHE染色および免疫組織染色検査にて神経内分泌癌および癌肉腫と診断された.
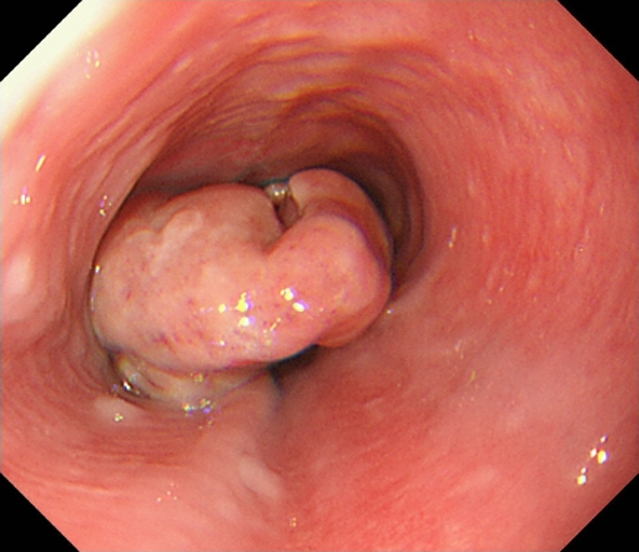
Esophagogastroscopy. Endoscopy shows an elevated tumor surrounded with intraepithelial spread in the middle esophagus.
胸腹部CT所見:胸部造影CTでは,胸部中部食道の腫瘍および内腔の狭窄を認め(Fig. 2A),また噴門周囲No. 2リンパ節の腫大を認めた(Fig. 2B).肺転移や肝転移は認めなかった.

A: CT. An esophageal tumor located in the middle thoracic esophagus is observed. B: CT. CT scan shows swollen lymph nodes around the gastric cardia.
FDG-PET所見:食道原発巣と腫大したNo. 2リンパ節にFDGの集積を認め,食道原発巣のstandardized uptake value maxは7.9であった.
以上より,食道癌肉腫あるいは神経内分泌癌の診断にて手術を行った.神経内分泌癌の可能性が存在しため術前化学療法あるいは化学放射線療法の提示を行ったが希望されず,右開胸開腹食道切除,3領域リンパ節郭清,胸骨後経路胃管再建術を施行した.術後は肺炎や縫合不全を認めず,軽快退院した.また,術後化学療法を推奨したが希望されず,外来経過観察中で,術後1年無再発生存中である.
切除標本肉眼所見:中部食道に40×30 mmの1型の亜有茎性の隆起性病変を認めた(Fig. 3).腫瘍の表面は分葉状であった.
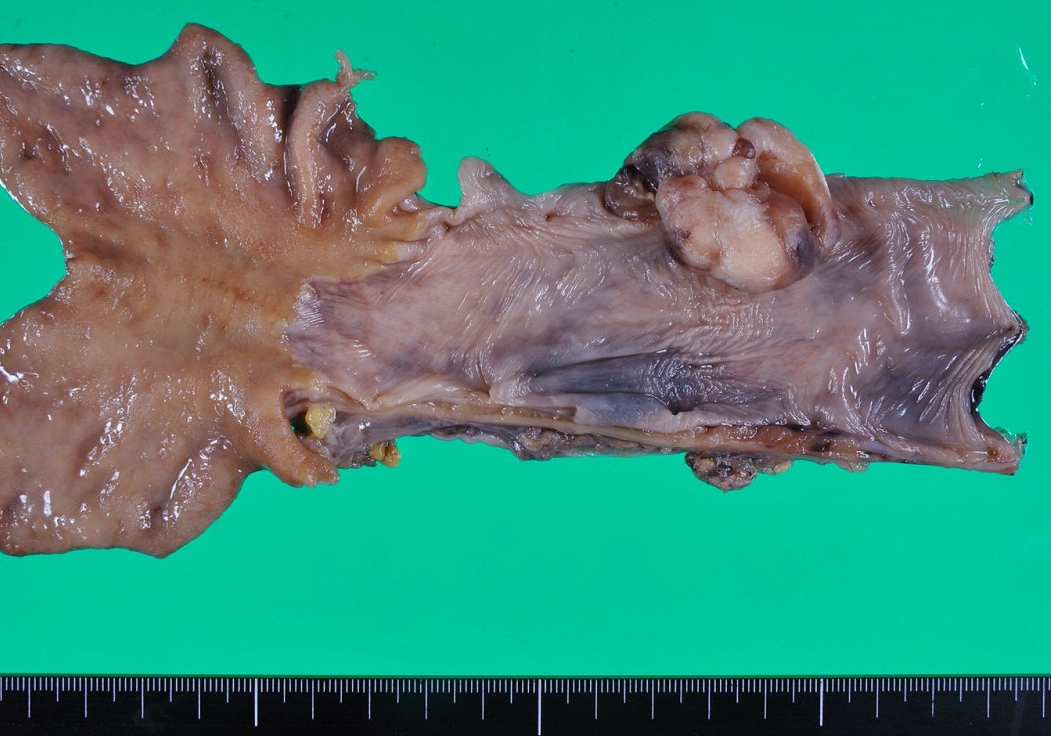
Macroscopic findings. The resected specimen shows an elevated tumor in the esophagus (40×30 mm), and the tumor shows a lobulated surface.
病理組織学的検査所見:腫瘍標本のHE染色をFig. 4Aに示す.腫瘍の大部分は細胞質に乏しく,クロマチンに富んだ腫大した核を有する比較的大型の腫瘍細胞が充実性胞巣を形成し,浸潤増殖を認めた.これらの腫瘍細胞は,免疫染色検査ではsynaptophysin陽性およびchromogranin A陽性で,神経内分泌癌(大細胞型)と診断された(Fig. 4B).一部に腺癌様のfocal ductal differentiationが認められ,産生された管腔内の粘液はMUC5Bで陽性であった(Fig. 4C).また,胞巣間には腫大したbizarreな核を有する紡錘形の腫瘍細胞が錯綜して浸潤増殖していた(Fig. 4D).これらの腫瘍細胞はCK AE1/AE3,synaptophisinおよびchromogranin Aはいずれも陰性で,vimentin陽性であった.さらに,腫瘍の辺縁部には扁平上皮癌の存在が認められた(Fig. 4E).免疫染色検査の結果をTable 1に示す.腫瘍組織の存在割合としては神経内分泌癌9割,癌肉腫成分1割,腺癌成分と扁平上皮癌成分はわずかと判断された.リンパ節転移の成分は神経内分泌癌であった.以上より,neuroendocrine carcinoma(large cell type)with sarcomatous,squamous and glandular components と診断された.Mt,4 cm,1型,pT1b,pN3,ly1,v3,pIM0,pPM0,pDM0,pRM0,多発癌なし,sM0:fStage III(食道癌取扱い規約第10版).

Histopathological findings. A: Histologic section of the tumor (H.E.). The histological findings show four types of tumor components. B: Neuroendocrine component (chromogranin A). Immunostain shows positive reaction of the tumor cells for chromogranin A. C: Glandular component (MUC5B). MUC5B stain shows mucus with positive reaction in glandular formation. D: Sarcomatous component (left: H.E. right: CK AE1/AE3). Spindle tumor cells infiltrate in the stroma of the tumor nest and CK AE1/AE3 stain shows negative reaction of spindle tumor cell whichconsisted of carcinosarcoma. E: Squamous component (H.E.). Squamous cell carcinoma is shown.
| Antigens | Neuroendocrine component | Sarcomatous component | Squamous component | Glandular component |
|---|---|---|---|---|
| Synaptophisin | + | – | – | – |
| Chromogranin A | + | – | – | – |
| vimentin | – | + | – | – |
| CK 5/6 | focal + | – | + | + |
| CK 34βE12 | – | – | + | + |
| CK AE1/AE3 | + | – | + | + |
| MUC5B | – | – | – | + |
| P63 | focal + | – | + | – |
本例の神経内分泌癌(大細胞型)には,癌肉腫,扁平上皮癌そして腺様成分が認められたが,これは極めてまれであり,PubMedで1950年から2012年までの間で「carcinosarcoma」,「neuroendocrine」,「squamous」,「glandular」をキーワードに文献検索したところRobertsonら2)およびKanamotoら3)の2例の報告のみであった.食道神経内分泌癌(小細胞型)における併存病変は,以前より詳細な検討が行われ,その多くに扁平上皮癌の合併が認められている4)5).一方,胃などの腺組織の臓器では神経内分泌癌に腺癌が合併するMANECが認められているが6)7),食道の神経内分泌癌に腺癌あるいは腺様成分が併存することはまれである.しかし,Maruら8)の報告によれば食道神経内分泌癌40例中15例(37.5%)に腺様成分の合併を認め,扁平上皮癌成分の合併は1例(2.5%)のみに認められたとしている.また,癌肉腫の成分が合併した食道内分泌癌は,従来の食道小細胞癌の報告をみても,非常にまれである.癌肉腫の定義は,同一腫瘍内に癌成分と肉腫成分が存在する腫瘍とされている.食道における癌肉腫に併存する腫瘍成分としては扁平上皮癌が一般的である9).2010年WHO分類10)では食道の癌肉腫はspindle cell(squamous)carcinomaとして扁平上皮癌の亜型として扱われている.また,Matsumotoら11)は扁平上皮癌成分と肉腫成分の遺伝子検索において対立遺伝子の欠失が共通であり,二つの成分は単一腫瘍から分化した可能性が高いと述べている.本例では神経内分泌癌(大細胞型)に癌肉腫,扁平上皮癌と腺様成分の混在が認められた.河本ら12)は,神経内分泌癌(小細胞型)に癌肉腫成分の併存した症例を報告している.神経内分泌癌に癌肉腫,扁平上皮癌と腺様成分を伴っていた症例はRobertsonら2)(神経内分泌癌の小細胞型)およびKanamotoら3)(神経内分泌癌のサブタイプ記載なし)によって報告されている.本例を含めこれらの4例においては,癌肉腫の併存の割合に差が認められ,非常にまれではあるが神経内分泌癌においてさまざまな分化を来した病変が存在しうるものと考えられた(Table 2)2)3)12).
| Cases | Author/ Ref. No |
Year | Age/Sex | Clinicopathologic features | Histologic components | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Location | Type | Size (mm) | Depth of invasion | Node metastasis | Distant metastasis | NEC | CS | SCC | AC | |||||
| 1 | Robertson2) | 1997 | 64M | upper | 0-I | 20 | submucosa | (–) | (–) | (+) | (+) | (+) | (+) | |
| 2 | Kanamoto3) | 2000 | 55M | lower | 0-I | 15 | submucosa | (–) | (–) | 60% | 25% | 10% | 5% | |
| 3 | Kawamoto12) | 2005 | 54M | middle | 2 | 25 | adventitia | (+) | (–) | (++) | (+) | (–) | (–) | |
| 4 | Our case | 64F | middle | 1 | 40 | submucosa | (+) | (–) | 90% | 10% | (+) | (+) | ||
NEC, neuroendocrine carcinoma; CS, carcinosarcoma; SCC, squamous cell carcinoma; AC, adenocarcinoma
本例では各組織型成分における免疫染色検査による形質発現を検討した.その結果,synaptophisinやchromogranin Aが陽性の神経内分泌癌は,扁平上皮癌成分と同じく扁平上皮に発現する上皮系マーカー(CK 5/6とCK AE1/AE3)およびP63が陽性となった.すなわち本例の神経内分泌癌は神経内分泌細胞への形質分化と扁平上皮への形質分化を併せ持っていると考えられた.食道腺の粘液を示すMUC5Bが陽性となった腺様成分も扁平上皮癌成分と同じ上皮系マーカーが陽性となり,扁平上皮癌由来の可能性を指摘することができる.一方で,肉腫様腫瘍細胞は神経内分泌癌の間質部に浸潤しており,これらの紡錘形細胞は上皮系マーカーと神経内分泌系マーカーは陰性で,間葉系マーカーのvimentinのみ陽性であった.さらに,肉腫様腫瘍細胞と神経内分泌癌細胞あるいは扁平上皮癌細胞との間に明らかな移行像は認められなかった.食道癌肉腫における扁平上皮癌と肉腫成分は腫瘍組織としては分別されて存在し,両者の間に移行像が示されることが多い9).扁平上皮癌の浸潤に伴って扁平上皮癌細胞が紡錘形化したものを鑑別しなければならないが,この場合の紡錘形腫瘍細胞は上皮系マーカーが陽性となり,間葉系マーカーは陰性となり,癌肉腫とは鑑別すべきとされている13).したがって,本例では肉腫成分は癌肉腫と捉えることが可能である.しかし,神経内分泌癌と腺様成分が扁平上皮癌由来と考えられるが,神経内分泌癌の間質に肉腫様細胞が認められたため,同じく扁平上皮癌由来なのか,それとも神経内分泌癌由来とすべきなのか,明らかにすることは困難である.
本例の肉眼型は亜有茎性の隆起型病変を呈し,腫瘍の基部には扁平上皮癌の上皮内進展がみられた.この肉眼所見は癌肉腫に特徴的な所見であると考えられている13)14).神経内分泌癌の肉眼型においても隆起型が主体であるが,進行するとともに潰瘍型となり,病変辺縁に上皮の被覆が認められて粘膜下腫瘍様の上皮下発育を示すとされている5).本例では内視鏡所見より癌肉腫を疑ったが,生体組織診断では癌肉腫あるいは神経内分泌癌の両者が疑われた.
食道神経内分泌癌の臨床的な特徴は小細胞型(小細胞癌)において検討され,リンパ節や遠隔臓器に転移を来しやすく,その治療成績は不良である15)16).食道内分泌細胞癌(小細胞型)は腫瘍細胞の増殖能が高く,血管新生が亢進していることが転移を起こしやすく,一方で化学療法により腫瘍細胞の細胞死が見られやすく化学療法の効果が期待できる腫瘍である17).小細胞癌を含む食道内分泌癌に対する標準的な治療は現在のところ定まっていないが,多くの症例において本疾患の治療は化学療法を含めた集学的な治療が必要とされている18)~20).本邦における食道神経内分泌癌(小細胞型)の長期生存例には手術と化学療法を用いて集学的治療を行った症例が多いとされる20).本例では,術後の病理組織学的検査所見では病変の主体が神経内分泌癌であり,さらにリンパ節転移が神経内分泌癌の転移であったため,術後補助療法として化学療法の追加を提示したが,患者の希望により施行できていない.一方,食道神経内分泌癌に対する手術治療はいまだcontroversialで,外科的切除は転移を伴わない症例に対して適応するのが良いとする報告がある21).各施設における食道神経内分泌癌の症例数が多くないため,全国規模の多施設共同研究などによる食道神経内分泌癌に対する臨床病理学的および分子生物学的な検討と標準的治療の策定が期待される.
利益相反:なし