2013 年 46 巻 9 号 p. 669-677
2013 年 46 巻 9 号 p. 669-677
Multiple endocrine neoplasia type 1(MEN-1型)の診断をうけた66歳の男性で,高ガストリン血症と腹部CTで膵体部に約20 mm大の腫瘍を認めた.血管造影では膵体部腫瘍は上腸間膜動脈より濃染されたが,selective arterial calcium injection test(以下,SACI検査と略記)では胃十二指腸動脈が陽性で,上腸間膜動脈からの刺激では陰性だった.よってガストリン産生腫瘍が存在する領域は画像検査で異常を認めなかった十二指腸もしくは膵頭部と診断し,膵体部腫瘍も含めた亜全胃温存膵頭十二指腸切除術(subtotal stomach-preserving pancreatoduodenectomy;SSPPD)を施行した.切除検体で十二指腸および膵体部にガストリノーマを認めた.膵体部腫瘍を高ガストリン血症の責任病変と断定せずにSACI検査結果を重視し,腫瘍性病変を認めなかった胃十二指腸動脈領域の臓器切除を行ったことで根治的治療に至った.術後10か月が経過したが,ガストリノーマの再発を認めていない.
膵臓や消化管に発生する神経内分泌腫瘍(neuroendocrine tumor;以下,NETと略記)の中でもmultiple endocrine neoplasia type 1(以下,MEN-1型と略記)に伴うガストリノーマは多臓器に発生することが多く,生物学的悪性度が高いと認識されているが,正しい局在診断の下に行われる外科的切除術であれば十分に治療可能と考えられている1).現在,その局在診断には選択的動脈内カルシウム注入試験(selective arterial calcium injection test;以下,SACI検査と略記)が最も有用な方法とされている1)2).今回,我々はMEN-1型に伴う患者にガストリノーマの存在を疑い,画像所見で膵体部腫瘍を認めながらもこの試験を施行した.その結果,膵体部腫瘍以外に病変の存在を確認し,ガストリノーマに対する根治的切除術が可能であった1例を経験したので文献的考察を含めて報告する.
患者:66歳,男性
既往歴:30歳代より現在まで十二指腸潰瘍で内服治療を継続し,40歳代に副甲状腺機能亢進症に対して切除術を受けていたが,詳細は不明であった.63歳時に遺伝子検査でMEN-1型と診断されていた.
家族歴:長男がインスリノーマで手術していた.
現病歴:3年前に他院で長男がインスリノーマの診断・治療を受けた際に,MEN-1型と判明し,下垂体腫瘍と膵体部腫瘍を認めたが経過観察となっていた.その後上部消化管内視鏡検査を施行したところ,胃体上部に約15 mm大の腫瘍を認め内視鏡的胃粘膜剥離術が施行された.病理組織学的診断で胃NETと診断され経過観察となったが,6か月後の上部消化管内視鏡検査で胃体上部の大彎に初回治療時と同様な腫瘍を認めたため精査・加療目的に外科紹介となった.
来院時現症:身長161 cm,体重74 kg,体温35.9℃,血圧117/64 mmHg,脈拍60回/min,身体所見に特記すべき異常は認めず.
血液生化学検査所見:一般血液生化学検査では異常は認めなかったが,血清ガストリン値が540 pg/ml(プロトンポンプインヒビター内服中)と上昇していた.抗胃壁細胞抗体は陰性だった.その他にプロラクチンが46.2 ng/mlと軽度上昇を認めた.
上部消化管内視鏡所見:胃体上部の大彎に初回の内視鏡治療による瘢痕を認め,その約4 cm離れた後壁寄りに最大径が約10 mmの腫瘍を認めた(Fig. 1a).十二指腸球部にも潰瘍瘢痕を認めたが変形はなかった.また,十二指腸を水平脚まで可能なかぎり十分に観察したが明らかな腫瘍は同定できなかった.
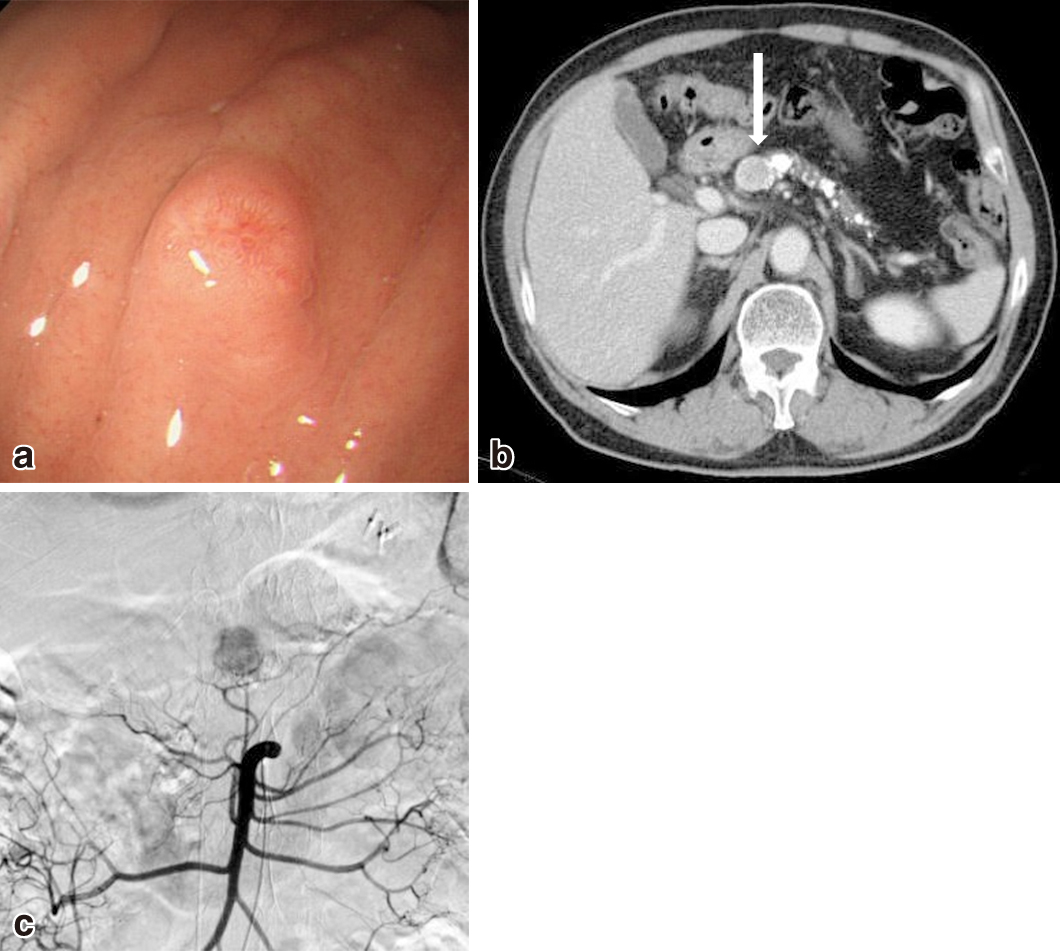
Preoperative findings. a) Gastrointestinal endoscopic examination reveals a small elevated lesion on the greater curvature of the upper gastric body. b) Upper abdominal enhanced CT shows a hypervascular tumor at the pancreatic head near the portal vein. c) The pancreatic tumor’s feeder was the dorsal pancreatic artery originating from the superior mesenteric artery.
腹部造影CT所見:門脈左側寄りの膵体部に造影効果の強い約20 mm大の充実性腫瘍を認めた(Fig. 1b).有意なリンパ節の腫大は認めなかった.
SACI検査所見:まず腹部血管造影を行い,膵体部腫瘍の栄養血管が上腸間膜動脈から分岐する後膵動脈であることを確認した(Fig. 1c).次に肝静脈にカテーテルを留置し,脾動脈,上腸間膜動脈,胃十二指腸動脈,固有肝動脈のそれぞれにグルコン酸カルシウム2 mlを急速注入した.肝静脈からの血液採取は20秒後,40秒後,60秒後,90秒後,120秒後に行った.60秒後の値を判断材料とし,診断基準を満たす血清ガストリン値の上昇を示した動脈は胃十二指腸動脈のみで,膵体部腫瘍が造影される上腸間膜動脈からの注入では有意な上昇を示さなかった(Fig. 2).なお,各動脈へのグルコン酸カルシウム投与間隔は10分とした.
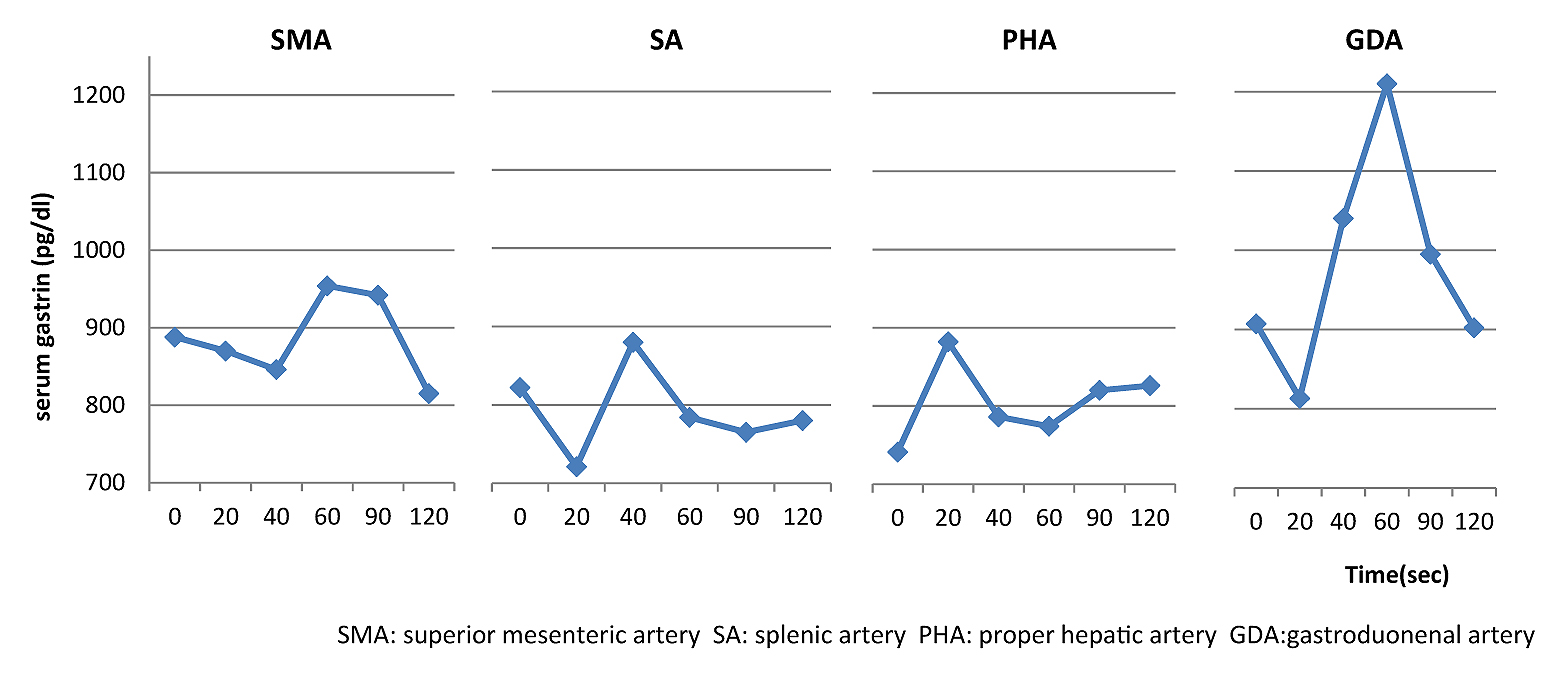
Results of the selective arterial calcium injection test. The responses indicate that the serum gastrin level was elevated in only the gastroduodenal artery.
以上より,画像所見では十二指腸や膵頭部に肉眼的に確認可能な腫瘍性病変はないが,SACI検査で胃十二指腸動脈領域にガストリノーマの存在が示唆され,そして膵体部腫瘍はSACI検査におけるガストリノーマの診断基準を満たさないことから非機能性腫瘍と診断した.術式は膵体部腫瘍を含めた亜全胃温存膵頭十二指腸切除術(subtotal stomach-preserving pancreatoduodenectomy;以下,SSPPDと略記)を施行した.また,10 mm大の胃腫瘍は術前に内視鏡的胃粘膜剥離術にて切除した.
手術所見:腹腔内に転移や播種を疑う所見は認めなかった.膵体部腫瘍は門脈の左側に位置していたため,膵臓の離断は腫瘍左縁より約1 cmの距離を取り膵体部で行った.リンパ節郭清は膵頭部の癌取扱い規約に準じたD2郭清を行い膵体部腫瘍に対する郭清として脾動脈幹近位の郭清を追加した.
病理組織学的検査所見:膵体部腫瘍は最大径22 mmで,割面は均一な充実性腫瘍(Fig. 3a)であった.さらに,十二指腸下行脚に小さな腫瘍性病変を3か所認め,最も大きいもので最大径4 mmだった(Fig. 3b).膵体部腫瘍および十二指腸のいずれの腫瘍も類円形の細胞が島状の胞巣を形成して増生し(Fig. 4a),シナプトフィジン陽性,クロモグラニンA陽性,ガストリン陽性,インスリン陰性で全ての腫瘍をガストリノーマと診断した.ガストリンの染色強度は中等度であった(Fig. 4b).また,十二指腸および膵臓のガストリノーマのいずれもKi-67 labeling index は2%以下でありG1相当のNETと診断した(Fig. 4c).リンパ節は13aと17aに転移を認めKi-67 labeling index は原発巣と同様の2%以下であった(Fig. 4d).European Neuroendocrine Tumor Society(ENETS)のTNM分類では,十二指腸ガストリノーマはT1N1M0のstage IIIb,膵ガストリノーマはT2N0M0のstage IIaと診断した.術前に切除した胃腫瘍は最大径10 mmの胃NETであった.
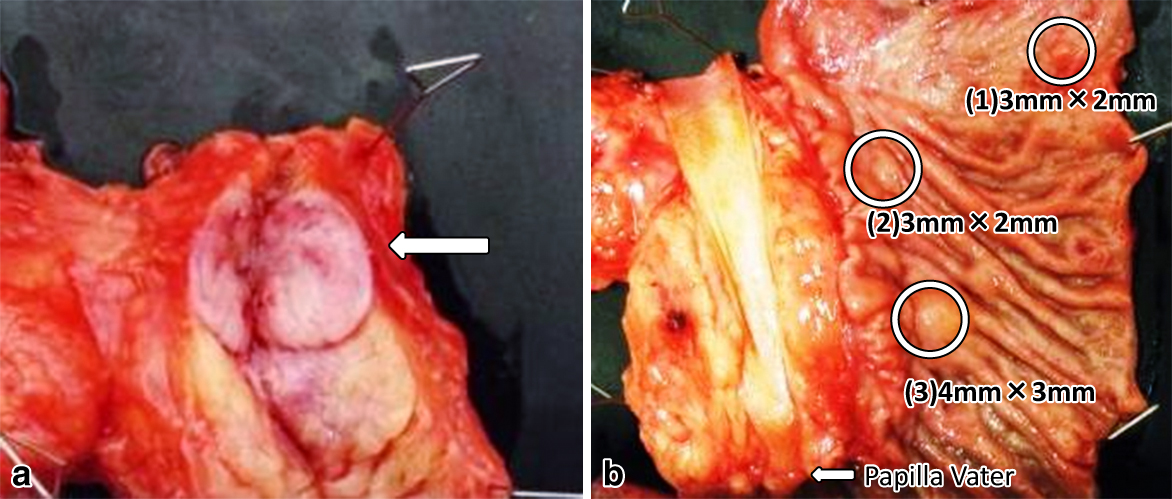
Macroscopic findings of the pancreas and duodenum. a) Macroscopic findings of the pancreatic tumor. b) Macroscopic findings of the duodenal multiple tumors.

Histopathological findings of the tumor. a) Duodenal gastrinoma: HE staining (×10). b) Pancreatic gastrinoma: Gastrin staining (×20). c) Duodenal gastrinoma: MIB-1 staining (×20). d) Metastatic lymphnode (No. 13a): MIB-1 staining (×20).
術後経過:食事開始後の3日目より食後の腹痛を認めたため上部消化管内視鏡検査を施行したところ,胃空腸吻合部に多発する吻合部潰瘍を認めた.休止していたプロトンポンプインヒビターを再開すると自覚症状は消失し吻合部潰瘍は改善を認めた.その後特に合併症なく術後20日で退院となった.術後2か月目の血液検査にてガストリン値は154 pg/mlまで低下し,現在までに胃NETおよびガストリノーマの再発は認めていない.
NETの多くは非遺伝性に発症するが,一部は遺伝性疾患の部分症として発症し,そのうち高頻度でNETを伴うものとしてMEN-1型が知られている.そしてそれらに発生する膵・十二指腸NETのうち約40%はガストリノーマで最も多く,ほぼ全症例で十二指腸粘膜下に散在してみられる臨床的特徴があるため3),この部位が外科的治療の主体を占めている.本症例は初回の胃腫瘍の内視鏡治療時にMEN-1型を念頭においた検査や治療をすべきであったが,長期にわたりプロトンポンプインヒビターを内服していたため二次的な血中ガストリンの上昇と判断していたこと,さらに内視鏡的に十二指腸に腫瘍性病変は認めなかったことが診断を遅らせた要因と考えられた.手術の直前に採取したガストリン値は1,100 pg/dlであり,変動が大きいと考えられるため 初回診療時から経時的に検査すべきであった.
本症例のように腫瘍巣が2臓器以上にわたって認める例はMEN-1型の病態には珍しくなく,MEN-1型のガストリノーマ患者の約13%に膵ガストリノーマが併存しているとの報告がある4).本症例では,異時性に認めた胃腫瘍の存在からRindi分類5)でのII型が疑われ,高ガストリン血症の存在と腹部CTで膵体部腫瘍を認めた.しかし,MEN-1型患者に高頻度で合併する十二指腸ガストリノーマを内視鏡検査では認めなかったことから,膵体部腫瘍が高ガストリン血症と関連性があるのかを判断する必要があった.したがって,我々は腫瘍の局在診断で用いられるSACI検査を行った.これは製造中止となったセクレチンに変わるカルシウムを注入することによって腫瘍の局在とその質的診断を行う方法である.その結果,膵体部腫瘍の栄養血管は上腸間膜動脈からの分枝である後膵動脈と判明し,同血管からのカルシウム注入試験ではガストリノーマの診断基準を満たさなかった.手技的には推奨された方法を用いて行ったため,膵ガストリノーマの質的診断に至らなかった原因は不明だが,カルシウム刺激はセクレチン刺激に比較すると感度が低い6)との報告がある一方で,その感度自体は80%と報告されている7).セクレチンを使用していれば,膵ガストリノーマを診断しえた可能性はあるが,SACI検査を行ったことで他の画像検査では同定できなかった十二指腸ガストリノーマの存在を確定することができた.
手術は腫瘍が肉眼的に確認できていなかったために全十二指腸を含めた胃十二指腸動脈領域の臓器を全て切除する必要があった.また,膵体部腫瘍は門脈の左側にあるため,膵実質離断を体部で行うことで十分に切除可能であると判断し,SSPPDとそれに膵体部腫瘍を含める形での切除を行った.MEN-1型に伴う膵腫瘍に関しては,非機能性腫瘍でも46.1%が悪性との報告がある一方で8),その術式には核出術も有用との意見もあるためいまだ議論の余地を残している9)10).また,非機能性腫瘍であれば血行性転移が主体といわれ,リンパ節郭清の意義に一定の見解はないが10),本症例では膵体部腫瘍の局在を考慮して脾動脈近位リンパ節の郭清も追加して行った.
医学中央雑誌にて選択的動脈内刺激薬注入試験の報告がなされるようになった1983年~2012年の間を対象とし,「膵臓」,「十二指腸」,「ガストリノーマ」,「MEN-1」のキーワードを用いて検索したところ21例の報告を認め,それらに自験例を加えた計22例の臨床的特徴について検討した(Table 1)11)~31).年齢は30歳代から50歳代までが14例と全体の約2/3を占めた.いずれも潰瘍の既往があり有症状であったことが比較的若年で診断された一因になっていると考えられるが.それらのガストリン値は100~9,500 pg/dlと幅が非常に広いため,潰瘍形成とガストリン値に一定した関係を見出すことは困難であった.特に潰瘍治療の目的で制酸薬を継続投与されることでガストリン値は1,000 pg/dl前後にまで上昇することがあるため,高ガストリン血症を疑った場合は投薬を中止したうえで経時的に検査することが重要と考えられた.全症例のうち術前画像検査でガストリノーマを認めたものは15例(68%)であった.それらのうちMEN-1型の検索は9例,selective arterial secretagogue injection test(SASI)/SACI施行例は8例であった.ガストリノーマの約20%にMEN-1型が合併するとされ,画像所見以外にも多発の可能性を判断する方法の一つとして,MEN-1型の遺伝子検査は有用であると考える.SACI検査を施行しなかった7例においては,画像検査で認めた腫瘍が高ガストリン血症の責任病変だと判断していた可能性があると思われる.特に画像診断で単発と診断し治療した症例8に関してはガストリン高値が継続したままであり,腫瘍の残存が疑わしいことを著者自身も言及している.初回治療時にSACI検査は施行されていたものの,MEN-1型の遺伝子検索や,SACI再検査をすることが追加治療には重要と考えられた.
| Author/Year | Age/Sex | SACI/SASI (※) | Pre-operative gastrin (pg/dl) | Tumor site (by imaging) |
Ulcer location | Surgical treatment | Gastirinoma | The number of tumor | Post-operative gastrin (pg/dl) | MEN | Follow-up (months) | Recurrence | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | Imamura/198611) | 54/M | GDA (※) | 100~250 | None | Jejunum | PD | Duodenum/P. head | multiple | 30~40 | Unknown | Unknown | N |
| 2 | Shibata/199112) | 35/F | GDA (※) | 1,550 | P. head | Duodenum | PD | P. head | multiple | 17 | Unknown | 5 | N |
| 3 | Ueda/199313) | 37/M | GDA·SMA (※) | 602 | None | Duodenum/jejunum | Enucleation | Duodenum | 1 | 32 | Unknown | 34 | N |
| 4 | Imamura/199514) | 53/F | None | 492~1,060 | P. tail | Duodenum | DP | P. tail | 1 | 44 | Unknown | 6 | N |
| 5 | Oota/199615) | 50/F | GDA (※) | 420~1,224 | None | Duodenum/jejunum | PD | Duodenum | 2 | 39 | Unknown | 36 | N |
| 6 | Takasu/199816) | 60/M | CHA (※) | 9,500 | None | Duodenum | Distal Gastrectomy | Duodenal bulb | 1 | 6,400 | Unknown | 12 | N |
| 7 | Uesugi/200217) | 42/M | None | 3,000 | None | Duodenum | PD | Duodenum/P. head (Non-functioning) | multiple | 26 | Unknown | 33 | N |
| 8 | Yamane/200418) | 72/F | GDA (※) | 1,770 | Duodenal bulb | None | Enucleation | Duodenal bulb | 1 | 2,600~3,000 | Unknown | Unknown | Unknown |
| 9 | Zenda/200519) | 51/M | GDA | 937 | None | None | PD | Duodenal bulb | 1 | 62 | Unknown | 12 | N |
| 10 | Takahashi/200520) | 46/M | GDA (※) | 6,514 | None | Duodenum/jejunum | PD | Duodenum/P. head | multiple | 24 | Y | 6 | N |
| 11 | Suzuki/200521) | 70/F | None | 749 | P. tail | None | DP | P. tail | 1 | 400? | Y | 8 | Unknown |
| 12 | Sakai/200622) | 58/F | None | 2,400 | Duodenum | Duodenum | Enucleation | P. head | 1 | 37 | N | Unknown | Unknown |
| 13 | Kamiyama/200723) | 74/F | CHA | 1,850 | Lesser omentum | Duodenum | Enucleation | Lesser omentum | 1 | 118 | Unknown | 24 | N |
| 14 | Inoue/200724) | 56/F | None | 1,850 | P. head | Duodenum | SSPPD | P. head/PALN | multiple | 174 | Unknown | 5 | Y |
| 15 | Meguri/200825) | 41/F | GDA | 6,500 | Gall bladder/P. tail | None | PPPD/DP | Duodenum/P. tail (Non-functioning) | multiple | normal range | Y | Unknown | N |
| 16 | Shinji/200826) | 55/F | None | 1,130 | Liver/P. tail | Duodenum | Left lateral hepatectomy | Liver/P. tail | 2 | 400 | Y | Unknown | Unknown |
| 17 | Kotake/200827) | 71/F | None | Unknown | P. head | None | PD | P. head | 1 | 39 | N | 12 | N |
| 18 | Itaba/200828) | 61/F | GDA | 1,031 | Duodenum | Duodenum | Enucleation | Lymph node | 1 | normal range | N | 4 | N |
| 19 | Tada/200829) | 63/F | None | 1,900 | P. head | Duodenum | PD | P. head | 1 | 120 | N | 8 | N |
| 20 | Kamo/200930) | 59/M | SMA | 5,650 | P. head | Gaster-duodenum | Enucleation | P. head | 1 | 115 | Unknown | Unknown | Unknown |
| 21 | Shoji/201131) | 50/M | GDA | 1,400 | Duodenum | Duodenum | Enucleation | Duodenum | 1 | 140 | Y | 36 | N |
| 22 | Our case | 66/M | GDA | 540~1,100 | P. body | Duodenum | SSPPD/P. body resection | Duodenum/P. body | multiple | 154 | Y | 4 | N |
GDA: gastroduonenal artery, SMA: superior mesenteric artery, CHA: common hepatic artery, P. head: pancreatic head, P. body: pancreatic body, P. tail: pancreatic tail, PALN: para-aortic lymph node, PD: pancreatoduodenectomy, DP: distal pancreatectomy, SSPPD: subtotal stomach preseving pancreatoduodenectomy, (※); SASI
本症例では腹部CTで膵体部に腫瘍を認めたが,MEN-1型のガストリノーマの多くは十二指腸に存在すること,多発する特徴を持つことからSACI検査を施行し,それが膵体部腫瘍切除のみではなく胃十二指腸動脈領域の臓器切除を施行する決定的根拠となった.したがって,ガストリノーマを疑う患者に対しては画像で腫瘍を認めてもその他に指摘できない病変の描出を目的としてのSACI検査は非常に有用であると考えられた.
利益相反:なし