2014 年 47 巻 4 号 p. 238-243
2014 年 47 巻 4 号 p. 238-243
今回,我々は5年間CT上経時的変化を確認した後に切除した上行結腸癌の同時性孤立性後腹膜転移の症例を経験した.症例は66歳の女性で,2006年11月上行結腸癌に対して右結腸切除術,D3リンパ節郭清術を施行した.病理組織学的診断は,中分化型腺癌,pSS,pN2,H0,P0,M0,f-stage IIIbであった.術後5年のCTで後腹膜の右後腎傍腔に結節を認めた.同病変は術前CTにおいても径4 mm大の小結節として描出されていた.経時的に観察すると,術後4年のCTと比較し径の増大を認めた.転移検索目的のFDG-PET CTで18F-FDGの集積の亢進を同部位に認め,他の部位には認めなかった.以上より,同時性孤立性後腹膜転移と診断し,初回手術より5年経過した2011年11月腫瘍摘出術を施行した.摘出した後腹膜腫瘍の病理組織学的診断は粘液腺癌であり,初回手術時と同様の病理組織像を呈し,上行結腸癌の転移と診断した.
大腸癌の転移好発部位は,リンパ節・肝臓・肺などであることが知られている1).後腹膜へ転移することはまれであり,その多くは,癌の進展に伴う多臓器転移の終末像としてであり,根治切除が可能となる同時性孤立性転移はまれである.今回,我々は大腸癌の同時性後腹膜転移を認め,5年経過した後に切除した症例を経験した.極めてまれな症例であると考えられるので報告する.
患者:66歳,女性
主訴:特になし.
既往歴:虫垂炎手術
家族歴:特記すべきことなし.
現病歴:上行結腸癌にて2006年11月右結腸切除術,D3リンパ節郭清術を施行した.病理組織学的所見は,中分化型腺癌,pSS,int,INFc,ly3,v1,pN2,H0,P0,M0,f-stage IIIbであった.
術後経過は良好で,術後補助化学療法としてユーエフティ®/ユーゼル®療法(ユーエフティ:300 mg/day/body day 1~28,ユーゼル:75 mg/day/body,day 1~28/5 weeks)を6か月間施行した.以後,外来で経過観察していた.
術後サーベイランスとして,年1回のCTを施行していた.2011年9月(術後約5年)のCTで,右後腹膜に径11 mm大の占居性病変を認めた.以前のCTを見直すと,初回手術前のCTで径4 mm大の同病変を既に認めていた.その当時,原発巣はCT上では後腹膜とは接してはおらず,同病変とはCT上で直線距離にして5 cm程度離れていた.経時的に,同病変をCT上観察することが可能であった.2010年11月(術後4年)と比較し,同病変は術後5年目で径の増大を認めた.同時性後腹膜転移を疑い精査を施行した.
血液生化学検査所見(2011年10月):CEA:7.5 ng/mlと上昇を認めた.それ以外に特記すべき異常は認めなかった.
腹部造影CT(2011年9月):右後腎傍腔に相当する後腹膜に径11 mm大の占居性病変を認めた.同病変は,類円形で比較的境界が明瞭であったが,軽度のspiculaの形成を認め,辺縁が不整であった(Fig. 1).

Enhanced abdominal CT reveals a solitary tumor in the right pararenal lesion of the retroperitoneal space (arrowhead).
18F-FDG PET/CT(2011年10月):同病変にFDGの集積の亢進を認めた.他の部位に転移を疑う集積の亢進は認めなかった(Fig. 2).

FDG-positron emission tomography CT shows uptake of 18F-FDG in the same lesion as seen in the CT (arrowhead).
腹部造影CT(経時的変化):初回手術時より経時的にCTを見直すと,同病変は既に初回手術前より存在し,一旦縮小したものの,再び増大傾向となり,2010年9月より2011年9月はさらに増大傾向を示していた.腫瘍マーカーCEAも腫瘍径の変化に伴い同期性に変動し,腫瘍径の増大に伴い上昇傾向を認めた(Fig. 3).腫瘍の縮小,CEAの低下は,術後補助化学療法が部分奏効したことによるものと推察された.
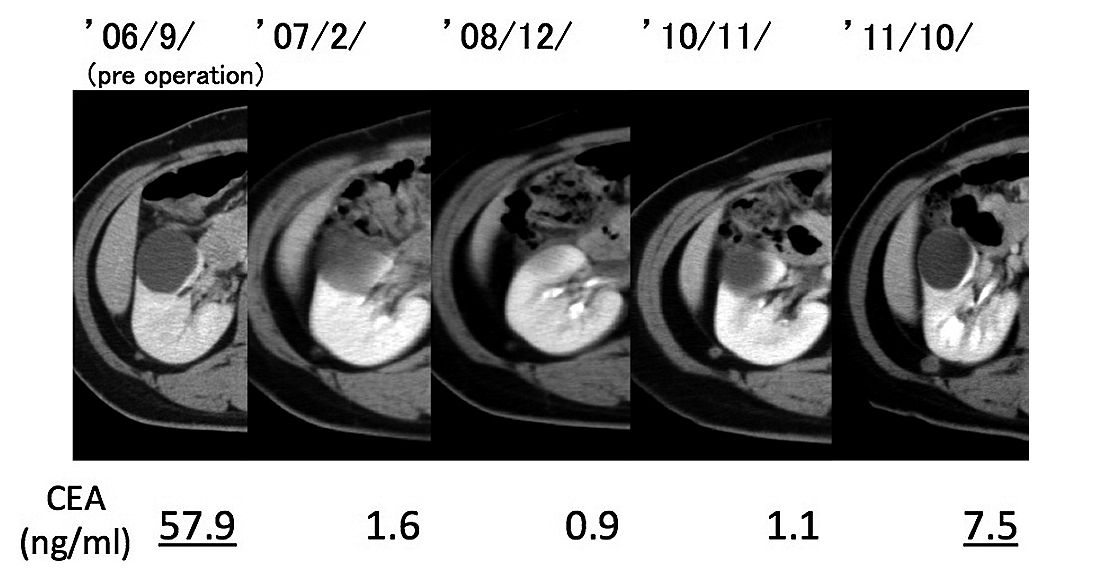
Follow up CT examination reveals that the retroperitoneal tumor had increased in size in accordance with the serum level of CEA.
以上より,大腸癌同時性孤立性後腹膜転移と診断した.他に転移は認めず,単発転移であったので,切除することとした.2011年11月手術を施行,左側臥位,腹膜外アプローチで術野を展開し,腫瘍を摘出した.Gerota筋膜と腹膜が癒合するレベルの後腹膜に腫瘍は局在していて,腹腔内へは露出しておらず,マージンを確保して切除したが腹腔との交通は認めなかった.
摘出標本病理組織学的検査所見:初回手術時の摘出標本の病理組織像は,管状型中分化型腺癌の像を認めた(Fig. 4A).一部に粘液癌の像を認めた.切除した後腹膜腫瘍は,病理組織学的に初回手術時の原発巣と同様に腺癌の増殖を認め,粘液癌の像も認めた.腫瘍周囲には,リンパ節構造はないものの胚中心を伴うリンパ濾胞形成を認めた.大腸癌の転移と診断した(Fig. 4B).

Microscopic findings of the resected specimens. (A) Primary lesion of the ascending colon was diagnosed as moderately differentiated adenocarcinoma (tub2) (H.E.×20). (B) Retroperitoneal tumor was also adenocarcinoma (H.E.×10). Histopathological diagnosis was the metastatic tumor from the ascending colon cancer.
術後経過は良好で,術後第6病日退院した.根治切除できたので,術後補助化学療法は行わず,外来で経過観察中で,初回手術(右結腸切除術)後6年6か月,後腹膜転移性腫瘍摘出術後1年6か月経過し,再発を認めず健在である.後腹膜腫瘍摘出術後,CEAは正常化し,現在も正常範囲内で推移している.
大腸癌の同時性遠隔転移臓器は,肝臓・腹膜・肺の頻度が高く,それぞれ,10.7%,5.0%,1.6%である.以下,骨:0.3%,脳:0.1%,Virchowリンパ節:0.1%となっている1).この「腹膜」とは,腹膜結節であり,本症例の後腹膜の脂肪組織内への転移とは異なる.
癌腫の転移経路としては,播種性,血行性,リンパ行性の経路が一般的に考えられている.本症例は,腹腔とは膜構造を介して異なる層構造(右後腎傍腔)の脂肪組織内に腫瘍を認めた.したがって,前述の「腹膜」への転移とは異なると考えられ,播種性転移は否定的であると思われる.したがって,転移経路は,血行性あるいはリンパ行性と考えられる.右側結腸のリンパ流は,結腸近傍から上腸間膜動静脈に沿って大血管近傍へ流れるので,リンパ節転移も通常それにしたがって進行し,リンパ節郭清もその概念に沿って行われている.本症例は,そのリンパ流の経路からははずれており,また初回手術時に原発巣は深達度SSであり,背側(後腹膜側)の膜構造を破壊して右後腎傍腔へ浸潤している所見も画像上・術中所見上認めていない.リンパ流という観点からは,リンパ行性には転移しにくい部位であると考えられるが,原発巣のリンパ管浸潤が高度であること,腫瘍周囲にリンパ濾胞の形成を認めている点からも,特殊なリンパ流の存在が介在する可能性は否定できない.一方,血行性という点からは,体循環にのった癌細胞が後腹膜へ定着し,単発に転移・増殖するという機序も合理的な説明が難しい.したがって,転移経路についての断定は困難であり,さらなる症例の蓄積と転移のメカニズムの一層の解明が必要である.
本症例のように癌腫が後腹膜へ転移することはまれで,多くは癌の進展に伴う多臓器転移の終末像としてであり,同時性でかつ孤立性の転移は原発巣にかかわらず,極めてまれである.医学中央雑誌で「転移性後腹膜腫瘍」をキーワードに検索すると,6例が報告されていた(1983年から2013年6月まで,会議録を除く)(Table 1)2)~7).原発臓器は,食道,胃,肺,肝臓,乳腺,精巣とさまざまであるが,大腸が原発であるのは,本症例のみであった.低分化腺癌や粘液癌など病理組織学的悪性度が高いとされる症例が多く認められた.同時性転移と考えられる症例は,肺癌症例5)と本症例の2例のみであった.
| Author | Year | Age/Sex | Primary | Size (mm) | Pathology | Recurrence | Outcome |
|---|---|---|---|---|---|---|---|
| Ogino2) | 1987 | 21/M | testis | child head | teratocarcinoma | 1 year | unknown |
| Ohta3) | 1994 | 64/M | esophagus | 70×50 | SCC | 6 months | unknown |
| Oka4) | 1995 | 70/M | stomach | 100×100 | mucinous adenoca. | 12 years | 1y alive |
| Toyama5) | 1997 | 89/M | lung | 86×55 | anaplastic adenoca. | simultaneous | hospital death |
| Kobayashi6) | 2011 | 54/M | liver | 54×40 | poorly diff. HCC | 9 years | 1y alive |
| Yoneyama7) | 2011 | 57/F | breast | unknown | unknown | 10 years | 10m alive |
| Our case | 66/F | colon | 15×20 | mucinous adenoca. | simultaneous | 6y4m alive |
adenoca.: adenocarcinoma, SCC: squamous cell carcinoma, HCC: hepatocellular carcinoma
大腸癌転移巣の治療は,大腸癌治療ガイドラインに,切除可能であれば外科的切除を考慮すると記載されている8).ただし,本症例のような後腹膜転移は,肝臓・肺とは異なり,症例の蓄積が少なくエビデンスに乏しい.大腸癌治療ガイドラインには,副腎・皮膚・脾臓といった臓器は,他の臓器への転移を伴うことが多く,化学療法・放射線療法の適応となることが多いと記載されている8).しかし,本症例は,術後5年を経過し,PET-CTで他に転移を疑う所見を認めなかった.よって根治切除により癌腫がコントロールできると考え,積極的に切除することとした.
術後補助化学療法は,後腹膜転移がまれであるので,そのエビデンスは当然確立されていない.他の臓器としては,根治切除後の肝転移において,ガイドライン上その有効性は確立されていないので,臨床試験として検証していくことが望ましい(推奨カテゴリーB)と記載されている9).また,本症例は初回手術時から5年生存が得られていることも合わせて考え,後腹膜転移切除術後の補助化学療法は行っていない.経過観察中であるが,再発は認めていない.
本症例は,初回手術時に同時性後腹膜転移巣が画像上描出されていたが,術後5年が経過するまで指摘できなかった.その結果,転移巣をCT上経時的に見直すことが可能となった.術後補助化学療法により転移巣が一旦縮小し,その後,治療終了とともに再び増大し,腫瘍マーカーCEAも比例して低下・上昇する経過が確認された.かつ,その転移巣を切除することにより良好な転帰が幸い得られた貴重な症例であった.ただし,結果的に6年以上を経過して無再発生存しているが,初回手術前は転移病変は指摘できておらず,画像を入念に読影することが重要であることを再認識する症例であった.
本論文の要旨は,第38回愛知臨床外科学会(2012年7月名古屋)で発表した.
利益相反:なし