2017 年 50 巻 5 号 p. 339-349
2017 年 50 巻 5 号 p. 339-349
目的:合成吸収性癒着防止剤(セプラフィルム®;以下,癒着防止剤と略記)の大腸癌術後腸閉塞に対する発症予防効果を明らかにする.方法:原発巣切除を施行した大腸癌583症例を,創下へ癒着防止剤を使用したSF群(n=316)と使用しなかったcontrol群(n=267)で,腸閉塞の頻度・発症形式・治療内容・再開腹時所見を後方視的に比較・検討した.さらに,多変量解析で腸閉塞発症に関連する因子を解析した.結果:両群の術後合併症・在院日数・腫瘍学的転帰に有意差はなかった.腸閉塞はSF群で27例(4.6%),control群で29例(4.9%)に発症し(P=0.397),それぞれ7例,8例に手術を要した(P=1.000).このうち各群2例が創への癒着が原因だった(P=0.625).各群で再開腹時の手術創に対する癒着の有無・程度に有意差はなかった.多変量解析で,American Society of Anesthesiologists(ASA)スコア・body mass index・腹部手術の既往・直腸癌・手術時間・術中出血量・開腹手術・人工肛門造設・癒着防止剤使用のうち,人工肛門造設のみが腸閉塞に対する有意な関連を示した(ハザード比2.68,95%信頼区間1.21~5.96).結語:創への癒着に起因する腸閉塞は少なく,今回の検討で癒着防止剤による有意な腸閉塞発症予防効果は示されなかった.
腹部手術後の腹腔内癒着は上腹部手術の93~100%,下腹部手術の67~93%に発生し,術後腸閉塞の65~75%は腹腔内癒着に起因すると報告されている1).腹部外科領域においては癒着防止材の使用によって癒着の頻度,範囲および程度が軽減するとされるが,腸閉塞発症予防効果について確固たるエビデンスは示されていない2).
合成吸収性癒着防止剤(セプラフィルム®;以下,癒着防止剤と略記)はヒアルロン酸ナトリウムおよびカルボキシルメチルセルロースからなるフィルム状の吸収性癒着防止剤で,1997年に本邦での使用が承認された.ラットを用いた試験では,適用後24~48時間以内で水和したゲル状になり,およそ7日間貼付した組織に留まり物理的バリアとして癒着防止効果を発揮する3).今回,自施設において原発巣切除手術を行った大腸癌583症例について,腸閉塞の頻度・発症形式・治療内容・再開腹時の所見を後方視的に評価し,癒着防止剤の腸閉塞に対する発症予防効果を検討した.
2008~2014年の間に,開腹または臍部小開腹を伴う腹腔鏡下手術により,原発巣に対する外科的切除を行った大腸癌583症例を対象とした.閉創前に開腹創直下の腹腔に合成吸収性癒着防止剤(セプラフィルム®;科研製薬,東京)1枚(12.7×15.2 cm)を貼付したSF群(n=316),癒着防止剤を使用しなかったcontrol群(n=267)を後方視的に解析した.癒着防止剤使用の要否,および必要に応じた適当なサイズへの切り分けについては術者の判断で決定した.全例に術後4日目あるいは 5日目から流動食が開始となるクリニカルパスが適応された.
2. 評価方法SF群・control群において患者因子・手術因子・術後合併症・腫瘍因子を比較した.患者因子において,腫瘍による腸管狭窄のため,手術までの待機期間中に絶食を要すると判断された症例を術前腸閉塞ありとした.また,開腹操作を伴う腹部手術の既往を検索した.術後に発症した腸閉塞について,発症時期・発症頻度・治療内容を両群で比較した.今回の研究では,麻痺性腸閉塞を検討から可及的に除外する目的で,排ガスなど大腸機能の回復徴候を示し,クリニカルパスに従って流動食摂取を開始後,排ガスの停止・腹部膨満・嘔吐などの臨床症状が出現し,X線単純写真またはCTで小腸の拡張を認めたものを腸閉塞と定義した.腸閉塞の発症日は画像検査による診断の確定が得られた時点とした.さらに,手術あるいは生検検体にて病理学的に癌の再発が関連することが診断された腸閉塞は検討対象から除外した.
検討期間に再開腹手術を施行された症例について,大腸癌手術からの期間・再開腹理由・再開腹創の位置,および再開腹時の大腸癌手術創部に対する癒着の有無・程度・関連臓器について診療録の記載を調査し,結果をSF群・control群で比較した.癒着の程度については,診療録に「高度な癒着」と記載されたもの,それ以外の癒着を認めたもの,記載なしに分類した.
検討因子のうち,術後癒着性腸閉塞の発症あるいは発症予防に関与する可能性があると考えられている4)~6),American Society of Anesthesiologists(以下,ASAと略記)スコア・body mass index(以下,BMIと略記)・腹部手術の既往・直腸癌・手術時間・術中出血量・開腹手術・人工肛門造設・癒着防止剤について,有意な関連があるか多変量解析で検討した.
3. 統計量的因子,質的因子の単変量解析は,それぞれMann-WhitneyのU検定,Fisherの正確確率検定またはχ2検定で,SF群・control群の補正生存率および腸閉塞罹患率についてはlog-rank検定で,Prizm 5®(GraphPad Software, Inc, CA, USA)を用いて行った.多変量解析はCox比例ハザードモデルで,XLSTAT®(Addinsoft, Paris, France)を用いて行い,単変量・多変量解析ともP値<0.05を統計学的有意とした.
自施設における癒着防止剤使用頻度は2008年以降増加し,2011年度から使用例数が非使用例数を上回るようになった(Fig. 1).
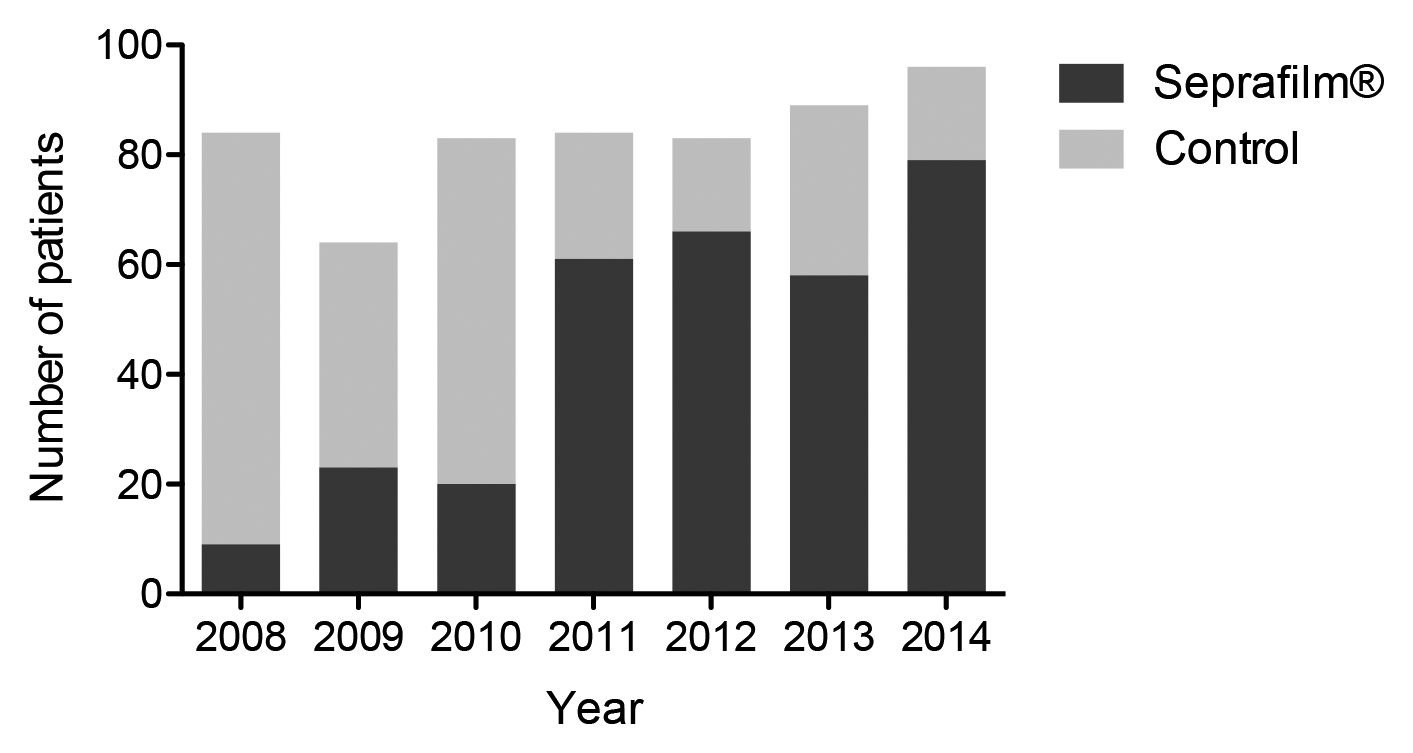
Percentage of Seprafilm® group and control group by year.
患者背景において,SF群とcontrol群の年齢・性別・ASAスコア・BMI・腹部手術歴・術前腸閉塞の有無・腫瘍の局在に差を認めなかった(Table 1).
| Seprafilm® (n=316) | Control (n=267) | P value | |
|---|---|---|---|
| Age (yr) | 72 (30–96) | 72 (39–97) | 0.497 |
| Gender | 0.274 | ||
| Male | 189 | 147 | |
| Female | 127 | 120 | |
| ASA class | 1.9±0.4 | 1.9±0.5 | 0.221 |
| BMI (kg/m2) | 23 (14–46) | 22 (14–39) | 0.897 |
| Previous abdominal surgery | 0.383 | ||
| Present | 114 | 87 | |
| Absent | 202 | 180 | |
| Preoperative bowel obstruction | |||
| Present | 78 | 69 | 0.774 |
| Absent | 238 | 198 | |
| Tumor location | 0.140 | ||
| Colon | 201 | 180 | |
| Rectum | 105 | 85 | |
| Colon and rectum | 5 | 0 | |
| Colon (multiple) | 5 | 2 |
Data are numbers or mean±standard deviation or median with range in parentheses. ASA: American Society of Anesthesiologists, BMI: body mass index
手術因子では,穿孔などによる緊急手術がcontrol群で有意に多く(P=0.001),回腸瘻造設がSF群でより高頻度に行われていたが(P=0.027),手術時間・出血量・腹腔鏡手術の割合・吻合個数に差はなかった(Table 2).
| Seprafilm® (n=316) | Control (n=267) | P value | |
|---|---|---|---|
| Urgency | 0.001 | ||
| Emergency | 2 | 13 | |
| Elective | 314 | 254 | |
| Length of surgery (min) | 105 (32–318) | 96 (33–330) | 0.080 |
| Blood loss (ml) | 50 (0–1,800) | 60 (2–1,740) | 0.345 |
| Approach | 0.650 | ||
| Open | 224 | 184 | |
| Laparoscopic | 92 | 83 | |
| Anastomosis | 0.069 | ||
| None | 39 | 36 | |
| One | 268 | 230 | |
| Greater than one | 9 | 1 | |
| Stoma creation | 0.027 | ||
| None | 251 | 225 | |
| Ileostomy | 26 | 8 | |
| Colostomy | 39 | 34 |
Data are numbers or median with range in parentheses.
腫瘍因子では,腹膜播種の有無・術後抗癌剤使用率・病理学的進行度に有意な差はなかった(Table 3).また,両群の補正生存率に有意な差は認めなかった(P=0.983)(Fig. 2).
| Seprafilm® (n=316) | Control (n=267) | P value | |
|---|---|---|---|
| Peritoneal dissemination | 0.277 | ||
| Present | 18 | 15 | |
| Absent | 298 | 252 | |
| Postoperative chemotherapy | 0.278 | ||
| Present | 149 | 114 | |
| Absent | 166 | 153 | |
| Pathological stage | 0.392 | ||
| 0 | 9 | 14 | |
| I | 59 | 58 | |
| II | 99 | 70 | |
| III | 93 | 79 | |
| IV | 56 | 46 | |
| Five-year survival rate (%)* | 75.6 | 77.3 | 0.983 |
Data are numbers. *Cause-specific rate
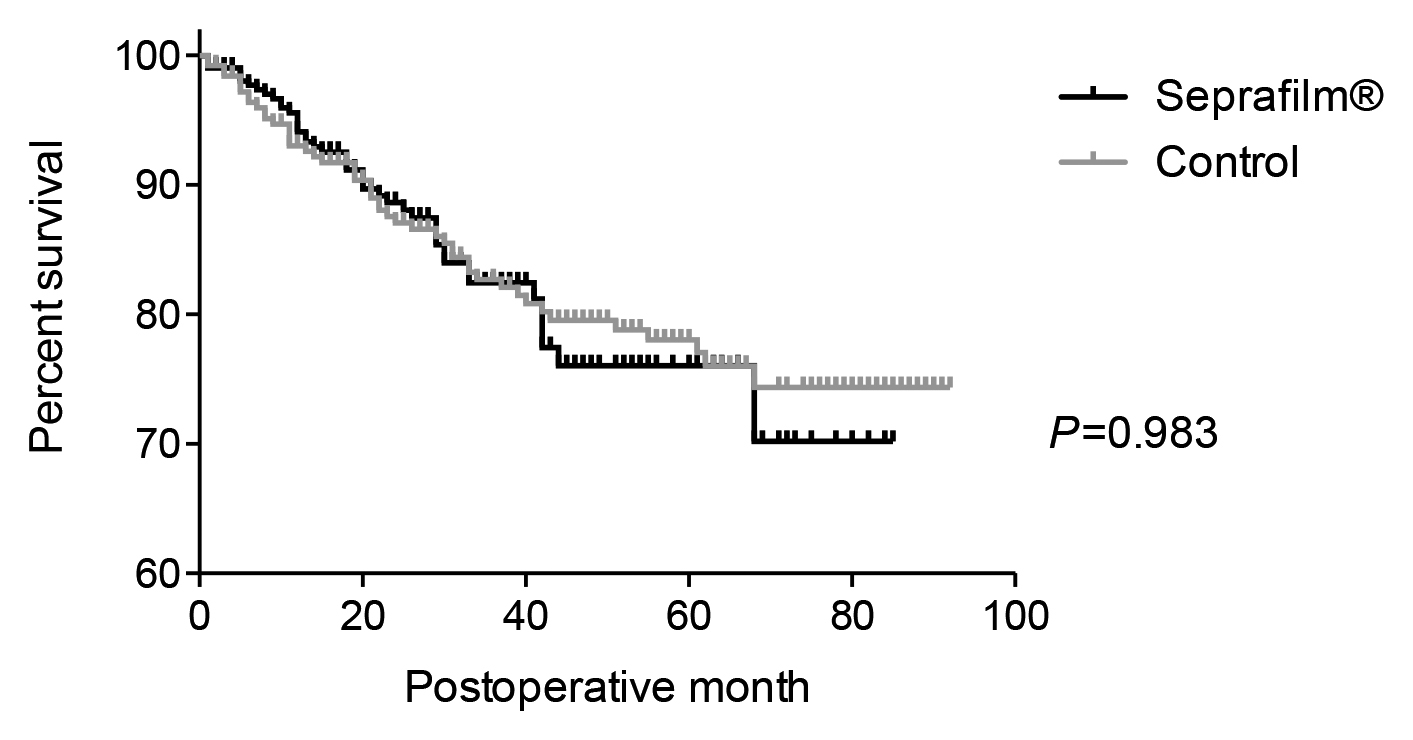
Kaplan-Meier cause-specific survival curve of patients. Note: P values are from log-rank test. CI: confidence interval.
対象患者全体の術後観察期間中央値は28(0~92)か月で,手術関連死亡を5例(0.8%)認めた.観察期間はcontrol群がSF群より有意に長かった(P<0.001).術後に腸管運動の回復が不良で流動食開始が遅延した,いわゆる麻痺性と考えられる腸閉塞は,SF群で11例,control群で2例に認めた(P=0.044).また,SF群9例,control群3例に癌の再発に伴う腸閉塞を認めた(P=0.240).これらを除外した腸閉塞は,SF群で27例(4.6%),control群で29例(4.9%)に認め,発症頻度に差はなかった(P=0.397).両群の手術関連死亡,手術部位感染,縫合不全,Clavien-Dindo分類グレードIIIa以上の術後合併症の発症率,および術後在院日数にも有意な差はなかった(Table 4).
| Seprafilm® (n=316) | Control (n=267) | P value | |
|---|---|---|---|
| Observation period (month) | 24 (0–85) | 39 (19–92) | <0.001 |
| Mortality (%) | 0.6 | 1.1 | 0.664 |
| Bowel obstruction | 0.397 | ||
| Present | 27 | 29 | |
| Absent | 289 | 238 | |
| Surgical site infection | 0.191 | ||
| Present | 119 | 86 | |
| Absent | 197 | 181 | |
| Anastmotic failure | 0.801 | ||
| Present | 8 | 8 | |
| Absent | 269 | 225 | |
| Complications | 1.000 | ||
| ≥CDG IIIa | 31 | 27 | |
| <CDG IIIa | 285 | 240 | |
| Length of hospital stay (day) | 18 (9–337) | 17 (9–183) | 0.123 |
Data are numbers or median with range in parentheses. CDG: Clavien-Dindo grade
腸閉塞を発症した時期の比較では,術後30日,90日,1年以内に発症した割合は,SF群で36%,45%,53%,control群で31%,33%,38%と,control群で発症までの期間が長い傾向だったが,Kaplan-Meier法でSF群・control群の腸閉塞の累積発症曲線を比較したところ,両群に有意な差を認めなかった(P=0.617)(Fig. 3).
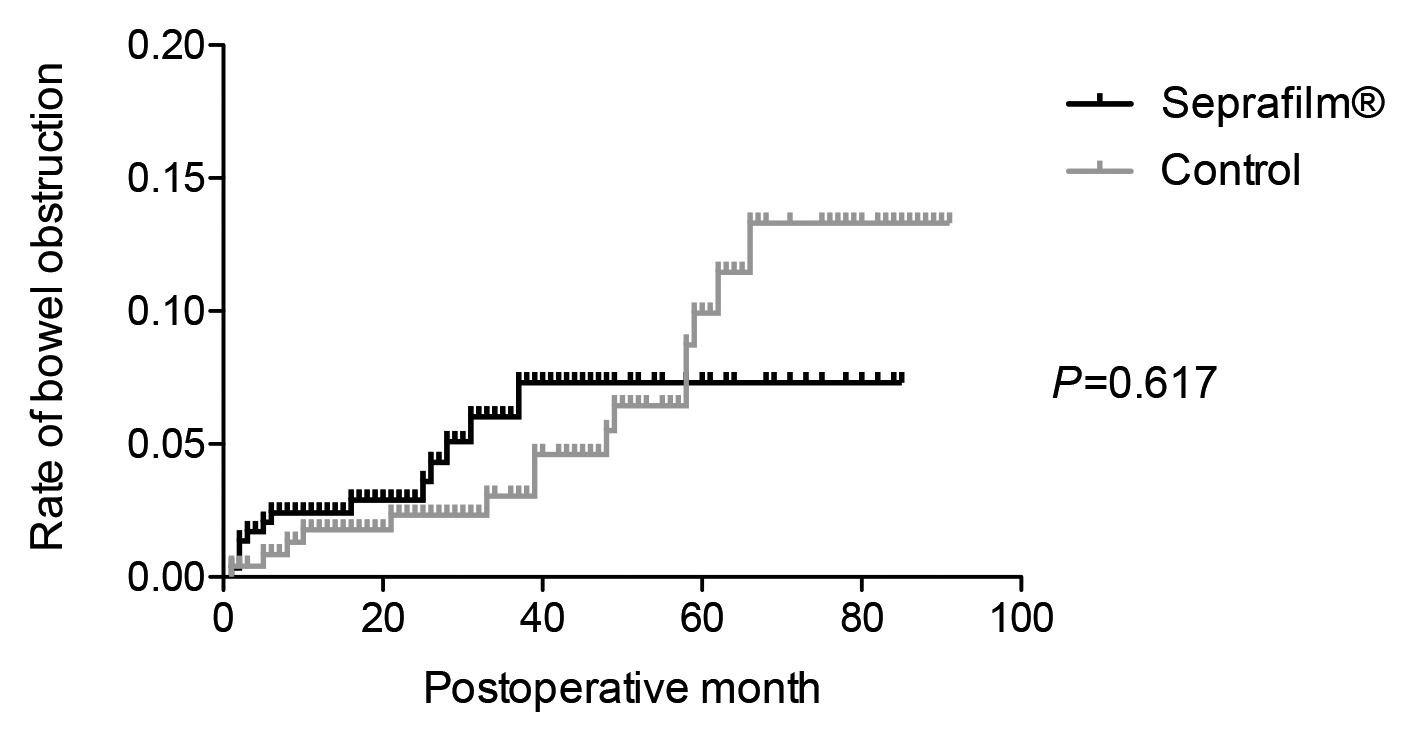
Kaplan-Meier morbidity curve of patients with first small bowel obstruction excluding cancer-associated conditions. Note: Hazard ratios (HR) and P values are from log-rank test. CI: confidence interval.
初回の腸閉塞発症までの期間・腸閉塞の罹患回数・手術を要した症例の割合・腸切除を行った割合は,いずれも両群で差はなかった.手術を要した腸閉塞はSF群7例,control群8例で(P=1.000),腸切除を行ったものはSF群1例,control群3例だった(P=0.378).手術により診断された腸閉塞の発症機転は,各群とも2例が創部への癒着によるもの,5例がその他の部位への癒着によるもので,control群で1例に内ヘルニアによる腸閉塞を認めた(P=0.579)(Table 5).
| Seprafilm® (n=27) | Control (n=29) | P value | |
|---|---|---|---|
| Time to first bowel obstruction (day) | 29 (6–1,138) | 17 (5–2,018) | 0.353 |
| ≥10 POD | 20 | 23 | 0.755 |
| ≥30 POD | 13 | 14 | 1.000 |
| Frequency | 0.414 | ||
| 1 | 23 | 27 | |
| ≥ 2 | 4 | 2 | |
| Treatment | 1.000 | ||
| Conservative | 20 | 21 | |
| Surgical | 7 | 8 | |
| Operative procedure | 0.378 | ||
| Adhesiolysis | 5 | 5 | |
| Bowel resection | 1 | 3 | |
| Bypass | 1 | 0 | |
| Confirmed cause by surgery | 0.625 | ||
| Adhesion to wound | 2 | 2 | |
| Other adhesion | 5 | 5 | |
| Internal hernia | 0 | 1 |
Data are numbers or median with range in parentheses. POD: postoperative day
観察期間において再開腹手術を受けた症例は,SF群49例(15%),control群28例(10%)であった.再開腹の理由として,回腸人工肛門閉鎖や,異時性癌・転移性腫瘍に対する切除を含む他部位悪性腫瘍に対する手術が多かった.再開腹手術を受けた症例のうち,SF群26例(53%),control群19例(67%)で,大腸癌手術時の開腹創を含む皮膚切開が行われていた.癒着の範囲について正確な情報は検索しえなかったが,癒着の有無・程度・癒着臓器について両群に有意な差はなかった(Table 6).
| Seprafilm® (n=49) | Control (n=28) | P value | |
|---|---|---|---|
| Time to re-laparotomy (month) | 7 (0–37) | 22 (0–62) | 0.005 |
| Reason* | 0.491 | ||
| Ileostomy closure | 21 | 8 | |
| Other malignancy | 13 | 10 | |
| Bowel obstruction | 7 | 8 | |
| Incisional hernia | 5 | 3 | |
| Peritonitis | 3 | 1 | |
| Inclusion of previous wound | 0.236 | ||
| Yes | 26 | 19 | |
| No | 23 | 9 | |
| Adhesion to previous wound | 0.832 | ||
| Present | 21 | 14 | |
| Absent | 2 | 1 | |
| Not stated | 26 | 13 | |
| Organ involved in adhesion* | 0.335 | ||
| Omentum | 11 | 3 | |
| Bowel | 12 | 4 | |
| Not stated | 31 | 20 | |
| Extent of adhesion | 0.517 | ||
| Severe | 3 | 2 | |
| Less than severe | 15 | 12 | |
| Not stated | 29 | 13 |
Data are numbers or median with range in parentheses. *Overlapping data are included
多変量解析では,ASAスコア・BMI・腹部手術の既往・術前腸閉塞・直腸癌・手術時間・術中出血量・開腹手術・癒着防止剤使用の有無はいずれも腸閉塞の発症と有意な関連はなく,人工肛門造設のみが独立した腸閉塞の発症リスクであった(P=0.015,ハザード比2.68,95%信頼区間1.21~5.96)(Fig. 4).
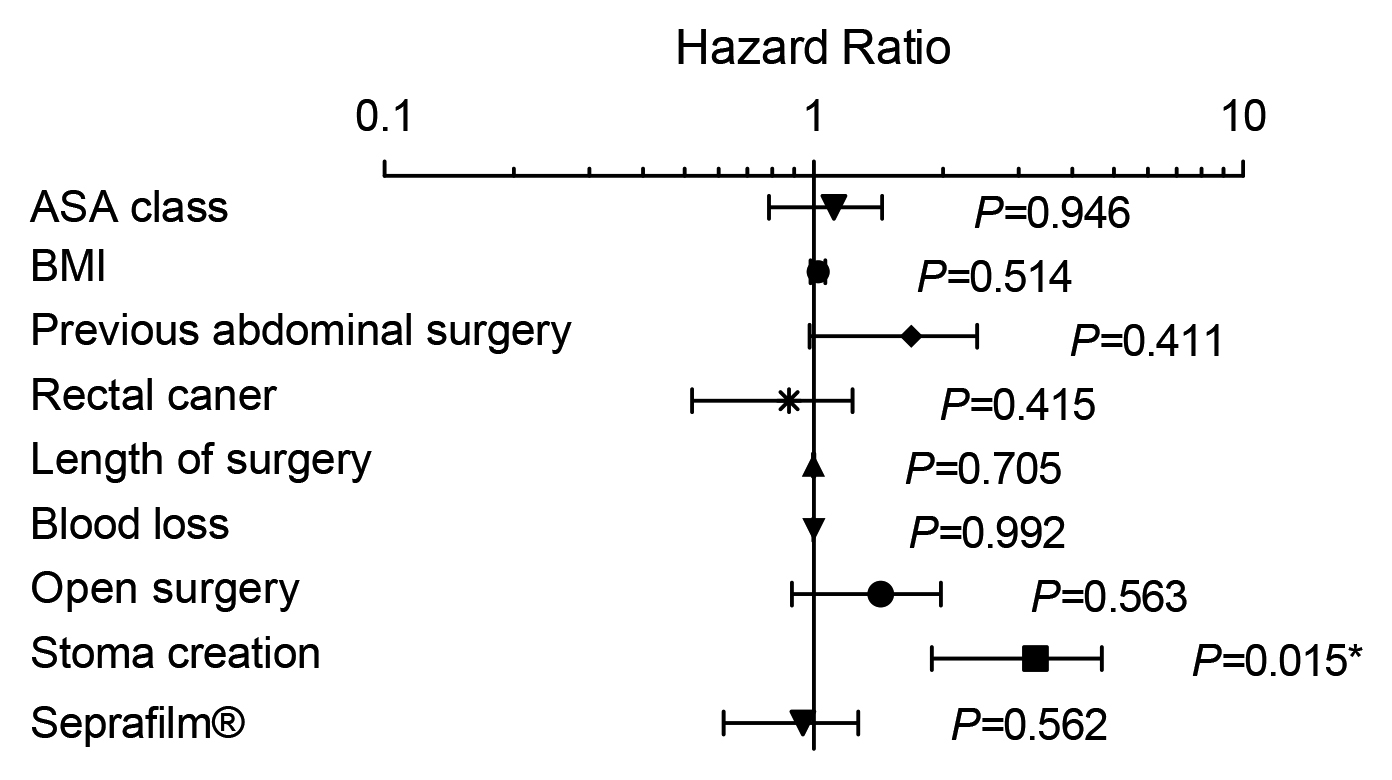
Hazard ratios and 95% confidence intervals for factors related to small bowel obstruction excluding cancer-associated conditions. Note: Hazard ratios and P values are from Cox proportional hazard analysis. *Statistically significant. BMI: body mass index, ASA: American Society of Anesthesiologists.
検索用語を「合成吸収性癒着防止剤」または「セプラフィルム」または「ヒアルロン酸ナトリウム/カルボキシルメチルセルロース」とし,検索対象を症例報告・会議録を除く「原著論文」,「ヒト」として,1998年から2016年3月までの医学中央雑誌を検索した.このうち対照群の設定および統計学的検証のなされている腹部外科領域の論文7編と自験例の報告内容をまとめた(Table 7)5)7)~12).5編が腸閉塞の発症頻度を癒着防止剤使用群と対照群とで比較し5)7)9)~11),うち3編が癒着防止剤使用群で有意に腸閉塞が少なかったと報告した5)9)10).しかし,腸閉塞の定義が明確に示されているものは2編のみで5)7),示された定義はいずれも麻痺性腸閉塞を含みうるものであった.これまでに癒着防止剤と麻痺性腸閉塞との関連は示されておらず,麻痺性腸閉塞は腸閉塞として検討する対象から除外することが望ましいと考えた.また,既報の3編においては,検討対象が術後30日から2か月の間に発症した腸閉塞に限定されていた5)7)9).癒着性腸閉塞に対する手術を行った500症例を長期にわたり追跡調査したFevangら13)は,直近腹部手術から初回癒着性腸閉塞手術までの期間を,1年以内が41%,1~5年が26%,5~10年が11%,10年以上が22%であったと述べている.癒着性腸閉塞以前の手術に関する詳細は記載がなく,手術を要した癒着性腸閉塞を広く対象にした研究ではあるが,大腸癌術後症例を対象にした我々の検討でも,術後1年以内に発症した腸閉塞は,観察期間内に診断された腸閉塞全体の半数に満たず,長期経過観察後の症例も多く含まれていた.このことから,癒着防止剤の腸閉塞に対する予防効果を検証するうえでは,少なくとも年単位の観察期間が必要と考えられた.Fazioら4)は,セプラフィルム®の腸閉塞発症減少効果を検証する多施設共同ランダム化比較試験を行うにあたり,腸閉塞の発症頻度を2年間で20%と見込み,癒着防止剤による腸閉塞の相対的減少効果が25%と仮定すると,80%の検出力で有意水準5%のもと必要なサンプルサイズはおよそ1,700症例であるとしている.Table 7に示す本邦報告例の腸閉塞発症頻度にはばらつきがあり一律な評価は困難であるが,自施設の研究を含め後方視的研究でサンプルサイズが小さいものが多く,癒着防止剤の治療効果を正確に評価しているとはいえない.
| No. | Author | Year | Design | Objectives | No. of patients | Observation period (months) | No. of SP sheet* applied | Application site of SP | Incidence of SBO | Definition of SBO | Outcomes measures | Results summary | |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| SP | Control | ||||||||||||
| 1 | Akahane7) | 2002 | RCS | Open surgery with incision length >10 cm | 86 | 87 | NS | 1 or 2 | Incision | SP: 9.3% Control: 14.9% | Clinical symptoms persisting for ≥4 days with X-ray confirmation of bowel dilatation or treated by long tube | Incidence of SBO onset within 1 month after surgery | No difference in both incidence and treatment of SBO (P=0.256 and P=0.078) |
| 2 | Katoh5) | 2005 | RCS | Open colorectal cancer surgery | 72 | 96 | NS | 1 | Incision | SP: 1.3% Control: 11.5% | Clinical symptoms with X-ray confirmation of bowel dilatation | Incidence of SBO onset within 2 months after surgery | Decreased incidence of SBO (P=0.041) |
| 3 | Kusunoki8) | 2005 | PRCS | Two-staged operation for Stage II rectal cancer with preoperative radiotherapy and postoperative chemotherapy | 30 | 29 | 43.6 (24–66) | NS | Incision, limb of the ileostomy | NS | NS | Severity and extent of adhesion. Laparoscopic evaluation at ileostomy closure by blinded assessor | Decreased severity and extent of both midline (P<0.001 and P<0.001) and peristomal adhesions (P=0.007 and P<0.001). Comparable oncological outcomes |
| 4 | Ikenaga9) | 2010 | RCS | Open, elective surgery for colorectal cancer | 556 | 226 | NS | 1 or 2 | Incision | SP: 17.6% Control: 37.5% | NS | Incidence of SBO onset within 30 POD | Decreased incidence of SBO requiring radiological examination and/or N-G tube and/or fasting and/or long tube and/or surgery (P<0.001) |
| 5 | Hashimoto10) | 2012 | RCS | Unplanned re-laparotomy excluding laparoscopic surgery, appendectomy, inguinal hernia repair | 60 | 63 | NS | NS | Incision | SP: 17.7% Control: 44.4% | NS | Incidence of SBO, severity of adhesion | Decreased extent of adhesion (P<0.01) and incidence of SBO (P<0.01) |
| 6 | Katoh11) | 2014 | RCS | Inguinal hernia with transabdominal preperitoneal repair | 493 | 75 | NS | NS | Peritoneal closure | SP: 0% Control: 0% |
NS | Incidence of SBO, severity of adhesion at re-laparotomy (n=21) |
No SBO in all cases. Decreased incidence of adhesion at re-laparotomy (P=0.015) |
| 7 | Ikenaga12) | 2015 | RCS | Metachronous liver metastasis from colorectal cancer | 39 | 19 | NS | NS | Incision | NS | NS | Severity of adhesion at re-laparotomy |
No difference in severity of adhesion (P=0.059) |
| 8 | Our case | RCS | Colorectal cancer surgery | 316 | 267 | 28 (0–92) | 1 | Incision | SP: 4.6% Control: 4.9% | Clinical symptoms occurred after the return of bowel function. X-ray and/or CT confirmation of bowel dilatation | Incidence of SBO | No difference in morbidity, oncological outcomes, SBO incidence, SBO treatment | |
SP: Seprafilm®, SBO: small bowel obstruction, RCS: retrospective cohort study, PRCS: prospective randomized control study, NS: not stated, POD: postoperative day. *1 sheet=12.7×14.7 cm
さらに,今回の研究は後方視的研究であるため,再手術時の所見については診療録の記載に頼らざるをえず,特に癒着の程度についての記載は術者の主観的な評価によるものである.また,患者背景として大腸穿孔などによる緊急手術症例がcontrol群に多く含まれること,癒着防止剤の要否が術者判断で行われたことにより,得られた結果は慎重に評価すべきと考える.しかしながら,興味深い知見として,人工肛門造設が腸閉塞と関連するとの結果を得た.当院ではハルトマン手術や直腸切断術の際に腹腔経路で人工肛門を挙上している.人工肛門造設を併施した108例のうち,22例が腸閉塞に罹患し,このうち閉塞部位を同定できたのは7例で,4例が人工肛門周囲への癒着に起因する腸閉塞であった.Kusunokiら8)は,自施設における直腸癌患者を対象にした前向きランダム化試験において,正中創直下およびイレオストミー周囲へ癒着防止剤を貼付することで,イレオストミー閉鎖時に正中創・イレオストミー両者に対する癒着の程度・範囲が有意に軽減していたと報告した.人工肛門周囲の癒着の程度や範囲と腸閉塞発症との関連は明らかではないが14),人工肛門周囲への癒着防止剤貼付により,どの程度の腸閉塞発症予防効果が得られるかは今後検証されるべき課題である.
赤羽ら7)は,癒着防止剤使用群で在院日数短縮や腸閉塞の減少を認め,患者一人当たりの医療費が38,608円削減されたと報告した.また,前述のFazioら4)の研究では,手術を要した腸閉塞は癒着防止剤使用群で15例(1.8%)であったのに対し,非使用群では29例(3.4%)と,癒着防止剤による47%の相対的腸閉塞減少効果が示された(P<0.05).一方,我々の研究では,術後在院日数はSF群とcontrol群とは同等で,腸閉塞の発症頻度はSF群で27例(4.6%),control群で29例(4.9%)と有意な差はなかった.また,手術を要した腸閉塞は,SF群とcontrol群でそれぞれ7例(2.2%),8例(2.9%)であり,このうち創部への癒着に起因する腸閉塞と診断されたものは両群ともわずか2例ずつ計4例(0.6%)と,癒着防止剤の明らかな予防効果は示されなかった.ただし,Fazioら4)の研究で使用されたセプラフィルムは平均4.4枚で,創部以外にも癒着の原因となりうる組織を被覆したと記載されているのに対し,本邦では373.38 cm2が保険適応の上限であることから,報告例における使用量は自施設を含め1ないし2枚となっていること,またほとんどが創部直下の腹腔内容を被覆するように用いられているため,結果を単純に比較することは困難である.
癒着防止剤の使用により期待される腸閉塞予防以外の効果として,癒着の範囲や程度を軽減することで,再開腹の際に癒着剥離操作が容易になる可能性が指摘されている8)14)15).我が国においては平均寿命の延長に伴い,大腸癌を含む悪性腫瘍の罹患率は増加傾向にある16).また,分子標的薬の登場などで従来,切除適応とならなかった遠隔転移が切除可能となる症例も増えている17).こうした現状をふまえると,今後転移巣の切除や異時性癌に対する手術など,複数回の腹部手術を受ける患者は増加すると予想される.事実,今回検討した症例のうち201例(34%)が大腸癌手術に先立ち何らかの腹部手術を受けており,77例(13%)が術後に再度開腹手術を受けていた.腸閉塞に対する予防効果と再開腹時の癒着剥離関連合併症に対する予防効果を合わせて検討することで,癒着防止剤使用における真のベネフィットが明らかにされる.また,今回の検討では,腸閉塞に関する腹腔鏡手術の開腹手術に対する優位性は示されなかった.腹腔鏡手術における癒着防止剤の有効性についても,癒着性腸閉塞の発症予防および再開腹時の癒着予防の双方の観点から,今後明らかにすべき課題であると考えられた.
利益相反:なし