2020 年 53 巻 12 号 p. 992-1001
2020 年 53 巻 12 号 p. 992-1001
症例は57歳の女性で,肛門右側の紅班を主訴に当院を受診した.皮膚生検で表皮にPaget細胞を認め,免疫組織化学染色で肛門管癌のPagetoid spreadと診断された.大腸内視鏡検査で直腸に腫瘤性病変を認めず,step biopsyでも陰性であった一方,直視下での肛門粘膜マッピング生検では陽性を示し,根治切除には肛門近傍の皮膚を含めた病変の切除が必要と考えた.深部浸潤を疑う所見はなく,粘膜下層での切除で根治性の確保と肛門温存が可能と考え,消化器外科・消化器内科・皮膚科合同で内視鏡的粘膜下層剥離術,経肛門的粘膜下層切除術,皮膚悪性腫瘍切除術を施行した.術後は順調に17病日に退院した.今回,我々はPagetoid spreadを伴う肛門管癌に対して腹会陰式直腸切断術を回避し肛門温存が可能であった症例を経験した.比較的まれな症例のため我々が行った術式および経過概要を含め報告する.
A 57-year-old woman was admitted to our hospital because of erythema on the right side of her anus. A skin biopsy showed Paget cells in the epidermis, and immunohistochemical staining revealed pagetoid spread of anal canal cancer. Although colonoscopy showed no mass lesions in the rectum and step biopsy was negative, mapping biopsy from the anal mucosa was positive. Therefore, we thought it necessary to remove the lesion, including the skin near the anus, to obtain curative resection. There was no evidence of infiltration to the muscularis propria, and we thought that resection in the submucosal layer would ensure a radical cure and preserve anal function. ESD, trans-anal submucosal resection, and cutaneous malignant tumor resection were performed jointly by gastrointestinal surgery, gastroenterology, and dermatology surgeons, respectively. The patient was discharged from hospital 17 days after surgery. In this case of anal canal cancer with pagetoid spread, abdominoperineal rectal resection was avoided and anal function was preserved. We report this relatively rare case including our surgery and the progress of the patient.
肛門周囲Paget病は皮膚原発癌と隣接臓器悪性腫瘍の表皮内浸潤(Pagetoid spread)の2型に区別され1),これらは治療法や予後が大きく異なるため,鑑別診断が非常に重要である.今回,我々はPagetoid spreadを伴う肛門管癌に対して腹会陰式直腸切断術が回避され,肛門温存が可能であった症例を経験した.Pagetoid spreadを伴う肛門管癌に対して肛門温存が可能であった症例はまれであり,これに内視鏡的粘膜下層剥離術(ESD)の手技を加えて肛門温存に成功した症例は報告がなく,今回,我々は良好な成績を得ることができたためこれを報告する.
患者:57歳,女性
既往歴:脂質異常症,慢性蕁麻疹
現病歴:検診で肛門右側の紅斑を指摘され近医より当院皮膚科紹介となった.皮膚生検の結果からは乳房外Paget病も疑われたが,免疫組織化学染色の結果を併せて,肛門管癌のPagetoid spreadの診断となり,当科へ紹介され手術方針となった.
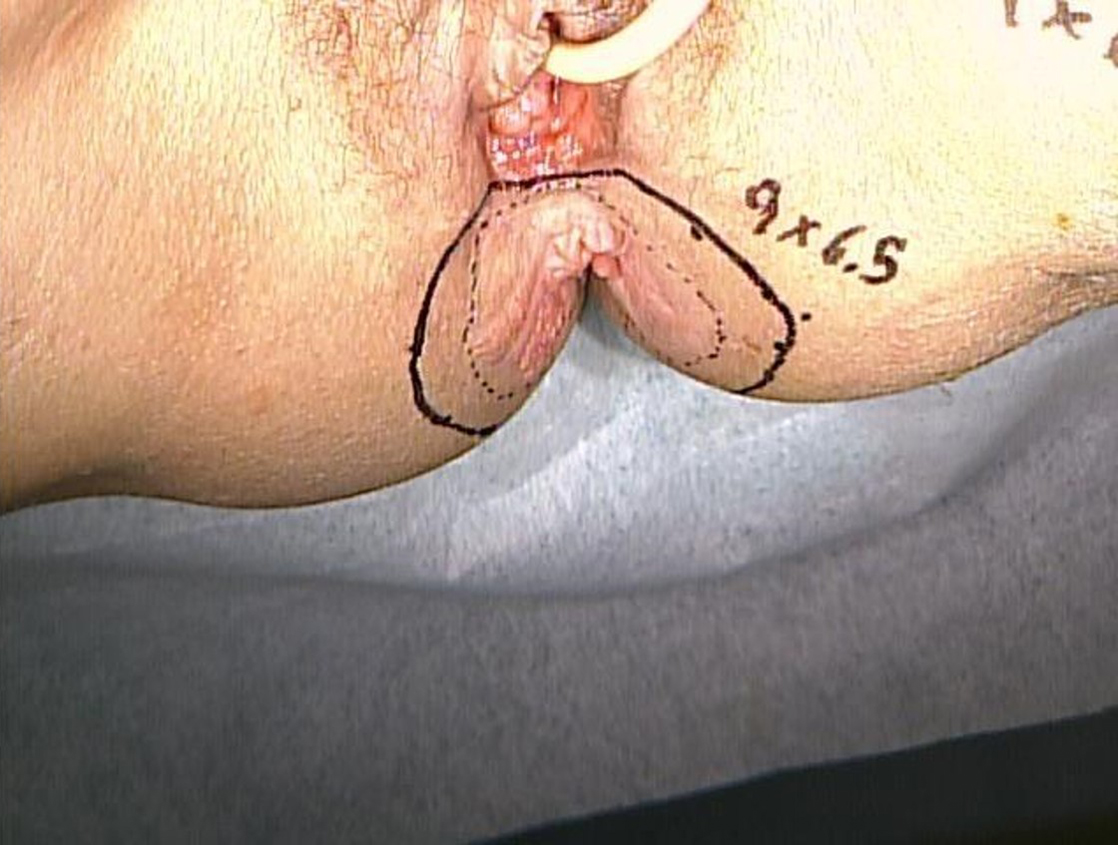
視診・直腸指診所見:肛門右側に肛門に接して,40×15 mmの範囲に扁平でわずかに隆起した紅斑局面を認めた.尾骨側は爪甲大で比較的境界明瞭,膣側は連続して境界不明瞭な局面を認めた.直腸指診で肛門管内に明らかな腫瘤は触知しなかった(Fig. 1).
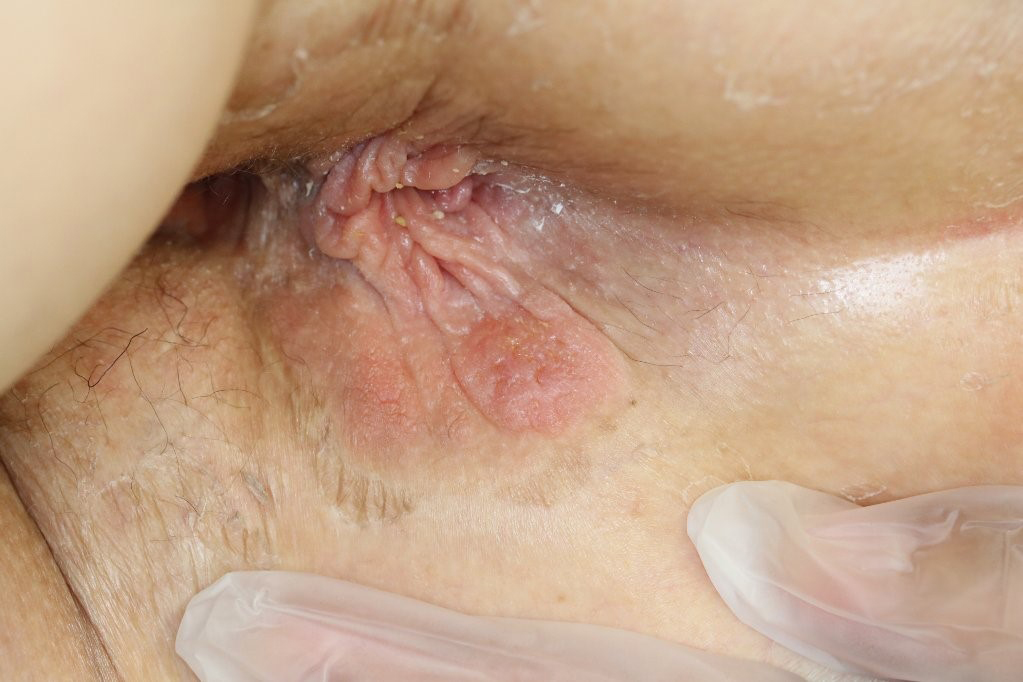
On the right side of the anus, there was a flat, raised erythema of size 40×15 mm.
病理組織学的検査所見:同部位からの皮膚生検を行った.表皮に乳頭状・網目状の構築を示す増生肥厚と,淡明な胞体と圧排された核をもつ異型細胞(Paget細胞)が伸展していた.免疫組織化学染色ではCK7+,PAS陽性であり,extramammary Paget’s diseaseを疑う結果であった.
マッピング生検所見:①肛門部と会陰の間,②右大陰唇,③左臀部紅斑境界域,④肛門粘膜のひだから,マッピング生検を行うと(Fig. 2),③と④でPaget細胞の浸潤を認め,extramammary Paget’s disease疑いの結果であった.膣粘膜からも追加生検されたが,病理結果は陰性であった.
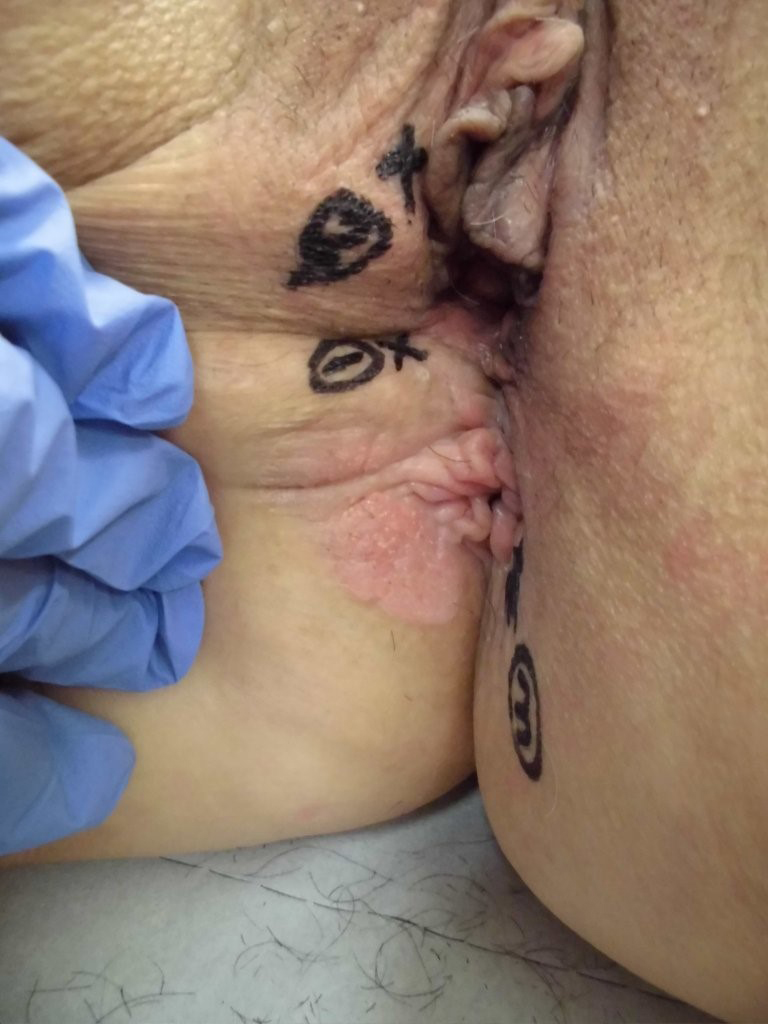
Mapping biopsy was performed from four places: right great labia, erythema of left buttocks, anal mucosa, and between the anus and perineum.
下部消化管内視鏡検査所見:口側の肛門管内への病変の伸展を検索するため大腸内視鏡検査も施行されたが,直腸に明らかな腫瘤性病変の指摘はされなかった.直腸粘膜には血管拡張像を認め,肛門管内からの伸展を疑う所見であった.歯状線口側4か所の生検からはPaget細胞は指摘されなかった(Fig. 3).
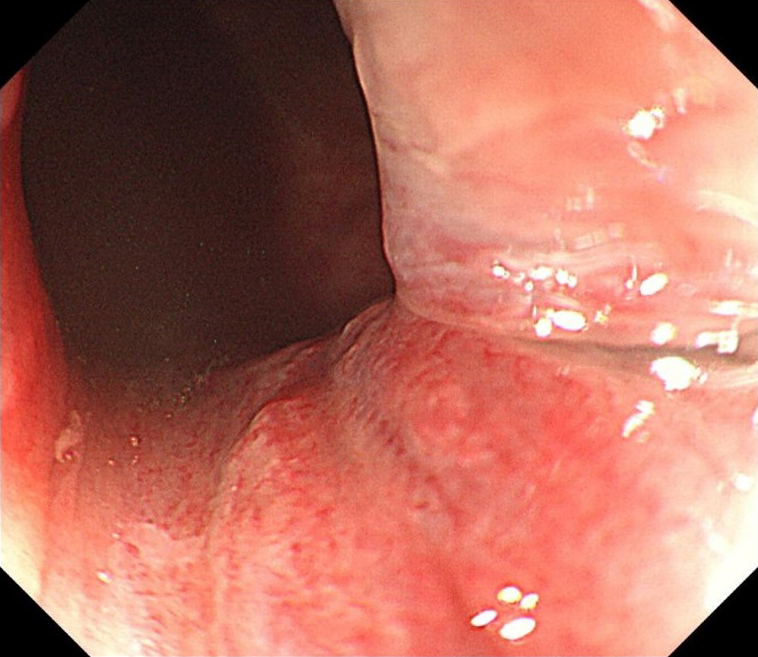
On preoperative colonoscopy, there was no tumorous lesion in the rectum. However, vascular dilation was observed in the rectal mucosa, which was suspected to be a finding of extension from the anal canal.
造影CT所見:明らかな遠隔転移を疑う所見は認めなかった.
PET-CT所見:肛門左側壁から直腸に淡いFDG集積亢進を認めた.明らかな転移を示唆する異常集積は認めなかった.
免疫組織学検査所見:肛門部皮膚の検体の追加で行った免疫組織学染色の結果はcytokeratin 20(+),CDX2(+),GCDFP15(−)で,下部消化管由来が強く示唆された.肛門管癌のPaget様伸展を疑う結果であった.
肛門周囲の皮膚病変は肛門内へと連続性に伸展し,同部の皮膚生検の結果からも下部消化管由来であることが示唆される一方,下部消化管内視鏡では歯状線口側において腫瘍の指摘はできなかった.肛門管内から伸展する血管拡張像を認めることから,腫瘍の局在は肛門管内と判断した.肛門皮膚の病変は下部消化管由来の肛門管癌に伴う,続発性乳房外Paget病と判断し,Pagetoid spreadを伴った肛門管癌(cTis,N0,M0)の術前診断となった.根治切除には肛門近傍の皮膚を含めた直腸粘膜までの切除が必要と考えられた.一方で,深部浸潤を疑う所見はなく,粘膜下層での切除により根治性の確保と肛門温存が可能と判断した.
手術術式:根治切除と肛門温存を両立すべく,消化器外科・消化器内科・皮膚科での合同手術の方針となった.①ESD(消化器内科),②皮膚悪性腫瘍切除術(皮膚科),③経肛門的粘膜下層切除術,S状結腸双孔式人工肛門造設術(消化器外科),④分層植皮術(皮膚科)の予定術式とした.
全身麻酔後,まず側臥位で消化器内科にて内視鏡的粘膜切除術を施行,次に砕石位に体位変換後,皮膚科にて会陰側から肛門にかけての皮膚病変を切除することとした.続いて消化器外科にて肛門管を直腸粘膜剥離断端とつなげるように,括約筋は温存し病変の切除を予定した.最後に腹腔鏡補助下に人工肛門を造設し,皮膚欠損部には分層シート植皮を行う方針とした.
①ESD(消化器内科)
まずは消化器内科にて口側から病変の切除を開始した.口側の肛門管伸展が不良でやや境界同定が困難であったが,陰性であったmapping biopsy後の瘢痕を目印に,歯状線から口側に10 mmのmarginを確保した位置から粘膜下層剥離術を施行した.Dual knife 1.5 mmを用いて全周切開・剥離し肛門側に連続させた(Fig. 4).
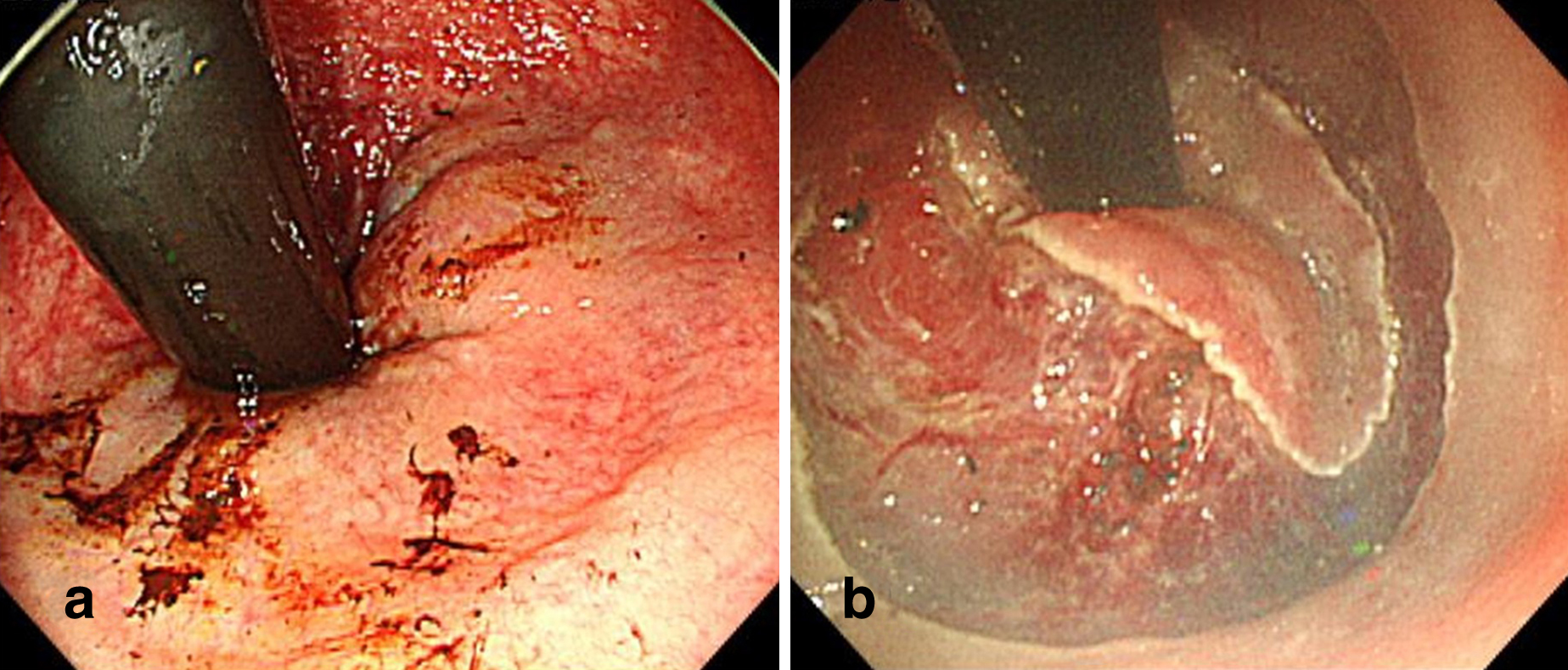
a, b: ESD was performed with a margin of 1 cm from the dentate line to the oral side.
②皮膚悪性腫瘍切除術(皮膚科)
続いて皮膚側の剥離に移った.肛門全周性の紅斑あり,脱色素斑も認め皮膚側の境界は明瞭であった.境界部より10 mmのmarginを確保し切除した.膣方向はmappingで陰性であり膣後壁境界領域で切除ラインを設定した(Fig. 5).
Anal side resection was started by a dermatologist. There was erythema all around the anus, but the border on the skin side was clear. The tumor was resected with a margin of 10 mm from the border. The vaginal direction was excised just behind the vaginal wall because it was negative on the mapping biopsy.
③経肛門的粘膜下層切除術,S状結腸双孔式人工肛門造設(消化器外科)
続いて当科にて肛門管の操作に移行した.内肛門括約筋を温存するよう肛門管の剥離を口側に進め,口側のESDの剥離ラインと連続させるよう粘膜下層を剥離し,検体を筒状に切除した(Fig. 6).植皮部の汚染回避のためS状結腸で人工肛門を造設した.

a: Gastrointestinal surgery for resection of the anal canal toward the oral side was performed to preserve the internal anal sphincter. b: The submucosa was exfoliated so as to be continuous with the oral dissection line by endoscopic submucosal dissection, so the sample was resected in a tubular shape.
④分層植皮術(皮膚科)
最後に皮膚科にて分層植皮術を施行した.左大腿前面から7×5 cmの大きさで2枚採皮した.そのうち1枚には1.5倍メッシュをかけた.粘膜面側の切離断端にはシート植皮を用いて全周性に縫合した.皮膚側にはメッシュ植皮を用いて,皮膚断端に固定した.粘膜側切離断端から皮膚側剥離断端を植皮で被覆し手術を終了した(Fig. 7).
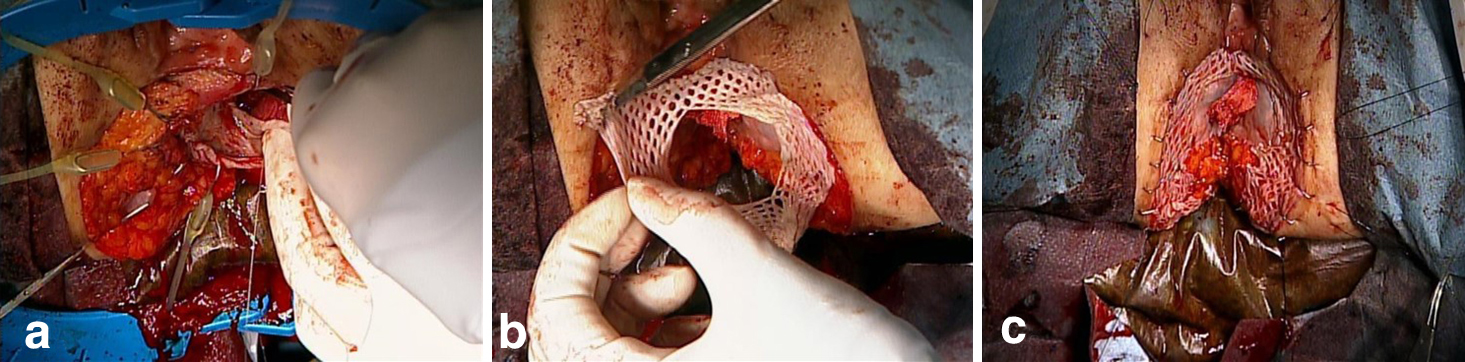
a, b, c: In the dermatology department, the exfoliated part was covered with sheet skin on the mucous membrane side and mesh skin on the skin side.
摘出標本・切除検体病理結果:肛門管を中心とする病変で,肛門周囲皮膚には肛門を中心として45×25 mmのびらんを伴う隆起性変化を認めた(Fig. 8).切除標本の病理組織学的診断結果は,anal canal cancer,adenocarcinoma with Pagetoid spreadであった.淡明で豊かな胞体を有する大型腫瘍細胞が小胞巣状・個細胞性にPaget様伸展しており,肛門管粘膜に管状構造を示す高分化腺癌の増殖がみられた(Fig. 9).

a: A tumor centered on the anal canal, with erosion in the skin around the anus. b: Growth of well-differentiated adenocarcinoma in the anal canal mucosa and pagetoid spread on perianal skin.

Large tumor cells with a rich reticulum and abundant endoplasmic reticulum progressing from a Paget-like to small alveolar co-cellular type. Proliferation of well-differentiated adenocarcinoma showed a tubular structure in the anal canal mucosa.
免疫組織化学染色は,CK7(+),CK20(+),AM5.2(+),GCDFP15(−),CDX2(+),p53(−)で肛門管癌adenocarcinomaに矛盾しない結果で,同病変の皮膚へのPaget様伸展と判断された(Fig. 10).直腸側,皮膚側の切除断端は陰性で,剥離面にも腫瘍の露出はみられなかった.
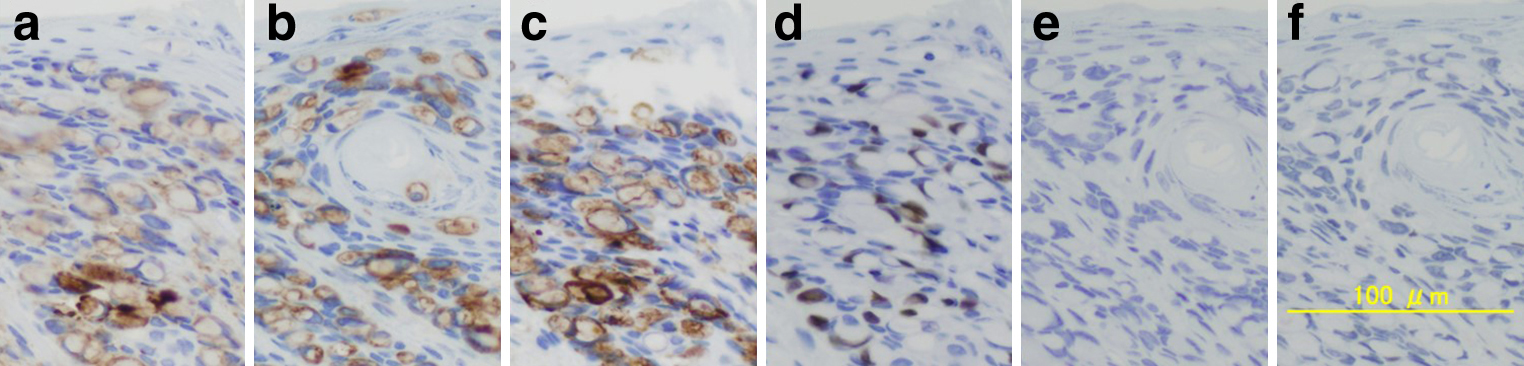
Immunohistochemical staining results were as follows: CK7 (+), CK 20 (+), AM 5.2 (+), GCDFP 15 (−), CDX 2 (+) p 53 (−), which supported the diagnosis of anal canal cancer. a: CK7 (+), b: CK 20 (+), c: AM 5.2 (+), d: GCDFP 15 (−), e: CDX 2 (+), f: p 53 (−).
最終診断:Pagetoid spreadを伴う肛門管癌:P,type 0-IIb,pTis(M),cN0,cM0,pStage 0(tub1,ly0,v0,PN0,pPM0,pDM0,pRM0)
術後経過:術後経過良好であり会陰部植皮の生着および感染のないことを確認した後に17 PODで退院となった.術後8か月経過し外来で骨盤底筋群訓練などを行い,肛門機能も良好であることを確認し,人工肛門閉鎖術(結腸部分切除,functional end-to-end anastomosis;FEEA)を施行した.
術後の漏便はなく,7~8回/日の頻便は認めたが,1か月程度で症状は改善した.また,術後肛門狭窄は来さず,ブジーも要しなかった.現在ではWexner scoreも0点と良好な排便機能を保っている.
Paget病は明るい胞体を持ったPaget細胞と呼ばれる大型の異型細胞の表皮内増殖像を特徴とする悪性腫瘍で,乳房に生ずる乳房Paget病と乳房外に発生する乳房外Paget病に分類される1)2).なかでも肛門周囲Paget病は乳房外Paget病の5%程度の頻度で,まれな疾患とされている2)3).
一方,直腸癌や肛門管癌が上皮性に表皮内へ直接浸潤してPaget病様の像を示すことがあり,これをPagetoid spreadまたはPaget現象という4).肛門管癌に伴うPagetoid spreadの頻度は6.1%と報告されており,比較的まれな病態といわれている5).
狭義のPaget病は非浸潤癌であり予後は良好とされているが,Pagetoid spreadの本態は直腸・肛門管癌の表皮内への浸潤であり予後は不良である.治療法が両者で全く異なるために,鑑別診断は非常に重要となってくる.これら二つの病態の鑑別には皮膚病変の免疫染色検査が有用とされており,アポクリン汗腺,エクリン汗腺細胞に存在するGCDFP15やCK7と消化腺粘膜上皮に発現するCK20を用いて鑑別される.肛門周囲PagetはCK7やGCDFP15が陽性,CK20陰性を示すのに対し,Pagetoid spreadではCK7,GCDFP15陰性,CK20が陽性を示す6)~9).
Pagetoid spreadを伴う肛門管癌に関して,森本ら10) 32例の集計によると23例で腹会陰式直腸切断術が選択されており,そのうち局所切除後病理検査で腹会陰式直腸切断術追加例が5例であった.また,一方で局所切除のみの症例は6 例のみで,そのほか仙骨式直腸切断術が1例,化学療法が1例,化学放射線療法が1例あったことが示されている.
このように多くの症例で,切除可能病変については腹会陰式直腸切断術が選択されることが多く,局所手術のみで終われた症例は少なくなっている.逆に,本症例のように術前明らかな肛門管癌を認めないものの免疫組織染色においてそれが強く疑われる症例では術式の選択がより困難で,肛門温存や患者のQOLを考慮するうえで大きな問題となる11).
術式決定に関しては肛門温存の判断と肛門管および皮膚再建法が主な問題となる.肛門を温存した局所切除を選択することが難しい要因として,皮膚病変の切除を要し,またその切除範囲の決定が難しいことやfree marginを含む肛門管粘膜の完全切除は肛門管の解剖を熟視した大腸肛門病外科医でも難易度の高い手技であることが大きな要因となっていると考えられる.また,Pagetoid spreadを伴う肛門管癌の予後が通常の肛門管癌に比べ不良といわれていること,進行症例が多いこと,組織型が未分化型や粘液癌が多い傾向にあること,術前mappingの限界やPaget細胞が残存し非治癒切除となる可能性,非治癒切除に伴う早期遠隔転移の可能性などが挙げられている12).
局所切除例の報告はむしろ,グラフト再建に主眼を置いた報告が多く13)~16),皮膚側の切除範囲に関して一定の見解は得られていないが,肉眼的病変より3~5 cmのmarginを確保し,筋膜上あるいは脂肪組織中~深層で切除することが一般的とされている17)~19).また,皮膚悪性腫瘍ガイドラインでは,肉眼的に境界明瞭な部分やmapping biposyで陰性と判断された部位は1 cm程度のmarginとし,境界不明瞭な部分では3 cm程度のmarginとすることが推奨されている20).
一方,肛門粘膜側の切除に関して,深達度や進行度に応じた局所切除の適応や,垂直marginの確保に関して見解を示した報告はなく,今後の検討が期待されるところではある.しかし,術前診断より深部浸潤のない表在癌が疑われ,垂直断端陰性が期待できる症例に関しては,自然肛門温存や患者のQOLを保つためにも,局所切除の適応を積極的に考慮するべきと考える.また,肛門縁から歯状線までの長さは一般的に2 cm程度とされており,Nakaharaら21)によると,歯状線から口側2 cmの切除であれば,残存直腸粘膜を下層の筋層と剥離して肛門側に引き出し,露出した肛門括約筋を被覆することにより比較的安全に肛門機能を温存できるとされている.
井上ら22)や前田ら23)の報告のように,肛門機能温存と根治性を確保したPagetoid spreadを伴う肛門管癌の切除例は散見されるが,いずれも経肛門操作のみによるものや皮弁による肛門温存に主眼を置いた報告で,他の報告を診ても本症例のように消化器内科とのコラボレーションにより,ESDを併用した手術報告は確認されない.また,皮膚再建に関しても,皮弁を用いた報告は多いものの,再建法として植皮術を選択し,感染予防に一時的な人工肛門を造設した症例は,「Pagetoid spread」,「肛門管癌」をキーワードに1964年から2018年を対象期間として医学中央雑誌にて検索を行ったが報告は認めなかった.
肛門管にかかる病変は,大型病変や回盲部病変,虫垂開口部病変,回盲弁病変,などとならび代表的なESD困難部位として挙げられている24).その要因として肛門管は内腔が狭く視野確保が困難なことや,スコープの先端のみが肛門縁に接した不安定な状態での手技操作を余儀なくされる点などが挙げられている.また,この部位には連合縦走筋や粘膜支持靱帯で形成される粘膜下層の強固な繊維性筋組織の存在や,発達した静脈層があり出血を来しやすいこともESDを難渋させる要因として指摘されている.中には肛門管領域へ伸展を認める下部直腸腫瘍に対するESD単独治療において14例中12例に術中出血,4例に術後出血を認めたという報告もある25).一方で,経肛門的局所切除の適応は肛門縁から5 cmとされており,脊椎麻酔でも可能な手術となる24).合併症も少なく有用な手技であるが,病変口側の視認性不良による口側縁切離の不確実性や局所再発のriskを指摘する報告もあり,中には30%前後で局所再発するとの報告もある26)~28).
本症例のようにESDと経肛門的局所切除を併用することで,肛門管領域の発達した静脈層からの出血のリスクの回避や,腫瘍口側の確実なmarginの確保を担保することができると考える.従来,内視鏡施行医がESDを行う際には,腫瘍の局在による操作の調整や,剥離した粘膜が術野の視野の妨げにならないよう体位変換を行いながら手技を進めることも多い.幸い,本症例では難渋することなくESDでの操作を終えることができたが,全身麻酔後で患者の体位変換の協力が得られないときには,SO clipなどのけん引クリップ29)を使用するなどの工夫が必要な場合もあると考えられる.他にも,ESDと経肛門切除の境界をどこに置くかが問題となってくるが,経肛門局所切除の適応に準じた外科的肛門操作ができるような十分な内視鏡的剥離が肝要と考えられ,肛門縁から5 cm,歯状線から口側2 cmより肛門側までのESDによる剥離が必要と考えられた.
本症例は術前に明らかな腫瘤性病変を肛門管内に認めないものの,免疫染色検査の結果から肛門管由来のinvasiveな悪性腫瘍であることが強く示唆された.腹会陰式直腸切断術も考慮されたが,腫瘍の深部浸潤を疑う所見や遠隔転移などを疑う所見は認めず,局所切除による自然肛門の温存と,根治性の両立が求められた症例であった.
本症例のように直腸内から消化器内科医が内視鏡を用いて歯状線口側の切除を開始することで,経肛門操作では得ることのできない視野で確実な口側marginの確保ができるだけでなく,経肛門操作では術野が深くなり術操作に難渋するような部位からも,より確実に剥離層を確認しながら切除を進めることが可能であると考えられた.また,口側の剥離がある程度進められていることで,外科医もより確実・安全に肛門側からの剥離操作を進めることができ,経肛門的粘膜下層切除術の難易度を相対的に下げることが期待されただけでなく,より確実な括約筋温存による,肛門機能の温存に寄与できたと考えられる.また,皮膚再建に関しても,シート植皮と一時的な人工肛門造設を併用することで,植皮の生着は非常に良好で,順調な術後経過につながったと考える.もちろん,これらの術式を選択するには,術前の肛門機能が良好であることが前提であると考える.
術後8か月には人工肛門閉鎖術施行となり,術後2 年以上が経過した現在も肛門機能は良好で無再発生存中であり,根治性,QOL,患者満足度を高いレベルで達成できた.
内視鏡診断の著しい進歩もあり,術前深達度診断がより正確になってきている現在,適応は慎重に考慮されるべきではあるものの,自験例のような症例においては,内視鏡や植皮術を併用することで肛門温存可能となる可能性も示され,今後のさらなる症例の集積が期待される.
本稿を終えるにあたり,本症例の治療にご協力いただきました岐阜大学医学部付属病院消化器内科・荒木寛司先生,皮膚科・松山かなこ先生に深謝いたします.
利益相反:なし